1) Нитрат меди прокалили, полученный твёрдый осадок растворили в серной кислоте. Через раствор пропустили сероводород, полученный чёрный осадок подвергли обжигу, а твёрдый остаток растворили при нагревании в концентрированной азотной кислоте.
2) Фосфат кальция сплавили с углём и песком, затем полученное простое вещество сожгли в избытке кислорода, продукт сжигания растворили в избытке едкого натра. К полученному раствору прилили раствор хлорида бария. Полученный осадок обработали избытком фосфорной кислоты.
| Показать | |
|---|---|
Ca 3 (PO 4) 2 → P → P 2 O 5 →Na 3 PO 4 → Ba 3 (PO 4) 2 → BaHPO 4 или Ba(H 2 PO 4) 2 Ca 3 (PO 4) 2 + 5C + 3SiO 2 → 3CaSiO 3 + 2P + 5CO |
|
3) Медь растворили в концентрированной азотной кислоте, полученный газ смешали с кислородом и растворили в воде. В полученном растворе растворили оксид цинка, затем к раствору прибавили большой избыток раствора гидроксида натрия.
4) На сухой хлорид натрия подействовали концентрированной серной кислотой при слабом нагревании, образующийся газ пропустили в раствор гидроксида бария. К полученному раствору прилили раствор сульфата калия. Полученный осадок сплавили с углем. Полученное вещество обработали соляной кислотой.
5) Навеску сульфида алюминия обработали соляной кислотой. При этом выделился газ и образовался бесцветный раствор. К полученному раствору добавили раствор аммиака, а газ пропустили через раствор нитрата свинца. Полученный при этом осадок обработали раствором пероксида водорода.
| Показать | |
|---|---|
Al(OH) 3 ←AlCl 3 ←Al 2 S 3 → H 2 S → PbS →PbSO 4 Al 2 S 3 + 6HCl → 3H 2 S + 2AlCl 3 |
|
6) Порошок алюминия смешали с порошком серы, смесь нагрели, полученное вещество обработали водой, при этом выделился газ и образовался осадок, к которому добавили избыток раствора гидроксида калия до полного растворения. Этот раствор выпарили и прокалили. К полученному твёрдому веществу добавили избыток раствора соляной кислоты.
7) Раствор иодида калия обработали раствором хлора. Полученный осадок обработали раствором сульфита натрия. К полученному раствору прибавили сначала раствор хлорида бария, а после отделения осадка - добавили раствор нитрата серебра.
8) Серо-зелёный порошок оксида хрома (III) сплавили с избытком щёлочи, полученное вещество растворили в воде, при этом получился тёмно-зелёный раствор. К полученному щелочному раствору прибавили пероксид водорода. Получился раствор желтого цвета, который при добавлении серной кислоты приобретает оранжевый цвет. При пропускании сероводорода через полученный подкисленный оранжевый раствор он мутнеет и вновь становится зелёным.
| Показать | |
|---|---|
Cr 2 O 3 → KCrO 2 → K →K 2 CrO 4 →K 2 Cr 2 O 7 → Cr 2 (SO 4) 3 Cr 2 O 3 + 2KOH → 2KCrO 2 + H 2 O |
|
9) Алюминий растворили в концентрированном растворе гидроксида калия. Через полученный раствор пропускали углекислый газ до прекращения выделения осадка. Осадок отфильтровали и прокалили. Полученный твердый остаток сплавили с карбонатом натрия.
10) Кремний растворили в концентрированном растворе гидроксида калия. К полученному раствору добавили избыток соляной кислоты. Помутневший раствор нагрели. Выделившийся осадок отфильтровали и прокалили с карбонатом кальция. Напишите уравнения описанных реакций.
11) Оксид меди(II) нагрели в токе угарного газа. Полученное вещество сожгли в атмосфере хлора. Продукт реакции растворили в воде. Полученный раствор разделили на две части. К одной части добавили раствор иодида калия, ко второй – раствор нитрата серебра. И в том и в другом случае наблюдали образование осадка. Напишите уравнения четырех описанных реакций.
12) Нитрат меди прокалили, образовавшееся твердое вещество растворили в разбавленной серной кислоте. Раствор полученной соли подвергли электролизу. Выделившееся на катоде вещество растворили в концентрированной азотной кислоте. Растворение протекало с выделением бурого газа. Напишите уравнения четырех описанных реакций.
13) Железо сожгли в атмосфере хлора. Полученное вещество обработали избытком раствора гидроксида натрия. Образовался бурый осадок, который отфильтровали и прокалили. Остаток после прокаливания растворили в иодоводородной кислоте. Напишите уравнения четырех описанных реакций.
14) Порошок металлического алюминия смешали с твердым иодом и добавили несколько капель воды. К полученной соли добавили раствор гидроксида натрия до выпадения осадка. Образовавшийся осадок растворили в соляной кислоте. При последующем добавлении раствора карбоната натрия вновь наблюдали выпадение осадка. Напишите уравнения четырех описанных реакций.
15) В результате неполного сгорания угля получили газ, в токе которого нагрели оксид железа(III). Полученное вещество растворили в горячей концентрированной серной кислоте. Образовавшийся раствор соли подвергли электролизу. Напишите уравнения четырех описанных реакций.
16) Некоторое количество сульфида цинка разделили на две части. Одну из них обработали азотной кислотой, а другую подвергли обжигу на воздухе. При взаимодействии выделившихся газов образовалось простое вещество. Это вещество нагрели с концентрированной азотной кислотой, причем выделился бурый газ. Напишите уравнения четырех описанных реакций.
17) Хлорат калия нагрели в присутствии катализатора, при этом выделился бесцветный газ. Сжиганием железа в атмосфере этого газа была получена железная окалина. Её растворили в избытке соляной кислоты. К полученному при этом раствору добавили раствор, содержащий дихромат натрия и соляную кислоту.
| Показать | |
|---|---|
1) 2КClО 3 → 2КСl + 3О 2 2) ЗFe + 2O 2 → Fе 3 O 4 3) Fе 3 O 4 + 8НСІ → FeCl 2 + 2FeCl 3 + 4Н 2 О 4) 6 FeCl 2 + Na 2 Cr 2 O 7 + 14 НСІ → 6 FeCl 3 + 2 CrCl 3 + 2NaCl + 7Н 2 О 18) Железо сожгли в хлоре. Полученную соль добавили к раствору карбоната натрия, при этом выпал бурый осадок. Этот осадок отфильтровали и прокалили. Полученное вещество растворили в иодоводородной кислоте. Напишите уравнения четырех описанных реакций. 1) 2Fe + 3Cl 2 → 2FeCl 3 2)2FeCl 3 +3Na 2 CO 3 →2Fe(OH) 3 +6NaCl+3CO 2 3) 2Fe(OH) 3 Fe 2 O 3 + 3H 2 O 4) Fe 2 O 3 + 6HI → 2FeI 2 + I 2 + 3H 2 O |
|
19) Раствор иодида калия обработали избытком хлорной воды, при этом наблюдали сначала образование осадка, а затем – его полное растворение. Образовавшуюся при этом иодосодержащую кислоту выделили из раствора, высушили и осторожно нагрели. Полученный оксид прореагировал с угарным газом. Запишите уравнения описанных реакций.
20) Порошок сульфида хрома(III) растворили в серной кислоте. При этом выделился газ и образовался окрашенный раствор. К полученному раствору добавили избыток раствора аммиака, а газ пропустили через нитрата свинца. Полученный при этом черный осадок побелел после обработки его пероксидом водорода. Запишите уравнения описанных реакций.
21) Порошок алюминия нагрели с порошком серы, полученное вещество обработали водой. Выделившийся при этом осадок обработали избытком концентрированного раствора гидроксида калия до его полного растворения. К полученному раствору добавили раствор хлорида алюминия и вновь наблюдали образование белого осадка. Запишите уравнения описанных реакций.
22) Нитрат калия нагрели с порошкообразным свинцом до прекращения реакции. Смесь продуктов обработали водой, а затем полученный раствор профильтровали. Фильтрат подкислили серной кислотой и обработали иодидом калия. Выделившееся простое вещество нагрели с концентрированной азотной кислотой. В атмосфере образовавшегося при этом бурого газа сожгли красный фосфор. Запишите уравнения описанных реакций.
23) Медь растворили в разбавленной азотной кислоте. К полученному раствору добавили избыток раствора аммиака, наблюдая сначала образование осадка, а затем – его полное растворение с образованием темно-синего раствора. Полученный раствор обработали серной кислотой до появления характерной голубой окраски солей меди. Запишите уравнения описанных реакций.
| Показать | |
|---|---|
1)3Cu+8HNO 3 →3Cu(NO 3) 2 +2NO+4H 2 O 2)Cu(NO 3) 2 +2NH 3 H 2 O→Cu(OH) 2 + 2NH 4 NO 3 3)Cu(OH) 2 +4NH 3 H 2 O →(OH) 2 + 4H 2 O 4)(OH) 2 +3H 2 SO 4 → CuSO 4 +2(NH 4) 2 SO 4 + 2H 2 O |
|
24) Магний растворили в разбавленной азотной кислоте, причем выделение газа не наблюдалось. Полученный раствор обработали избытком раствора гидроксида калия при нагревании. Выделившийся при этом газ сожгли в кислороде. Запишите уравнения описанных реакций.
25) Смесь порошков нитрита калия и хлорида аммония растворили в воде и раствор осторожно нагрели. Выделившийся газ прореагировал с магнием. Продукт реакции внесли в избыток раствора соляной кислоты, при этом выделение газа не наблюдалось. Полученную магниевую соль в растворе обработали карбонатом натрия. Запишите уравнения описанных реакций.
26) Оксид алюминия сплавили с гидроксидом натрия. Продукт реакции внесли в раствор хлорида аммония. Выделившийся газ с резким запахом поглощен серной кислотой. Образовавшуюся при этом среднюю соль прокалили. Запишите уравнения описанных реакций.
27) Хлор прореагировал с горячим раствором гидроксида калия. При охлаждении раствора выпали кристаллы бертолетовой соли. Полученные кристаллы внесли в раствор соляной кислоты. Образовавшееся простое вещество прореагировало с металлическим железом. Продукт реакции нагрели с новой навеской железа. Запишите уравнения описанных реакций.
28) Медь растворили в концентрированной азотной кислоте. К полученному раствору добавили избыток раствора аммиака, наблюдая сначала образование осадка, а затем – его полное растворение. Полученный раствор обработали избытком соляной кислоты. Запишите уравнения описанных реакций.
29) Железо растворили в горячей концентрированной серной кислоте. Полученную соль обработали избытком раствора гидроксида натрия. Выпавший бурый осадок отфильтровали и прокалили. Полученное вещество сплавили с железом. Напишите уравнения четырёх описанных реакций.
30) В результате неполного сгорания угля получили газ, в токе которого нагрели оксид железа(ІІІ). Полученное вещество растворили в горячей концентрированной серной кислоте. Образовавшийся раствор соли обработали избытком раствора сульфида калия.
31) Некоторое количество сульфида цинка разделили на две части. Одну из них обработали соляной кислотой, а другую подвергли обжигу на воздухе. При взаимодействии выделившихся газов образовалось простое вещество. Это вещество нагрели с концентрированной азотной кислотой, причём выделился бурый газ.
32) Серу сплавили с железом. Продукт реакции обработали соляной кислотой. Выделившийся при этом газ сожгли в избытке кислорода. Продукты горения поглотили водным раствором сульфата железа(ІІІ).
Соляная кислота.
В химических реакциях соляная кислота проявляет все свойства сильных кислот: взаимодействует с металлами , стоящими в ряду напряжений левее водорода, с оксидами (основными, амфотерными), основаниями, амфотерными гидроксидами и солями:
2HCl + Fe = FeCl 2 + H 2
2HCl + CaO = CaCl 2 + H 2 O
6HCl + Al 2 O 3 = 2AlCl 3 + 3H 2 O
HCl + NaOH = NaCl + H 2 O
2HCl + Cu(OH) 2 = CuCl 2 + 2H 2 O
2HCl + Zn(OH) 2 = ZnCl 2 + 2H 2 O
HCl + NaHCO 3 = NaCl + CO 2 + H 2 O
HCl + AgNO 3 = AgCl↓ + HNO 3 (качественная реакция на галогенид-ионы)
6HCl (конц.) + 2HNO 3(конц.) = 3Cl 2 + 2NO + 4H 2 O
HClO 2 – хлористая
HClO 3 – хлорноватая
HClO 4 – хлорная
HClO HClO 2 HClO 3 HClO 4
усиление кислотных свойств
2HClO 2HCl + O 2
HClO + 2HI = HCl + I 2 + H 2 O
HClO + H 2 O 2 = HCl + H 2 O + O 2
Соли.
Соли соляной кислоты – хлориды.
NaCl + AgNO 3 = AgCl↓ + NaNO 3 (качественная реакция на галогенид-ионы)
AgCl + 2(NH 3 ∙ H 2 O) = Cl + 2H 2 O
2AgCl 2Ag + Cl 2
Соли кислородсодержащих кислот.
Ca(ClO) 2 + H 2 SO 4 = CaSO 4 + 2HCl + O 2
Ca(ClO) 2 + CO 2 + H 2 O = CaCO 3 + 2HClO
Ca(ClO) 2 + Na 2 CO 3 = CaCO 3 + 2NaClO
Ca(ClO) 2 CaCl 2 + O 2
4KClO 3 3KClO 4 + KCl
2KClO 3 2KCl + 3O 2
2KClO 3 + 3S 2KCl + 3SO 2
5KClO 3 + 6P 5KCl + 3P 2 O 5
KClO 4 2O 2 + KCl
3KClO 4 + 8Al = 3KCl + 4Al 2 O 3
Бром. Соединения брома.
Br 2 + H 2 = 2HBr
Br 2 + 2Na = 2NaBr
Br 2 + Mg = MgBr 2
Br 2 + Cu = CuBr 2
3Br 2 + 2Fe = 2FeBr 3
Br 2 + 2NaOH (разб) = NaBr + NaBrO + H 2 O
3Br 2 + 6NaOH (конц.) = 5NaBr + NaBrO 3 + 3H 2 O
Br 2 + 2NaI = 2NaBr + I 2
3Br 2 + 3Na 2 CO 3 = 5NaBr + NaBrO 3 + 3CO 2
3Br 2 + S + 4H 2 O = 6HBr + H 2 SO 4
Br 2 + H 2 S = S + 2HBr
Br 2 + SO 2 + 2H 2 O = 2HBr + H 2 SO 4
4Br 2 + Na 2 S 2 O 3 + 10NaOH = 2Na 2 SO 4 + 8NaBr + 5H 2 O
14HBr + K 2 Cr 2 O 7 = 2KBr + 2CrBr 3 + 3Br 2 + 7H 2 O
4HBr + MnO 2 = MnBr 2 + Br 2 + 2H 2 O
2HBr + H 2 O 2 = Br 2 + 2H 2 O
2KBr + 2H 2 SO 4 (конц.) = 4K 2 SO 4 + 4Br 2 + SO 2 + 2H 2 O
2KBrO 3 3O 2 + 2KBr
2KBrO 4 O 2 + 2KBrO 3 (до 275°С)
KBrO 4 2O 2 + KBr (выше 390°С)
Йод. Соединения йода.
3I 2 + 3P = 2PI 3
I 2 + H 2 = 2HI
I 2 + 2Na = 2NaI
I 2 + Mg = MgI 2
I 2 + Cu = CuI 2
3I 2 + 2Al = 2AlI 3
3I 2 + 6NaOH (гор.) = 5NaI + NaIO 3 + 3H 2 O
I 2 + 2NaOH (разб) = NaI + NaIO + H 2 O
3I 2 + 10HNO 3 (разб) = 6HIO 3 + 10NO + 2H 2 O
I 2 + 10HNO 3 (конц.) = 2HIO 3 + 10NO 2 + 4H 2 O
I 2 + 5NaClO + 2NaOH = 5NaCl + 2NaIO 3 + H 2 O
I 2 + 5Cl 2 + 6H 2 O = 10HCl + 2HIO 3
I 2 + Na 2 SO 3 + 2NaOH = 2NaI + Na 2 SO 4 + H 2 O
2HI + Fe 2 (SO 4) 3 = 2FeSO 4 + I 2 + H 2 SO 4
2HI + NO 2 = I 2 + NO + H 2 O
2HI + S = I 2 + H 2 S
8KI + 5H 2 SO 4 (конц.) = 4K 2 SO 4 + 4I 2 + H 2 S + 4H 2 O или
KI + 3H 2 O + 3Cl 2 = HIO 3 + KCl + 5HCl
10KI + 8H 2 SO 4 + 2KMnO 4 = 5I 2 + 2MnSO 4 + 6K 2 SO 4 + 8H 2 O
6KI + 7H 2 SO 4 + K 2 Cr 2 O 7 = Cr 2 (SO 4) 3 + 3I 2 + 4K 2 SO 4 + 7H 2 O
2KI + H 2 SO 4 + H 2 O 2 = I 2 + K 2 SO 4 + 2H 2 O
2KI + Fe 2 (SO 4) 3 = I 2 + 2FeSO 4 + K 2 SO 4
2KI + 2CuSO 4 + K 2 SO 3 + H 2 O = 2CuI + 2K 2 SO 4 + H 2 SO 4
2HIO 3 I 2 O 5 + H 2 O
2HIO 3 + 10HCl = I 2 + 5Cl 2 + 6H 2 O
2HIO 3 + 5Na 2 SO 3 = 5Na 2 SO 4 + I 2 + H 2 O
2HIO 3 + 5H 2 SO 4 + 10FeSO 4 = Fe 2 (SO 4) 3 + I 2 + 6H 2 O
I 2 O 5 + 5CO I 2 + 5CO 2
2KIO 3 3O 2 + 2KI
2KIO 3 + 12HCl (конц.) = I 2 + 5Cl 2 + 2KCl + 6H 2 O
KIO 3 + 3H 2 SO 4 + 5KI = 3I 2 + 3K 2 SO 4 + 3H 2 O
KIO 3 + 3H 2 O 2 = KI + 3O 2 + 3H 2 O
2KIO 4 O 2 + 2KIO 3
5KIO 4 + 3H 2 O + 2MnSO 4 = 2HMnO 4 + 5KIO 3 + 2H 2 SO 4
Галогены.
1. Вещество, полученное на аноде при электролизе расплава иодида натрия с инертными электродами, выделили и ввели во взаимодействие с сероводородом. Газообразный продукт последней реакции растворили в воде и к полученному раствору добавили хлорное железо. Образовавшийся осадок отфильтровали и обработали горячим раствором гидроксида натрия. Напишите уравнения описанных реакций.
2. Вещество, полученное на аноде при электролизе раствора иодида натрия с инертными электродами, ввели в реакцию с калием. Продукт реакции нагрели с концентрированной серной кислотой и выделившийся газ пропустили через горячий раствор хромата калия. Напишите уравнения описанных реакций.
3. Хлорная вода имеет запах хлора. При подщелачивании запах исчезает, а при добавлении соляной кислоты – становится более сильным, чем был ранее. Напишите уравнения описанных реакций.
4. Бесцветные газы выделяются при выдерживании концентрированной кислоты , как с хлоридом натрия, так и с иодидом натрия. При пропускании этих газов через водный раствор аммиака образуются соли. Напишите уравнения описанных реакций.
5. При термическом разложении соли А в присутствии диоксида марганца образовались бинарная соль Б и газ, поддерживающий горение и входящий в состав воздуха, при нагревании этой соли без катализатора образуются соль Б и соль кислородсодержащей кислоты. При взаимодействии соли А с соляной кислотой выделяется жёлто-зелёный газ (простое вещество) и образуется соль Б. соль Б окрашивает пламя в фиолетовый цвет, при её взаимодействии с раствором нитрата серебра выпадает осадок белого цвета. Напишите уравнения описанных реакций.
6) При добавлении раствора кислоты А к диоксиду марганца происходит выделение ядовитого газа жёлто-зелёного газа. Пропустив выделившийся газ через горячий раствор едкого кали, получают вещество, которое используется при изготовлении спичек и некоторых других зажигательных составов. При термическом разложении последнего в присутствии диоксида марганца образуется соль, из которой при взаимодействии с концентрированной серной кислотой можно получить исходную кислоту А, и бесцветный газ, входящий в состав атмосферного воздуха. Напишите уравнения описанных реакций.
7) Йод нагрели с избытком фосфора , и продукт реакции обработали небольшим количеством воды. Газообразный продукт реакции полностью нейтрализовали раствором едкого натра и добавили в полученный раствор нитрат серебра. Напишите уравнения описанных реакций.
8) Газ, выделившийся при нагревании твердой поваренной соли с концентрированной серной кислотой, пропустили через раствор перманганата калия. Газообразный продукт реакции поглотили холодным раствором едкого натра. После добавления в полученный раствор йодоводородной кислоты появляется резкий запах и раствор приобретает тёмную окраску. Напишите уравнения описанных реакций.
9) Через раствор бромида натрия пропустили газ, выделяющийся при взаимодействии соляной кислоты с перманганатом калия. После окончания реакции раствор выпарили, остаток растворили в воде и подвергли электролизу с графитовыми электродами. Газообразные продукты реакции смешали друг с другом и осветили. В результате произошел взрыв. Напишите уравнения описанных реакций.
10) К пиролюзиту осторожно прибавили раствор соляной кислоты, и выделившийся газ пропустили в химический стакан, наполненный холодным раствором едкого кали. После окончания реакции стакан накрыли картонкой и оставили , при этом стакан освещали солнечные лучи; через некоторое время в стакан внесли тлеющую лучинку, которая ярко вспыхнула. Напишите уравнения описанных реакций.
11) Вещество, выделяющееся на катоде и аноде при электролизе раствора йодида натрия с графитовыми электродами, реагируют друг с другом. Продукт реакции взаимодействуют с концентрированной серной кислотой с выделением газа, который пропустили через раствор гидроксида калия. Напишите уравнения описанных реакций.
12) К оксиду свинца (IV) при нагревании добавили концентрированную соляную кислоту. Выделяющийся газ пропустили через нагретый раствор едкого кали. Раствор охладили, соль кислородсодержащей кислоты отфильтровали и высушили. При нагревании полученной соли с соляной кислотой выделяется ядовитый газ, а при нагревании её в присутствии диоксида марганца – газ, входящий в состав атмосферы. Напишите уравнения описанных реакций.
13) Йод обработали концентрированной азотной кислотой при нагревании. Продукт реакции осторожно нагрели. Образовавшийся при оксид вступил в реакцию с угарным газом. Выделившееся простое вещество растворили в теплом растворе гидроксида калия. Напишите уравнения описанных реакций.
14) Раствор иодида калия обработали избытком хлорной воды , при этом сначала наблюдали образование осадка, а затем – его полное растворение. Образовавшуюся при этом йодсодержащую кислоту выделили из раствора, высушили и осторожно нагрели. полученный оксид прореагировал с угарным газом. Напишите уравнения описанных реакций.
15) Йод обработали хлорноватой кислотой. Продукт реакции осторожно нагрели. продукт реакции осторожно нагрели. Образующийся оксид реагирует с угарным газом с образованием двух веществ – простого и сложного. Простое вещество растворяется в теплом щелочном растворе сульфита натрия. Напишите уравнения описанных реакций.
16) Перманганат калия обработали избытком раствора соляной кислоты, образовался раствор и выделился газ. Раствор разделили на две части: к первой добавили гидроксид калия, а ко второй – нитрат серебра. Выделившийся газ прореагировал газ прореагировал с гидроксидом калия при охлаждении. Напишите уравнения описанных реакций.
17) Расплав хлорида натрия подвергли электролизу. Газ, выделившийся на аноде, прореагировал с водородом с образованием нового газообразного вещества с характерным запахом. Его растворили в воде и обработали расчетным количеством перманганата калия, при этом образовался газ желто-зеленого цвета. Это вещество вступает при охлаждении с гидроксидом натрия. Напишите уравнения описанных реакций.
18) Перманганат калия обработали концентрированной соляной кислотой. Выделившийся при этом газ собрали , а к реакционной массе по каплям прибавили раствор гидроксида калия до прекращения выделения осадка. Собранный газ пропустили через горячий раствор гидроксида калия, при этом образовалась смесь двух солей. Раствор выпарили, твердый остаток прокалили в присутствии катализатора, после чего в твердом остатке осталась одна соль. Напишите уравнения описанных реакций.
Галогены.
1) 2NaI ![]() 2Na + I 2
2Na + I 2
на катоде на аноде
I 2 + H 2 S = 2HI + S↓
2HI + 2FeCl 3 = I 2 + 2FeCl 2 + 2HCl
I 2 + 6NaOH (гор.) = NaIO 3 + 5NaI + 3H 2 O
2) 2NaI + 2H 2 O ![]() 2H 2 + 2NaOH + I 2
2H 2 + 2NaOH + I 2
На катоде на аноде
8KI + 8H 2 SO 4(конц.) = 4I 2 ↓ + H 2 S + 4K 2 SO 4 + 4H 2 O или
8KI + 9H 2 SO 4 (конц.) = 4I 2 ↓ + H 2 S + 8KHSO 4 + 4H 2 O
3H 2 S + 2K 2 CrO 4 + 2H 2 O = 2Cr(OH) 3 + 3S + 4KOH
3) Cl 2 + H 2 O ↔ HCl + HClO
HCl + NaOH = NaCl + H 2 O
HClO + NaOH = NaClO + H 2 O
NaClO + 2HCl = NaCl + Cl 2 + H 2 O
4) H 2 SO 4(конц.) + NaCl (тверд.) = NaHSO 4 + HCl
9H 2 SO 4(конц.) + 8NaI (тверд.) = 8NaHSO 4 + 4I 2 ↓ + H 2 S + 4H 2 O
NH 4 OH + HCl = NH 4 Cl + H 2 O
NH 4 OH + H 2 S = NH 4 HS + H 2 O
5) 2KClO 3 2KCl + 3O 2
4KClO 3 KCl + 3KClO 4
KClO 3 + 6HCl = KCl + 3Cl 2 + 3H 2 O
KCl + AgNO 3 = AgCl↓ + KNO 3
6) 4HCl + MnO 2 = MnCl 2 + Cl 2 + 2H 2 O
3Cl 2 + 6KOH (гор.) = 5KCl + KClO 3 + 3H 2 O
2KClO 3 2KCl + 3O 2
H 2 SO 4(конц.) + NaCl (тверд.) = NaHSO 4 + HCl
7) 3I 2 + 3P = 2PI 3
PI 3 + 3H 2 O = H 3 PO 3 + 3HI
HI + NaOH = NaI + H 2 O
NaI + AgNO 3 = AgI↓ + NaNO 3
8) H 2 SO 4(конц.) + NaCl (тверд.) = NaHSO 4 + HCl
16HCl + 2KMnO 4 = 5Cl 2 + 2KCl + 2MnCl 2 + 8H 2 O
Cl 2 + 2NaOH (хол.) = NaCl + NaClO + H 2 O
NaClO + 2HI = NaCl + I 2 + H 2 O
9) 16HCl + 2KMnO 4 = 5Cl 2 + 2KCl + 2MnCl 2 + 8H 2 O
Щелочные металлы легко реагируют с неметаллами:
2K + I 2 = 2KI
2Na + H 2 = 2NaH
6Li + N 2 = 2Li 3 N (реакция идет уже при комнатной температуре)
2Na + S = Na 2 S
2Na + 2C = Na 2 C 2
В реакциях с кислородом каждый щелочной металл проявляет свою индивидуальность: при горении на воздухе литий образует оксид, натрий – пероксид, калий – надпероксид.
4Li + O 2 = 2Li 2 O
2Na + O 2 = Na 2 O 2
K + O 2 = KO 2
Получение оксида натрия:
10Na + 2NaNO 3 = 6Na 2 O + N 2
2Na + Na 2 O 2 = 2Na 2 O
2Na + 2NaOН = 2Na 2 O + Н 2
Взаимодействие с водой приводит к образованию щелочи и водорода.
2Na + 2H 2 O = 2NaOH + H 2
Взаимодействие с кислотами:
2Na + 2HCl = 2NaCl + H 2
8Na + 5H 2 SO 4(конц.) = 4Na 2 SO 4 + H 2 S + 4H 2 O
2Li + 3H 2 SO 4(конц.) = 2LiHSO 4 + SO 2 + 2H 2 O
8Na + 10HNO 3 = 8NaNO 3 + NH 4 NO 3 + 3H 2 O
При взаимодействии с аммиаком образуются амиды и водород:
2Li + 2NH 3 = 2LiNH 2 + H 2
Взаимодействие с органическими соединениями:
Н ─ C ≡ С ─ Н + 2Na → Na ─ C≡C ─ Na + H 2
2CH 3 Cl + 2Na → C 2 H 6 + 2NaCl
2C 6 H 5 OH + 2Na → 2C 6 H 5 ONa + H 2
2СН 3 ОН + 2Na → 2 CH 3 ONa + H 2
2СH 3 COOH + 2Na → 2CH 3 COOONa + H 2
Качественной реакцией на щелочные металлы является окрашивание пламени их катионами. Ион Li + окрашивает пламя в кармино-красный цвет, ион Na + – в желтый, К + – в фиолетовый
Соединения щелочных металлов
Оксиды.
Оксиды щелочных металлов типичные основные оксиды. Вступают в реакции с кислотными и амфотерными оксидами, кислотами, водой.
3Na 2 O + P 2 O 5 = 2Na 3 PO 4
Na 2 O + Al 2 O 3 = 2NaAlO 2
Na 2 O + 2HCl = 2NaCl + H 2 O
Na 2 O + 2H + = 2Na + + H 2 O
Na 2 O + H 2 O = 2NaOH
Пероксиды .
2Na 2 O 2 + CO 2 = 2Na 2 CO 3 + O 2
Na 2 O 2 + CO = Na 2 CO 3
Na 2 O 2 + SO 2 = Na 2 SO 4
2Na 2 O + O 2 = 2Na 2 O 2
Na 2 O + NO + NO 2 = 2NaNO 2
2Na 2 O 2 = 2Na 2 O + O 2
Na 2 O 2 + 2H 2 O (хол.) = 2NaOH + H 2 O 2
2Na 2 O 2 + 2H 2 O (гор.) = 4NaOH + O 2
Na 2 O 2 + 2HCl = 2NaCl + H 2 O 2
2Na 2 O 2 + 2H 2 SO 4 (разб. гор.) = 2Na 2 SO 4 + 2H 2 O + O 2
2Na 2 O 2 + S = Na 2 SO 3 + Na 2 O
5Na 2 O 2 + 8H 2 SO 4 + 2KMnO 4 = 5O 2 + 2MnSO 4 + 8H 2 O + 5Na 2 SO 4 + K 2 SO 4
Na 2 O 2 + 2H 2 SO 4 + 2NaI = I 2 + 2Na 2 SO 4 + 2H 2 O
Na 2 O 2 + 2H 2 SO 4 + 2FeSO 4 = Fe 2 (SO 4) 3 + Na 2 SO 4 + 2H 2 O
3Na 2 O 2 + 2Na 3 = 2Na 2 CrO 4 + 8NaOH + 2H 2 O
Основания (щелочи).
2NaOH (избыток) + CO 2 = Na 2 CO 3 + H 2 O
NaOH + CO 2 (избыток) = NaHCO 3
SO 2 + 2NaOH (избыток) = Na 2 SO 3 + H 2 O
SiO 2 + 2NaOH Na 2 SiO 3 + H 2 O
2NaOH + Al 2 O 3 2NaAlO 2 + H 2 O
2NaOH + Al 2 O 3 + 3H 2 O = 2Na
NaOH + Al(OH) 3 = Na
2NaOH + 2Al + 6Н 2 О = 2Na + 3Н 2
2KOH + 2NO 2 + O 2 = 2KNO 3 + H 2 O
KOH + KHCO 3 = K 2 CO 3 + H 2 O
2NaOH + Si + H 2 O = Na 2 SiO 3 + H 2
3KOH + P 4 + 3H 2 O = 3KH 2 PO 2 + PH 3
2KOH (холодный) + Cl 2 = KClO + KCl + H 2 O
6KOH (горячий) + 3Cl 2 = KClO 3 + 5KCl + 3H 2 O
6NaOH + 3S = 2Na 2 S + Na 2 SO 3 + 3H 2 O
2NaNO 3 2NaNO 2 + O 2
NaHCO 3 + HNO 3 = NaNO 3 + CO 2 + H 2 O
NaI → Na + + I –
на катоде: 2Н 2 О + 2e → H 2 + 2OH – 1
на аноде: 2I – – 2e → I 2 1
2Н 2 О
+ 2I –![]() H 2
+ 2OH –
+ I 2
H 2
+ 2OH –
+ I 2
2H 2 O
+ 2NaI![]() H 2
+ 2NaOH + I 2
H 2
+ 2NaOH + I 2
2NaCl![]() 2Na
+ Cl 2
2Na
+ Cl 2
на катоде на аноде
4KClO 3 KCl + 3KClO 4
2KClO 3![]() 2KCl + 3O 2
2KCl + 3O 2
Na 2 SO 3 + S = Na 2 S 2 O 3
2NaI + Br 2 = 2NaBr + I 2
2NaBr + Cl 2 = 2NaCl + Br 2
I A группа.
1. Над поверхностью налитого в колбу раствора едкого натра пропускали электрические разряды, при этом воздух в колбе окрашивался в бурый цвет, который исчезает через некоторое время. Полученный раствор осторожно выпарили и установили, что твердый остаток представляет собой смесь двух солей. При нагревании этой смеси выделяется газ и остается единственное вещество. Напишите уравнения описанных реакций.
2. Вещество, выделяющееся на катоде при электролизе расплава хлорида натрия, сожгли в кислороде. Полученный продукт поместили в газометр, наполненный углекислым газом. Образовавшееся вещество добавили в раствор хлорида аммония и раствор нагрели. Напишите уравнения описанных реакций.
3) Азотную кислоту нейтрализовали пищевой содой, нейтральный раствор осторожно выпарили и остаток прокалили. Образовавшееся вещество внесли в подкисленный серной кислотой раствор перманганата калия, при этом раствор обесцветился. Азотсодержащий продукт реакции поместили в раствор едкого натра и добавили цинковую пыль, при этом выделился газ с резким запахом. Напишите уравнения описанных реакций.
4) Вещество, полученное на аноде при электролизе раствора иодида натрия с инертными электродами, внесли в реакцию с калием. Продукт реакции нагрели с концентрированной серной кислотой, и выделившийся газ пропустили через горячий раствор хромата калия. Напишите уравнения описанных реакций
5) Вещество, полученное на катоде при электролизе расплава хлорида натрия, сожгли в кислороде. Поученный продукт последовательно обработали сернистым газом и раствором гидроксида бария. Напишите уравнения описанных реакций
6) Белый фосфор растворяется в растворе едкого кали с выделением газа с чесночным запахом, который самовоспламеняется на воздухе. Твердый продукт реакции горения прореагировал с едким натром в таком соотношении, что в образовавшемся веществе белого цвета содержится один атом водорода; при прокаливании последнего вещества образуется пирофосфат натрия. Напишите уравнения описанных реакций
7) Неизвестный металл сожгли в кислороде. Продукт реакции, взаимодействует с углекислым газом, образует два вещества: твердое, которое взаимодействует с раствором соляной кислоты с выделением углекислого газа, и газообразное простое вещество, поддерживающее горение. Напишите уравнения описанных реакций.
8) Через избыток раствора едкого кали пропустили бурый газ в присутствии большого избытка воздуха. В образовавшийся раствор добавили магниевую стружку и нагрели, выделившимся газом нейтрализовали азотную кислоту. Полученный раствор осторожно выпарили, твердый продукт реакции прокалили. Напишите уравнения описанных реакций.
9) При термическом разложении соли А в присутствии диоксида марганца образовались бинарная соль Б и газ, поддерживающий горение и входящий в состав воздуха; при нагревании этой соли без катализатора образуются соль Б и соль высшей кислородсодержащей кислоты. При взаимодействии соли А с соляной кислотой выделяется желто-зеленый газ (простое вещество) и образуется соль Б. Соль Б окрашивает пламя в фиолетовый цвет, при ее взаимодействии с раствором нитрата серебра выпадает осадок белого цвета. Напишите уравнения описанных реакций.
10) К нагретой концентрированной серной кислотой добавили медную стружку и выделившийся газ пропустили через раствор едкого натра (избыток). Продукт реакции выделили, растворили в воде и нагрели с серой, которая в результате проведения реакции растворилась. В полученный раствор добавили разбавленную серную кислоту. Напишите уравнения описанных реакций.
11) Поваренную соль обработали концентрированной серной кислотой. Полученную соль обработали гидроксидом натрия. Полученный продукт прокалили с избытком угля. Выделившийся при этом газ прореагировал в присутствии катализатора с хлором. Напишите уравнения описанных реакций.
12) Натрий прореагировал с водородом. Продукт реакции растворили в воде, при этом образовался газ, реагирующий с хлором, а полученный раствор при нагревании прореагировал с хлором с образованием смеси двух солей. Напишите уравнения описанных реакций.
13) Натрий сожгли в избытке кислорода, полученное кристаллическое вещество поместили в стеклянную трубку и пропустили через неё углекислый газ. Газ, выходящий из трубки, собрали и сожгли в его атмосфере фосфор. Полученное вещество нейтрализовали избытком раствора гидроксида натрия. Напишите уравнения описанных реакций.
14) К раствору, полученному в результате взаимодействия пероксида натрия с водой при нагревании, добавили раствор соляной кислоты до окончания реакции. Раствор образовавшейся соли подвергли электролизу с инертными электродами. Газ, образовавшийся в результате электролиза на аноде, пропустили через суспензию гидроксида кальция. Напишите уравнения описанных реакций.
15) Через раствор гидроксида натрия пропустили сернистый газ до образования средней соли. К полученному раствору прилили водный раствор перманганата калия. Образовавшийся осадок отделили и подействовали на него соляной кислотой. Выделившийся газ пропустили через холодный раствор гидроксида калия. Напишите уравнения описанных реакций.
16) Смесь оксида кремния (IV) и металлического магния прокалили. Полученное в результате реакции простое вещество обработали концентрированным раствором гидроксида натрия. Выделившийся газ пропустили над нагретым натрием. Образовавшееся вещество поместили в воду. Напишите уравнения описанных реакций.
17) Продукт взаимодействия лития с азотом обработали водой. Полученный газ пропустили через раствор серной кислоты до прекращения химических реакций. Полученный раствор обработали раствором хлорида бария. Раствор профильтровали, а фильтрат смешали с раствором нитрата натрия и нагрели. Напишите уравнения описанных реакций.
18) Натрий нагрели в атмосфере водорода. При добавлении к полученному веществу воды наблюдали выделение газа и образование прозрачного раствора. Через этот раствор пропустили бурый газ, который был получен в результате взаимодействия меди с концентрированным раствором азотной кислоты. Напишите уравнения описанных реакций.
19) Гидрокарбонат натрия прокалили. Полученную соль растворили в воде и смешали с раствором алюминия, в результате образовался осадок и выделился бесцветный газ. Осадок обработали избытком раствора азотной кислоты, а газ пропустили через раствор силиката калия. Напишите уравнения описанных реакций.
20) Натрий сплавили с серой. Образовавшееся соединение обработали соляной кислотой, выделившийся газ нацело прореагировал с оксидом серы (IV). Образовавшееся вещество обработали концентрированной азотной кислотой. Напишите уравнения описанных реакций.
21) Натрий сожгли в избытке кислорода. Образовавшееся вещество обработали водой. Полученную смесь прокипятили, после чего в горячий раствор добавили хлор. Напишите уравнения описанных реакций.
22) Калий нагрели в атмосфере азота. Полученное вещество обработали избытком соляной кислоты, после чего к образовавшейся смеси солей добавили суспензию гидроксида кальция и нагрели. Полученный газ пропустили рад раскаленным оксидом меди (II).Напишите уравнения описанных реакций.
23) Калий сожгли в атмосфере хлора, образовавшуюся соль обработали избытком водного раствора нитрата серебра. Выпавший осадок отфильтровали, фильтрат выпарили т осторожно нагрели. Образовавшуюся соль обработали водным раствором брома. Напишите уравнения описанных реакций.
24) Литий прореагировал с водородом. Продукт реакции растворили в воде, при этом образовался газ, реагирующий с бромом, а полученный раствор при нагревании прореагировал с хлором с образованием смеси двух солей. Напишите уравнения описанных реакций.
25) Натрий сожгли на воздухе. Образовавшееся при этом твердое вещество поглощает углекислый газ с выделением кислорода и соли. Последнюю соль растворили в соляной кислоте, а к полученному при этом раствору добавили раствор нитрата серебра. При этом выпал белый осадок. Напишите уравнения описанных реакций.
26) Кислород подвергли воздействию электроразряда в озонаторе. Полученный газ пропустили через водный раствор йодида калия, при этом выделился новый газ без цвета и запаха, поддерживающий горение и дыхание. В атмосфере последнего газа сожгли натрий, а полученное при этом твердое вещество прореагировало с углекислым газом. Напишите уравнения описанных реакций.
I A группа.
1.
N 2
+ O 2
![]() 2NO
2NO
2NO + O 2 = 2NO 2
2NO 2 + 2NaOH = NaNO 3 + NaNO 2 + H 2 O
2NaNO 3 2NaNO 2 + O 2
2.
2NaCl![]() 2Na + Cl 2
2Na + Cl 2
на катоде на аноде
2Na + O 2 = Na 2 O 2
Na 2 CO 3 + 2NH 4 Cl = 2NaCl + CO 2 + 2NH 3 + Н 2 О
3. NaHCO 3 + HNO 3 = NaNO 3 + CO 2 + H 2 O
2NaNO 3 2NaNO 2 + O 2
5NaNO 2 + 2KMnO 4 + 3H 2 SO 4 = 5NaNO 3 + 2MnSO 4 + K 2 SO 4 + 3H 2 O
NaNO 3 + 4Zn + 7NaOH + 6H 2 O = 4Na 2 + NH 3
4.
2H 2 O
+ 2NaI![]() H 2
+ 2NaOH + I 2
H 2
+ 2NaOH + I 2
2K + I 2 = 2KI
8KI + 5H 2 SO 4(конц.) = 4K 2 SO 4 + H 2 S + 4I 2 + 4H 2 O
3H 2 S + 2K 2 CrO 4 + 2H 2 O = 2Cr(OH) 3 ↓ + 3S↓ + 4KOH
5.
2NaCl![]() 2Na
+ Cl 2
2Na
+ Cl 2
на катоде на аноде
2Na + O 2 = Na 2 O 2
Na 2 O 2 + SO 2 = Na 2 SO 4
Na 2 SO 4 + Ba(OH) 2 = BaSO 4 ↓ + 2NaOH
6. P 4 + 3KOH + 3H 2 O = 3KH 2 PO 2 + PH 3
2PH 3 + 4O 2 = P 2 O 5 + 3H 2 O
P 2 O 5 + 4NaOH = 2Na 2 HPO 4 + H 2 O
2Na 2 HPO 4 Na 4 P 2 O 7 + H 2 O
7. 2Na + O 2 Na 2 O 2
2Na 2 O 2 + 2CO 2 = 2Na 2 CO 3 + O 2
C + O 2 = CO 2
8. 2KOH + 2NO 2 + O 2 = 2KNO 3 + H 2 O
KNO 3 + 4Mg + 6H 2 O = NH 3 + 4Mg(OH) 2 + KOH
NH 3 + HNO 3 = NH 4 NO 3
NH 4 NO 3 N 2 O + 2H 2 O (190 – 245°C)
2NH 4 NO 3 2NO + N 2 + 4H 2 O (250 – 300°C)
2NH 4 NO 3 2N 2 + О 2 + 4H 2 O (выше 300°C)
9. 2KClO 3 2KCl + 3O 2
4KClO 3 KCl + 3KClO 4
KClO 3 + 6HCl = KCl + 3Cl 2 + 3H 2 O
KCl + AgNO 3 = AgCl↓ + KNO 3
10. 2H 2 SO 4(конц.) + Cu = CuSO 4 + SO 2 + 2H 2 O
SO 2 + 2NaOH = Na 2 SO 3 + H 2 O
Na 2 SO 3 + S = Na 2 S 2 O 3
Na 2 S 2 O 3 + H 2 SO 4 = Na 2 SO 4 + S↓ + SO 2 + H 2 O
11. NaCl (тверд.) + H 2 SO 4(конц.) = NaHSO 4 + HCl
NaHSO 4 + NaOH = Na 2 SO 4 + H 2 O
Na 2 SO 4 + 4C Na 2 S + 4CO
CO
+ Cl 2
![]() COCl 2
COCl 2
12) 2Na + H 2 = 2NaH
NaH + H 2 O = NaOH + H 2
H 2 + Cl 2 = 2HCl
6NaOH + 3Cl 2 = NaClO 3 + 5NaCl + 3H 2 O
13) 2Na + O 2 = Na 2 O 2
2Na 2 O 2 + 2CO 2 = 2Na 2 CO 3 + O 2
4P + 5O 2 = 2P 2 O 5
P 2 O 5 + 6NaOH = 2Na 3 PO 4 + 3H 2 O
14) 2Na 2 O 2 + 2H 2 O = 4NaOH + O 2
NaOH + HCl = NaCl + H 2 O
2H 2 O
+ 2NaCl
![]() H 2
+ 2NaOH + Cl 2
H 2
+ 2NaOH + Cl 2
2Cl 2 + 2Ca(OH) 2 = CaCl 2 + Ca(ClO) 2 + 2H 2 O
15) 2NaOH + SO 2 = Na 2 SO 3 + H 2 O
3Na 2 SO 3 + 2KMnO 4 + H 2 O = 3Na 2 SO 4 + 2MnO 2 + 2KOH
MnO 2 + 4HCl = MnCl 2 + Cl 2 + 2H 2 O
2NaOH (холодный) + Cl 2 = NaCl + NaClO + H 2 O
16) SiO 2 + 2Mg = 2MgO + Si
2NaOH + Si + H 2 O = Na 2 SiO 3 + 2H 2
2Na + H 2 = 2NaH
NaH + H 2 O = NaOH + H 2
17) 6Li + N 2 = 2Li 3 N
Li 3 N + 3H 2 O = 3LiOH + NH 3
2NH 3 + H 2 SO 4 = (NH 4) 2 SO 4
(NH 4) 2 SO 4 + BaCl 2 = BaSO 4 + 2NH 4 Cl
18) 2Na + H 2 = 2NaH
NaH + H 2 O = NaOH + H 2
Cu + 4HNO 3(конц.) = Cu(NO 3) 2 + 2NO 2 + 2H 2 O
2NaOH + 2NO 2 = NaNO 3 + NaNO 2 + H 2 O
19) 2NaHCO 3 Na 2 CO 3 + CO 2 + H 2 O
3Na 2 CO 3 + 2AlBr 3 + 3H 2 O = 2Al(OH) 3 ↓ + 3CO 2 + 6NaBr
Al(OH) 3 + 3HNO 3 = Al(NO 3) 3 + 3H 2 O
К 2 SiO 3 + 2CO 2 + 2H 2 O = 2КHCO 3 + H 2 SiO 3 ↓
20) 2Na + S = Na 2 S
Na 2 S + 2HCl = 2NaCl + H 2 S
SO 2 + 2H 2 S = 3S + 2H 2 O
S + 6HNO 3 = H 2 SO 4 + 6NO 2 + 2H 2 O
21) 2Na + O 2 = Na 2 O 2
Na 2 O 2 + 2H 2 O = 2NaOH + H 2 O 2
2H 2 O 2 2H 2 O + O 2
6NaOH (гор.) + 3Cl 2 = NaClO 3 + 5NaCl + 3H 2 O
22) 6K + N 2 = 2K 3 N
K 3 N + 4HCl = 3KCl + NH 4 Cl
2NH 4 Cl + Ca(OH) 2 = CaCl 2 + 2NH 3 + 2H 2 O
2NH 3 + 3CuO = N 2 + 3Cu + 3H 2 O
23) 2K + Cl 2 = 2KCl
KCl + AgNO 3 = KNO 3 + AgCl↓
2KNO 3 2KNO 2 + O 2
KNO 2 + Br 2 + H 2 O = KNO 3 + 2HBr
24) 2Li + H 2 = 2LiH
LiH + H 2 O = LiOH + H 2
H 2 + Br 2 = 2HBr
6LiOH (гор.) + 3Cl 2 = LiClO 3 + 5LiCl + 3H 2 O
25) 2Na + O 2 = Na 2 O 2
2Na 2 O 2 + 2CO 2 = 2Na 2 CO 3 + O 2
Na 2 CO 3 + 2HCl = 2NaCl + CO 2 + H 2 O
NaCl + AgNO 3 = AgCl↓ + NaNO 3
26) 3O 2 ↔ 2O 3
O 3 + 2KI + H 2 O = I 2 + O 2 + 2KOH
2Na + O 2 = Na 2 O 2
2Na 2 O 2 + 2CO 2 = 2Na 2 CO 3 + O 2
Задания к итоговой аттестации по биологии за курс
средней (полной) школы
Вариант 1
На выполнение экзаменационной работы по биологии дается 1 час (60 минут). Работа состоит из 3 частей, включающих 37 заданий.
Часть 1 включает 30 задания (А1-А30). К каждому заданию дается 4 ответа, один из которых правильный.
Часть 2 содержит 5 задания (B1-B5) с выбором нескольких верных ответов. При выполнении этих заданий в таблицу ответа надо записать цифры, обозначающие элементы правильного ответа.
Внимательно прочитайте каждое задание и предлагаемые варианты ответа, если они имеются. Отвечайте только после того, как Вы поняли вопрос и проанализировали все варианты ответа.
Выполняйте задания в том порядке, в котором они даны. Если какое-то задание вызывает у Вас затруднение, пропустите его и постарайтесь выполнить те, в ответах на которые Вы уверены. К пропущенным заданиям можно будет вернуться, если у Вас останется время.
Критерии оценок
· Для получения отметки «3» достаточно выполнить верно любые 15 заданий из всей работы.
· Для получения отметки «4» необходимо выполнять задания из частей 1 и 2 . Причем часть 1 должна быть выполнена без ошибок. А в части 2 допускается выполнение правильно 1 задания.
· Оценка «5» ставится при выполнении заданий 1,2,3 без ошибок.
Желаем успеха!
Часть 1 варианта 1
При выполнении заданий (А1-А30) на листок ответов записывается № ответа. Ответ может быть только 1.
А1. Какой уровень организации живой природы представляет собой совокупность всех экосистем земного шара в их взаимосвязи?
2) экосистемный
3) популяционно-видовой
4) биогеоценотический
А2. Сходство строения и жизнедеятельности клеток организмов разных царств живой природы – одно из положений
1) теории эволюции
2) клеточной теории
3) учения об онтогенезе
4) законов наследственности
А3. Азотистое основание аденин, рибоза и три остатка фосфорной кислоты входят в состав
А4. Мономерами молекул каких органических веществ являются аминокислоты?
2) углеводов
4) липидов
А5. Изображённую на рисунке растительную клетку можно узнать по наличию в ней
2) плазматической мембраны
3) вакуолей
4) эндоплазматической сети
А6. Клетки организмов всех царств живой природы имеют
1) оболочку из клетчатки
3) комплекс Гольджи
4) плазматическую мембрану
А7. Определите, какой процесс в клетке изображён с помощью схемы.

1) темновая фаза фотосинтеза
2) биосинтез белка
3) реакции гликолиза
4) реакция окисления веществ
А8. Благодаря какому процессу в ходе митоза образуются дочерние клетки с набором хромосом, равным материнскому?
1) образования хроматид
2) спирализации хромосом
3) растворения ядерной оболочки
4) деления цитоплазмы
А9. Почему бактерии относят к организмам прокариотам?
1) состоят из одной клетки
2) имеют мелкие размеры
3) не имеют оформленного ядра
4) являются гетеротрофными
А10. Вирус СПИДа может функционировать в клетках
1) нервных
2) мышечных
3) эпителиальных
А11. Процесс образования диплоидной зиготы в результате слияния мужской и женской гаплоидных гамет называют
1) конъюгацией
2) опылением
3) оплодотворением
4) кроссинговером
А12. Как называется метод, сущность которого составляет скрещивание родительских форм, различающихся по ряду признаков, анализ их проявления в ряде поколений?
1) гибридологическим
2) цитогенетическим
А13. От гибридов первого поколения во втором поколении рождается 1/4 особей с рецессивными признаками, что свидетельствует о проявлении закона
1) сцепленного наследования
2) расщепления
3) независимого наследования
4) промежуточного наследования
А14. Употребление наркотиков оказывает вредное влияние на потомство, так как они вызывают
1) нарушение психики
2) нарушение работы печени
3) изменение работы почек
4) изменение генетического аппарата клетки
А15. Открытие центров многообразия и происхождения культурных растений послужило основой для создания
1) Главного ботанического сада
Часть 2 варианта 1
При выполнении заданий В1-3 на листок ответов запишите номера правильного ответа не более 3 цифр.
В1. Какие признаки характеризуют рефлекс, проявляющийся у школьников в ответ на звонок с урока? Запишите соответствующие цифры.
1) Каждый школьник реагирует индивидуально.
2) На него одинаково реагируют все школьники.
3) Передается по наследству.
4) Не передается по наследству.
5) Врожденный.
6) Приобретенный в течение жизни.
В2. Каково значение круговорота веществ в биосфере? Запишите соответствующие цифры.
1) Обеспечивает приток энергии извне.
2) Способствует образованию приспособленности организмов к среде.
3) Поддерживает биологические ритмы.
4) Обеспечивает многократное использование веществ.
5) В его основе лежат пищевые связи между организмами.
6) В его основе лежат территориальные связи между организмами.
В3. Чем мейоз отличается от митоза? Запишите соответствующие цифры.
1) Образуются четыре гаплоидные клетки.
2) Образуются две диплоидные клетки.
3) Происходит коньюгация и кроссинговер хромосом.
4) Происходит спирализация хромосом.
5) Делению клеток предшествует одна интерфаза.
6) Происходит два деления.
При выполнении заданий В4,5 установите соответствие между содержанием первого и второго столбцов. Впишите буквы выбранных ответов на листок ответов
Установите соответствие между признаками изменчивости и её видами.
ПРИЗНАКИ ИЗМЕНЧИВОСТИ
ИЗМЕНЧИВОСТЬ
обусловлена появлением новых сочетаний генов
мутационная
обусловлена изменением генов и хромосом
у потомков появляются новые признаки
комбинативная
у потомков сочетаются родительские признаки
у особей изменяется количество или структура ДНК
у особей не изменяется количество или структура ДНК
Установите соответствие между строением и функциями эндоплазматической сети и комплекса Гольджи: к каждой позиции, данной в первом столбце, подберите соответствующую позицию из второго столбца. Получившуюся последовательность букв перенесите в листок ответов.
СТРОЕНИЕ И ФУНКЦИИ
органоидов
ОРГАНОИДЫ
состоит из группы полостей с пузырьками на концах
эндоплазматическая сеть
состоит из системы связанных между собой канальцев
комплекс Гольджи
участвует в биосинтезе белка
участвует в образовании лизосом
участвует в образовании клеточной оболочки
осуществляет транспорт органических веществ в разные части клетки
Часть 3 варианта 1
Часть 3 содержит 2 задания С1, С2 где надо дать ответ из одного-двух предложений.
С 1. Назовите не менее 3-х особенностей наземных растений, которые позволили им первыми освоить сушу. Ответ обоснуйте.
С 2. Для борьбы с насекомыми-вредителями человек применяет химические вещества. Укажите не менее 3-х изменений жизни дубравы в случае, если в ней химическим способом будут уничтожены все растительноядные насекомые. Объясните, почему они произойдут.
Ответы к вопросам варианта 1
Часть 1
№ задания
Ответ
№ задания
Ответ
№ задания
Ответ
Часть 2 вариант 1
№ задания
Ответ
БААБАБ
БААББА
Ответ С1
Элементы ответа:
1) возникновение покровной ткани – эпидермиса с устьицами, способствующей защите от испарения;
2) появление слабо развитой проводящей системы, обеспечивающей транспорт веществ;
3) развитие механической ткани, выполняющей опорную функцию;
4) образование ризоидов, с помощью которых они закреплялись в почве.
Ответ С2
Элементы ответа:
1) численность насекомоопыляемых растений резко сократится, так как растительноядные насекомые являются опылителями растений;
2) резко сократится численность или исчезнут насекомоядные организмы (консументы II порядка) из-за нарушения цепей питания;
3) часть химических веществ, которыми уничтожали насекомых, попадет в почву, что приведет к нарушению жизнедеятельности растений, гибели почвенной флоры и фауны, все нарушения могут привести к гибели дубравы.
2017 Федеральная служба по надзору в сфере образования и науки
Российской Федерации
Проверочная работа включает в себя 16 заданий. На выполнение работы по биологии отводится 1 час 30 минут (90 минут).
Записывайте ответы на задания в отведённом для этого месте в работе. В случае записи неверного ответа зачеркните его и запишите рядом новый.
При выполнении работы разрешается использовать калькулятор.
При выполнении заданий Вы можете использовать черновик. Записи в черновике проверяться и оцениваться не будут.
Советуем выполнять задания в том порядке, в котором они даны. Для экономии времени пропускайте задание, которое не удаётся выполнить сразу, и переходите к следующему. Если после выполнения всей работы у Вас останется время, Вы сможете вернуться к пропущенным заданиям.
Баллы, полученные Вами за выполненные задания, суммируются. Постарайтесь выполнить как можно больше заданий и набрать наибольшее количество баллов.
Желаем успеха!
ВАРИАНТ 1
1. Выберите из приведённого перечня систематических таксонов три таксона, которые являются общими при описании изображённых организмов.
Перечень таксонов:
1) класс Двудольные
2) империя Неклеточные
3) надцарство Прокариоты
4) царство Растения
5) подцарство Многоклеточные
6) отдел Цветковые
ОТВЕТ
Все существующие на нашей планете растения объединяют в одно царство , которое называется Растения .
Растения делятся на два подцарства – высшие и низшие.
К низшим растениям относят водоросли.
А высшие растения делятся на Споровые и Семенные. К споровым относят отделы Мхи, Хвощи, Плауны и Папоротники. А к семенным – отдел Голосеменные и отдел Покрытосеменные (Цветковые).
Голосеменные растения не имеют травянистых форм, а так как мы видим, что данные нам растения точно не деревья и не кустарники, то они относятся к отделу Цветковые (такой же вывод можно было сделать и по наличию цветков и плодов).
Капуста огородная – растение семейства Крестоцветные (Капустные), горох посевной принадлежит к семейству Бобовые, а картофель из семейства Паслёновые. Растения этих семейств принадлежат к классу Двудольные .
Таким образом, правильными ответами являются пункты 1 , 4 ,6 .
Давайте, исключим остальные варианты ответов.
Эти растения не относят к империи Неклеточные, т.к. они имеют клеточное строение, т.е. состоят из клеток. Их не относят к надцарству Прокариоты, так как прокариоты – организмы, не имеющие ядра в клетке, а у растений ядро есть. Они не относятся к подцарству Многоклеточные, так как в систематике растений есть подцарства Высшие и Низшие, а подцарства Многоклеточны0е вообще нет.
2. Правило Аллена гласит, что среди родственных форм теплокровных животных,
ведущих сходный образ жизни, те, которые обитают в более холодном климате, имеют относительно меньшие выступающие части тела:
уши, ноги, хвосты и т.д.
1. Запишите в таблицу соответствующую последовательность цифр, которыми обозначены
фотографии.

2. Используя знания в области терморегуляции, объясните правило Аллена.
ОТВЕТ
Ответ на 1 вопрос: 312 Ответ на 2 вопрос: чем больше поверхность тела теплокровного животного, тем интенсивнее идёт отдача тепла. Этому способствуют большие уши.
Ответить на 1 вопрос совсем не трудно. Стоит учесть, что требуется расставить животных, начиная с самого северного, а по правилу Аллена у северных животных выступающие части тела меньше. Значит, мы должны расставить животных, начиная с того, которое имеет самые маленькие уши.
Уменьшение у животных выступающих частей тела приводит к уменьшению поверхности тела, а следовательно, к уменьшению теплоотдачи. Это помогает животным, обитающим в холодных условиях, экономить тепло. На этом должен основываться ответ на 2 вопрос.
1. Распределите организмы по их положению в пищевой цепи.
В каждую ячейку запишите
название одного из предложенных организмов.
Перечень организмов:
кузнечики, растения, змеи, лягушки, орёл.
Пищевая цепь
2. Правило гласит: «не более 10% энергии поступает от каждого предыдущего трофического уровня к последующему». Используя это правило, рассчитайте величину энергии (в кДж), которая переходит на уровень консументов II порядка при чистой годовой первичной продукции экосистемы 10 000 кДж.
ОТВЕТ
1. растения – кузнечики – лягушки – змеи – орёл
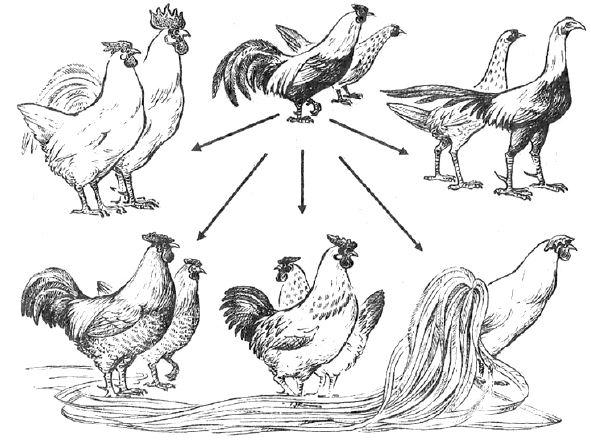
4. Изучите рисунок. Благодаря какому процессу образовалось такое многообразие изображённых организмов?
ОТВЕТ
Искусственный отбор,
ИЛИ мутационная изменчивость,
ИЛИ наследственная изменчивость
5. Изучите график, отражающий зависимость скорости реакции, катализируемой ферментом, от температуры тела собаки (по оси х отложена температура тела собаки (в °С), а по оси у – скорость химической реакции (в усл. ед.)).

Известно, что температура тела здоровой собаки находится в пределах 37,5–38,5 °С. Как изменится скорость химических реакций в организме собаки, если температура её тела будет выше нормальной?
ОТВЕТ
Скорость химических реакций будет снижаться (падать)
6. Заполните пустые ячейки таблицы, используя приведённый ниже список пропущенных элементов: для каждого пропуска, обозначенного буквой, выберите и запишите в таблицу номер нужного элемента.
Пропущенные элементы:
1) ДНК
2) анатомия
3) организменный
4) хлоропласт
5) молекулярно-генетический
6) цитология
ОТВЕТ
7. Холестерин играет важную роль в обмене веществ и работе нервной системы. Он поступает в организм из продуктов животного происхождения. В растительных продуктах его практически нет. Количество холестерина, поступающего в организм с пищей, не должно превышать 0,3–0,5 г в сутки.
1. Используя данные таблицы, рассчитайте количество холестерина в завтраке человека, который съел 100 г нежирного творога, 25 г «Голландского» сыра, 20 г сливочного масла и две сосиски.

2. Какую опасность для здоровья человека представляет избыток холестерина в организме человека?
ОТВЕТ
2. поражение кровеносных сосудов,
ИЛИ развитие атеросклероза,
ИЛИ ишемическая болезнь сердца
8. Сергей пришёл к врачу из-за плохого самочувствия. Врач дал ему направление на анализ, результаты которого показали, что количество лейкоцитов равно 2,5×108 при норме 4–9×109. Какой анализ предложил сдать врач и какой диагноз он поставил на основе полученных результатов? Выберите ответы из следующего списка и запишите в таблицу их номера.
Список ответов:
1) нарушение углеводного обмена
2) кислородная недостаточность
3) анализ крови
4) снижение иммунитета
5) анализ кала
ОТВЕТ 34
Запишите номер каждой из болезней в списке в соответствующую ячейку таблицы. В ячейках таблицы может быть
записано несколько номеров.
Список болезней человека:
1) ветряная оспа
2) синдром Дауна
3) инфаркт миокарда
4) дизентерия
5) малярия
ОТВЕТ
10. медицинской генетике широко используется генеалогический метод. Он основан на составлении родословной человека и изучении наследования того или иного признака. В подобных исследованиях используются определённые обозначения. Изучите фрагмент родословного древа одной семьи, у некоторых членов которой имеется глухонемота.
Фрагмент родословного древа семьи
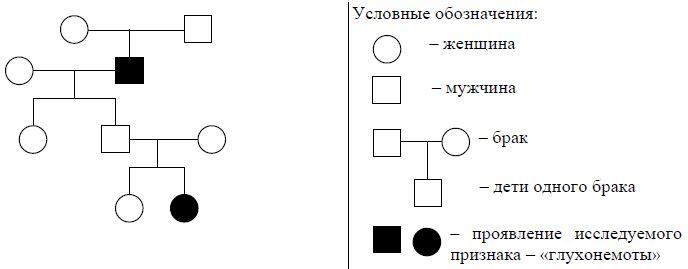
Используя предложенную схему, определите:
1) данный признак доминантный или рецессивный;
2) данный признак не сцеплен или сцеплен с половыми хромосомами.
ОТВЕТ
рецессивный признак
2. признак не сцеплен с полом
11. Света всегда хотела иметь такие же «ямочки» на щеках, как у её мамы (доминантный признак (А) не сцеплен с полом). Но «ямочки» у Светы отсутствовали, как у её отца. Определите генотипы членов семьи по признаку наличия или отсутствия «ямочек». Ответы занесите в таблицу.
ОТВЕТ
Мать – Аа; отец – аа; дочь – аа
12. В суде рассматривался иск об установлении отцовства ребёнка.
Был сделан анализ крови ребёнка и его матери. У ребёнка она оказалась II(А), а у матери – I(0). Проанализируйте
данные таблицы и ответьте на вопросы.

1. Мать ребёнка заявляла в суде, что отцом её сына является мужчина с IV(АВ) группой крови. Мог ли он быть отцом ребёнка?
2. Руководствуясь правилами переливания крови, решите, может ли ребёнок быть донором крови для своей матери.
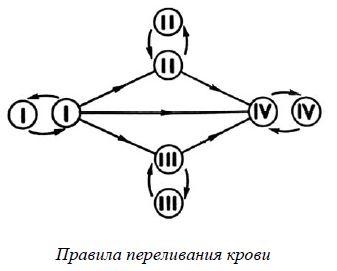
3. Используя данные таблицы «Группы крови по системе АВ0» объясните своё решение.

* Примечание.
Антиген - любое вещество, которое организм рассматривает как чужеродное или потенциально опасное и против которого обычно начинает вырабатывать собственные антитела.
Антитела - белки плазмы крови, образующиеся в ответ на введение в организм человека бактерий, вирусов, белковых токсинов и других антигенов.
ОТВЕТ
Ответ на 1 вопрос: да
Ответ на 2 вопрос: нет
Ответ на 3 вопрос: в результате одновременного нахождения в кровяном русле матери, при переливании, одноименных антигенов А ребёнка и антител α (матери) произойдёт склеивание эритроцитов, что может привести к смерти матери
13. В биохимической лаборатории изучался нуклеотидный состав фрагмента молекулы ДНК пшеницы.
Было установлено, что в пробе доля адениновых нуклеотидов составляет 10%.
Пользуясь правилом Чаргаффа, описывающим количественные соотношения между различными типами азотистых оснований в ДНК (Г + Т = А + Ц), рассчитайте в этой пробе процент нуклеотидов с цитозином.
ОТВЕТ 40%

1. Рассмотрите изображение двумембранного органоида эукариотической клетки. Как он называется?
2. Нарушение какого процесса произойдёт в клетке в случае повреждений (нарушений в работе) данных органоидов?
ОТВЕТ
1. митохондрия
2. энергетического обмена,
ИЛИ процесса дыхания,
ИЛИ биологического окисления
15. Генетический код - свойственный всем живым организмам способ
кодирования последовательности аминокислотных остатков в составе белков при помощи
последовательности нуклеотидов в составе нуклеиновой кислоты.
Изучите таблицу генетического кода, в которой продемонстрировано соответствие аминокислотных остатков составу кодонов. На примере аминокислоты серин (Сер), объясните следующее свойство генетического кода: код триплетен.
Таблица генетического кода

ОТВЕТ
1) каждой аминокислоте соответствует сочетание из трёх нуклеотидов
(триплетов, кодонов);
2) кодирование аминокислоты серин (Сер) может произойти с
помощью одного из следующих кодонов (триплетов): ТЦТ, ТЦЦ,
ТЦА, ТЦГ, АГТ, АГЦ
16. На рисунке изображён археоптерикс – вымершее животное, обитавшее 150–147 млн лет назад.

Используя фрагмент геохронологической таблицы, установите эру и период, в который обитал данный организм, а также его возможного предка уровня класса (надотряда) животных.

Эра: ______________________________________________________________
Период:___________________________________________________________
Возможный предок:_________________________________________________
ОТВЕТ
Эра: мезозойская эра;
Период: юрский период;
Возможный предок: древние пресмыкающиеся, ИЛИ
пресмыкающиеся, ИЛИ рептилии, ИЛИ динозавры
ВАРИАНТ 2

Перечень таксонов:
1) царство Растения
2) класс Папоротниковидные
3) класс Моховидные
4) отдел Папоротникообразные
5) отдел Голосеменные
6) подцарство Низшие растения
Запишите номера выбранных таксонов.
ОТВЕТ
На рисунках изображены растения (есть органы растений – листья, стебли); класс Папоротниковидные отдел Папоротникообразные – Папоротникообразные имеют корни и побеги (стебли с листьями), размножаются спорами.
Листья нарастают верхушкой (как побеги), молодые листья образуют на верхушке завитки - «улитки», которые защищают верхушечную меристему. Из-за этих особенностей, не свойственных листьям, их называют вайями. На корневище образуются придаточные корни. На 2 рисунке – водный папоротник.
Ответ: 142.
2. Закон лимитирующего фактора гласит, что наиболее важным для выживания вида является тот фактор, который больше отклоняется от оптимальных для него значений. Факторы, которые сдерживают развитие организмов из-за недостатка или их избытка по сравнению с потребностями, называют лимитирующими (ограничивающими).

На рисунках изображены различные природные экосистемы. Расположите эти экосистемы в той последовательности, в которой значение лимитирующего фактора (недостаток тепла) снижается.
Запишите в таблицу соответствующую последовательность цифр, которыми обозначены экосистемы.
2. Наглядной иллюстрацией закона лимитирующего фактора является бочка Либиха. Что на рисунке символизирует лимитирующий фактор?

ОТВЕТ
2.1: 231
2.2: короткая доска символизирует лимитирующий фактор; её длина определяет уровень, до которого бочку можно наполнить, причём длина других досок уже не имеет значения
2.1. На рисунках изображены природные зоны: 1 - степь; 2 - тундра; 3 - широколиственный лес.
По условию задания значение
лимитирующего фактора (недостаток тепла) снижается
, т.е. среднегодовая температура повышается: тундра→ широколиственный лес →степь
2.2. Существуют разные формулировки этого закона. Но суть закона минимума (или закона ограничивающего фактора) можно сформулировать так:
Жизнь организма зависит от множества факторов. Но, наиболее значимым в каждый момент времени является тот фактор, который наиболее уязвим.
Иными словами, если в организме какой-то из факторов существенно отклоняется от нормы, то именно этот фактор в данный момент времени является наиболее значимым, наиболее критическим для выживания организма.
Важно понимать, что для одного и того же организма в разное время такими критически важными (или по-другому лимитирующими) факторами могут совершенно разные факторы.
В этой полусломанной бочке – лимитирующим фактором является высота доски. Очевидно, что вода будет переливаться через самую маленькую доску в бочке. В этом случае нам уже будет не важной высота остальных досок – все равно бочку наполнить будет нельзя.
Наименьшая доска – это и есть тот самый фактор, который наиболее отклонился от нормального значения.
1. Распределите организмы по их положению в пищевой цепи. В каждую ячейку запишите название одного из предложенных организмов. Перечень организмов: ласка, листовой опад, крот, дождевой червь.
Пищевая цепь
2. «Правило 10%»: при переходе с одного трофического уровня на другой 90 % энергии рассеивается. Используя «Правило 10%», рассчитайте массу дождевых червей (в кг), необходимых для нормальной жизнедеятельности одной ласки массой 102 г, в цепи питания листовой опад → дождевые черви → крот → ласка
ОТВЕТ
1. листовой опад→дождевой червь→крот→ласка
Детритные пищевые цепи (цепи разложения) - пищевые цепи, которые начинаются с детрита – отмерших остатков растений, трупов и экскрементов животных. Гетеротрофные организмы, питающиеся непосредственно детритом, называются детритофагами. Далее следуют консументы (вторчные потребители)
Количество растительного вещества, служащего основой цепи питания, примерно в 10 раз больше, чем масса растительноядных животных, и каждый последующий пищевой уровень также имеет массу, в 10 раз меньшую. Это правило известно как правило Линдемана, или правило 10 процентов.
При расчете массы и энергии снизу вверх – убираем по одному нулю при переходе на каждый уровень, а если движемся сверху вниз – добавляем по одному нулю.
Собственно, цепь питания: листовой опад → дождевые черви → крот → ласка
Кротов 102 г *10 = 1020 г
Червей 1020 г * 10= 10200 г или 10 кг 200 г
4. Изучите рисунок. В результате какого процесса образовалось такое многообразие изображённых на рисунке живых организмов?

ОТВЕТ
искусственный отбор ИЛИ мутационная изменчивость ИЛИ наследственная изменчивость.
Многообразие пород голубей является результатов искусственного отбора - это отбор производимый человекам на основе мутационной (наследственной) изменчивости.
Человек вел отбор в определенном направлении: величине зоба, надклювье, хвост.
5. Изучите график, который отражает выживаемость вида в зависимости от температуры.

Определите, какое количество (в %) особей будет выживать в диапазоне температур от 15 до 25 °C.
ОТВЕТ 75-100%.
| Метод биологии | Описание метода | Пример |
| Наблюдение | ||
| Возможность не учитывать ряд | ||
| Центрифугирование, |
Пропущенные элементы:
1) абстрагирование
2) открытие новых видов
3) эволюционные процессы
4) использование специальных приборов
5) инструментальный
6) сбор фактов
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
ОТВЕТ
1. Жиры - необходимая часть рациона человека.
Сергею 12 лет (вес 36 кг). Зимой на каникулах он посещал г. Кисловодск. После длительной прогулки по Курортному парку он обедал в кафе. В заказ входили следующие блюда: сложный горячий бутерброд со свининой, салат овощной, мороженое с шоколадным наполнителем, вафельный рожок и «Кока-кола». Используя данные таблиц 1 и 2, определите количество жиров, поступивших с пищей во время обеда, и их отношение к суточной норме.
Суточные нормы питания и энергетическая потребность детей и подростков
| Возраст, лет | Энергетическая | Белки, г/кг | Жиры, г/кг | Углеводы, г |
| 16 и старше |
Таблица энергетической и пищевой ценности готовых блюд
| Блюда и напитки | Энергетическая | Белки (г) | Жиры (г) | Углеводы (г) |
| Сложный горячий бутерброд | ||||
| Сложный горячий бутерброд | ||||
| Сложный горячий бутерброд | ||||
| Омлет с ветчиной | ||||
| Салат овощной (свежие помидоры, | ||||
| Салат Цезарь (курица, салат, | ||||
| Картофель по-деревенски | ||||
| Маленькая порция картофеля | ||||
| Стандартная порция картофеля | ||||
| Мороженное с шоколадным | ||||
| Вафельный рожок | ||||
| «Кока-кола» | ||||
| Апельсиновый сок | ||||
| Чай без сахара | ||||
| Чай с сахаром (две чайные ложки) |
2. Жиры - необходимая часть рациона человека.
Почему врачи-диетологи для похудения советуют уменьшить в рационе количество жиров, а не полностью от них отказаться?
ОТВЕТ
1. Количество жиров в обеде = 33 + 0 + 11 + 4 + 0 = 48 г; отношение поступивших с пищей жиров к суточной норме = 48: 61,2 (суточная потребность в жирах - 36 кг x 1,7) 0,78 (или 78%)
2. Полностью исключать жиры из рациона нельзя, так как жиры являются компонентами структур клетки (мембран) и входят в состав гормонов, способствуют усвоению некоторых витаминов.
8. На приёме у терапевта пациент жалуется на повышенную возбудимость, учащённый пульс, пучеглазие, дрожание рук, потливость, снижение массы тела при хорошем аппетите, перепады настроения. Какой диагноз поставит врач? К какому специалисту отправит пациента для уточнения диагноза? Выберите ответы из следующего списка и запишите в таблицу их номера.
Список ответов:
1) бронзовая болезнь
2) базедова болезнь
3) нарушение белкового обмена
4) невролог
5) эндокринолог
ОТВЕТ
Базедова болезнь, иначе называемая болезнью Грейвса (медицинское название – диффузный токсический зоб) представляет собой заболевание, связанное с отклонением работы щитовидной железы (ее увеличение в размере и чрезмерная выработка гормонов).
Начинается Базедова болезнь для обычного человека практически незаметно. Ее первыми признаками могут быть: повышенная потливость, частое дрожание верхних конечностей, бессонница, перепады в настроении. Кожа больного с течением времени становится более смуглой, в районе его нижних конечностей можно заметить небольшие постоянные отеки.
Эндокринолог - врач этой специализации следит за состоянием эндокринной системы организма. Эндокринолог занимается диагностированием и лечением, а также предотвращением проблем гормональной регуляции в нашем организме.
9. Определите происхождение болезней, приведённых в списке. Запишите номер каждой из болезней в списке в соответствующую ячейку таблицы. В ячейках таблицы может быть записано несколько номеров.
Список болезней человека:
1) гепатит
2) туберкулёз
3) ангина
4) сколиоз
5) грипп
ОТВЕТ
10. Изучите фрагмент родословной.

Установите характер наследования признака, выделенного на схеме чёрным цветом.
1) Данный признак доминантный или рецессивный?
2) Данный признак сцеплен или не сцеплен с полом?
ОТВЕТ
1. Признак является доминантным аутосомным, т. к. проявляется в каждом поколении.
2. С одинаковой вероятностью встречается и у мужчин и у женщин - не сцеплен с Х-хромосомой.
11. У родителей карие глаза. Их дочь имеет голубые глаза. Определите генотипы членов семьи по признаку «карие/голубые глаза». Ответы занесите в таблицу.
ОТВЕТ мать - Аа, отец - Аа, ребёнок - аа.
12. У матери четвёртая (AB) группа крови, у отца - первая (00). Проанализируйте данные таблицы и ответьте на вопросы.
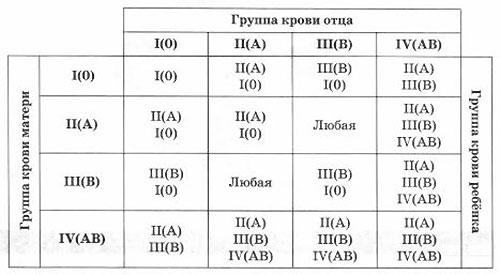
1. Кровь какой группы имеет их дочь?
2. Руководствуясь правилами переливания крови, решите, может ли отец быть донором крови для своей дочери.

3. Используя данные таблицы «Классификация крови по группам», объясните своё решение.
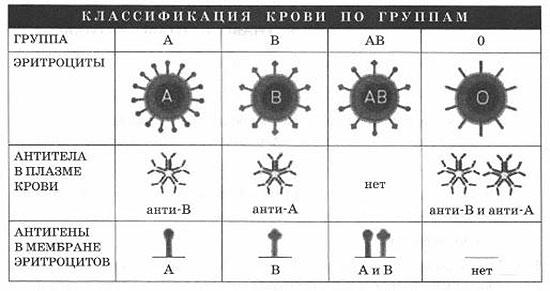
* Примечание.
Антиген - любое вещество, которое организм рассматривает как чужеродное или потенциально опасное и против которого обычно начинает вырабатывать собственные антитела.
Антитела - белки плазмы крови, образующиеся в ответ на введение в организм человека бактерий, вирусов, белковых токсинов и других антигенов.
ОТВЕТ
Элементы ответа:
12.1. Ответ: II (A) или III (B)
Воспользуемся таблицей. Находим столбец с группой крови отца I (0), ищем строку – IV (AB)группу крови у матери. На пересечении находим группу крови возможных детей –II (A), III (B)
12.2. Ответ: да.
Воспользуемся схемой “переливание крови”. МОЖЕТ, НО – при переливании больших количеств крови следует использовать только одногруппную кровь.
12.3. Ответ: человек с первой группой крови (отец) является «универсальным донором», → его кровь можно переливать в кровь любой группы.
13. При изучении нуклеотидного состава фрагмента молекулы ДНК речного рака было установлено, что в пробе доля нуклеотидов с гуанином составляет 18%. Пользуясь правилом Чаргаффа, описывающим количественные соотношения между различными типами азотистых оснований в ДНК (Г + T = A + Ц), рассчитайте в этой пробе процент нуклеотидов с тимином.
ОТВЕТ
По правилу комплементарности количество гуанина равно количеству цитозина; количество нуклеотидов с тимином равно количеству нуклеодидов с аденином.
18% цитозина = 18% гуанина по правилу комплементарности,
64% на тимин и аденин, а так как их равное количество, то
32% аденина = 32% тимина.
Процент нуклеотидов с тимином 100% – (18% Ц + 18% Г) = 64%:2=32
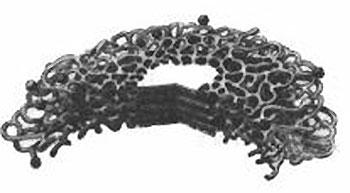
1. Рассмотрите изображение органоида. Как он называется?
2. Рассмотрите изображение органоида. Какие процессы обеспечивает изображённый органоид?
ОТВЕТ
1. На рисунке Аппарат Гольджи. Он представляет собой стопку дискообразных мембранных мешочков (цистерн), система трубочек и на концах пузырьки (образуются лизосомы)
2. Накопление и химическая модификация (процессинг) веществ, которые синтезируются в каналах ЭПС (эндоплазматической сети) в неактивной форме; транспорт модифицированных химических веществ; образование лизосом.
15. Генетический код - способ кодирования последовательности аминокислот в составе белков при помощи последовательности нуклеотидов в составе нуклеиновой кислоты у всех живых организмов. Изучите таблицу генетического кода, в которой продемонстрировано соответствие аминокислотных остатков составу кодонов. На примере аминокислоты метионин (MET) объясните такое свойство генетического кода, как однозначность (специфичность).
Генетический код
| Первое | Второе основание | Третье |
||||
| Фен | Сер | Тир | Цис | У(А)
|
||
| Лей | Про | Гис | Арг | У(А)
|
||
| Иле | Тре | Асн | Сер | У(А)
|
||
| Вал | Ала | Асп | Гли | У(А)
|
||
ОТВЕТ
Однозначность – один триплет не может кодировать более одной аминокислоты.
Аминокислота метионин (МЕТ) кодируется только одним триплетом. По иРНК АУГ; по ДНК ТАЦ
16. На рисунке изображены псилофиты - вымершие растения.
Используя фрагмент геохронологической таблицы, установите эру и период, в который появились данные организмы, а также возможного предка уровня отдела растений.
Геохронологическая таблица
| ЭРА, возраст | Период | Растительный мир |
| Мезозойская, 240 | Появляются и распространяются покрытосеменные; сокращаются папоротники и голосеменные |
|
| Триас | ||
| Палеозойская, 570 | Пермь | |
| Карбон | Расцвет древовидных папоротников, плаунов и хвощей (образовывали «каменноугольные леса»); появляются семенные папоротники; псилофиты исчезают |
|
| Девон | Развитие, а затем вымирание псилофитов; возникновение основных групп споровых растений - плауновидных, хвощевидных, папоротниковидных; появление первых примитивных голосеменных; возникновение грибов |
|
| Силур | Господство водорослей; выход растений на сушу - появление риниофитов (псилофитов) |
|
| Ордовик | Расцвет водорослей |
|
| Кембрий | Дивергентная эволюция водорослей; появление многоклеточных форм |
|
| Протерозойская, 2600 | Широко распространены синезелёные и зелёные одноклеточные водоросли, бактерии; появляются красные водоросли |
ОТВЕТ
Воспользуемся таблицей, в третьей колонке найдем псилофиты; определяем по второй и первой колонкам эру и период, когда обитали псилофиты
Ответ: Эра: палеозойская
Период: Силур
Предками псилофитов являются многоклеточные зеленые водоросли.
ВАРИАНТ 3
1. Выберите из приведённого перечня систематических таксонов три таксона, которые являются общими при описании изображённых организмов.
Перечень таксонов:
1) царство Животные
2) класс Ресничные черви
3) класс Сосальщики
4) тип Плоские черви
5) тип Кольчатые черви
6) тип Нематоды
Запишите номера выбранных таксонов.
2. Правило Бергмана гласит, что среди родственных форм теплокровных животных, ведущих сходный образ жизни, те, которые обитают в областях с преобладающими низкими температурами, имеют, как правило, более крупные размеры тела по сравнению с обитателями более теплых зон и областей.
Рассмотрите фотографии, на которых изображены представители трёх близкородственных видов млекопитающих. Расположите этих животных в той последовательности, в которой их природные ареалы расположены по поверхности Земли с севера на юг.
1. Запишите в таблицу соответствующую последовательность цифр, которыми обозначены фотографии.
2. Используя знания в области терморегуляции, объясните правило Бергмана.
3.1. Расставьте в правильной последовательности организмы в соответствии с их местом в цепи питания заливного луга. В каждую ячейку запишите название одного из предложенных организмов.
Перечень организмов: дождевой червь, сокол, уж, землеройка, перегной.
Пищевая цепь
_________ → _________ → _________ → _________ → _________
3.2. Правило гласит: «не более 10 % энергии поступает от каждого предыдущего трофического уровня к последующему». Используя это правило, рассчитайте величину энергии, которая переходит на уровень консументов I порядка при чистой годовой первичной продукции экосистемы 200 кДж.
4. Изучите рисунок. Какой тип взаимоотношений иллюстрирует рисунок?
5. Проанализируйте график скорости размножения молочнокислых бактерий и ответьте на следующий вопрос: как изменится скорость размножения бактерий в пределах температуры от 24°С до 34°С?
6. Заполните пустые ячейки таблицы, используя приведённый ниже список пропущенных элементов : для каждого пропуска, обозначенного буквой, выберите и запишите в таблицу номер нужного элемента.
Пропущенные элементы:
1) биосинтез белка;
2) экология;
3) организменный;
4) пищевые цепи;
5) проведение нервного импульса;
6) цитология;
7.1. Ниже приведена таблица, отражающая содержание витаминов в некоторых плодовых соках (по данным Популярной медицинской энциклопедии). В нижней строке показана средняя суточная потребность в этих веществах (в мг). Пользуясь таблицей, ответьте на вопросы, при расчетах используйте максимальный показатель данных (например, 2-8 – используем 8).
Достаточно ли выпить 250 мл цитрусового микса, состоящего из апельсинового (100мл), лимонного (50 мл) и мандаринового сока (100мл), чтобы удовлетворить суточную потребность в витамине А?
7.2. Аня, 14 лет, вес 55 кг, вегетарианка. Почему Юлии необходимо обращать особое внимание на содержание белков в заказываемых блюдах?
8. При прохождении обследования у Анастасии (19 лет) был установлен уровень сахара 12 ммоль/л при норме 3,2-5,5 ммоль/л. Какой анализ сдавала Анастасия? Какой диагноз предположительно поставит врач на основе полученных результатов? Выберите ответ из списка и запишите в таблицу номер ответа.
1) анализ крови
2) анализ мочи
3) нарушение углеводного обмена
4) воспалительный процесс
5) аллергическая реакция
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
9. Определите, какие органы из приведённых в списке, получили свое развитие из каких зародышевых листков. Запишите номер органа в списке в соответствующую ячейку таблицы. В ячейках таблицы может быть записано несколько номеров.
Список органов человека:
1) ногти
2) бицепс
3) лёгкие
4) бедренная кость
5) головной мозг
10.1. По изображенной на рисунке родословной установите характер проявления признака (доминантный, рецессивный), обозначенного черным цветом. Определите генотип родителей и детей в первом поколении.
10.2. Изучите схему скрещивания кур.
Установите характер наследования чёрной окраски оперения у кур.
Данный признак наследуется по принципу полного или неполного доминирования?
11. У человека глаукома наследуется как аутосомно-рецессивный признак (а). Жена страдает глаукомой, а муж гетерозиготен по данному признаку. Определите генотипы родителей и вероятность рождения здорового ребёнка. Ответы занесите в таблицу.
| Вероятность ррождения |
||
12. Перед судебно-медицинской экспертизой поставлена задача выяснить: является ли мальчик, имеющийся в семье супругов Р 1 , родным или приемным. Исследование крови мужа, жены и ребенка показало: жена -IV группа крови, муж - I, ребенок - I группа крови. Проанализируйте данные и ответьте на вопросы.
1. Какое заключение должен дать эксперт?
2. Какая группа крови может быть у ребенка данных родителей?
3. Объясните решение эксперта.
13. Какое число аминокислот в белке, если его кодирующий ген состоит из 600 нуклеотидов? В ответ запишите ТОЛЬКО соответствующее число.
14.1. Рассмотрите рисунок части растения, какая структура изображена на рисунке. Как она называется?
14.2. Какую функцию выполняет данная структура?
15. Генетический код - способ кодирования последовательности аминокислот в составе белков при помощи последовательности нуклеотидов в составе нуклеиновой кислоты у всех живых организмов.
Изучите таблицу генетического кода, в которой продемонстрировано соответствие аминокислотных остатков составу кодонов.
На примере аминокислоты глутамин (ГЛН) поясните, какими триплетами может быть закодирована данная аминокислота на информационной РНК (иРНК), укажите все возможные комбинации триплетов. Поясните такое свойство генетического кода, как вырожденность, или избыточность.
16. На рисунке изображен белемнит – вымершее животное, обитавшее 440-410 млн лет назад.
Используя фрагмент геохронологической таблицы, установите эру и период, в который обитал данный организм, а также «близких родственников» данного животного в современной фауне (ответ – на уровне рода)
Геохронологическая таблица
ОТВЕТЫ:
213; Теплопродукция (выделение тепла клетками организма) пропорциональна объему тела. Теплоотдача (потеря тепла, его передача в окружающую среду) пропорциональна площади поверхности тела. С увеличением объема площадь поверхности растет относительно медленно, что позволяет увеличить «отношение теплопродукция / теплоотдача» и таким образом компенсировать потери тепла с поверхности тела в холодном климате.
1. перегной→дождевой червь→землеройка→уж→сокол; 2. 20
Повышается
А - 2, Б - 4, В - 3, Г - 5, Д - 6, Е - 1.
1. Нет; 2. Белок - это основной строительный материал для тела, а при вегетарианстве может не хватать белков в пище.
Эктодерма - 15, энтодерма - 3, мезодерма - 24.
Признак рецессивный, т.к. наблюдается “проскок” через поколение.
Генотипы родителей: мать - аа, отец - АА или Аа;
Генотипы детей: сын и дочь гетерозиготы - Аа
2. Неполное доминирование
Мать - aa, отец - Aa, вероятность - 50.
1. Воспользуемся таблицей. Находим столбец с группой крови отца II (A), ищем строку – 2 группу крови у матери. На пересечении находим группу крови возможных детей – два ответа II (A) и I (0) .
3. При переливании больших количеств крови следует использовать только одногруппную кровь. С кровью донора в кровь детям поступает большое количество агглютининов, которые могут вызвать гемолиз собственных эритроцитов реципиента.В результате склеивания эритроцитов антигена А (отца) и антител плазмы α (у детей), дети могут погибнуть.
1. Побег, ИЛИ стебель с листьями и почками;
2. На рисунке изображены хромосомы. Плотные продолговатые или нитевидные образования, которые можно рассмотреть только при делении клетки. Содержат ДНК – носитель наследственной информации, которая передается от поколения к поколению.
Функция хромосом – хранение наследственной информации, ИЛИ регуляция всех процессов жизнедеятельности.
1) кодирование аминокислоты глутамин (ГЛН) может произойти с помощью одного из следующих триплетов: ЦАА, ЦАГ;
2) вырожденность, или избыточность,- одну аминокислоту может кодировать несколько триплетов.
В силурийском периоде (440-410 миллионов лет назад) в морях впервые появляются крупные животные, до этого их размеры не превышали нескольких сантиметров. Крупнейшими морскими животными силура были головоногие моллюски с наружной раковиной размером в телеграфный столб, ее длина иногда достигала 4-5 метров.
Белемниты очень похожи на современных кальмаров и подобно им были хорошими пловцами. На голове у них располагались большие глаза и десять рук с присосками - две длинные и восемь более коротких. Как и некоторые кальмары, белемниты имели раковину внутри тела - эти раковины часто встречаются в мезозойских отложениях и называются «чертовыми пальцами». По форме и размерам они действительно похожи на остроконечные пальцы. Большинство ученых считают, что раковина была известковой, как раковины других моллюсков, но некоторые думают, что у живых белемнитов раковина была мягкой, хрящевой и окаменела после смерти. Аммониты и белемниты полностью вымерли в конце мезозойской эры.
ЭРА: Палеозой
Период: Силурский
Возможный «родственник»: кальмар
