Е.Н.ФРЕНКЕЛЬ
Самоучитель по химии
Пособие для тех, кто не знает, но хочет узнать и понять химию
Часть I. Элементы общей химии
(первый уровень сложности)
Я, Френкель Евгения Николаевна, заслуженный работник высшей школы РФ, выпускница химического факультета МГУ 1972 г., педагогический стаж 34 года. Кроме того, я мать троих детей и бабушка четырех внуков, старший из которых школьник.
Меня волнует проблема школьных учебников. Главная беда многих из них – тяжелый язык, который требует дополнительного «перевода» на понятный школьнику язык изложения учебного материала. Ко мне часто обращаются ученики средней школы с такой просьбой: «Переведите текст учебника, чтобы понятно было». Поэтому я написала «Самоучитель по химии», в котором многие сложные вопросы изложены вполне доступно и в то же время научно. На основе этого «Самоучителя», который был написан в 1991 г., я разработала программу и содержание подготовительных курсов. На них обучались сотни школьников. Многие из них начинали с нуля и за 40 занятий понимали предмет настолько, что сдавали экзамены на «4» и «5». Поэтому в нашем городе мои пособия-самоучители расходятся как горячие пирожки.
Может, и другим пригодятся мои наработки?
Статья подготовлена при поддержке учебного центра «МакарОФФ». Учебный центр предлагает Вам пройти курсы маникюра в Москве недорого . Профессиональная школа маникюра проводит обучение по маникюру, педикюру, наращиванию и дизайну ногтей, а также курсы мастеров-универсалов ногтевого сервиса, наращивание ресниц, микроблейдинг, шугаринг и эпиляция воском. Центр выдаёт дипломы после обучения и гарантированное трудоустройство. Подробная информация обо всех программах обучения, цены, расписание, акции и скидки, контакты на сайте: www.akademiyauspeha.ru .
Предисловие
Уважаемые читатели! Предлагаемый вашему вниманию «Самоучитель по химии» – не обычный учебник. В нем не просто излагаются какие-то факты или описываются свойства веществ. «Самоучитель» объясняет и учит даже в том случае, если вы, к сожалению, не знаете и не понимаете химии, а к учителю обратиться за разъяснениями не можете или стесняетесь. В виде рукописи эта книга используется школьниками с 1991 г., и не было ни одного ученика, который бы провалился на экзамене по химии и в школе, и в вузах. Причем многие из них совсем не знали химии.
«Самоучитель» рассчитан на самостоятельную работу ученика. Главное – отвечать по ходу чтения на те вопросы, которые встречаются в тексте. Если вы не смогли ответить на вопрос, то читайте внимательнее текст еще раз – все ответы имеются рядом. Желательно также выполнять все упражнения, которые встречаются по ходу объяснения нового материала. В этом помогут многочисленные обучающие алгоритмы, которые практически не встречаются в других учебниках. С их помощью вы научитесь:
Составлять химические формулы по валентности;
Составлять уравнения химических реакций, расставлять в них коэффициенты, в том числе в уравнениях окислительно-восстановительных процессов;
Составлять электронные формулы (в том числе краткие электронные формулы) атомов и определять свойства соответствующих химических элементов;
Предсказывать свойства некоторых соединений и определять, возможен данный процесс или нет.
В пособии два уровня сложности. Самоучитель первого уровня сложности состоит из трех частей.
I часть. Элементы общей химии (публикуемая ).
II часть. Элементы неорганической химии.
III часть. Элементы органической химии.
Книг второго уровня сложности тоже три.
Теоретические основы общей химии.
Теоретические основы неорганической химии.
Теоретические основы органической химии.
|
Глава 1. Основные понятия химии.
Глава 2. Важнейшие классы неорганических соединений.
Глава 3. Элементарные сведения о строении атома. Периодический закон Д.И.Менделеева.
Глава 4. Понятие о химической связи. Глава 5. Растворы. Глава 6. Электролитическая диссоциация.
Глава 7. Понятие об окислительно-восстановительных реакциях. Глава 8. Расчеты по химическим формулам и уравнениям.
Приложение. |
Глава 1. Основные понятия химии
Что такое химия? Где мы встречаемся с химическими явлениями?
Химия – везде. Сама жизнь – это бесчисленное множество разнообразных химических реакций, благодаря которым мы дышим, видим голубое небо, ощущаем изумительный запах цветов.
Что изучает химия?
Химия изучает вещества, а также химические процессы, в которых участвуют эти вещества.
Что такое вещество?
Вещество – это то, из чего состоит окружающий нас мир и мы сами.
Что такое химический процесс (явление)?
К химическим явлениям относятся процессы, в результате которых изменяется состав или строение молекул, образующих данное вещество*. Изменились молекулы – изменилось вещество (оно стало другим), изменились его свойства. Например, свежее молоко стало кислым, зеленые листья стали желтыми, сырое мясо при обжаривании изменило запах.
Все эти изменения – следствие сложных и многообразных химических процессов. Однако признаки простых химических реакций, в результате которых изменяется состав и строение молекул, такие же: изменение цвета, вкуса или запаха, выделение газа, света или тепла, появление осадка.
Что же такое молекулы, изменение которых влечет за собой столь разнообразные проявления?
Молекулы – это мельчайшие частицы вещества, отражающие его качественный и количественный состав и его химические свойства.
Изучая состав и строение одной молекулы, можно предсказать многие свойства данного вещества в целом. Такие исследования – одна из главных задач химии.
Как устроены молекулы? Из чего они состоят?
Молекулы состоят из атомов. Атомы в молекуле соединены при помощи химических связей. Каждый атом обозначается при помощи символа (химического знака). Например, Н – атом водорода, О – атом кислорода.
Число атомов в молекуле обозначают при помощи индекса – цифры внизу справа после символа.
Например:
Примеры молекул:
О 2 – это молекула вещества кислорода, состоящая из двух атомов кислорода;
Н 2 О – это молекула вещества воды, состоящая из двух атомов водорода и одного атома кислорода.
Если атомы не связаны химической связью, то их число обозначают при помощи коэффициента – цифры перед символом:

Аналогично изображают число молекул:
2Н 2 – две молекулы водорода;
3Н 2 О – три молекулы воды.
Почему атомы водорода и кислорода имеют разные названия и разные символы? Потому что это атомы разных химических элементов.
Химический элемент – это вид атомов с одинаковым зарядом ядер.
Что такое ядро атома? Почему заряд ядра является признаком принадлежности атома к данному химическому элементу? Чтобы ответить на эти вопросы, следует уточнить: изменяются ли атомы в химических реакциях, из чего состоит атом?
Нейтральный атом не имеет заряда, хотя и состоит из положительно заряженного ядра и отрицательно заряженных электронов:
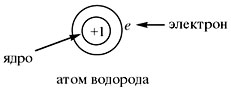
В ходе химических реакций число электронов любого атома может изменяться, а вот заряд ядра атома не меняется . Поэтому заряд ядра атома – своеобразный «паспорт» химического элемента. Все атомы с зарядом ядра +1 принадлежат химическому элементу под названием водород. Атомы с зарядом ядра +8 относятся к химическому элементу кислороду.
Каждому химическому элементу присвоен химический символ (знак), порядковый номер в таблице Д.И.Менделеева (порядковый номер равен заряду ядра атома), определенное название, а для некоторых химических элементов – особое прочтение символа в химической формуле (табл. 1).
Таблица 1
Символы (знаки) химических элементов
| № п/п | № в таблице Д.И.Менделеева | Символ | Прочтение в формуле | Название |
| 1 | 1 | H | аш | Водород |
| 2 | 6 | C | це | Углерод |
| 3 | 7 | N | эн | Азот |
| 4 | 8 | O | о | Кислород |
| 5 | 9 | F | фтор | Фтор |
| 6 | 11 | Na | натрий | Натрий |
| 7 | 12 | Mg | магний | Магний |
| 8 | 13 | Al | алюминий | Алюминий |
| 9 | 14 | Si | силициум | Кремний |
| 10 | 15 | P | пэ | Фосфор |
| 11 | 16 | S | эс | Сера |
| 12 | 17 | Cl | хлор | Хлор |
| 13 | 19 | K | калий | Калий |
| 14 | 20 | Ca | кальций | Кальций |
| 15 | 23 | V | ванадий | Ванадий |
| 16 | 24 | Cr | хром | Хром |
| 17 | 25 | Mn | марганец | Марганец |
| 18 | 26 | Fe | феррум | Железо |
| 19 | 29 | Cu | купрум | Медь |
| 20 | 30 | Zn | цинк | Цинк |
| 21 | 35 | Br | бром | Бром |
| 22 | 47 | Ag | аргентум | Серебро |
| 23 | 50 | Sn | станнум | Олово |
| 24 | 53 | I | йод | Йод |
| 25 | 56 | Ba | барий | Барий |
| 26 | 79 | Au | аурум | Золото |
| 27 | 80 | Hg | гидраргирум | Ртуть |
| 28 | 82 | Pb | плюмбум | Cвинец |
Вещества бывают простые и сложные . Если молекула состоит из атомов одного химического элемента, это простое вещество. Простые вещества – Са, Сl 2 , О 3 , S 8 и т. д.
Молекулы сложных веществ состоят из атомов разных химических элементов. Сложные вещества – H 2 O, NO, H 3 PO 4, C 12 H 22 O 11 и т. д.
Задание 1.1. Укажите число атомов в молекулах сложных веществ H 2 O, NO, H 3 PO 4 , C 12 H 22 O 11 , назовите эти атомы.
Возникает вопрос: почему для воды всегда записывается формула Н 2 О, а не НО или НО 2 ? Опыт доказывает, что состав воды, полученной любым способом или взятой из любого источника, всегда соответствует формуле Н 2 О (речь идет о чистой воде).
Дело в том, что атомы в молекуле воды и в молекуле любого другого вещества соединены при помощи химических связей. Химическая связь соединяет как минимум два атома. Поэтому, если молекула состоит из двух атомов и один из них образует три химические связи, то другой также образует три химические связи.
Число химических связей , образуемых атомом, называют его валентностью .
Если обозначить каждую химическую связь черточкой, то для молекулы из двух атомов АБ получим АБ, где тремя черточками показаны три связи, образуемые элементами А и Б между собой.
В данной молекуле атомы А и Б трехвалентны.
Известно, что атом кислорода двухвалентен, атом водорода одновалентен.
В о п р о с. Сколько атомов водорода может присоединиться к одному атому кислорода?
О т в е т. Два атома. Состав воды описывают формулой Н–О–Н, или Н 2 О.
П о м н и т е! В устойчивой молекуле не может быть «свободных», «лишних» валентностей. Поэтому для двухэлементной молекулы число химических связей (валентностей) атомов одного элемента равно общему числу химических связей атомов другого элемента.
Валентность атомов некоторых химических элементов постоянна (табл. 2).
Таблица 2
Значение постоянных валентностей некоторых элементов
Для других атомов валентность** можно определить (вычислить) из химической формулы вещества. При этом нужно учитывать изложенное выше правило о химической связи. Например, определим валентность x марганца Mn по формуле вещества MnO 2:
Общее число химических связей, образуемых
одним и другим элементом (Mn и О), одинаково:
x
· 1 = 4; II · 2 = 4. Отсюда х
= 4, т.е. в этой
химической формуле марганец четырехвалентен.
П р а к т и ч е с к и е в ы в о д ы
1. Если один из атомов в молекуле одновалентен, то валентность второго атома равна числу атомов первого элемента (см. на индекс!):
2. Если число атомов в молекуле одинаково, то валентность первого атома равна валентности второго атома:
3. Если у одного из атомов индекс отсутствует, то его валентность равна произведению валентности второго атома на его индекс:
![]()
4. В остальных случаях ставьте валентности «крест-накрест», т.е. валентность одного элемента равна индексу другого элемента:
Задание 1.2. Определите валентности элементов в соединениях:
CO 2 , CO, Mn 2 O 7 , Cl 2 O, P 2 O 3 , AlP, Na 2 S, NH 3 , Mg 3 N 2 .
П о д с к а з к а. Сначала укажите валентность атомов, у которых она постоянная. Аналогично определяется валентность атомных групп ОН, РО 4 , SО 4 и др.
Задание 1.3. Определите валентности атомных групп (в формулах подчеркнуты):
H 3 PO 4 , Ca(OH ) 2 , Ca 3 (PO 4) 2 , H 2 SO 4 , CuSO 4 .
(Обратите внимание! Одинаковые группы атомов имеют одинаковые валентности во всех соединениях.)
Зная валентности атома или группы атомов, можно составить формулу соединения. Для этого пользуются следующими правилами.
Если валентности атомов одинаковы, то и число атомов одинаково, т.е. индексы не ставим:
Если валентности кратны (обе делятся на одно и то же число), то число атомов элемента с меньшей валентностью определяем делением:
В остальных случаях индексы определяют «крест-накрест»:
Задание 1.4. Составьте химические формулы соединений:

Вещества, состав которых отражают химические формулы, могут участвовать в химических процессах (реакциях). Графическая запись, соответствующая данной химической реакции, называется уравнением реакции . Например, при сгорании (взаимодействии с кислородом) угля происходит химическая реакция:
С + O 2 = CO 2 .
Запись показывает, что один атом углерода С, соединяясь с одной молекулой кислорода O 2 , образует одну молекулу углекислого газа СО 2 . Число атомов каждого химического элемента до и после реакции должно быть одинаково . Это правило – следствие закона сохранения массы вещества. Закон сохранения массы: масса исходных веществ равна массе продуктов реакции.
Закон был открыт в XVIII в. М.В.Ломоносовым и, независимо от него, А.Л.Лавуазье.
Выполняя этот закон, необходимо в уравнениях химических реакций расставлять коэффициенты так, чтобы число атомов каждого химического элемента не изменялось в результате реакции. Например, при разложении бертолетовой соли KClO 3 получается соль KСl и кислород О 2:
KClO 3 KСl + О 2 .
Число атомов калия и хлора одинаково, а кислорода – разное. Уравняем их:

Теперь изменилось число атомов калия и хлора до реакции. Уравняем их:
![]()
Наконец, между правой и левой частями уравнения можно поставить знак равенства:
2KClO 3 = 2KСl + 3О 2 .
Полученная запись показывает, что при разложении сложного вещества KClO 3 получаются два новых вещества – сложное KСl и простое – кислород O 2 . Числа перед формулами веществ в уравнениях химических реакций называют коэффициентами .
При подборе коэффициентов необязательно считать отдельные атомы. Если в ходе реакции не изменился состав некоторых атомных групп, то можно учитывать число этих групп, считая их единым целым. Составим уравнение реакции веществ CaCl 2 и Na 3 PO 4:
CaCl 2 + Na 3 PO 4 ……………… .
П о с л е д о в а т е л ь н о с т ь д е й с т в и й
1) Определим валентность исходных атомов и группы PO 4:
![]()
2) Напишем правую часть уравнения (пока без индексов, формулы веществ в скобках надо уточнить):
3) Составим химические формулы полученных веществ по валентностям составных частей:
![]()
4) Обратим внимание на состав самого сложного соединения Ca 3 (PO 4) 2 и уравняем число атомов кальция (их три) и число групп РО 4 (их две):

5) Число атомов натрия и хлора до реакции теперь стало равным шести. Поставим соответствующий коэффициент в правую часть схемы перед формулой NaCl:
3CaCl 2 + 2Na 3 PO 4 = Ca 3 (PO 4) 2 + 6NaCl.
Пользуясь такой последовательностью, можно уравнять схемы многих химических реакций (за исключением более сложных окислительно-восстановительных реакций, см. главу 7).
Типы химических реакций. Химические реакции бывают разных типов. Основными являются четыре типа – соединение, разложение, замещение и обмен.
1. Реакции соединения – из двух и более веществ образуется одно вещество:
Например:
Са + Сl 2 = CaCl 2 .
2. Реакции разложения – из одного вещества получаются два вещества или более:
Например:
Ca(HCO 3) 2 CaCO 3 + CO 2 + H 2 O.
3. Реакции замещения – реагируют простое и сложное вещества, образуются также простое и сложное вещества, причем простое вещество замещает часть атомов сложного вещества:
А + ВХ АХ + В.
Например:
Fe + CuSO 4 = Cu + FeSO 4 .
4. Реакции обмена – здесь реагируют два сложных вещества и получаются два сложных вещества. В ходе реакции сложные вещества обмениваются своими составными частями:
Упражнения к главе 1
1. Выучите табл. 1. Проверьте себя, напишите химические символы: серы, цинка, олова, магния, марганца, калия, кальция, свинца, железа и фтора.
2. Напишите символы химических элементов, которые в формулах произносятся как: «аш», «о», «купрум», «эс», «пэ», «гидраргирум», «станнум», «плюмбум», «эн», «феррум», «це», «аргентум». Назовите эти элементы.
3. Укажите число атомов каждого химического элемента в формулах соединений:
Al 2 S 3 , СаS, МnО 2 , NH 3 , Mg 3 P 2 , SO 3 .
4. Определите, какие из веществ – простые, а какие – сложные:
Na 2 O, Na, O 2 , CaCl 2 , Cl 2 .
Прочитайте формулы этих веществ.
5. Выучите табл. 2. Составьте химические формулы веществ по известной валентности элементов и атомных групп:
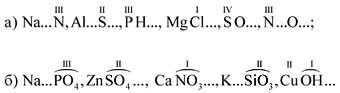
6. Определите валентность химических элементов в соединениях:
N 2 O, Fe 2 O 3 , PbO 2 , N 2 O 5, HBr, SiH 4 , H 2 S, MnO, Al 2 S 3 .
7. Расставьте коэффициенты и укажите типы химических реакций:
а) Mg + O 2 MgO;
б) Al + CuCl 2 AlCl 3 + Cu;
в) NaNO 3 NaNO 2 + O 2 ;
г) AgNO 3 + BaCl 2 AgCl + Ba(NO 3) 2 ;
д) Al + HCl AlCl 3 + H 2 ;
е) KOH + H 3 PO 4 K 3 PO 4 + H 2 O;
ж) CH 4 C 2 H 2 + H 2 .
* Существуют вещества, построенные не из молекул. Но об этих веществах речь пойдет позже (см. главу 4).
** Строго говоря, по нижеизложенным правилам определяют не валентность, а степень окисления (см. главу 7). Однако во многих соединениях числовые значения этих понятий совпадают, поэтому по формуле вещества можно определять и валентность.
Печатается с продолжением
Все книги можно скачать бесплатно и без регистрации.
NEW.
В.Н. Верховский, Я.Л. Гольдфарб, Л.М. Сморгонский. Органическая химия. Учебник для 10 класса. 1946 год. 156 стр. djvu. 19.2 Мб.
Этот учебник написан практиками и рассчитан на то, что дети будут понимать химию, а не вызубривать различные правила-скороговорки.
Объем изложенного материала значительно превышает таковой для учебника Цветкова. Очень рекомендую книгу, особенно учителям.
Сопоставление данной книги с современными учебниками четко показывает тенденции современных учебников:
учебники пишутся все более абстрактными и скупыми на материал и все более оторванными от практики.
Скачать.
NEW.
Никольский А.Б., Суворов А.В. Химия. 2001 год. 512 стр. djvu. 4.1 Мб.
В учебнике нового типа, рассчитанном прежде всего на формирование химического мышления студентов, системно и точно и в то же время ясно и доступно изложен огромный объем современных общехимических знаний.
На современном уровне рассмотрено учение о химическом процессе с акцентом на механизм реакции. Прослежена взаимосвязь между электронным строением и химическим поведением веществ. Логичность и популярность изложения материала, оригинальность контрольных вопросов, доступность иллюстраций способствуют усвоению химических знаний и развитию научного мышления.
Предназначен студентам вузов, учащимся средних специальных учебных заведений, будет полезен преподавателям вузов и учителям школ. Полезно посмотреть и школьникам, неЕГЭотикам, хотя бы первые главы.
Скачать.
Алексинский В.Н. Занимательные опыты по химии. 2-е испр. изд. 1995 год. 95 стр. djvu. 1.9 Мб.
Книга для учитилей.
В книге рассмотрены опыты, которые можно использовать не только на внеклассных мероприятиях, но и при подготовке к урокам. Опыты, обладая элементом развлекательности, способствуют развитию у учащихся умения наблюдать и объяснять химические явления. Пособие окажет помощь учителям в воспитании у учащихся интереса к изучению химии, в выработке более глубокого и сознательного усвоения ими теоретического материала.
Скачать.
Т.М. Варламова, А.И. Кракова. ОБЩАЯ И НЕОРГАНИЧЕСКАЯ ХИМИЯ: БАЗОВЫЙ КУРС. 263 стр. djvu. 2.2 Мб.
В данном пособии изложены основные вопросы общей и неорганической химии, многие из которых вызывают трудности у учащихся и абитуриентов. Подробно рассмотрены типовые задачи по всем разделам школьного курса химии и предложены задания для самостоятельного решения.
Пособие предназначено слушателям подготовительных отделений при высших учебных заведениях, а также лицам, готовящимся для поступления в вузы самостоятельно, учащимся старших классов средних школ, лицеев, гимназий и колледжей.
Скачать.
Габриелян О.С., Маскаев Ф.Н., Теренин В.И. Химия 10 класс. Учебник.2002 год. 304 стр. djvu. 3.9 Мб.
Книга для учитилей.
Учебник продолжает и развивает курс химии, изложенный в учебниках "Химия-8" и "Химия-9" автора О.С.Габриеляна. Учебный материал по органической химии излагается с учетом того, что первоначальные сведения об органических веществах учащиеся получили в 9 классе. Учебник соответствует обязательному минимуму содержания образования. Материал учебника распределен по двум уровням – базисному и углубленному и дается в связи с экологией, медициной, биологией. В курсе приводятся сведения о жизненно важных веществах: витаминах, ферментах, гормонах, лекарствах. Широко представлен химический эксперимент, в том числе новые практические работы, в ходе которых рассматриваются свойства витаминов, ферментов, лекарственных препаратов.
Скачать.
П.А. Гуревич, М.А. Кубешов. Органическая химия. Полезные сведения для школьников и учителей - история, теория, задачи и решения. 2004 год. 350 стр. djvu. 4.6 Мб.
Скачать.
Егоров А.С. ред. Репетитор по химии. 2003 год. 770 стр. PDF. 16.3 Мб.
Пособие содержит подробное изложение основ общей, неорганической и органической химии, а также типовые задачи с решениями и большое число заданий разной степени сложности для самостоятельной работы (в том числе элективные тесты).
Рекомендуется учащимся школ, гимназий и лицеев, абитуриентам химических и медико-биологических вузов.
Скачать.
Кузьменко Н.Е., Еремин В.В., Попков В.А. Начала химии. Современный курс для поступающих в вузы. В 2-х томах. 7-е изд. перераб. доп. 2002 год. 384+384 стр. djvu. в одном архиве 16.9 Мб.
Книга представляет собой попытку современного, всеобъемлющего и систематического изложения основ химии, которые необходимо знать в первую очередь поступающим в вузы. Ее содержание основано на тщательном анализе программ вступительных экзаменов по химии большинства вузов (химических, медицинских, биологических и т.д.), а также конкретных экзаменационных заданий.
Пособие предназначено для школьников, абитуриентов и учителей. В пособии изложены основы современной химии, которые надо понимать каждому выпускнику средней школы и совершенно обязательно знать каждому, кто видит себя студентом - химиком, медиком или биологом XXI века. В новом издании отражены последние достижения химии и приведены новые задачи вступительных экзаменов.
Скачать.
Н.Е. Кузьменко и др. Начала химии. Современный курс для поступающих в вузы. 2001 год. 360 стр. djvu. 16.3 Мб.
Скачать.
Кузьменко и др. Химия. Для школьнико старших классов и поступающих в вузы. Пособие представляет собой учебник и справочник по химии. 525 стр. Размер 4.7 Мб. djvu.
Скачать.
Кузьменко, Еремин, Попков. Краткий курс химии. Для поступающих в ВУЗы. 2002 год. 410 стр. PDF. Размер 12.4 Мб.
Пособие предназначено для школьников, абитуриентов и учителей. В пособии в краткой, но информативной и ясной форме изложены современные основы химии. Это - основы, которые надо понимать каждому выпускнику средней школы и совершенно обязательно знать каждому, кто видит себя студентом-химиком, медиком или биологом XXI века.
В тех частях: 1. Теоретическая химия, 2. Неорганическая химя. 3. Органическая химия.
Скачать
Т.Н. Литвинова, Е.Д. Мельникова, М.В. Соловьёва, Л.Т. Ажипа, Н.К. Выскубова. Химия в задачах для поступающих в вузы. 2009 год. 832 стр. PDF. 4.7 Мб.
Сборник содержит более 2500 задач, охватывающих основные темы школьного курса химии. Среди них представлены качественные и расчетные типовые задачи с решениями и задачи разного уровня сложности для самостоятельного решения. Ко всем задачам даны ответы, а к наиболее трудным - подробные решения.
По каждой теме приведен теоретический материал, преимущественно в виде таблиц, - основные понятия, законы химии, формулы, классификации, свойства, способы получения неорганических и органических веществ.
Пособие поможет при подготовке к выпускным экзаменам в средней школе, сдаче ЕГЭ и вступительным экзаменам в вуз. Книга адресована школьникам старших классов, абитуриентам и преподавателям.
Скачать.
Некрашевич И. Химия. 8 - 11 классы. 2008 год. 304 стр. PDF. 1.7 Мб.
Химия кажется вам сложным и непонятным предметом? Вы не знаете, как решать химические задачи, составлять уравнения реакций, строить формулы?
Репетитор по химии, который вы держите в руках, поможет решить эти проблемы.
Скачать.
Г.К. Прохорова. Качественный химический анализ. Практикум для школьников. 2002 год. 33 стр. PDF. в общем архиве 424 Кб.
Практикум предназначен для учащихся 9 классов школ с углубленным
изучением химии и школы юных химиков для ознакомления их с основами аналитической химии.
Подготовлен на Химфаке МГУ.
Скачать.
Рудзитис Г.Е., Фельдман Ф.Г. Химия. 7-11 класс. В 2-х книгах. 1985 год. djvu. две книги в одном архиве. 12.3 Мб.
Книга 1. 204 стр. Учебное пособие для 7-11 классов вечерней (сменной) средней общеобразовательной школы. Учебник соответствует действующим школьным программам и обязательному минимуму химического образования. Он имеет классическую структуру школьного учебника по химии и включает весь необходимый теоретический и практический материал для изучения курса неорганической химии.
Книга 1. 306 стр. Учебное пособие для 7-11 классов вечерней (сменной) средней общеобразовательной школы. Учебник соответствует действующим школьным программам и обязательному минимуму химического образования. Он имеет классическую структуру школьного учебника по химии и включает весь необходимый теоретический и практический материал для изучения курса неорганической органической химии. Во второй книге органическая химия занимает половину его объема.
Материал дифференцирован по уровням сложности.
Многочисленные таблицы, схемы и рисунки способствуют усвоению и повторению теоретического и практического материала. Доступность и наглядность изложения основных понятий, определений и законов химии позволяют рекомендовать этот учебник не только для школьного обучения, но и для самообразования.
При изучении химии с нуля лучше пользоваться этим учебником, а не современными, так как он лучше и понятней. Это не мое мнение, а химика-профессионала.
Скачать.
Семенов. Химия: пособие для поступающих в вузы. 1989 год. 225 стр. djvu. 3.7 Мб.
В отличие от существующих в данном пособии сделан упор на углубленное повторение основных понятий и законов химии, «узловых» вопросов, от понимания которых зависит осмысление изучаемого в школе фактического материала. На небольшом числе примеров показаны главные закономерности поведения химических систем, общие приемы подхода к их рассмотрению, то, как свойства вещества определяют его применение. Приводимые вопросы и упражнения выбраны из тех, которые предлагались на вступительных экзаменах в химические вузы или использовались автором на Подготовительном отделении ЛГУ. Как правило, для ответа не нужны громоздкие расчет и - надо лишь хорошо усвоить основные законы химии.
Предназначено прежде всего для абитуриентов, самостоятельно готовящихся к экзамену в вуз, но будет полезно также слушателям подготовительных отделений и курсов.
Скачать.
Стахеев. Вся химия в 50 таблицах. Приведены все основные понятия ШКОЛЬНОЙ хими. Представляет собой этакую шпаргалку - напоминалку. 60 стр. Размер 1.2 Мб. djvu.
Скачать.
Хомченко Г.П. Пособие по химии для поступающих в вузы. 2002 год. 480 стр. PDF. Размер 11.6 Мб.
В пособии освещены все вопросы приемных экзаменов по химии. Для лучшего усвоения курса химии приведены некоторые дополнительные сведения. В конце каждой главы даются типовые задачи с решениями и задачи для самостоятельной работы.
Книга предназначена поступающим в вузы. Она также может быть рекомендована преподавателям химии при подготовке учащихся к сдаче выпускных экзаменов за курс средней школы. Мне пособие понравилось.
Скачать
Черникова Л.П. Шпаргалки по химии. 2003 год. 144 стр. PDF. 2.4 Мб.
Материал разбит на три темы: Основные понятия хими, Общая химия, Органическая химия. Нормальное пособие. Не понял зачем такое название.
Всем известно, что школьный курс является той основой, которая дает самые необходимые знания о мире, в котором мы живем. Это действительно так и такой предмет как химия прекрасное тому подтверждение, так как, по сути, абсолютно все, что нас окружает и есть химия — химические элементы, их соединения, процессы взаимодействия и т.д. Поэтому неудивительно, что в школьный курс входит много тем по химии .
Важность изучения химии
Изучая предмет химии, школьник не только познает мир и определенные законы его существования, но и развивает память, логическое и абстрактное мышление, аналитические способности и интеллектуальные возможности в целом. ЕГЭ по химии, который является предметом по выбору, есть ни что иное как закономерное подведение итогов учебно-образовательной деятельности.
Кроме того, успешная сдача ЕГЭ по химии после окончания школы облегчит получение высшего образования, ведь его результаты высшими учебными заведениями засчитываются как вступительные экзамены. Поэтому нужно относиться к этому экзамену как к важному этапу в вашем будущем. Благодаря полученным знаниям будет проще потом осваивать другие сложные предметы в университете.
Что представляет собой подготовка к ЕГЭ по химии
Конечно, залогом успешного изучения и усвоения материала является постоянная работа — это касается абсолютно всех предметов. Однако такой специфический предмет как химия, зачастую требует особого подхода и применения дополнительных методов обучения. Например, таковыми являются самостоятельная работа или систематические занятия с репетитором. Но что делать, когда возможности для дополнительных занятий с преподавателем нет, а некоторые разобрать по учебнику практически не реально, впрочем, как и систематизировать все полученные знания, когда это необходимо для подготовки к ЕГЭ по химии?
Сегодня существует прекрасная возможность для дополнительного образования, расширения, углубления знаний и закрепления пройденных материалов — химия онлайн бесплатно. Такие уроки основаны на многолетнем педагогическо-психологическом опыте. Всемирная сеть в этом случае становится надежным другом и помощником современной молодежи, предлагая изучение различных тем по химии, включая различные методы подачи материала — видеоуроки с пояснениями, примерами опытов, решением практических задач и многое другое, систематизированные оптимальным образом электронные конспекты и таблицы.
Эта наука столь сложна, сколь и интересна. Однако уроки химии онлайн позволяют наиболее эффективно усвоить даже самую сложную тему, а при необходимости — проконсультироваться с квалифицированным преподавателем, в том числе и по вопросам, касающимся ЕГЭ по химии. Все это делает обучение легким и понятным, каждый может избежать сложных вопросов, разобраться в темах, которые пропустил ранее.
Итого
Занимаясь химией онлайн и бесплатно , вы в доступной для усвоения форме перенимаете многолетний опыт и получаете багаж систематизированных знаний. Каждый может выбрать для себя различные режимы и варианты обучения. Выпускники могут повторять пройденный в школе материал и восполнять имеющиеся пробелы в знаниях, выполняя задания различной сложности и изучая темы по химии по той системе, на которой и основан ЕГЭ. Конечно, готовых ответов никто не предоставит, тем более что каждый год список вопросов и заданий меняется. Однако структура в основном остается прежней, позволяя разработчикам совершенствовать эффективность оценки, а учащимся — наиболее полно раскрывать свой потенциал. Возможно, это поможет и школам показывать лучшую успеваемость своих учеников.
Кроме того, уроки химии онлайн — это удобно, а также может пригодиться как практикующим преподавателям для перенятия опыта, так и родителям, для того чтобы быть в курсе того, как сегодня строится процесс обучения их детей. Занятия химией онлайн помогут освежить знания будущим абитуриентам, желающим получить еще одно образование. Поэтому трудно поспорить с тем, что благодаря возможностям Интернета учиться становится проще абсолютно всем.
Химия считается одним из самых сложных и трудных предметов. Причем сложности возникают в освоении этого предмета и у школьников, и у студентов. Почему? Школьники ожидают от урока фокусов, интересных опытов и демонстраций. Но уже после первых занятий разочаровываются: лабораторных работ с реактивами совсем не много, в основном приходится изучать новую терминологию, делать объемные домашние задания. Химический язык совершенно не похож на повседневный, поэтому нужно ускоренными темпами изучать термины и названия. Кроме того, нужно уметь логически мыслить и применять математические знания.
Можно ли выучить химию самостоятельно?
Ничего невозможного нет. Несмотря на сложность науки, химию можно выучить с нуля. В ряде случаев, когда тема особенно сложная или требует дополнительных знаний, можно воспользоваться услугами онлайн репетитора. Самый удобный способ обучения – с помощью репетиторов по химии по скайпу . Дистанционное обучение позволяет подробно изучить отдельную тему или уточнить сложные моменты. По скайпу можно в любое время связаться с квалифицированным преподавателем.
Для того чтобы процесс изучения был эффективным, нужно несколько факторов:
- Мотивация . В любом деле необходима цель, к которой стремятся. Не важно, для чего изучается химия – для поступления в мединститут или биологический факультет, просто для саморазвития. Главное, поставить цель и определить способ ее достижения. Мотивация будет основным движущим фактором, который заставит продолжать самообучение.
- Важность деталей . За короткое время выучить большой объем информации просто невозможно. Чтобы выучить химию эффективно и уметь правильно использовать знания, нужно уделять внимание деталям: формулам, решать большое количество примеров, задач. Для качественного усвоения материала требуется систематизация информации: самостоятельно изучают новую тему, в дополнение решают задачи и примеры, учат формулы и т.д.
- Проверка знаний . Для закрепления пройденного материала рекомендуется периодически делать проверочные работы. Умение понимать и логически анализировать позволяет усваивать знания лучше, чем «зубрежка». Преподаватели рекомендуют периодически делать себе зачеты и контрольные работы. Не лишним будут повторения пройденного материала. Самостоятельно выучить химию помогают решебники и самоучители.
- Практика и еще раз практика… Не достаточно хорошо владеть теоретическими знаниями, нужно их уметь применять на практике, во время решения задач. Практические занятия помогают выявить слабые места в знаниях и закрепить пройденный материал. Кроме того, развиваются аналитические способности и логическое построение цепочки решения. Во время решения примеров и задач вы делаете выводы и происходит систематизация полученных знаний. Когда задачи становятся абсолютно понятными, можно приступать к изучению следующей темы.
- Учите сами . Не уверены в полноценном освоении химии? Попробуйте обучить этому предмету кого-нибудь. Во время объяснения материала выявляются слабые места в знаниях, выстраивается системность. Важно не торопиться, уделяя внимание деталям и практическим моментам.
Выучить химию самостоятельно с нулевого уровня можно, если есть сильная мотивация и время. Если же материал сложный, разобраться в премудростях темы помогут профессиональные репетиторы. Будет ли это очное консультирование или с помощью скайпа – зависит только от вас. Не обязательно брать полный курс у репетитора, в ряде случаев можно взять урок по отдельной теме.
Глава 1.
Общие химические и экологические закономерности.
С чего начинается химия?
Cложный ли это вопрос? На него каждый ответит по-своему.
В середней школе учащиеся изучают химию в течение ряда лет. Многие довольно хорошо сдают выпускной экзамен по химии. Однако…
Беседы с абитуриентами и затем и студентами первых курсов говорят о том, что остаточные знания по химии после средней школы незначительные. Одни путаются в различных определениях и химических формулах, а другие вообще не могут воспроизвести даже основные понятия и законы химии, не говоря уже о понятиях и законах экологии.
У них химия так и не начиналась.
Химия, по-видимому, начинается с глубокого освоения ее основ, и прежде всего, основных понятий и законов.
1.1. Основные химические понятия.
В таблице Д.И.Менделеева рядом с символом элемента стоят цифры. Одна цифра обозначает порядковый номер элемента, а вторая атомную массу. Порядковый номер имеет свой физический смысл. О нем мы будем вести разговор позже, здесь остановимся на атомной массе и выделим в каких единицах она измеряется.
Следует сразу оговориться, что атомная масса элемента, приведенная в таблице, величина относительная. За единицу относительной величины атомной массы принята 1/12 часть массы атома углерода, изотопа с массовым числом 12, и назвали ее атомной единицей массы /а.е.м./. Следовательно, 1 а.е.м. равна 1/12 части массы изотопа углерода 12 С. И она равна 1,667*10 –27 кг. /Абсолютная масса атома углерода равна 1,99*10 –26 кг./
Атомная масса , приведенная в таблице, является массой атома, выраженной в атомных единицах массы. Величина безразмерная. Конкретно для каждого элемента атомная масса показывает, во сколько раз масса данного атома больше или меньше 1/12 части массы атома углерода.
Аналогичное можно сказать и о молекулярной массе.
Молекулярная масса – это масса молекулы, выраженная в атомных единицах массы. Величина тоже относительная. Молекулярная масса конкретного вещества равна сумме масс атомов всех элементов, входящих в состав молекулы.
Важным понятием химии является понятие «моль». Моль – такое количество вещества, которое содержит 6,02*10 23 структурных единиц /атомов, молекул, ионов, электронов и т.д./. Моль атомов, моль молекул, моль ионов и т.д.
Масса одного моля данного вещества называется его молярной /или мольной/ массой. Она измеряется в г/моль или кг/моль и обозначается буквой «М». Например, молярная масса серной кислоты М Н 2 SO4 =98г/моль.
Следующее понятие «Эквивалент». Эквивалентом /Э/ называют такое весовое количество вещества, которое взаимодействует с одним молем атомов водорода или замещают такое его количество в химических реакциях. Следовательно, эквивалент водорода Э Н равен единице. /Э Н =1/. Эквивалент кислорода Э О равен восьми /Э О =8/.
Различают химический эквивалент элемента и химический эквивалент сложного вещества.
Эквивалент элемента – величина переменная. Она зависит от атомной массы /А/ и валентности /В/, которую элемент имеет в конкретном соединении. Э=А/В. Например, определим эквивалент серы в оксидах SO 2 и SO 3 . В SO 2 Э S =32/4=8, а в SO 3 Э S =32/6=5,33.
Молярную массу эквивалента, выраженную в граммах, называют эквивалентной массой. Следовательно, эквивалентная масса водорода МЭ Н =1г/моль, эквивалентная масса кислорода МЭ О =8г/моль.
Химический эквивалент сложного вещества /кислоты, гидроксида, соли, оксида/– такое количество соответствующего вещества, которое взаимодействует с одним молем атомов водорода, т.е. с одним эквивалентом водорода или замещает такое количество водорода или любого другого вещества в химических реакциях.
Эквивалент кислоты /Э К / равен частному от деления молекулярной массы кислоты на число атомов водорода, участвующих в реакции. Для кислоты H 2 SO 4 , когда оба атома водорода вступают в реакцию H 2 SO 4 +2NaOH=Na 2 SO+2H 2 O эквивалент будет равен Э Н 2 SO4 = М Н 2 SO 4 /n Н =98/2=49
Эквивалент гидроксида /Э гидр. / определяется как частное от деления молекулярной массы гидроксида на число гидроксогрупп, вступающих в реакцию. Например, эквивалент NaOH будет равен: Э NaOH =М NaOH /n ОН =40/1=40.
Эквивалент соли /Э соли / можно рассчитать, поделив ее молекулярную массу на произведение числа атомов металла, вступающих в реакцию, и их валентность. Так, эквивалент соли Al 2 (SO 4) 3 будет равен Э Al 2 (SO 4) 3 =М Al 2 (SO 4) 3 /6=342/2,3=342/6=57.
Эквивалент оксида /Э ок / можно определить, как сумму эквивалентов соответствующих элемента и кислорода. Например, эквивалент СО 2 будет равен сумме эквивалентов углерода и кислорода: Э СО 2 =Э С +Э О =3+8=7.
Для газообразных веществ удобно пользоваться эквивалентными объемами /Э V /. Так как при нормальных условиях моль газа занимает объем 22,4л, то исходя из этой величины, легко определить эквивалентный объем любого газа. Рассмотрим водород. Мольная масса водорода 2г занимает объем 22,4л, тогда его эквивалентная масса 1г занимает объем 11,2л /или 11200мл /. Следовательно Э V Н =11,2л. Эквивалентный объем хлора равен 11,2л /Э VCl =11,2л/. Эквивалентный объем СО равен 3,56 /Э VC О =3,56л/.
Химический эквивалент элемента или сложного вещества используется в стехиометрических расчетах обменных реакций, а в соответствующих расчетах окислительно–восстановительных реакций применяют уже окислительный и восстановительный эквиваленты.
Окислительный эквивалент определяют как частное от деления молекулярной массы окислителя на число электронов, которое он принимает в данной окислително–восстановительной реакции.
Восстановительный эквивалент равен молекулярной массе восстановителя поделенной на число электронов, которое он отдает в данной реакции.
Напишем окислително–восстановительную реакцию и определим эквивалент окислителя и восстановителя:
5N 2 aS+2KMnO 4 +8H 2 SO 4 =S+2MnSO 4 +K 2 SO 4 +5Na 2 SO 4 +8H 2 O
Окислителем в этой реакции является перманганат калия. Эквивалент окислителя будет равен массе KMnO 4 деленной на число электронов, принятых окислителем в реакции (nе=5). Э KMnO 4 =М KMnO 4 /nе=158/5=31,5. Молярная масса эквивалента окислителя KMnO 4 в кислой среде равна 31,5г/моль.
Эквивалент восстановителя Na 2 S будет: Э Na 4 S =М Na 4 S /nе=78/2=39. Молярная масса эквивалента Na 2 S равна 39г/моль.
В электрохимических процессах, в частности при электролизе веществ, пользуются электрохимическим эквивалентом. Электрохимический эквивалент определяют как частное от деления химического эквивалента вещества, выделяемого на электроде, на число Фарадея /F/. Электрохимический эквивалент более подробно будет рассмотрен в соответствующем параграфе курса.
Валентность . При взаимодействии атомов между ними образуется химическая связь. Каждый атом может образовывать только определенное количество связей. Количество связей предопределяет такое уникальное свойство каждого элемента, которое называют валентностью. В наиболее общем виде валентностью называют способность атома образовывать химическую связь. За единицу валентности принимают одну химическую связь, которую способен образовать атом водорода. В связи с этим, водород является одновалентным элементом, а кислород – двухвалентным, т.к. с атомом кислорода могут образовывать связь не более двух водородов.
Умение определять валентность каждого элемента, в том числе и в химическом соединении, является необходимым условием успешного усвоения курса химии.
С валентностью соприкасается и такое понятие химии как степень окисления . Подстепенью окисления понимают тот заряд, который имеет элемент в ионном соединении или имел бы в ковалентном соединении, если бы общая электронная пара бала бы полностью смещена к более электроотрицательному элементу. Степень окисления имеет не только цифровое выражение, но и соответствующий знак заряда (+) или (–). Валентность не имеет этих знаков. Например, в H 2 SO 4 степень окисления: водорода +1, кислорода –2, серы +6, а валентность, соответственно, будет 1, 2, 6.
Валентность и степень окисления в числовых значениях не всегда совпадают по величине. Например, в молекуле этилового спирта СН 3 –СН 2 –ОН валентность углерода 6, водорода 1, кислорода 2, а степень окисления, например, углерода первого –3, второго –1: –3 СН 3 – –1 СН 2 –ОН.
1.2. Основные экологические понятия.
За последнее время понятие “экология” глубоко входит в наше сознание. Это понятие, введенное еще в 1869г Э.Геккелем /происходит от греческого oikos – дом, место, жилище, logos – учение/ все больше и больше тревожит человечество.
В учебниках биологии экологию определяют как науку о взаимоотношениях живых организмов и среды их обитания. Практически созвучное определение экологии дает Б.Небел в своей книге «Наука об окружающей среде» – Экология – наука о различных аспектах взаимодействия организмов между собой и с окружающей средой. В других источниках можно встретить и более широкое толкование. Например, Экология – 1/. Наука, изучающая отношение организмов и их системных совокупностей и окружающей среды; 2/. Совокупность научных дисциплин, исследующих взаимоотношение системных биологических структур /от макромолекул до биосферы/ между собой и с окружающей средой; 3/. Дисциплина, изучающая общие законы функционирования экосистем различного иерархического уровня; 4/. Комплексная наука, исследующая среду обитания живых организмов; 5/. Исследование положения человека как вида в биосфере планеты, его связей с экологическими системами и воздействие на них; 6/. Наука о выживании в окружающей среде. /Н.А.Агиджанян, В.И.Торшик. Экология человека./. Однако под термином «экология» понимают не только экологию как науку, а само состояние окружающей среды и его влияние на человека, животный и растительный мир.
