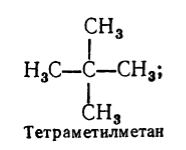
Alcani :
Alcanii sunt hidrocarburi saturate, în moleculele cărora toți atomii sunt legați prin legături simple. Formulă -
Proprietăți fizice :
- Punctele de topire și de fierbere cresc cu greutatea moleculară și lungimea lanțului principal de carbon
- În condiţii normale, alcanii neramificati de la CH4 la C4H10 sunt gaze; de la C5H12 la C13H28 - lichide; după C14H30 - solide.
- Punctele de topire și de fierbere scad de la mai puțin ramificat la mai ramificat. Deci, de exemplu, la 20 °C, n-pentanul este un lichid, iar neopentanul este un gaz.
Proprietăți chimice:
· Halogenare
aceasta este una dintre reacțiile de substituție. Atomul de carbon cel mai puțin hidrogenat este mai întâi halogenat (atomul terțiar, apoi atomii secundari, primari sunt halogenați ultimii). Halogenarea alcanilor are loc în etape - nu mai mult de un atom de hidrogen este înlocuit într-o singură etapă:
- CH 4 + Cl 2 → CH 3 Cl + HCl (clormetan)
- CH 3 Cl + Cl 2 → CH 2 Cl 2 + HCl (diclormetan)
- CH 2 Cl 2 + Cl 2 → CHCl 3 + HCl (triclormetan)
- CHCI3 + CI2 → CCl4 + HCI (tetraclormetan).
Sub acțiunea luminii, molecula de clor se descompune în radicali, apoi atacă moleculele de alcan, luând din ele un atom de hidrogen, în urma cărora se formează radicali metil CH 3 care se ciocnesc cu moleculele de clor, distrugându-le și formând noi. radicali.
· Combustie
Principala proprietate chimică a hidrocarburilor saturate, care determină utilizarea lor ca combustibil, este reacția de ardere. Exemplu:
CH4 + 2O2 → CO2 + 2H2O+ Q
În caz de lipsă de oxigen, în loc de dioxid de carbon se obține monoxid de carbon sau cărbune (în funcție de concentrația de oxigen).
În general, reacția de ardere a alcanilor poate fi scrisă după cum urmează:
Cu n H 2 n +2 +(1,5n+0,5)O 2 \u003d n CO 2 + ( n+1) H20
· Descompunere
Reacțiile de descompunere apar numai sub influența temperaturilor ridicate. O creștere a temperaturii duce la ruperea legăturii de carbon și formarea de radicali liberi.
Exemple:
CH4 → C + 2H2 (t > 1000 °C)
C2H6 → 2C + 3H2
Alchenele :
Alchenele sunt hidrocarburi nesaturate care conțin în moleculă, pe lângă legăturile simple, o legătură dublă carbon-carbon.Formula este C n H 2n
Apartenența unei hidrocarburi la clasa alchenelor este reflectată de sufixul generic -ene din numele său.
Proprietăți fizice :
- Punctele de topire și de fierbere ale alchenelor (simplificate) cresc cu greutatea moleculară și lungimea lanțului de carbon principal.
- În condiţii normale, alchenele de la C 2 H 4 la C 4 H 8 sunt gaze; de la C 5 H 10 la C 17 H 34 - lichide, după C 18 H 36 - solide. Alchenele sunt insolubile în apă, dar ușor solubile în solvenți organici.
Proprietăți chimice :
· Deshidratare este procesul de scindare a unei molecule de apă dintr-o moleculă de compus organic.
· Polimerizare- acesta este un proces chimic de combinare a multor molecule inițiale ale unei substanțe cu greutate moleculară mică în molecule mari de polimer.
Polimer este un compus cu greutate moleculară mare, ale cărui molecule constau din multe unități structurale identice.
Alcadiene :
Alcadienele sunt hidrocarburi nesaturate care conțin în moleculă, pe lângă legăturile simple, două legături duble carbon-carbon.Formula este
. Dienele sunt izomeri structurali ai alchinelor.Proprietăți fizice :
Butadiena este un gaz (fierbere -4,5 °C), izoprenul este un lichid care fierbe la 34 °C, dimetilbutadiena este un lichid care fierbe la 70 °C. Izoprenul și alte hidrocarburi diene sunt capabile să se polimerizeze în cauciuc. Cauciucul natural in stare purificata este un polimer cu formula generala (C5H8)n si se obtine din latexul anumitor plante tropicale.
Cauciucul este foarte solubil în benzen, benzină, disulfură de carbon. La temperatură scăzută devine casantă, când este încălzită devine lipicios. Pentru a îmbunătăți proprietățile mecanice și chimice ale cauciucului, acesta este transformat în cauciuc prin vulcanizare. Pentru a obține produse din cauciuc, acestea sunt mai întâi turnate dintr-un amestec de cauciuc cu sulf, precum și cu umpluturi: funingine, cretă, argilă și unii compuși organici care servesc la accelerarea vulcanizării. Apoi produsele sunt încălzite - vulcanizare la cald. În timpul vulcanizării, sulful se leagă chimic cu cauciucul. În plus, în cauciucul vulcanizat, sulful este conținut în stare liberă sub formă de particule minuscule.
Hidrocarburile diene sunt ușor de polimerizat. Reacția de polimerizare a hidrocarburilor diene stă la baza sintezei cauciucului. Intră în reacții de adiție (hidrogenare, halogenare, hidrohalogenare):
H 2 C \u003d CH-CH \u003d CH 2 + H 2 -> H 3 C-CH \u003d CH-CH 3
Alchinele :
Alchinele sunt hidrocarburi nesaturate ale căror molecule conţin, pe lângă legăturile simple, o legătură triplă carbon-carbon.Formula-C n H 2n-2
Proprietăți fizice :
Alchinele sunt similare ca proprietăți fizice cu alchenele corespunzătoare. Inferioare (până la C 4) - gaze fără culoare și miros, având puncte de fierbere mai mari decât omologii lor în alchene.
Alchinele sunt slab solubile în apă, mai bune în solvenți organici.
Proprietăți chimice :
reacții de halogenare
Alchinele sunt capabile să adauge una sau două molecule de halogen pentru a forma derivații de halogen corespunzători:
Hidratarea
În prezența sărurilor de mercur, alchinele adaugă apă pentru a forma acetaldehidă (pentru acetilenă) sau cetonă (pentru alte alchine)

DEFINIȚIE
Alcani se numesc hidrocarburi saturate, ale căror molecule constau din atomi de carbon și hidrogen, legați între ele doar prin legături σ.
În condiții normale (la 25 o C și presiunea atmosferică), primii patru membri ai seriei omoloage de alcani (C 1 - C 4) sunt gaze. Alcanii normali de la pentan la heptadecan (C 5 - C 17) sunt lichizi, începând de la C 18 și mai sus sunt solide. Pe măsură ce greutatea moleculară relativă crește, punctele de fierbere și de topire ale alcanilor cresc. Cu același număr de atomi de carbon într-o moleculă, alcanii ramificati au puncte de fierbere mai mici decât alcanii normali. Structura moleculei de alcani folosind metanul ca exemplu este prezentată în fig. unu.
Orez. 1. Structura moleculei de metan.
Alcanii sunt practic insolubili în apă, deoarece moleculele lor sunt de polaritate scăzută și nu interacționează cu moleculele de apă. Alcanii lichizi se amestecă ușor între ei. Se dizolvă bine în solvenți organici nepolari, cum ar fi benzen, tetraclorură de carbon, dietil eter etc.
Obținerea alcanilor
Principalele surse de diferite hidrocarburi saturate care conțin până la 40 de atomi de carbon sunt petrolul și gazele naturale. Alcanii cu un număr mic de atomi de carbon (1 - 10) pot fi izolați prin distilarea fracționată a gazului natural sau a fracțiunii de benzină a petrolului.
Există metode industriale (I) și de laborator (II) pentru obținerea alcanilor.
C + H2 → CH4 (kat = Ni, t 0);
CO + 3H2 → CH4 + H2O (kat \u003d Ni, t 0 \u003d 200 - 300);
CO2 + 4H2 → CH4 + 2H20 (kat, t0).
— hidrogenarea hidrocarburilor nesaturate
CH3-CH \u003d CH2 + H2 →CH3-CH2-CH3 (kat \u003d Ni, t 0);
— reducerea haloalcanilor
C2H5I + HI → C2H6 + I2 (t0);
- reactii alcaline de topire a sarurilor acizilor organici monobazici
C2H5-COONa + NaOH → C2H6 + Na2CO3 (t0);
- interacțiunea haloalcanilor cu sodiul metalic (reacția Wurtz)
2C2H5Br + 2Na → CH3-CH2-CH2-CH3 + 2NaBr;
– electroliza sărurilor acizilor organici monobazici
2C2H5COONa + 2H2O → H2 + 2NaOH + C4H10 + 2CO2;
K (-): 2H2O + 2e → H2 + 2OH-;
A (+): 2C 2 H 5 COO - -2e → 2C 2 H 5 COO + → 2C 2 H 5 + + 2CO 2.
Proprietățile chimice ale alcanilor
Alcanii sunt printre cei mai puțin reactivi compuși organici, ceea ce se explică prin structura lor.
Alcanii în condiții normale nu reacționează cu acizi concentrați, alcaline topite și concentrate, metale alcaline, halogeni (cu excepția fluorului), permanganat de potasiu și dicromat de potasiu într-un mediu acid.
Pentru alcani, reacțiile care se desfășoară conform mecanismului radicalilor sunt cele mai caracteristice. Clivajul homolitic al legăturilor C-H și C-C este energetic mai favorabil decât clivajul lor heterolitic.
Reacțiile de substituție radicală au loc cel mai ușor la atomul de carbon terțiar, mai ușor la atomul de carbon secundar și, în sfârșit, la atomul de carbon primar.
Toate transformările chimice ale alcanilor au loc prin scindare:
1) Legături C-H
- halogenare (S R)
CH 4 + Cl 2 → CH 3 Cl + HCl ( hv);
CH3-CH2-CH3 + Br2 → CH3-CHBr-CH3 + HBr ( hv).
- nitrare (S R)
CH3-C (CH3) H-CH3 + HONO2 (diluat) → CH3-C (NO2) H-CH3 + H20 (t0).
– sulfoclorurare (S R)
R-H + SO 2 + Cl 2 → RSO 2 Cl + HCI ( hv).
– dehidrogenare
CH 3 -CH 3 → CH 2 \u003d CH 2 + H 2 (kat \u003d Ni, t 0).
— dehidrociclizare
CH3 (CH2)4CH3 → C6H6 + 4H2 (kat = Cr2O3, t0).
2) Legături C-H și C-C
- izomerizare (rearanjare intramoleculară)
CH3-CH2-CH2-CH3 →CH3-C (CH3) H-CH3 (kat \u003d AlCI3, t 0).
- oxidare
2CH3-CH2-CH2-CH3 + 5O2 → 4CH3COOH + 2H20 (t0, p);
Cn H2n + 2 + (1,5n + 0,5) O2 → nCO2 + (n + 1) H2O (t 0).
Aplicarea alcanilor
Alcanii și-au găsit aplicații în diverse industrii. Să luăm în considerare mai detaliat, folosind exemplul unor reprezentanți ai seriei omoloage, precum și amestecuri de alcani.
Metanul este materia primă de bază a celor mai importante procese industriale chimice de producere a carbonului și hidrogenului, acetilenei, compușilor organici care conțin oxigen - alcooli, aldehide, acizi. Propanul este folosit ca combustibil pentru automobile. Butanul este folosit pentru a produce butadienă, care este o materie primă pentru producția de cauciuc sintetic.
Un amestec de alcani lichizi și solizi până la C 25, numit vaselină, este folosit în medicină ca bază pentru unguente. Un amestec de alcani solizi C 18 - C 25 (parafină) este utilizat pentru a impregna diverse materiale (hârtie, țesături, lemn) pentru a le conferi proprietăți hidrofobe, adică. impermeabilitate la apă. În medicină, este utilizat pentru proceduri fizioterapeutice (tratament cu parafină).
Exemple de rezolvare a problemelor
EXEMPLUL 1
| Exercițiu | La clorurarea metanului s-au obținut 1,54 g de compus, a cărui densitate a vaporilor în aer este de 5,31. Calculați masa de dioxid de mangan MnO 2 care va fi necesară pentru a produce clor dacă raportul dintre volumele de metan și clor introduse în reacție este 1:2. |
| Decizie | Raportul dintre masa unui gaz dat și masa altui gaz luată în același volum, la aceeași temperatură și aceeași presiune, se numește densitatea relativă a primului gaz față de al doilea. Această valoare arată de câte ori primul gaz este mai greu sau mai ușor decât al doilea gaz. Greutatea moleculară relativă a aerului este considerată egală cu 29 (ținând cont de conținutul de azot, oxigen și alte gaze din aer). Trebuie remarcat faptul că conceptul de „greutate moleculară relativă a aerului” este utilizat condiționat, deoarece aerul este un amestec de gaze. Să aflăm masa molară a gazului format în timpul clorării metanului: M gaz \u003d 29 × D aer (gaz) \u003d 29 × 5,31 \u003d 154 g / mol. Aceasta este tetraclorura de carbon - CCl 4 . Scriem ecuația reacției și aranjam coeficienții stoichiometrici: CH 4 + 4Cl 2 \u003d CCl 4 + 4HCl. Calculați cantitatea de substanță tetraclorură de carbon: n(CC14) = m(CC14) / M(CC14); n (CCl 4) \u003d 1,54 / 154 \u003d 0,01 mol. Conform ecuației reacției n (CCl 4 ) : n (CH 4 ) = 1: 1, atunci n (CH 4) \u003d n (CCl 4) \u003d 0,01 mol. Apoi, cantitatea de substanță cu clor ar trebui să fie egală cu n(Cl 2) = 2 × 4 n(CH 4), adică. n(Cl 2) \u003d 8 × 0,01 \u003d 0,08 mol. Scriem ecuația reacției pentru producerea de clor: MnO2 + 4HCl \u003d MnCl2 + Cl2 + 2H2O. Numărul de moli de dioxid de mangan este de 0,08 moli, deoarece n (Cl 2) : n (MnO 2) = 1: 1. Aflați masa dioxidului de mangan: m (MnO 2) \u003d n (MnO 2) × M (MnO 2); M (MnO 2) \u003d Ar (Mn) + 2 × Ar (O) \u003d 55 + 2 × 16 \u003d 87 g / mol; m (MnO 2) \u003d 0,08 × 87 \u003d 10,4 g. |
| Răspuns | Masa dioxidului de mangan este de 10,4 g. |
EXEMPLUL 2
| Exercițiu | Setați formula moleculară a tricloroalcanului, fracția de masă a clorului în care este de 72,20%. Alcătuiți formulele structurale ale tuturor izomerilor posibili și dați denumirile substanțelor conform nomenclaturii substituționale IUPAC. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Răspuns | Să scriem formula generală a tricloroalchenei: CnH2n-1CI3. Conform formulei ω(Cl) = 3×Ar(Cl) / Mr(C n H 2 n -1 Cl 3) × 100% Calculați greutatea moleculară a tricloroalcanului: Mr(C n H 2 n -1 Cl 3) = 3 × 35,5 / 72,20 × 100% = 147,5. Să găsim valoarea lui n: 12n + 2n - 1 + 35,5x3 = 147,5; Prin urmare, formula tricloroalcanului este C 3 H 5 Cl 3. Să compunem formulele structurale ale izomerilor: 1,2,3-triclorpropan (1), 1,1,2-triclorpropan (2), 1,1,3-triclorpropan (3), 1,1,1-triclorpropan (4) și 1,2,2-triclorpropan (5). CH2CI-CHCI-CH2CI (1); CHCI2-CHCI-CH3 (2); CHCI2-CH2-CH2CI (3); CC13-CH2-CH3(4); Alcani (metanul și omologii săi) au formula generală C n H2 n+2. Primele patru hidrocarburi se numesc metan, etan, propan, butan. Numele membrilor superiori ai acestei serii constau din rădăcina - cifra grecească și sufixul -an. Numele alcanilor formează baza nomenclaturii IUPAC.Reguli pentru nomenclatura sistematică:
Circuitul principal este selectat pe baza următoarelor criterii în secvență:
Lanțul principal este numerotat de la un capăt la altul cu cifre arabe. Fiecare substituent primește numărul atomului de carbon din lanțul principal de care este atașat. Secvența de numerotare este aleasă în așa fel încât suma numerelor de substituenți (locanți) să fie cea mai mică. Această regulă se aplică și numerotării compușilor monociclici.
Toate grupările laterale de hidrocarburi sunt considerate radicali monovalenți (legați simple). Dacă radicalul lateral însuși conține lanțuri laterale, atunci un lanț principal suplimentar este selectat în el conform regulilor de mai sus, care este numerotat pornind de la atomul de carbon atașat la lanțul principal.
Numele compusului începe cu o listă de substituenți, indicând numele acestora în ordine alfabetică. Numele fiecărui substituent este precedat de numărul său în lanțul principal. Prezența mai multor substituenți este indicată prin prefixe-numeratoare: di-, tri-, tetra- etc. După aceea, se numește hidrocarbura corespunzătoare lanțului principal. În tabel. 12.1 arată denumirile primelor cinci hidrocarburi, radicalii acestora, posibilii izomeri și formulele corespunzătoare. Numele radicalilor se termină cu sufixul -il.
Exemplu. Numiți toți izomerii hexanului. Exemplu. Numiți alcanul din următoarea structură În acest exemplu, dintre două lanțuri de doisprezece atomice, se alege cel în care suma numerelor este cea mai mică (regula 2). Folosind denumirile radicalilor ramificati date in tabel. 12.2,
numele acestui alcan este oarecum simplificat: 10-terţ-butil-2,2-(dimetil)-7-propil-4-izopropil-3-etil dodecan. Când lanțul de hidrocarburi este închis într-un ciclu cu pierderea a doi atomi de hidrogen, se formează monocicloalcani cu formula generală C n H2 n. Ciclizarea începe de la C 3, numele sunt formate din C n prefixat cu ciclo: alcani policiclici. Numele lor sunt formate din prefixul biciclo-, triciclo- etc. Compușii biciclici și triciclici conțin în moleculă două și, respectiv, trei cicluri, pentru a descrie structura lor, în paranteze pătrate indicați în ordine descrescătoare numărul de atomi de carbon din fiecare dintre ele. lanțurile care leagă atomii nodali; sub formula numele atomului: Această hidrocarbură triciclică este denumită în mod obișnuit adamantan (din cehă adamant, diamant) deoarece este o combinație de trei inele ciclohexan topite într-o formă care are ca rezultat un aranjament asemănător unui diamant al atomilor de carbon în rețeaua cristalină. Hidrocarburile ciclice cu un atom de carbon comun se numesc spirani, de exemplu, spiro-5,5-undecan: Moleculele ciclice plane sunt instabile, astfel încât se formează diverși izomeri conformaționali. Spre deosebire de izomerii configuraționali (aranjarea spațială a atomilor într-o moleculă fără a ține cont de orientare), izomerii conformaționali diferă între ei doar prin rotația atomilor sau a radicalilor în jurul legăturilor formal simple, menținând în același timp configurația moleculelor. Energia de formare a unui conformer stabil se numește conformațional. Conformerii sunt în echilibru dinamic și sunt transformați unul în altul prin forme instabile. Instabilitatea ciclurilor plane este cauzată de o deformare semnificativă a unghiurilor de legătură. În timp ce se mențin unghiurile de legătură tetraedrice pentru ciclohexanul C 6H 12, sunt posibile două conformații stabile: sub formă de scaun (a) și sub formă de baie (b):
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||