एंटोनी लॉरेंट LAVOISIER () () ने ऑक्सीजन की जांच की और दहन के ऑक्सीजन सिद्धांत का निर्माण किया, जिसने फ्लॉजिस्टन सिद्धांत को बदल दिया। उन्होंने ऑक्सीजन का अध्ययन किया और दहन के ऑक्सीजन सिद्धांत का निर्माण किया, जिसने फ्लॉजिस्टन सिद्धांत को बदल दिया।

ऑक्सीजन पृथ्वी पर सबसे आम तत्व है हवा में 21% (मात्रा के अनुसार), हवा में 21% (मात्रा के अनुसार), पृथ्वी की पपड़ी में 49% (द्रव्यमान से), पृथ्वी की पपड़ी में 49% (द्रव्यमान से), जलमंडल में 89% (द्रव्यमान से), जलमंडल में 89% (द्रव्यमान से), जीवित जीवों में द्रव्यमान द्वारा 65% तक। जीवित जीवों में द्रव्यमान का 65% तक।

भौतिक गुण समग्र अवस्था - सामान्य परिस्थितियों में गैस। बहुत कम तापमान (-183 डिग्री सेल्सियस) पर यह एकत्रीकरण की तरल अवस्था (नीला तरल) में बदल जाता है, और इससे भी कम तापमान (-219 डिग्री सेल्सियस) पर यह ठोस (नीला बर्फ क्रिस्टल) बन जाता है। कुल अवस्था - सामान्य परिस्थितियों में गैस। बहुत कम तापमान (-183 डिग्री सेल्सियस) पर यह एकत्रीकरण की तरल अवस्था (नीला तरल) में बदल जाता है, और इससे भी कम तापमान (-219 डिग्री सेल्सियस) पर यह ठोस (नीला बर्फ क्रिस्टल) बन जाता है। रंगहीन - रंगहीन। रंगहीन - रंगहीन। गंध - गंधहीन। गंध - गंधहीन। पानी में घुलनशीलता - खराब घुलनशील। पानी में घुलनशीलता - खराब घुलनशील। हवा से भारी (एम हवा = 29 ग्राम / मोल, और एम ओ 2 = 32 ग्राम / मोल। हवा से भारी (एम हवा = 29 ग्राम / मोल, और एम ओ 2 = 32 ग्राम / मोल।

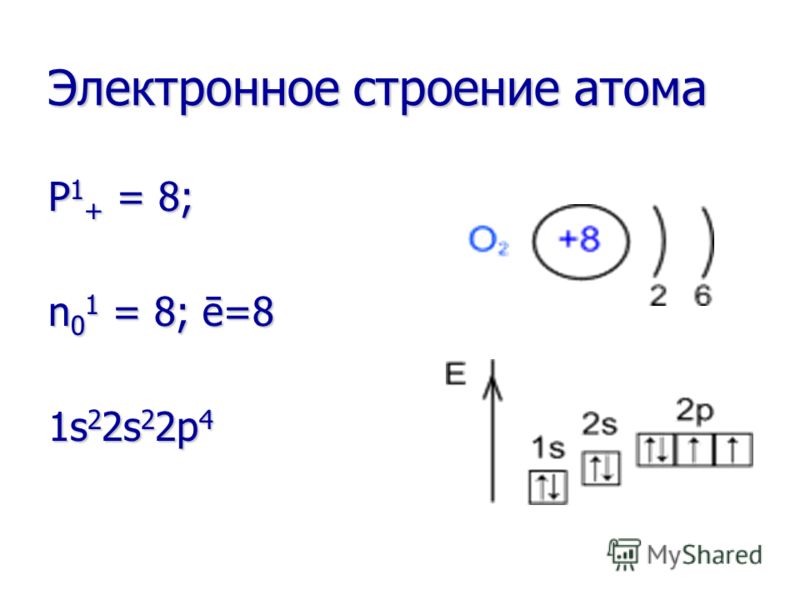
रासायनिक गुण ऑक्सीजन एक बहुत मजबूत ऑक्सीकरण एजेंट है! यह पहले से ही कमरे के तापमान (धीमी ऑक्सीकरण) पर कई पदार्थों का ऑक्सीकरण करता है और इससे भी ज्यादा जब पदार्थ को गर्म या जला दिया जाता है (तेज ऑक्सीकरण)। ऑक्सीजन एक बहुत मजबूत ऑक्सीकरण एजेंट है! यह पहले से ही कमरे के तापमान (धीमी ऑक्सीकरण) पर कई पदार्थों का ऑक्सीकरण करता है और इससे भी ज्यादा जब पदार्थ को गर्म या जला दिया जाता है (तेज ऑक्सीकरण)। सभी तत्वों (फ्लोरीन को छोड़कर) के साथ प्रतिक्रियाओं में, ऑक्सीजन हमेशा एक ऑक्सीकरण एजेंट होता है। सभी तत्वों (फ्लोरीन को छोड़कर) के साथ प्रतिक्रियाओं में, ऑक्सीजन हमेशा एक ऑक्सीकरण एजेंट होता है।

धातुओं के साथ अभिक्रियाएँ अभिक्रिया के परिणामस्वरूप इस धातु का एक ऑक्साइड बनता है। उदाहरण के लिए, एल्युमिनियम को ऑक्सीजन द्वारा समीकरण के अनुसार ऑक्सीकृत किया जाता है: प्रतिक्रिया के परिणामस्वरूप, इस धातु का एक ऑक्साइड बनता है। उदाहरण के लिए, एल्युमीनियम को समीकरण के अनुसार ऑक्सीजन द्वारा ऑक्सीकृत किया जाता है: t° 4Al + 3O 2 2Al 2 O 3 t° 4Al + 3O 2 2Al 2 O 3 एक अन्य उदाहरण। जब एक लाल-गर्म लोहे के तार को ऑक्सीजन की बोतल में उतारा जाता है, तो तार जल जाता है, चिंगारी के किनारों पर छिड़काव - लोहे के पैमाने के गर्म कण Fe 3 O 4: t ° 3Fe + 2O 2 Fe 3 O 4 t ° 3Fe + 2ओ 2 फे 3 ओ 4


गैर-धातुओं के साथ प्रतिक्रियाओं के अन्य उदाहरण सल्फर डाइऑक्साइड बनाने के लिए ऑक्सीजन में सल्फर का दहन SO 2: t ° S + O 2 SO 2 t ° S + O 2 SO 2 कार्बन डाइऑक्साइड बनाने के लिए ऑक्सीजन में कोयले का दहन: कोयले का दहन कार्बन डाइऑक्साइड बनाने के लिए ऑक्सीजन: t° C + O 2 CO 2 t° C + O 2 CO 2
कुछ जटिल पदार्थों के साथ अभिक्रियाएँ इस स्थिति में एक जटिल पदार्थ के अणु का निर्माण करने वाले तत्वों के ऑक्साइड बनते हैं। इस मामले में, एक जटिल पदार्थ के अणु बनाने वाले तत्वों के ऑक्साइड बनते हैं। उदाहरण के लिए, कॉपर (II) सल्फाइड की फायरिंग के दौरान उदाहरण के लिए, कॉपर (II) सल्फाइड की फायरिंग के दौरान t ° 2CuS + 3O 2 2CuO + 2SO 2 t ° 2CuS + 3O 2 2CuO + 2SO 2 दो ऑक्साइड बनते हैं कॉपर ( II) ऑक्साइड और सल्फर ऑक्साइड (IV)। दो ऑक्साइड बनते हैं, कॉपर (II) ऑक्साइड और सल्फर (IV) ऑक्साइड। सल्फाइड को भूनने के दौरान हमेशा सल्फर ऑक्साइड बनता है, जिसमें सल्फर की संयोजकता IV होती है। सल्फाइड को भूनने के दौरान हमेशा सल्फर ऑक्साइड बनता है, जिसमें सल्फर की संयोजकता IV होती है। एक अन्य उदाहरण मीथेन सीएच 4 का दहन है। चूंकि इस अणु में कार्बन सी और हाइड्रोजन एच तत्वों के परमाणु होते हैं, इसका मतलब है कि दो ऑक्साइड कार्बन मोनोऑक्साइड (IV) सीओ 2 और हाइड्रोजन ऑक्साइड, यानी पानी - एच 2 बनते हैं। ओ: टी डिग्री सीएच 4 + 2 ओ 2 सीओ 2 + 2 एच 2 ओ टी डिग्री सीएच 4 + 2 ओ 2 सीओ 2 + 2 एच 2 ओ

ऑक्सीजन के साथ किसी पदार्थ की रासायनिक बातचीत को ऑक्सीकरण प्रतिक्रिया कहा जाता है। गर्मी और प्रकाश की रिहाई के साथ ऑक्सीकरण प्रतिक्रियाओं को दहन प्रतिक्रियाएं कहा जाता है। पदार्थों की दहन प्रतिक्रियाएं तीव्र ऑक्सीकरण के उदाहरण हैं, लेकिन सड़ना, जंग लगना आदि। ये ऑक्सीजन द्वारा पदार्थों के धीमे ऑक्सीकरण के उदाहरण हैं। पदार्थों की दहन प्रतिक्रियाएँ तेज़ ऑक्सीकरण के उदाहरण हैं, लेकिन सड़ना, जंग लगना आदि। ये ऑक्सीजन द्वारा पदार्थों के धीमे ऑक्सीकरण के उदाहरण हैं

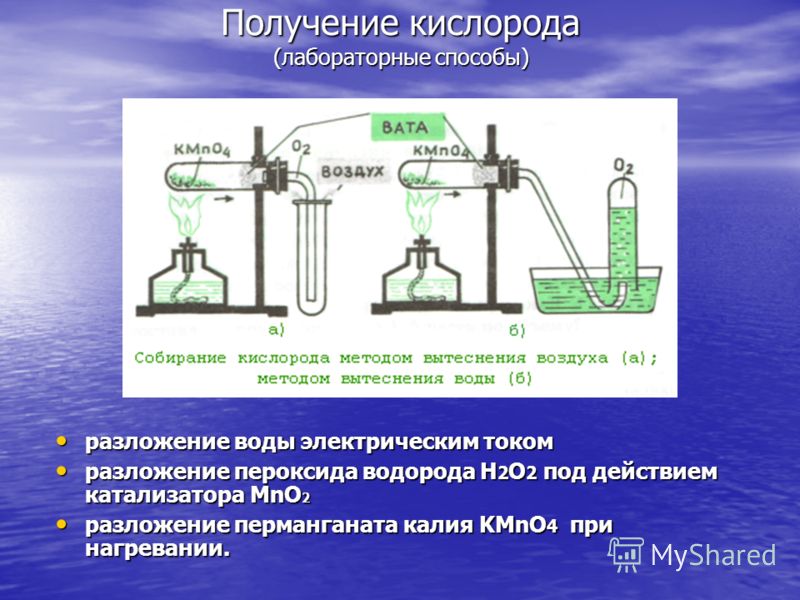
ऑक्सीजन उत्पादन (प्रयोगशाला विधियों) विद्युत प्रवाह द्वारा जल अपघटन हाइड्रोजन पेरोक्साइड एच 2 ओ 2 के विद्युत प्रवाह अपघटन द्वारा एमएनओ 2 उत्प्रेरक अपघटन हाइड्रोजन पेरोक्साइड एच 2 ओ 2 की क्रिया के तहत एमएनओ 2 उत्प्रेरक अपघटन पोटेशियम परमैंगनेट की क्रिया के तहत पानी अपघटन KMnO4 गर्म होने पर। गर्म करने पर पोटेशियम परमैंगनेट KMnO4 का अपघटन।
ऑक्सीजन प्राप्त करना (औद्योगिक विधि) उद्योग में, शुद्ध ऑक्सीजन प्राप्त करने के लिए, वायु घटकों के विभिन्न क्वथनांक के आधार पर, तरल वायु के आसवन का उपयोग किया जाता है। हवा को लगभग -200 डिग्री सेल्सियस तक ठंडा किया जाता है और फिर धीरे-धीरे गर्म किया जाता है। जब तापमान -183 डिग्री सेल्सियस तक पहुंच जाता है, तो ऑक्सीजन तरल हवा से निकल जाती है, इस तापमान पर तरलीकृत हवा के शेष घटक एकत्रीकरण की तरल अवस्था में रहते हैं। उद्योग में, शुद्ध ऑक्सीजन प्राप्त करने के लिए, वायु घटकों के विभिन्न क्वथनांक के आधार पर, तरल वायु के आसवन का उपयोग किया जाता है। हवा को लगभग -200 डिग्री सेल्सियस तक ठंडा किया जाता है और फिर धीरे-धीरे गर्म किया जाता है। जब तापमान -183 डिग्री सेल्सियस तक पहुंच जाता है, तो ऑक्सीजन तरल हवा से निकल जाती है, इस तापमान पर तरलीकृत हवा के शेष घटक एकत्रीकरण की तरल अवस्था में रहते हैं।

निर्माण और मैकेनिकल इंजीनियरिंग में ऑक्सीजन का उपयोग निर्माण और मैकेनिकल इंजीनियरिंग में - ऑक्सी-एसिटिलीन गैस वेल्डिंग और धातुओं की गैस काटने के लिए - ऑक्सी-एसिटिलीन गैस वेल्डिंग और धातुओं की गैस काटने के लिए - तेल उत्पादन में तेल उत्पादन में धातुओं के छिड़काव और सतह के लिए - जब धातु विज्ञान और खनन उद्योग में धातु विज्ञान और खनन उद्योग में विस्थापन ऊर्जा को बढ़ाने के लिए गठन में इंजेक्ट किया जाता है - संवहनी इस्पात उत्पादन में, ब्लास्ट फर्नेस में ऑक्सीजन विस्फोट, सोने और अयस्कों का निष्कर्षण, लौह मिश्र धातुओं का उत्पादन, निकल, जस्ता, सीसा का गलाने , जिरकोनियम और अन्य अलौह धातु - संवहनी इस्पात उत्पादन में, ब्लास्ट फर्नेस में ऑक्सीजन विस्फोट, सोने और अयस्कों का निष्कर्षण, लौह मिश्र धातुओं का उत्पादन, निकल, जस्ता, सीसा, जिरकोनियम और अन्य अलौह धातुओं के गलाने के साथ - की प्रत्यक्ष कमी के साथ लोहा - लोहे की सीधी कमी के साथ - फाउंड्री उत्पादन में आग की सफाई के साथ - फाउंड्री उत्पादन में आग की सफाई के साथ - आग ड्रिलिंग के साथ एक्स नस्लों

दवा में ऑक्सीजन का उपयोग - ऑक्सीबेरिक कक्षों में - ऑक्सीबेरिक कक्षों में - ऑक्सीजन मास्क, तकिए आदि भरते समय। - ऑक्सीजन मास्क, तकिए आदि भरते समय। - एक विशेष माइक्रॉक्लाइमेट वाले वार्डों में - एक विशेष माइक्रॉक्लाइमेट वाले वार्डों में - ऑक्सीजन कॉकटेल के उत्पादन के लिए - ऑक्सीजन कॉकटेल के उत्पादन के लिए - सूक्ष्मजीवों की खेती में - पारिस्थितिकी में सूक्ष्मजीवों की खेती में - पीने के शुद्धिकरण में पानी - पीने के पानी के शुद्धिकरण में - धातुओं के पुनर्चक्रण में - धातुओं के पुनर्चक्रण में - जब अपशिष्ट जल को ऑक्सीजन से उड़ाया जाता है - जब ऑक्सीजन के साथ अपशिष्ट जल को उड़ाया जाता है - जब भस्मक में उपचार संयंत्रों में रासायनिक रूप से सक्रिय अपशिष्ट को निष्क्रिय किया जाता है - जब उपचार संयंत्रों में रासायनिक रूप से सक्रिय अपशिष्ट को निष्क्रिय किया जाता है भस्मक में

रासायनिक उद्योग में रासायनिक उद्योग में ऑक्सीजन का उपयोग - एसिटिलीन, सेल्युलोज, मिथाइल अल्कोहल, अमोनिया, नाइट्रिक और सल्फ्यूरिक एसिड के उत्पादन में - एसिटिलीन, सेल्युलोज, मिथाइल अल्कोहल, अमोनिया, नाइट्रिक और सल्फ्यूरिक एसिड के उत्पादन में - में प्राकृतिक गैस का उत्प्रेरक रूपांतरण (सिंथेटिक अमोनिया के उत्पादन में) - प्राकृतिक गैस के उत्प्रेरक रूपांतरण में (सिंथेटिक अमोनिया के उत्पादन में) - मीथेन के उच्च तापमान रूपांतरण में - मीथेन के उच्च तापमान रूपांतरण में बिजली उद्योग में बिजली उद्योग - ठोस ईंधन के गैसीकरण में - ठोस ईंधन के गैसीकरण में - घरेलू और औद्योगिक बॉयलरों के लिए वायु संवर्धन के लिए - घरेलू और औद्योगिक बॉयलरों के लिए वायु संवर्धन के लिए - जल-कोयला मिश्रण को संपीड़ित करने के लिए - पानी को संपीड़ित करने के लिए- कोयले का मिश्रण

सैन्य उपकरणों में सैन्य उपकरणों में ऑक्सीजन का उपयोग - दबाव कक्षों में - दबाव कक्षों में - पानी के नीचे डीजल इंजनों के संचालन के लिए - पानी के नीचे डीजल इंजनों के संचालन के लिए - रॉकेट इंजनों के लिए ईंधन ऑक्सीडाइज़र के रूप में - ईंधन ऑक्सीडाइज़र के रूप में कृषि में रॉकेट इंजन - मछली पकड़ने में ऑक्सीजन के साथ जलीय पर्यावरण को समृद्ध करने के लिए - मछली पकड़ने में ऑक्सीजन के साथ जलीय पर्यावरण को समृद्ध करने के लिए - ऑक्सीजन कॉकटेल के निर्माण में - ऑक्सीजन कॉकटेल के निर्माण में - पशु वजन बढ़ाने के लिए - पशु वजन बढ़ाने के लिए

ओजोन ऑक्सीजन का एलोट्रोपिक संशोधन ओजोन ओ 3 एक तीखी गंध वाली नीली गैस है। जिस किसी ने भी इस बात पर ध्यान दिया है कि आंधी के बाद या बिजली के निर्वहन के स्रोत के पास हवा कैसे गंध करती है, वह इस गैस की गंध को अच्छी तरह से जानता है। ओजोन ओ 3 एक तीखी गंध वाली नीली गैस है। जिस किसी ने भी इस बात पर ध्यान दिया है कि आंधी के बाद या बिजली के निर्वहन के स्रोत के पास हवा कैसे गंध करती है, वह इस गैस की गंध को अच्छी तरह से जानता है। प्रकृति में, ओजोन सूर्य से पराबैंगनी विकिरण की क्रिया से बनता है, और यह वातावरण में विद्युत निर्वहन द्वारा भी निर्मित होता है:
ओजोन एक बहुत मजबूत ऑक्सीकरण एजेंट है, इसलिए इसका उपयोग पीने के पानी की कीटाणुशोधन में किया जाता है। अधिकांश ऑक्सीकरण योग्य पदार्थों के संपर्क में आने पर विस्फोट होता है। सौर विकिरण के प्रभाव में पृथ्वी के वायुमंडल में 25 किमी की ऊंचाई पर ओजोन बनता है, यह सूर्य से खतरनाक विकिरण को अवशोषित करता है। हालांकि, पृथ्वी के ओजोन "छाता" में, केवल लगभग 30 मीटर मोटी, "छेद" समय-समय पर दिखाई देते हैं। ओजोन के लिए अधिक से अधिक गैसें "हानिकारक", जैसे नाइट्रोजन मोनोऑक्साइड NO या वे पदार्थ जो प्रशीतन इकाइयों और एरोसोल के डिब्बे को भरने के लिए उपयोग किए जाते हैं, हवा में मिल रहे हैं। यहां तक कि पृथ्वी के ऊपर ओजोन परत के आंशिक रूप से गायब होने से सभी जीवित चीजों को मौत का खतरा है ... हालांकि, पृथ्वी के ओजोन "छाता" में, केवल 30 मीटर मोटी, "छेद" समय-समय पर दिखाई देते हैं। ओजोन के लिए अधिक से अधिक गैसें "हानिकारक", जैसे नाइट्रोजन मोनोऑक्साइड NO या वे पदार्थ जो प्रशीतन इकाइयों और एरोसोल के डिब्बे को भरने के लिए उपयोग किए जाते हैं, हवा में मिल रहे हैं। यहां तक कि पृथ्वी के ऊपर ओजोन परत के आंशिक रूप से गायब होने से भी सभी जीवित चीजों को मौत का खतरा है...


