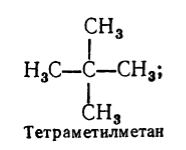
Alkány :
Alkány sú nasýtené uhľovodíky, v molekulách ktorých sú všetky atómy spojené jednoduchými väzbami. Vzorec -
Fyzikálne vlastnosti :
- Teploty topenia a varu sa zvyšujú s molekulovou hmotnosťou a dĺžkou hlavného uhlíkového reťazca
- Za normálnych podmienok sú nerozvetvené alkány od CH4 do C4H10 plyny; od C5H12 do C13H28 - kvapaliny; po C14H30 - pevné látky.
- Teploty topenia a varu klesajú z menej rozvetvených na viac rozvetvené. Takže napríklad pri 20 °C je n-pentán kvapalina a neopentán je plyn.
Chemické vlastnosti:
· Halogenácia
toto je jedna zo substitučných reakcií. Najmenej hydrogenovaný atóm uhlíka sa halogenuje ako prvý (terciárny atóm, potom sekundárny, primárne atómy sa halogenujú ako posledné). Halogenácia alkánov prebieha v etapách - v jednej etape sa nenahradí viac ako jeden atóm vodíka:
- CH 4 + Cl 2 → CH 3 Cl + HCl (chlorometán)
- CH3CI + Cl2 → CH2CI2 + HCl (dichlórmetán)
- CH2CI2 + Cl2 → CHCI3 + HCl (trichlórmetán)
- CHCI3 + Cl2 -> CCI4 + HCl (tetrachlórmetán).
Pôsobením svetla sa molekula chlóru rozkladá na radikály, tie potom atakujú molekuly alkánov, berú z nich atóm vodíka, v dôsledku čoho vznikajú metylové radikály CH 3, ktoré sa zrážajú s molekulami chlóru, ničia ich a vytvárajú nové. radikálov.
· Spaľovanie
Hlavnou chemickou vlastnosťou nasýtených uhľovodíkov, ktorá určuje ich použitie ako paliva, je spaľovacia reakcia. Príklad:
CH4 + 202 -> C02 + 2H20+ Q
V prípade nedostatku kyslíka sa namiesto oxidu uhličitého získava oxid uhoľnatý alebo uhlie (v závislosti od koncentrácie kyslíka).
Vo všeobecnosti možno reakciu spaľovania alkánov napísať takto:
S n H 2 n +2 +(1,5n+0,5) O2 \u003d n CO 2 + ( n+1) H20
· Rozklad
Rozkladné reakcie prebiehajú iba pod vplyvom vysokých teplôt. Zvýšenie teploty vedie k rozpadu uhlíkovej väzby a vzniku voľných radikálov.
Príklady:
CH4 -> C + 2H 2 (t > 1000 °C)
C2H6 -> 2C + 3H2
alkény :
Alkény sú nenasýtené uhľovodíky obsahujúce v molekule okrem jednoduchých väzieb aj jednu dvojitú väzbu uhlík-uhlík. Vzorec je C n H 2n
Príslušnosť uhľovodíka k triede alkénov je vyjadrená generickou príponou -én v jeho názve.
Fyzikálne vlastnosti :
- Teploty topenia a varu alkénov (zjednodušene) sa zvyšujú s molekulovou hmotnosťou a dĺžkou hlavného uhlíkového reťazca.
- Za normálnych podmienok sú alkény od C2H4 do C4H8 plyny; od C 5 H 10 do C 17 H 34 - kvapaliny, po C 18 H 36 - tuhé látky. Alkény sú nerozpustné vo vode, ale ľahko rozpustné v organických rozpúšťadlách.
Chemické vlastnosti :
· Dehydratácia je proces oddeľovania molekuly vody od molekuly organickej zlúčeniny.
· Polymerizácia- ide o chemický proces spájania mnohých počiatočných molekúl látky s nízkou molekulovou hmotnosťou do veľkých molekúl polyméru.
Polymér je zlúčenina s vysokou molekulovou hmotnosťou, ktorej molekuly pozostávajú z mnohých rovnakých štruktúrnych jednotiek.
Alkadiény :
Alkadiény sú nenasýtené uhľovodíky obsahujúce v molekule okrem jednoduchých väzieb aj dve dvojité väzby uhlík-uhlík. Vzorec je
. Diény sú štruktúrne izoméry alkínov.Fyzikálne vlastnosti :
Butadién je plyn (tvar −4,5 °C), izoprén je kvapalina s teplotou varu 34 °C, dimetylbutadién je kvapalina s teplotou varu 70 °C. Izoprén a iné diénové uhľovodíky sú schopné polymerizovať na gumu. Prírodný kaučuk vo svojom čistenom stave je polymér so všeobecným vzorcom (C5H8)n a získava sa z latexu určitých tropických rastlín.
Kaučuk je vysoko rozpustný v benzéne, benzíne, sírouhlíku. Pri nízkej teplote skrehne, pri zahriatí sa stáva lepkavým. Na zlepšenie mechanických a chemických vlastností gumy sa vulkanizáciou mení na gumu. Na získanie gumových výrobkov sa najskôr formujú zo zmesi gumy so sírou, ako aj s plnivami: sadze, krieda, hlina a niektoré organické zlúčeniny, ktoré slúžia na urýchlenie vulkanizácie. Potom sa výrobky zahrievajú - horúca vulkanizácia. Pri vulkanizácii sa síra chemicky viaže s gumou. Vo vulkanizovanom kaučuku je navyše síra obsiahnutá vo voľnom stave vo forme drobných čiastočiek.
Diénové uhľovodíky sa ľahko polymerizujú. Polymerizačná reakcia diénových uhľovodíkov je základom syntézy kaučuku. Vstúpiť do adičných reakcií (hydrogenácia, halogenácia, hydrohalogenácia):
H2C \u003d CH-CH \u003d CH2 + H2 -> H3C-CH \u003d CH-CH3
alkíny :
Alkíny sú nenasýtené uhľovodíky, ktorých molekuly obsahujú okrem jednoduchých väzieb aj jednu trojitú väzbu uhlík-uhlík Vzorec-C n H 2n-2
Fyzikálne vlastnosti :
Alkíny majú podobné fyzikálne vlastnosti ako zodpovedajúce alkény. Nižšie (do C 4) - plyny bez farby a zápachu, ktoré majú vyššie body varu ako ich náprotivky v alkénoch.
Alkíny sú slabo rozpustné vo vode, lepšie v organických rozpúšťadlách.
Chemické vlastnosti :
halogenačné reakcie
Alkíny sú schopné pridať jednu alebo dve halogénové molekuly za vzniku zodpovedajúcich halogénových derivátov:
Hydratácia
V prítomnosti ortuťových solí alkíny pridávajú vodu za vzniku acetaldehydu (pre acetylén) alebo ketónu (pre iné alkíny)

DEFINÍCIA
Alkány sa nazývajú nasýtené uhľovodíky, ktorých molekuly pozostávajú z atómov uhlíka a vodíka, ktoré sú navzájom spojené iba σ-väzbami.
Za normálnych podmienok (pri 25 o C a atmosférickom tlaku) sú prvé štyri členy homologickej série alkánov (C 1 - C 4) plyny. Normálne alkány od pentánu po heptadekán (C5 - C17) sú kvapaliny, počnúc od C18 a vyššie sú pevné látky. Keď sa relatívna molekulová hmotnosť zvyšuje, teploty varu a topenia alkánov sa zvyšujú. Pri rovnakom počte atómov uhlíka v molekule majú rozvetvené alkány nižšie teploty varu ako normálne alkány. Štruktúra molekuly alkánov s použitím metánu ako príkladu je znázornená na obr. jeden.
Ryža. 1. Štruktúra molekuly metánu.
Alkány sú prakticky nerozpustné vo vode, pretože ich molekuly majú nízku polaritu a neinteragujú s molekulami vody. Kvapalné alkány sa navzájom ľahko miešajú. Dobre sa rozpúšťajú v nepolárnych organických rozpúšťadlách, ako je benzén, tetrachlórmetán, dietyléter atď.
Získanie alkánov
Hlavnými zdrojmi rôznych nasýtených uhľovodíkov obsahujúcich až 40 atómov uhlíka sú ropa a zemný plyn. Alkány s malým počtom atómov uhlíka (1 - 10) možno izolovať frakčnou destiláciou zemného plynu alebo benzínovej frakcie ropy.
Na získanie alkánov existujú priemyselné (I) a laboratórne (II) metódy.
C + H2 -> CH4 (kat = Ni, to);
CO + 3H2 → CH4 + H20 (kat \u003d Ni, to \u003d 200 - 300);
C02 + 4H2 -> CH4 + 2H20 (kat, t0).
— hydrogenácia nenasýtených uhľovodíkov
CH3-CH \u003d CH2 + H2 ->CH3-CH2-CH3 (kat \u003d Ni, to);
— regenerácia halogénalkánov
C2H5I + HI -» C2H6 + I2 (to);
- alkalické reakcie topenia solí jednosýtnych organických kyselín
C2H5-COONa + NaOH -> C2H6 + Na2C03 (to);
- interakcia halogénalkánov s kovovým sodíkom (Wurtzova reakcia)
2C2H5Br + 2Na -> CH3-CH2-CH2-CH3 + 2NaBr;
– elektrolýza solí jednosýtnych organických kyselín
2C2H5COONa + 2H20 -> H2 + 2NaOH + C4H10 + 2C02;
K (-): 2H20 + 2e -> H2 + 2OH-;
A (+): 2C2H5COO--2e -> 2C2H5COO + -> 2C2H5+ + 2C02.
Chemické vlastnosti alkánov
Alkány patria medzi najmenej reaktívne organické zlúčeniny, čo sa vysvetľuje ich štruktúrou.
Alkány za normálnych podmienok nereagujú s koncentrovanými kyselinami, roztavenými a koncentrovanými zásadami, alkalickými kovmi, halogénmi (okrem fluóru), manganistanom draselným a dvojchrómanom draselným v kyslom prostredí.
Pre alkány sú najcharakteristickejšie reakcie prebiehajúce podľa radikálového mechanizmu. Homolytické štiepenie väzieb C-H a C-C je energeticky výhodnejšie ako ich heterolytické štiepenie.
Radikálové substitučné reakcie prebiehajú najľahšie na terciárnom atóme uhlíka, ľahšie na sekundárnom atóme uhlíka a nakoniec na primárnom atóme uhlíka.
Všetky chemické premeny alkánov prebiehajú štiepením:
1) C-H väzby
- halogenácia (SR)
CH 4 + Cl 2 → CH 3 Cl + HCl ( hv);
CH3-CH2-CH3 + Br2 → CH3-CHBr-CH3 + HBr ( hv).
- nitrácia (SR)
CH3-C (CH3) H-CH3 + HON02 (zriedený) -> CH3-C (N02) H-CH3 + H20 (to).
– sulfochlorácia (SR)
R-H + SO2 + Cl2 → RSO2Cl + HCl ( hv).
– dehydrogenácia
CH3-CH3 → CH2 \u003d CH2 + H2 (kat \u003d Ni, t 0).
— dehydrocyklizácia
CH3(CH2)4CH3 -> C6H6 + 4H2 (kat = Cr203, to).
2) C-H a C-C väzby
- izomerizácia (intramolekulárne preskupenie)
CH3-CH2-CH2-CH3 ->CH3-C (CH3) H-CH3 (kat \u003d AlCl3, to).
- oxidácia
2CH3-CH2-CH2-CH3 + 502 -> 4CH3COOH + 2H20 (to, p);
CnH2n + 2+ (1,5 n + 0,5) 02 -» nC02+ (n + 1) H20 (to).
Aplikácia alkánov
Alkány našli uplatnenie v rôznych priemyselných odvetviach. Pozrime sa podrobnejšie na príklade niektorých predstaviteľov homologickej série, ako aj zmesí alkánov.
Metán je surovinovým základom najdôležitejších chemických priemyselných procesov na výrobu uhlíka a vodíka, acetylénu, organických zlúčenín obsahujúcich kyslík - alkoholy, aldehydy, kyseliny. Propán sa používa ako automobilové palivo. Bután sa používa na výrobu butadiénu, ktorý je surovinou na výrobu syntetického kaučuku.
Ako základ mastí sa v medicíne používa zmes tekutých a pevných alkánov do C 25, nazývaná vazelína. Zmes pevných alkánov C 18 - C 25 (parafín) sa používa na impregnáciu rôznych materiálov (papier, tkaniny, drevo), aby získali hydrofóbne vlastnosti, t.j. nepriepustnosť vody. V medicíne sa využíva na fyzioterapeutické procedúry (parafínová liečba).
Príklady riešenia problémov
PRÍKLAD 1
| Cvičenie | Pri chlorácii metánu sa získalo 1,54 g zlúčeniny, ktorej hustota pár vo vzduchu je 5,31. Vypočítajte hmotnosť oxidu manganičitého MnO 2, ktorý bude potrebný na výrobu chlóru, ak je pomer objemov metánu a chlóru zavedeného do reakcie 1:2. |
| rozhodnutie | Pomer hmotnosti daného plynu k hmotnosti iného plynu odobratého v rovnakom objeme, pri rovnakej teplote a rovnakom tlaku sa nazýva relatívna hustota prvého plynu voči druhému. Táto hodnota ukazuje, koľkokrát je prvý plyn ťažší alebo ľahší ako druhý plyn. Relatívna molekulová hmotnosť vzduchu sa rovná 29 (berúc do úvahy obsah dusíka, kyslíka a iných plynov vo vzduchu). Je potrebné poznamenať, že pojem „relatívna molekulová hmotnosť vzduchu“ sa používa podmienečne, pretože vzduch je zmesou plynov. Nájdite molárnu hmotnosť plynu vzniknutého pri chlorácii metánu: M plyn \u003d 29 × D vzduch (plyn) \u003d 29 × 5,31 \u003d 154 g / mol. Toto je tetrachlórmetán - CCl4. Napíšeme reakčnú rovnicu a usporiadame stechiometrické koeficienty: CH4 + 4CI2 \u003d CCI4 + 4HCl. Vypočítajte množstvo látky tetrachlórmetánu: n(CC14) = m(CC14)/M(CC14); n (CCl 4) \u003d 1,54 / 154 \u003d 0,01 mol. Podľa reakčnej rovnice n (CCl 4): n (CH 4) = 1: 1, potom n (CH 4) \u003d n (CCl 4) \u003d 0,01 mol. Potom by sa množstvo chlórovej látky malo rovnať n(Cl 2) = 2 × 4 n(CH 4), t.j. n(Cl2) \u003d 8 x 0,01 \u003d 0,08 mol. Napíšeme reakčnú rovnicu na výrobu chlóru: Mn02 + 4 HCl \u003d MnCl2 + Cl2 + 2 H20. Počet mólov oxidu manganičitého je 0,08 mólov, pretože n (Cl 2) : n (MnO 2) = 1: 1. Nájdite hmotnosť oxidu manganičitého: m (Mn02) \u003d n (Mn02) x M (Mn02); M (Mn02) \u003d Ar (Mn) + 2 x Ar (O) \u003d 55 + 2 x 16 \u003d 87 g/mol; m (Mn02) \u003d 0,08 × 87 \u003d 10,4 g. |
| Odpoveď | Hmotnosť oxidu manganičitého je 10,4 g. |
PRÍKLAD 2
| Cvičenie | Nastavte molekulový vzorec trichlóralkánu, ktorého hmotnostný podiel chlóru je 72,20 %. Vytvorte štruktúrne vzorce všetkých možných izomérov a uveďte názvy látok podľa substitučnej nomenklatúry IUPAC. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Odpoveď | Napíšme všeobecný vzorec trichlóralkénu: CnH2n-1Cl3. Podľa vzorca ω(Cl) = 3×Ar(Cl) / Mr(C n H 2 n -1 Cl 3) × 100 % vypočítajte molekulovú hmotnosť trichlóralkánu: Mr(CnH2n-1Cl3) = 3 x 35,5 / 72,20 x 100 % = 147,5. Nájdite hodnotu n: 12n + 2n - 1 + 35,5 x 3 = 147,5; Preto je vzorec trichlóralkánu C3H5C13. Zostavme štruktúrne vzorce izomérov: 1,2,3-trichlórpropán (1), 1,1,2-trichlórpropán (2), 1,1,3-trichlórpropán (3), 1,1,1-trichlórpropán (4) a 1,2,2-trichlórpropán (5). CH2CI-CHCI-CH2CI (1); CHCI2-CHCI-CH3 (2); CHCI2-CH2-CH2CI (3); CCI3-CH2-CH3(4); Alkány (metán a jeho homológy) majú všeobecný vzorec C n H2 n+2. Prvé štyri uhľovodíky sa nazývajú metán, etán, propán, bután. Mená vyšších členov tohto radu pozostávajú z koreňa - gréckej číslice a prípony -an. Názvy alkánov tvoria základ nomenklatúry IUPAC.Pravidlá systematickej nomenklatúry:
Hlavný okruh sa vyberá na základe nasledujúcich kritérií v poradí:
Hlavná reťaz je očíslovaná od jedného konca k druhému arabskými číslicami. Každý substituent dostane číslo atómu uhlíka hlavného reťazca, ku ktorému je pripojený. Postupnosť číslovania sa volí tak, aby súčet počtov substituentov (lokantov) bol najmenší. Toto pravidlo platí aj pre číslovanie monocyklických zlúčenín.
Všetky uhľovodíkové vedľajšie skupiny sa považujú za jednoväzbové (jednoducho viazané) radikály. Ak vedľajší radikál sám obsahuje vedľajšie reťazce, potom sa v ňom podľa vyššie uvedených pravidiel vyberie ďalší hlavný reťazec, ktorý je očíslovaný od atómu uhlíka pripojeného k hlavnému reťazcu.
Názov zlúčeniny začína zoznamom substituentov s uvedením ich názvov v abecednom poradí. Pred názvom každého substituenta je uvedené jeho číslo v hlavnom reťazci. Prítomnosť niekoľkých substituentov je označená predponou-čitateľmi: di-, tri-, tetra- atď. Potom sa zavolá uhľovodík zodpovedajúci hlavnému reťazcu. V tabuľke. 12.1 uvádza názvy prvých piatich uhľovodíkov, ich radikály, možné izoméry a ich zodpovedajúce vzorce. Názvy radikálov končia príponou -yl.
Príklad. Vymenujte všetky izoméry hexánu. Príklad. Pomenujte alkán nasledujúcej štruktúry V tomto príklade z dvoch dvanásťatómových reťazcov sa vyberie ten, v ktorom je súčet čísel najmenší (pravidlo 2). Použitie názvov rozvetvených radikálov uvedených v tabuľke. 12.2,
názov tohto alkánu je trochu zjednodušený: 10-terc-butyl-2,2-(dimetyl)-7-propyl-4-izopropyl-3-etyldodekán. Keď je uhľovodíkový reťazec uzavretý v cykle so stratou dvoch atómov vodíka, vznikajú monocykloalkány so všeobecným vzorcom C n H2 n. Cyklizácia začína od C 3, mená sa tvoria od C n s predponou cyclo: polycyklické alkány. Ich názvy sú tvorené predponou bicyklo-, tricyklo- atď. Bicyklické a tricyklické zlúčeniny obsahujú v molekule dva a tri cykly, na opis ich štruktúry v hranatých zátvorkách v zostupnom poradí uveďte počet atómov uhlíka v každom z nich. reťazce spájajúce nodálne atómy; pod vzorcom názov atómu: Tento tricyklický uhľovodík sa bežne označuje ako adamantan (z českého adamant, diamant), pretože ide o kombináciu troch kondenzovaných cyklohexánových kruhov vo forme, ktorá má za následok diamantovité usporiadanie atómov uhlíka v kryštálovej mriežke. Cyklické uhľovodíky s jedným spoločným atómom uhlíka sa nazývajú spirány, napríklad spiro-5,5-undekán: Planárne cyklické molekuly sú nestabilné, preto vznikajú rôzne konformačné izoméry. Na rozdiel od konfiguračných izomérov (priestorové usporiadanie atómov v molekule bez ohľadu na orientáciu) sa konformačné izoméry navzájom líšia iba rotáciou atómov alebo radikálov okolo formálne jednoduchých väzieb pri zachovaní konfigurácie molekúl. Energia tvorby stabilného konforméra sa nazýva konformačné. Konforméry sú v dynamickej rovnováhe a navzájom sa premieňajú prostredníctvom nestabilných foriem. Nestabilita rovinných cyklov je spôsobená výraznou deformáciou väzbových uhlov. Pri zachovaní uhlov tetraedrickej väzby pre cyklohexán C 6H 12 sú možné dve stabilné konformácie: vo forme stoličky (a) a vo forme kúpeľa (b):
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||