Ang mga phenol ay maaaring mag-react sa parehong hydroxyl group at sa benzene ring.
1. Mga reaksyon sa pangkat ng hydroxyl
Ang carbon-oxygen bond sa mga phenol ay mas malakas kaysa sa mga alkohol. Halimbawa, ang phenol ay hindi maaaring ma-convert sa bromobenzene sa pamamagitan ng pagkilos ng hydrogen bromide, habang ang cyclohexanol, kapag pinainit ng hydrogen bromide, ay madaling na-convert sa bromocyclohexane:
Tulad ng mga alkoxide, ang mga phenoxide ay tumutugon sa mga alkyl halides at iba pang mga alkylating reagents upang bumuo ng mga halo-halong ester:
 (23)
(23)
Phenetol
 (24)
(24)
Anisole
Ang alkylation ng mga phenol na may mga halocarbon o dimethyl sulfate sa isang alkaline na medium ay isang pagbabago ng reaksyon ng Williamson. Ang reaksyon ng alkylation ng mga phenol na may chloroacetic acid ay gumagawa ng mga herbicide tulad ng 2,4-dichlorophenoxyacetic acid (2,4-D).
 (25)
(25)
2,4-Dichlorophenoxyacetic acid (2,4-D)
at 2,4,5-trichlorophenoxyacetic acid (2,4,5-T).
 (26)
(26)
2,4,5-trichlorophenoxyacetic acid (2,4,5-T)
Ang panimulang 2,4,5-trichlorophenol ay nakuha ayon sa sumusunod na pamamaraan:
 (27)
(27)
1,2,4,5-Tetrachlorophenol 2,4,5-trichlorophenoxide sodium 2,4,5-trichlorophenol
Kung sobrang init sa yugto ng paggawa ng 2,4,5-trichlorophenol, ang napakalason na 2,3,7,8-tetrachlorodibenzodioxine ay maaaring mabuo sa halip:
2,3,7,8-Tetrachlorodibenzodioxin
Ang mga phenol ay mas mahinang mga nucleophile kaysa sa mga alkohol. Para sa kadahilanang ito, hindi tulad ng mga alkohol, hindi sila pumapasok sa isang reaksyon ng esterification. Upang makakuha ng mga phenol ester, ginagamit ang mga acid chlorides at acid anhydride:
Phenylacetate
Diphenyl carbonate
Pagsasanay 17. Ang thymol (3-hydroxy-4-isopropyltoluene) ay matatagpuan sa thyme at ginagamit bilang medium-strength antiseptic sa mga toothpaste at mouthwashes. Inihanda ito ng Friedel–Crafts alkylation
m-cresol na may 2-propanol sa pagkakaroon ng sulfuric acid. Isulat ang reaksyong ito.
2. Pagpapalit sa isang singsing
Ang hydroxy group ng phenol ay napakalakas na pinapagana ang aromatic ring na may paggalang sa mga electrophilic substitution reactions. Ang mga oxonium ions ay malamang na nabuo bilang mga intermediate compound:


Kapag nagsasagawa ng mga reaksyon ng pagpapalit ng electrophilic sa kaso ng mga phenol, ang mga espesyal na hakbang ay dapat gawin upang maiwasan ang polysubstitution at oksihenasyon.
3. Nitrasyon
Ang phenol nitrates ay mas madali kaysa sa benzene. Kapag nalantad ito sa puro nitric acid, ang 2,4,6-trinitrophenol (picric acid) ay nabuo:

Picric acid
Ang pagkakaroon ng tatlong grupo ng nitro sa nucleus ay matalas na pinatataas ang kaasiman ng phenolic group. Ang picric acid, hindi katulad ng phenol, ay medyo malakas na acid. Ang pagkakaroon ng tatlong grupo ng nitro ay gumagawa ng picric acid na sumasabog at ginagamit upang maghanda ng melinite. Upang makakuha ng mononitrophenols, kinakailangan na gumamit ng dilute na nitric acid at isagawa ang reaksyon sa mababang temperatura:

Ito ay lumiliko ang isang timpla O- At P- nitrophenols na may nangingibabaw O- isomer. Ang halo na ito ay madaling naghihiwalay dahil sa ang katunayan na lamang O- ang isomer ay pabagu-bago ng isip na may singaw ng tubig. Mahusay na pagkasumpungin O- Ang nitrophenol ay ipinaliwanag sa pamamagitan ng pagbuo ng isang intramolecular hydrogen bond, habang nasa kaso
P- nitrophenol, isang intermolecular hydrogen bond ay nangyayari.

4. Sulfonation
Ang sulfonation ng phenol ay napakadali at humahantong sa pagbuo, depende sa temperatura, nakararami ortho- o pares- mga phenolsulfonic acid:

5. Halogenation
Ang mataas na reaktibiti ng phenol ay humahantong sa katotohanan na kahit na ginagamot ito ng bromine water, tatlong hydrogen atoms ang pinapalitan:
 (31)
(31)
Upang makakuha ng monobromophenol, dapat gawin ang mga espesyal na hakbang.
 (32)
(32)
P-Bromophenol
Pagsasanay 18. Ang 0.94 g ng phenol ay ginagamot ng bahagyang labis na tubig ng bromine. Anong produkto at sa anong dami ang nabuo?
6. Kolbe reaksyon
Ang carbon dioxide ay nagdaragdag sa sodium phenoxide ng Kolbe reaction, na isang electrophilic substitution reaction kung saan ang electrophile ay carbon dioxide
 (33)
(33)
Phenol Sodium phenoxide Sodium salicylate Salicylic acid
Mekanismo:
 (M 5)
(M 5)
Sa pamamagitan ng pagtugon sa salicylic acid na may acetic anhydride, ang aspirin ay nakuha:
 (34)
(34)
Acetylsalicylic acid
Kung pareho ortho-mga posisyon ay inookupahan, pagkatapos ay ang pagpapalit ay nagaganap ayon sa pares- posisyon:
 (35)
(35)
Ang reaksyon ay nagpapatuloy ayon sa sumusunod na mekanismo:
 (M 6)
(M 6)

7. Condensation na may carbonyl-containing compounds
Kapag ang phenol ay pinainit na may formaldehyde sa pagkakaroon ng acid, ang phenol-formaldehyde resin ay nabuo:
 (36)
(36)
Phenol formaldehyde resin
Sa pamamagitan ng condensation ng phenol na may acetone sa isang acidic medium, ang 2,2-di(4-hydroxyphenyl)propane ay nakuha, industrially na pinangalanang bisphenol A:
Bisphenol A
2,2-di(4-hydroxyphenyl)propane
di(4-hydroxyphenyl)dimethylmethane
Sa pamamagitan ng paggamot sa bisphenol A na may phosgene sa pyridine, nakuha ang Lexan:
Sa pagkakaroon ng sulfuric acid o zinc chloride, ang phenol ay namumuo sa phthalic anhydride upang bumuo ng phenolphthalein:
 (39)
(39)
Phthalic anhydride Phenolphthalein
Kapag ang phthalic anhydride ay pinagsama sa resorcinol sa pagkakaroon ng zinc chloride, ang isang katulad na reaksyon ay nangyayari at ang fluorescein ay nabuo:
 (40)
(40)
Resorcinol Fluorescein
Pagsasanay 19. Gumuhit ng diagram ng condensation ng phenol na may formaldehyde. Ano ang praktikal na kahalagahan ng reaksyong ito?
8. Claisen rearrangement
Ang mga phenol ay sumasailalim sa mga reaksyon ng alkylation ng Friedel-Crafts. Halimbawa, kapag ang phenol ay tumutugon sa allyl bromide sa pagkakaroon ng aluminum chloride, ang 2-allylphenol ay nabuo:
 (41)
(41)
Ang parehong produkto ay nabuo din kapag ang allylphenyl ether ay pinainit bilang resulta ng isang intramolecular na reaksyon na tinatawag na Pag-aayos ng Claisen:
 |
 |
Allylphenyl eter 2-Allylphenol
Reaksyon
 (43)
(43)
Nangyayari ito ayon sa sumusunod na mekanismo:
 (44)
(44)
Nagaganap din ang Claisen rearrangement kapag ang allyl vinyl ether o 3,3-dimethyl-1,5-hexadiene ay pinainit:
 (45)
(45)
Allyl vinyl eter 4-Penal
 (46)
(46)
3,3-Dimethyl-2-Methyl-2,6-
1,5-hexadiene hexadiene
Ang iba pang mga reaksyon ng ganitong uri ay kilala rin, halimbawa, ang Diels-Alder reaksyon. Tinawag sila mga reaksyong pericyclic.
Isang organikong sangkap mula sa pangkat ng mga phenol, isang simpleng diatomic phenol. Sa mga chemist, ginagamit din ang mga pangalang resorcinol at 1,3-dihydroxybenzene. Ang formula ng resorcinol ay katulad ng mga formula ng hydroquinone at pyrocatechin, ang pagkakaiba ay nasa istraktura ng molekula; sa paraan kung paano nakakabit ang mga pangkat ng OH.
Ari-arian
Ang sangkap ay mga kristal na hugis karayom na walang kulay o puting mala-kristal na pulbos na may masangsang na phenolic na amoy. Minsan ang pulbos ay maaaring magkaroon ng pinkish o madilaw-dilaw na tint. Kung ito ay nagiging mabigat na kulay, pink-orange o kayumanggi, nangangahulugan ito na ang reagent ay hindi naimbak nang tama at ito ay na-oxidize. Ang resorcinol ay isang panganib sa sunog. Mahusay itong natutunaw sa tubig, diethyl ether, ethyl alcohol, at acetone. Maaaring matunaw sa mga langis, gliserin. Halos hindi matutunaw sa chloroform, carbon disulfide, benzene.
Ang reagent ay nagpapakita ng mga kemikal na katangian ng mga phenol. Malakas na pagbabawas ng ahente, madaling ma-oxidized. Tumutugon sa alkalis, na bumubuo ng mga phenolate salt; na may ammonia, halogens, malakas na acids (halimbawa, nitric, sulfuric, picric, glacial acetic).

Para sa husay na pagpapasiya ng resorcinol, ang mga sumusunod na reaksyon ay ginagamit:
- na may ferric chloride - ang solusyon ay nagiging malalim na lila, halos itim;
- Ang pagsasanib sa phthalic anhydride sa pagkakaroon ng isang katalista ay humahantong sa pagbuo ng isang may kulay, berdeng fluorescent na substansiya - fluorescein. Ang Fluorescein mismo ay may dilaw-pula na solusyon sa kulay (ang reaksyon ay nakikilala ang resorcinol mula sa iba pang mga phenol).
Ang alikabok ng resorcinol at lalo na ang mga singaw nito ay nakakairita sa balat, mga organ sa paghinga, at mga mucous membrane ng mga mata. Ang paglanghap ng mga singaw at alikabok ng reagent ay nagdudulot ng pag-ubo, pagduduwal, mabilis na tibok ng puso, at pagkahilo, kaya kailangan mong gumamit ng resorcinol gamit ang mga respirator o maskara, mga salaming pangkaligtasan, espesyal na damit, at isang lugar na may bentilasyon. Kung pinaghihinalaan ang pagkalason, hugasan ang lugar kung saan nakalantad ang reagent ng maraming tubig, dalhin ang biktima sa sariwang hangin, at tumawag ng doktor.
Mag-imbak ng resorcinol sa isang lalagyan ng airtight, sa madilim, tuyo, malamig na mga silid, mahigpit na hiwalay sa mga nasusunog na sangkap.
Aplikasyon
Ang resorcinol ay hinihiling sa industriya ng kemikal bilang isang hilaw na materyal  para sa paggawa ng mga artipisyal na tina, fluorescein, resorcinol-formaldehyde resin, solvents, stabilizer, plasticizer at UV absorbers para sa mga plastik.
para sa paggawa ng mga artipisyal na tina, fluorescein, resorcinol-formaldehyde resin, solvents, stabilizer, plasticizer at UV absorbers para sa mga plastik.
- Sa analytical chemistry ito ay ginagamit sa colorimetric studies. Ito ay ginagamit upang matukoy ang nilalaman ng zinc, lead, carbohydrates, furfural, lignin, atbp.
- Sa industriya ng goma.
- Sa industriya ng balahibo, bilang pangkulay para sa balahibo.
- Napakalawak na ginagamit sa gamot at parmasyutiko. Ito ay ginagamit bilang isang disinfectant, cauterizing, sugat healing agent, at anthelmintic. Kasama sa mga solusyon at ointment para sa paggamot ng iba't ibang mga sakit sa balat, kabilang ang fungal at purulent; acne, seborrhea, dermatitis, eksema, age spots.
- Upang makakuha ng mga pampasabog.
Layunin ng trabaho
Ang layunin ng gawain ay upang isagawa ang mga reaksyon ng oksihenasyon at condensation para sa phenol at mga derivatives nito.
Teoretikal na bahagi
Ang mga phenol ay mga aromatic compound na mayroong mga hydroxyl group na direktang nakakabit sa aromatic ring. Batay sa bilang ng mga hydroxyls, ang monohydric, diatomic at polyatomic phenols ay nakikilala. Ang pinakasimpleng sa kanila, oxybenzene, ay tinatawag na phenol. Ang hydroxy derivatives ng toluene (methylphenols) ay tinatawag na ortho-, meta- at para-cresols, at ang hydroxy derivatives ng xylenes ay tinatawag na xylenols. Ang mga phenol ng serye ng naphthalene ay tinatawag na naphthols. Ang pinakasimpleng dihydric phenols ay tinatawag na: o - dioxybenzene - pyrocatechol, m - dioxybenzene - resorcinol, n-dioxybenzene - hydroquinone.
Maraming mga phenol ang madaling na-oxidized, kadalasang nagreresulta sa isang kumplikadong pinaghalong mga produkto. Depende sa ahente ng oxidizing at mga kondisyon ng reaksyon, maaaring makuha ang iba't ibang mga produkto. Kaya, sa panahon ng vapor-phase oxidation (t = 540 0) ng o - xylene, ang phthalic anhydride ay nakuha. Ang isang husay na reaksyon sa mga phenol ay isang pagsubok na may solusyon ng ferric chloride, na gumagawa ng isang kulay na ion. Ang Phenol ay nagbibigay ng pulang-lila na kulay, ang mga cresol ay nagbibigay ng asul na kulay, at ang iba pang mga phenol ay nagbibigay ng berdeng kulay.
Ang reaksyon ng condensation ay isang intramolecular o intermolecular na proseso ng pagbuo ng isang bagong C-C bond, kadalasang nangyayari kasama ng partisipasyon ng mga condensing reagents, ang papel nito ay maaaring ibang-iba: ito ay may catalytic effect, gumagawa ng mga intermediate reactive na produkto, o simpleng nagbubuklod. isang split-off na particle, na nagbabago ng equilibrium sa system.
Ang reaksyon ng condensation sa pag-aalis ng tubig ay na-catalyzed ng iba't ibang mga reagents: malakas na acids, malakas na alkalis (hydroxides, alcoholates, amides, alkali metal hydrides, ammonia, primary at secondary amines).
Order sa trabaho
Sa gawaing ito, sinubukan namin ang posibilidad ng oksihenasyon ng mga phenol at ang pagbuo ng mga phthaleins sa pamamagitan ng reaksyon ng condensation.
3.1 Oxidation ng phenol at naphthol
Ang oksihenasyon ay isinasagawa gamit ang isang solusyon ng potassium permanganate sa pagkakaroon ng isang solusyon ng sodium carbonate (soda).
3.1.1 kagamitan at reagents:
Mga tubo ng pagsubok;
Pipettes;
Phenol - may tubig na solusyon;
Naphthol - may tubig na solusyon;
Potassium permanganate (0.5% na may tubig na solusyon);
Sodium carbonate (5% na may tubig na solusyon);
3.1.2 Pagsasagawa ng eksperimento:
a) ilagay ang 1 ml ng isang may tubig na solusyon ng phenol o naphthol sa isang test tube;
b) magdagdag ng 1 ml ng sodium carbonate solution (soda);
c) magdagdag ng potassium permanganate solution patak-patak habang inaalog ang test tube. Obserbahan ang pagbabago ng kulay ng solusyon.
Ang oksihenasyon ng mga phenol ay karaniwang nangyayari sa iba't ibang direksyon at humahantong sa pagbuo ng isang kumplikadong pinaghalong mga sangkap. Ang mas madaling oksihenasyon ng mga phenol, kumpara sa mga aromatic hydrocarbons, ay dahil sa impluwensya ng hydroxyl group, na matalim na pinatataas ang kadaliang mapakilos ng mga atomo ng hydrogen sa iba pang mga carbon atom ng lason na benzene.
3.2 Pagbuo ng phthaleins.
3.2.1 Paghahanda ng phenolphthalein.
Ang phenolphthalein ay nabuo sa pamamagitan ng condensation reaction ng phenol na may phthalic anhydride sa pagkakaroon ng concentrated sulfuric acid.
Ang Phthalic anhydride ay namumuo sa mga phenol upang magbigay ng mga derivatives ng triphenylethane. Ang condensation ay sinamahan ng pag-aalis ng tubig dahil sa oxygen ng isa sa mga carbonyl group ng anhydride at ang mobile hydrogen atoms ng benzene nuclei ng dalawang phenol molecules. Ang pagpapakilala ng mga dewatering agent tulad ng concentrated sulfuric acid ay lubos na nagpapadali sa condensation na ito.
Ang phenol ay bumubuo ng phenolphthalein sa pamamagitan ng sumusunod na reaksyon:


 / \ /
/ \ /

 H H C
H H C
3.2.1.1 Kagamitan at reagents:
Mga tubo ng pagsubok;
Pipettes;
De-kuryenteng kalan;
Phthalic anhydride;
Sulfuric acid diluted 1:5;
3.2.1.2 Pagsasagawa ng eksperimento:
b) magdagdag ng humigit-kumulang dalawang beses sa dami ng phenol sa parehong test tube;
c) iling ang mga nilalaman ng test tube nang maraming beses at maingat na magdagdag ng 3-5 patak ng puro sulfuric acid dito, patuloy na nanginginig;
d) init ang test tube sa isang hotplate hanggang lumitaw ang isang madilim na pulang kulay;
e) palamigin ang test tube at magdagdag ng 5 ml ng tubig dito;
f) magdagdag ng isang patak na solusyon ng alkali sa resultang solusyon at obserbahan ang pagbabago ng kulay;
g) pagkatapos magpalit ng kulay, magdagdag ng ilang patak ng diluted sulfuric acid sa mga nilalaman ng test tube hanggang sa bumalik ang orihinal na kulay o hanggang sa mangyari ang pagkawalan ng kulay.
3.2.2 Paghahanda ng fluorescein.
Ang Fluorescein ay nabuo sa pamamagitan ng condensation reaction ng resorcinol na may phthalic anhydride sa pagkakaroon ng concentrated sulfuric acid.
Ang mga diatomic phenol na may mga hydroxyl group sa meta position, na pumapasok sa condensation, ay naglalabas ng dalawang molekula ng tubig, isa dahil sa oxygen ng isa sa mga carbonyl group ng anhydride at ang mga mobile hydrogen atoms ng benzene nuclei ng dalawang phenol molecules. ang pangalawang molekula ng tubig ay inilabas dahil sa mga pangkat ng hydroxyl ng dalawang molekula ng phenol upang bumuo ng isang singsing na may anim na miyembro.
Ang resorcinol ay bumubuo ng fluorescein sa pamamagitan ng sumusunod na reaksyon:
OH HO OH HO OH


 / \ / \ /
/ \ / \ /

 H H C
H H C
3.2.1.1.Kagamitan at reagents:
Mga tubo ng pagsubok;
Pipettes;
De-kuryenteng kalan;
Phthalic anhydride;
Resorcinol;
Puro sulfuric acid;
Caustic sodium solution (5-10%);
3.2.2.1 Pagsasagawa ng eksperimento:
a) timbangin ang 0.1-0.3 g ng phthalic anhydride at ilagay sa isang test tube;
b) magdagdag ng humigit-kumulang dalawang beses sa dami ng resorcinol sa parehong test tube at ihalo sa pamamagitan ng pag-alog;
c) maingat na magdagdag ng 3-5 patak ng puro sulfuric acid sa mga nilalaman ng test tube;
d) init ang timpla sa isang test tube hanggang lumitaw ang isang madilim na pulang kulay. Init sa isang electric stove;
e) palamig ang mga nilalaman ng test tube at magdagdag ng 5 ml ng tubig dito;
f) magdagdag ng 2-3 patak ng resultang solusyon sa isang malinis na test tube, magdagdag ng 1 ml ng alkali solution at maghalo ng maraming tubig. Obserbahan ang pagbabago ng kulay.
3.2.3 Pagbubuo ng Aurin
Ang Aurine ay nakuha sa pamamagitan ng paghalay ng oxalic acid na may phenol sa pagkakaroon ng sulfuric acid.
Kapag pinainit sa presensya ng sulfuric acid, ang oxalic acid ay namumuo sa tatlong molekula ng phenol, na naghihiwalay sa tubig at carbon monoxide upang bumuo ng aurin.
 |
|||
 |
|||
 H-O- -H H- -OH
H-O- -H H- -OH
 -H. OH O =
-H. OH O =
 | . C = O +3H 2 O+CO
| . C = O +3H 2 O+CO
 H - C
H - C
3.2.3.1. Kagamitan at reagents:
Mga tubo ng pagsubok;
Pipettes;
Oxalic acid;
Puro sulfuric acid;
3.2.3.2 Pagsasagawa ng eksperimento:
a) timbangin ang 0.02-0.05 g ng oxalic acid at humigit-kumulang dalawang beses na mas maraming phenol;
b) ilagay ang parehong reagents sa isang test tube at paghaluin sa pamamagitan ng pag-alog;
c) magdagdag ng 1-2 patak ng concentrated sulfuric acid sa test tube;
d) maingat na init ang test tube na may pinaghalong hanggang sa magsimula itong kumulo at lumitaw ang isang matinding dilaw na kulay;
e) palamigin ang test tube, magdagdag ng 3-4 ml ng tubig at iling. Obserbahan ang kulay na lilitaw;
f) magdagdag ng ilang patak ng alkali solution sa nagresultang solusyon at obserbahan ang pagbabago ng kulay;
3.3 Pagkabulok ng urea (carbomic acid amide) kapag pinainit.
Kapag pinainit sa itaas ng punto ng pagkatunaw nito, ang urea ay nabubulok, na naglalabas ng ammonia. Sa temperatura na 150 0 -160 0 C, dalawang molekula ng urea ang naghiwalay sa isang molekula ng ammonia at nagbibigay ng biureate, na lubos na natutunaw sa maligamgam na tubig:
H 2 N-OO-NH 2 +H-NH-OO-NH 2 H 2 N-CO-NH-CO-NH 2 +NH 3
Ang biureate ay nailalarawan sa pamamagitan ng pagbuo ng isang maliwanag na pulang kumplikadong tambalan sa isang alkalina na solusyon na may mga asin na tanso, na may sumusunod na komposisyon sa isang solusyon ng sodium hydroxide:
(NH 2 CO NH CONH 2) 2 *2NaOH*Cu(OH) 2
3.3.1 Kagamitan at reagents:
Mga tubo ng pagsubok;
De-kuryenteng kalan;
Urea (carbamide);
Caustic sodium solution (5-7%);
Copper sulfur solution (1%).
3.3.2 Pagsasagawa ng eksperimento:
a) timbangin ang 0.2-0.3 g ng urea at ilagay sa isang tuyong test tube;
b) init ang test tube sa isang electric stove;
c) obserbahan ang mga pagbabagong nagaganap: pagkatunaw, pagpapalabas ng ammonia, solidification;
d) palamigin ang test tube;
e) magdagdag ng 1-2 ml ng maligamgam na tubig sa isang cooled test tube, iling at ibuhos sa isa pang test tube;
f) magdagdag ng 3-4 na patak ng caustic soda solution sa nagreresultang maulap na solusyon hanggang sa transparent. Pagkatapos ay magdagdag ng isang patak ng solusyon ng tansong sulfuric acid at obserbahan ang pagbabago ng kulay (lumilitaw ang isang magandang kulay na lilang).
Kaugnay na impormasyon.
Phthalic anhydride Phenolphthalein
Kapag ang phthalic anhydride ay pinagsama sa resorcinol sa pagkakaroon ng zinc chloride, ang isang katulad na reaksyon ay nangyayari at ang fluorescein ay nabuo:
Resorcinol Fluorescein
3.8 Pag-aayos ng Claisen
Ang mga phenol ay sumasailalim sa mga reaksyon ng alkylation ng Friedel-Crafts. Halimbawa, kapag nakikipag-ugnayan f
enol na may allyl bromide sa pagkakaroon ng aluminum chloride, 2-allylphenol ay nabuo:
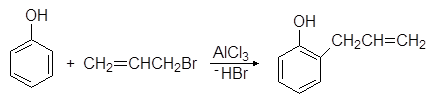
Ang parehong produkto ay nabuo din kapag ang allylphenyl ether ay pinainit bilang resulta ng isang intramolecular reaction na tinatawag na Claisen rearrangement:
 |
|||
 |
|||
Allylphenyl eter 2-Allylphenol
Reaksyon:

Nangyayari ito ayon sa sumusunod na mekanismo:

Nagaganap din ang Claisen rearrangement kapag pinainit ang allyl vinyl ether o 3,3-dimethyl-1,5-hexadiene: AAAAAAAAAAAAAAAAAAAAAAAAAAA

3.9 Polycondensation
Polycondensation ng phenol na may formaldehyde (ang reaksyong ito ay nagreresulta sa pagbuo ng phenol-formaldehyde resin:

3.10 Oksihenasyon
Ang mga phenol ay madaling na-oxidized kahit na sa ilalim ng impluwensya ng atmospheric oxygen. Kaya, kapag nakatayo sa hangin, ang phenol ay unti-unting nagiging pinkish-red. Sa panahon ng masiglang oksihenasyon ng phenol na may pinaghalong chromium, ang pangunahing produkto ng oksihenasyon ay quinone. Ang mga diatomic phenol ay mas madaling na-oxidize. Ang oksihenasyon ng hydroquinone ay gumagawa ng quinone.
3.11 Mga katangian ng acid
Ang mga acidic na katangian ng phenol ay nagpapakita ng kanilang sarili sa mga reaksyon sa alkalis (ang lumang pangalan na "carbolic acid" ay napanatili):
C6H5OH + NaOH<->C6H5ONa + H2O
Ang Phenol, gayunpaman, ay isang napakahinang acid. Kapag ang carbon dioxide o sulfur dioxide na mga gas ay dumaan sa isang solusyon ng mga phenolate, ang phenol ay inilabas - ang reaksyong ito ay nagmumungkahi na ang phenol ay isang mas mahinang acid kaysa sa carbonic at sulfur dioxide:
C6H5ONa + CO2 + H2O -> C6H5ON + NaHCO3
Ang mga acidic na katangian ng phenols ay humina sa pamamagitan ng pagpapakilala ng mga substituent ng unang uri sa singsing at pinahusay ng pagpapakilala ng mga substituent ng pangalawang uri.
4. Paraan ng pagkuha
Ang paggawa ng phenol sa isang pang-industriya na sukat ay isinasagawa sa tatlong paraan:
- Paraan ng Cumene. Ang pamamaraang ito ay gumagawa ng higit sa 95% ng lahat ng phenol na ginawa sa mundo. Sa isang cascade ng bubble column, ang cumene ay sumasailalim sa non-catalytic oxidation sa pamamagitan ng hangin upang bumuo ng cumene hydroperoxide (CHP). Ang nagreresultang CHP, na na-catalyze ng sulfuric acid, ay nabubulok upang bumuo ng phenol at acetone. Bilang karagdagan, ang α-methylstyrene ay isang mahalagang by-product ng prosesong ito.
- Humigit-kumulang 3% ng kabuuang phenol ay nakuha sa pamamagitan ng oksihenasyon ng toluene, na may intermediate na pagbuo ng benzoic acid.
– Lahat ng iba pang phenol ay nakahiwalay sa coal tar.
4.1 Oxidation ng cumene
Ang mga phenol ay nakahiwalay sa coal tar, gayundin sa mga produktong pyrolysis ng brown coal at wood (tar). Ang pang-industriya na pamamaraan para sa paggawa ng phenol C6H5OH mismo ay batay sa oksihenasyon ng aromatic hydrocarbon cumene (isopropylbenzene) na may atmospheric oxygen, na sinusundan ng agnas ng nagresultang hydroperoxide na diluted na may H2SO4. Ang reaksyon ay nagpapatuloy na may mataas na ani at kaakit-akit dahil pinapayagan nito ang isa na makakuha ng dalawang teknikal na mahalagang produkto nang sabay-sabay - phenol at acetone. Ang isa pang paraan ay ang catalytic hydrolysis ng halogenated benzenes.

4.2 Paghahanda mula sa mga halobenzene
Kapag ang chlorobenzene at sodium hydroxide ay pinainit sa ilalim ng presyon, ang sodium phenolate ay nakuha, sa karagdagang pagproseso kung saan may acid, ang phenol ay nabuo:
С6Н5-CI + 2NaOH -> С6Н5-ONa + NaCl + Н2O
4.3 Paghahanda mula sa mga aromatic sulfonic acid
Ang reaksyon ay isinasagawa sa pamamagitan ng pagsasama ng mga sulfonic acid na may alkalis. Ang mga unang nabuong phenoxide ay ginagamot ng mga malakas na acid upang makakuha ng mga libreng phenol. Ang pamamaraan ay karaniwang ginagamit upang makakuha ng polyhydric phenols:

4.4 Paghahanda mula sa chlorobenzene
Ito ay kilala na ang chlorine atom ay mahigpit na nakagapos sa benzene ring, samakatuwid ang reaksyon ng pagpapalit ng chlorine sa isang hydroxyl group ay isinasagawa sa ilalim ng malupit na mga kondisyon (300 °C, presyon 200 MPa):
C6H5-Cl + NaOH – > C6H5-OH + NaCl
5. Paglalapat ng mga phenol
Ang isang phenol solution ay ginagamit bilang isang disinfectant (carbolic acid). Ang mga diatomic phenols - pyrocatechol, resorcinol (Larawan 3), pati na rin ang hydroquinone (para-dihydroxybenzene) ay ginagamit bilang antiseptics (antibacterial disinfectants), idinagdag sa mga tanning agent para sa katad at balahibo, bilang mga stabilizer para sa lubricating oils at goma, at gayundin para sa pagproseso ng mga photographic na materyales at bilang mga reagents sa analytical chemistry.
Ang mga phenol ay ginagamit sa isang limitadong lawak sa anyo ng mga indibidwal na compound, ngunit ang kanilang iba't ibang mga derivatives ay malawakang ginagamit. Ang mga phenol ay nagsisilbing panimulang mga compound para sa paggawa ng iba't ibang mga produkto ng polimer - phenolic resins, polyamides, polyepoxides. Maraming mga gamot ang nakuha mula sa mga phenol, halimbawa, aspirin, salol, phenolphthalein, bilang karagdagan, mga tina, pabango, plasticizer para sa mga polimer at mga produktong proteksyon ng halaman.
Ang pagkonsumo ng mundo ng phenol ay may sumusunod na istraktura:
· 44% ng phenol ay ginugol sa paggawa ng bisphenol A, na, naman, ay ginagamit para sa paggawa ng polycarbonate at epoxy resins;
· 30% ng phenol ay ginugugol sa paggawa ng phenol-formaldehyde resins;
· 12% ng phenol ay na-convert sa pamamagitan ng hydrogenation sa cyclohexanol, na ginagamit upang makabuo ng mga artipisyal na fibers - nylon at nylon;
· ang natitirang 14% ay ginugugol sa iba pang mga pangangailangan, kabilang ang produksyon ng mga antioxidant (ionol), nonionic surfactants - polyoxyethylated alkylphenols (neonols), iba pang phenols (cresols), gamot (aspirin), antiseptics (xeroform) at pestisidyo.
· 1.4% phenol ay ginagamit sa gamot (oracept) bilang isang analgesic at antiseptic.
6. Mga nakakalason na katangian
Ang phenol ay lason. Nagdudulot ng dysfunction ng nervous system. Ang alikabok, singaw at phenol solution ay nakakairita sa mga mucous membrane ng mata, respiratory tract, at balat (MPC 5 mg/m³, sa mga reservoir na 0.001 mg/l).
Resorcinum Resorcinum
m-Dioxybenzene
Ang Resorcinol ay isang diatomic phenol at lumilitaw bilang walang kulay o bahagyang kulay-rosas o dilaw na hugis ng karayom na kristal o mala-kristal na pulbos. Minsan ang kulay ng mga kristal ay halos kayumanggi. Ito ay dahil sa hindi tamang pag-iimbak ng resorcinol, na napakadaling mag-oxidize. Hindi tulad ng iba pang mga phenol, ang resorcinol ay madaling natutunaw sa tubig, alkohol, at madali sa eter. Natutunaw sa mataba na langis at gliserin. Mahirap matunaw sa chloroform. Kapag pinainit, ito ay ganap na sumingaw.
Ang Resorcinol ay isang mahalagang bahagi ng maraming resins at tannins, ngunit ito ay nakuha sa synthetically - mula sa benzene sa pamamagitan ng paraan ng sulfonation at alkaline melting. Ang Benzene ay ginagamot ng concentrated sulfuric acid upang makakuha ng benzene metadisulfonic acid I.
Pagkatapos ang pinaghalong reaksyon ay ginagamot ng dayap: ang sulfonic acid sa ilalim ng mga kondisyong ito ay bumubuo ng isang nalulusaw sa tubig na calcium salt (II), ang labis na sulfuric acid ay inalis sa anyo ng calcium sulfate:

Ang resultang resorcinol ay dinadalisay sa pamamagitan ng distillation.
Ang resorcinol, tulad ng iba pang mga phenol, ay madaling na-oxidized at mismo ay nagiging isang reducing agent. Maaari itong mabawi ang pilak mula sa ammonia solution ng silver nitrate.
Ibinibigay ng Resorcinol ang lahat ng mga reaksyon na katangian ng mga phenol, kabilang ang mga may formaldehyde-sulfuric acid (isang pulang precipitate na bumubuo sa ilalim ng test tube). Ang isang tiyak na reaksyon sa resorcinol, na nakikilala ito mula sa lahat ng iba pang mga phenol, ay ang reaksyon ng pagsasanib nito sa phthalic anhydride sa pagkakaroon ng puro sulfuric acid na may pagbuo ng fluorescein - isang dilaw-pula na solusyon na may berdeng fluorescence (reaksyon ng pharmacopoeial).

Ang antiseptikong epekto ng resorcinol ay mas malinaw kaysa sa monohydric phenol. Ito ay dahil sa mas malakas nitong restorative properties.
Ang pagbabawas ng kakayahan ng resorcinol ay lalong maliwanag sa isang alkaline na kapaligiran.
Ginagamit ito sa labas para sa mga sakit sa balat (eksema, fungal disease, atbp.) Sa anyo ng 2-5% na may tubig at mga solusyon sa alkohol at 5-10-20% na mga pamahid.
Mag-imbak sa mahusay na selyadong orange na garapon ng salamin (ilaw ay nagpapasigla sa oksihenasyon).
