730. Bakit ginagamit ang tubig upang palamig ang ilang mekanismo?
Ang tubig ay may mataas na tiyak na kapasidad ng init, na nag-aambag sa mahusay na pag-alis ng init mula sa mekanismo.
731. Sa anong kaso dapat gumamit ng mas maraming enerhiya: para sa pagpainit ng isang litro ng tubig ng 1 °C o para sa pagpainit ng isang daang gramo ng tubig ng 1 °C?
Upang magpainit ng isang litro ng tubig, dahil mas malaki ang masa, mas maraming enerhiya ang kailangang gastusin.
732. Ang mga cupronickel at pilak na tinidor ng parehong masa ay inilubog sa mainit na tubig. Pareho ba silang natatanggap ng init mula sa tubig?
Ang isang cupronickel fork ay makakatanggap ng higit na init, dahil ang tiyak na init ng cupronickel ay mas malaki kaysa sa pilak.
733. Ang isang piraso ng tingga at isang piraso ng cast iron ng parehong masa ay hinampas ng tatlong beses ng isang sledgehammer. Aling bahagi ang naging mas mainit?
Higit na mag-iinit ang tingga dahil ang tiyak na kapasidad ng init nito ay mas mababa kaysa sa cast iron, at mas kaunting enerhiya ang kailangan upang mapainit ang tingga.
734. Ang isang prasko ay naglalaman ng tubig, ang isa naman ay naglalaman ng kerosene ng parehong masa at temperatura. Ang isang pantay na pinainit na bakal na kubo ay itinapon sa bawat prasko. Ano ang magpapainit sa mas mataas na temperatura - tubig o kerosene?
Kerosene.
735. Bakit hindi gaanong matalas ang pagbabagu-bago ng temperatura sa taglamig at tag-araw sa mga lungsod sa baybayin kaysa sa mga lungsod na nasa loob ng bansa?
Ang tubig ay umiinit at lumalamig nang mas mabagal kaysa sa hangin. Sa taglamig, lumalamig ito at nagpapagalaw ng mainit na hangin sa lupa, na ginagawang mas mainit ang klima sa baybayin.
736. Ang tiyak na kapasidad ng init ng aluminyo ay 920 J/kg °C. Anong ibig sabihin nito?
Nangangahulugan ito na nangangailangan ng 920 J upang mapainit ang 1 kg ng aluminyo sa pamamagitan ng 1 °C.
737. Ang mga aluminyo at tansong bar na may parehong masa na 1 kg ay pinalamig ng 1 °C. Magkano ang magbabago ng panloob na enerhiya ng bawat bloke? Aling bar ang mas magbabago at kung magkano?
738. Anong halaga ng init ang kailangan upang mapainit ang isang kilo ng iron billet ng 45 °C?

739. Gaano karaming init ang kinakailangan upang magpainit ng 0.25 kg ng tubig mula 30°C hanggang 50°C?

740. Paano magbabago ang panloob na enerhiya ng dalawang litro ng tubig kapag pinainit ng 5 °C?

741. Gaano karaming init ang kailangan para magpainit ng 5 g ng tubig mula 20 °C hanggang 30 °C?
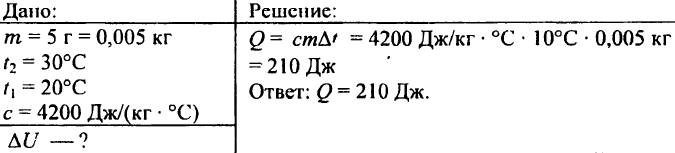
742. Anong dami ng init ang kailangan para magpainit ng aluminum ball na tumitimbang ng 0.03 kg ng 72 °C?

743. Kalkulahin ang dami ng init na kinakailangan upang magpainit ng 15 kg ng tanso ng 80 °C.
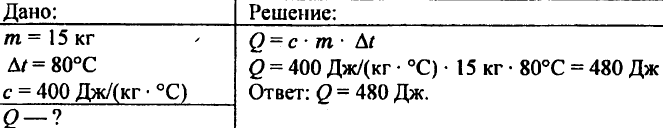
744. Kalkulahin ang dami ng init na kinakailangan upang magpainit ng 5 kg ng tanso mula 10 °C hanggang 200 °C.

745. Anong dami ng init ang kailangan para magpainit ng 0.2 kg ng tubig mula 15 °C hanggang 20 °C?

746. Ang tubig na tumitimbang ng 0.3 kg ay lumamig ng 20 °C. Gaano nababawasan ang panloob na enerhiya ng tubig?

747. Gaano karaming init ang kailangan para magpainit ng 0.4 kg ng tubig sa temperaturang 20 °C hanggang sa temperaturang 30 °C?

748. Magkano ang init na ginugugol sa pagpainit ng 2.5 kg ng tubig sa pamamagitan ng 20 °C?
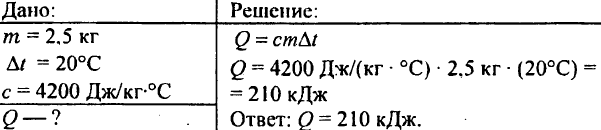
749. Gaano karaming init ang pinakawalan nang ang 250 g ng tubig ay lumamig mula 90 °C hanggang 40 °C?
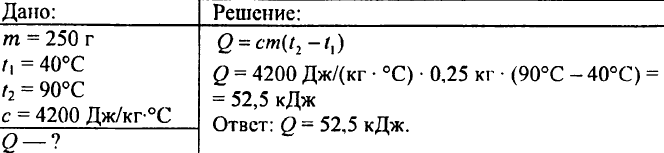
750. Anong halaga ng init ang kinakailangan upang magpainit ng 0.015 litro ng tubig sa pamamagitan ng 1 °C?

751. Kalkulahin ang dami ng init na kinakailangan upang magpainit ng isang lawa na may dami na 300 m3 ng 10 °C?
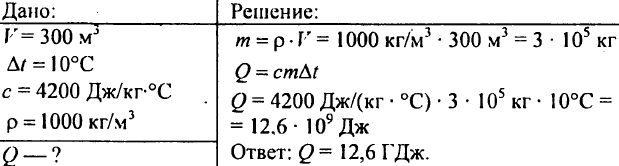
752. Gaano karaming init ang dapat ibigay sa 1 kg ng tubig upang mapataas ang temperatura nito mula 30°C hanggang 40°C?

753. Ang tubig na may dami na 10 litro ay lumamig mula sa temperaturang 100 °C hanggang sa temperaturang 40 °C. Gaano karaming init ang inilabas sa kasong ito?

754. Kalkulahin ang dami ng init na kinakailangan upang magpainit ng 1 m3 ng buhangin sa pamamagitan ng 60 °C.

755. Dami ng hangin 60 m3, tiyak na kapasidad ng init 1000 J/kg °C, air density 1.29 kg/m3. Gaano karaming init ang kailangan upang itaas ito sa 22°C?

756. Ang tubig ay pinainit ng 10 ° C, na gumagastos ng 4.20 103 J ng init. Tukuyin ang dami ng tubig.
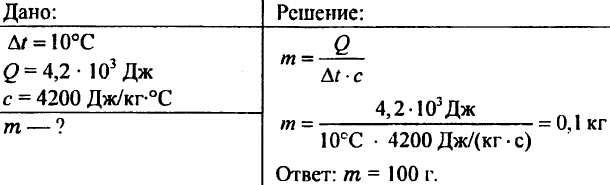
757. Ang tubig na tumitimbang ng 0.5 kg ay nag-ulat ng 20.95 kJ ng init. Ano ang temperatura ng tubig kung ang unang temperatura ng tubig ay 20°C?

758. 8 kg ng tubig sa 10 °C ay ibinuhos sa isang tansong kasirola na tumitimbang ng 2.5 kg. Gaano karaming init ang kailangan para kumulo ang tubig sa isang kasirola?

759. Ang isang litro ng tubig sa temperatura na 15 °C ay ibinubuhos sa isang tansong sandok na tumitimbang ng 300 g. Gaano karaming init ang kailangan upang mapainit ang tubig sa sandok ng 85 °C?

760. Ang isang piraso ng heated granite na tumitimbang ng 3 kg ay inilalagay sa tubig. Ang Granite ay naglilipat ng 12.6 kJ ng init sa tubig, na lumalamig ng 10 °C. Ano ang tiyak na kapasidad ng init ng bato?

761. Ang mainit na tubig sa 50°C ay idinagdag sa 5 kg ng tubig sa 12°C, na nakakuha ng pinaghalong may temperaturang 30°C. Gaano karaming tubig ang naidagdag?

762. Ang tubig sa 20°C ay idinagdag sa 3 litro ng tubig sa 60°C upang makakuha ng tubig sa 40°C. Gaano karaming tubig ang naidagdag?

763. Ano ang magiging temperatura ng pinaghalong kung ang 600 g ng tubig sa 80 °C ay ihalo sa 200 g ng tubig sa 20 °C?

764. Isang litro ng tubig sa 90°C ang ibinuhos sa tubig sa 10°C, at ang temperatura ng tubig ay naging 60°C. Gaano karaming malamig na tubig ang naroon?

765. Tukuyin kung gaano karaming mainit na tubig na pinainit hanggang 60°C ang dapat ibuhos sa isang sisidlan kung ang sisidlan ay naglalaman na ng 20 litro ng malamig na tubig sa temperatura na 15°C; ang temperatura ng pinaghalong ay dapat na 40 °C.

766. Tukuyin kung gaano karaming init ang kinakailangan upang magpainit ng 425 g ng tubig sa pamamagitan ng 20 °C.

767. Ilang degrees ang iinit ng 5 kg ng tubig kung ang tubig ay tumatanggap ng 167.2 kJ?

768. Gaano karaming init ang kinakailangan upang magpainit ng m gramo ng tubig sa temperaturang t1 hanggang sa temperaturang t2?
769. Ang 2 kg ng tubig ay ibinubuhos sa isang calorimeter sa temperatura na 15 °C. Sa anong temperatura magpapainit ang tubig ng calorimeter kung ang isang tansong timbang na 500 g na pinainit hanggang 100 °C ay ibababa dito? Ang tiyak na kapasidad ng init ng tanso ay 0.37 kJ/(kg °C).
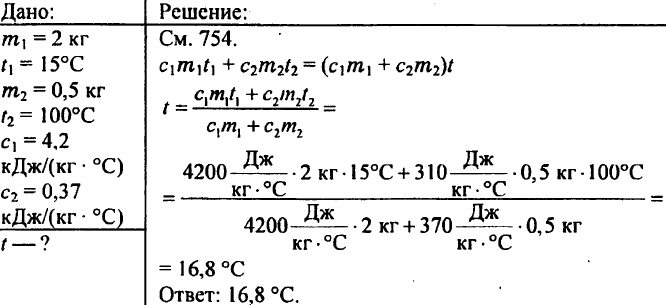
770. May mga piraso ng tanso, lata at aluminyo ng parehong dami. Alin sa mga pirasong ito ang may pinakamalaki at alin ang pinakamaliit na kapasidad ng init?

771. 450 g ng tubig, ang temperatura kung saan ay 20 °C, ay ibinuhos sa calorimeter. Kapag ang 200 g ng iron filing na pinainit hanggang 100°C ay inilubog sa tubig na ito, ang temperatura ng tubig ay naging 24°C. Tukuyin ang tiyak na kapasidad ng init ng sawdust.

772. Ang isang tansong calorimeter na tumitimbang ng 100 g ay nagtataglay ng 738 g ng tubig, na ang temperatura ay 15 °C. Ang 200 g ng tanso ay ibinaba sa calorimeter na ito sa temperatura na 100 °C, pagkatapos nito ang temperatura ng calorimeter ay tumaas sa 17 °C. Ano ang tiyak na kapasidad ng init ng tanso?

773. Ang isang bolang bakal na tumitimbang ng 10 g ay inilabas mula sa hurno at ibinaba sa tubig sa temperatura na 10 °C. Ang temperatura ng tubig ay tumaas hanggang 25°C. Ano ang temperatura ng bola sa oven kung ang masa ng tubig ay 50 g? Ang tiyak na kapasidad ng init ng bakal ay 0.5 kJ/(kg °C).

777. Ang 50 g ng tubig sa 19 °C ay ibinubuhos sa tubig na tumitimbang ng 150 g sa temperatura na 35 °C. Ano ang temperatura ng pinaghalong?

778. Ang tubig na tumitimbang ng 5 kg sa 90 °C ay ibinuhos sa isang cast-iron kettle na tumitimbang ng 2 kg sa temperatura na 10 °C. Ano ang temperatura ng tubig?

779. Ang isang bakal na pait na tumitimbang ng 2 kg ay pinainit sa temperatura na 800 °C at pagkatapos ay ibinaba sa isang sisidlan na naglalaman ng 15 litro ng tubig sa temperatura na 10 °C. Sa anong temperatura papainitin ang tubig sa sisidlan?

(Indikasyon. Upang malutas ang problemang ito, kinakailangan na lumikha ng isang equation kung saan ang nais na temperatura ng tubig sa sisidlan pagkatapos ibaba ang cutter ay kinuha bilang hindi alam.)
780. Anong temperatura ang makukuha ng tubig kung paghaluin mo ang 0.02 kg ng tubig sa 15 °C, 0.03 kg ng tubig sa 25 °C, at 0.01 kg ng tubig sa 60 °C?
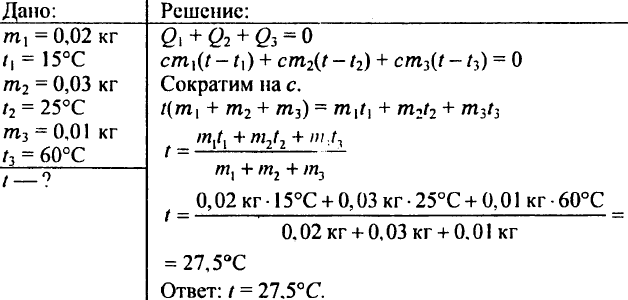
781. Ang pag-init ng isang well-ventilated na klase ay nangangailangan ng halaga ng init na 4.19 MJ bawat oras. Ang tubig ay pumapasok sa mga heating radiator sa 80°C at lumalabas sa 72°C. Gaano karaming tubig ang dapat ibigay sa mga radiator bawat oras?

782. Ang tingga na tumitimbang ng 0.1 kg sa temperatura na 100 °C ay inilubog sa isang aluminum calorimeter na tumitimbang ng 0.04 kg na naglalaman ng 0.24 kg ng tubig sa temperatura na 15 °C. Pagkatapos nito, ang temperatura ng 16 °C ay itinatag sa calorimeter. Ano ang tiyak na kapasidad ng init ng tingga?

Ano ang mas mabilis uminit sa kalan - isang takure o isang balde ng tubig? Ang sagot ay halata - isang takure. At ang pangalawang tanong ay bakit?
Ang sagot ay hindi gaanong halata - dahil ang masa ng tubig sa takure ay mas mababa. Magaling. At ngayon ay maaari mong gawin ang pinaka-tunay na pisikal na karanasan sa iyong sarili sa bahay. Upang gawin ito, kakailanganin mo ng dalawang magkaparehong maliliit na kasirola, isang pantay na dami ng tubig at langis ng gulay, halimbawa, kalahating litro bawat isa at isang kalan. Maglagay ng mga kaldero ng mantika at tubig sa iisang apoy. At ngayon panoorin mo na lang kung ano ang mas mabilis uminit. Kung mayroong thermometer para sa mga likido, maaari mo itong gamitin, kung hindi, maaari mo lamang subukan ang temperatura paminsan-minsan gamit ang iyong daliri, mag-ingat lamang na huwag masunog ang iyong sarili. Sa anumang kaso, makikita mo sa lalong madaling panahon na ang langis ay uminit nang mas mabilis kaysa sa tubig. At isa pang tanong, na maaari ding ipatupad sa anyo ng karanasan. Alin ang mas mabilis na kumukulo - mainit na tubig o malamig? Ang lahat ay halata muli - ang mainit ay ang unang matatapos. Bakit lahat ng mga kakaibang tanong at eksperimento na ito? Upang matukoy ang pisikal na dami na tinatawag na "ang dami ng init."
Dami ng init
Ang dami ng init ay ang enerhiya na nawawala o nakukuha ng katawan sa panahon ng paglipat ng init. Ito ay malinaw sa pangalan. Kapag lumalamig, ang katawan ay mawawalan ng isang tiyak na halaga ng init, at kapag pinainit, ito ay sumisipsip. At ipinakita sa amin ang mga sagot sa aming mga tanong ano ang nakasalalay sa dami ng init? Una, mas malaki ang masa ng katawan, mas malaki ang halaga ng init na dapat ibuhos upang mabago ang temperatura nito ng isang degree. Pangalawa, ang dami ng init na kinakailangan upang magpainit ng katawan ay depende sa sangkap kung saan ito binubuo, iyon ay, sa uri ng sangkap. At pangatlo, ang pagkakaiba sa temperatura ng katawan bago at pagkatapos ng paglipat ng init ay mahalaga din para sa ating mga kalkulasyon. Batay sa nabanggit, kaya natin matukoy ang dami ng init sa pamamagitan ng formula:
Q=cm(t_2-t_1) ,
kung saan ang Q ay ang dami ng init,
m - timbang ng katawan,
(t_2-t_1) - ang pagkakaiba sa pagitan ng una at huling temperatura ng katawan,
c - tiyak na kapasidad ng init ng sangkap, ay matatagpuan mula sa mga nauugnay na talahanayan.
Gamit ang formula na ito, maaari mong kalkulahin ang dami ng init na kinakailangan upang mapainit ang anumang katawan o ang ilalabas ng katawan na ito kapag lumamig ito.
Ang dami ng init ay sinusukat sa joules (1 J), tulad ng anumang iba pang anyo ng enerhiya. Gayunpaman, ang halagang ito ay ipinakilala hindi pa katagal, at ang mga tao ay nagsimulang sukatin ang dami ng init nang mas maaga. At gumamit sila ng isang yunit na malawakang ginagamit sa ating panahon - isang calorie (1 cal). Ang 1 calorie ay ang dami ng init na kinakailangan upang itaas ang temperatura ng 1 gramo ng tubig ng 1 degree Celsius. Ginagabayan ng mga datos na ito, ang mga mahilig sa pagbibilang ng mga calorie sa pagkain na kanilang kinakain ay maaaring, para sa interes, kalkulahin kung gaano karaming litro ng tubig ang maaaring pakuluan gamit ang enerhiya na kanilang kinakain sa araw.
Ang pagbabago sa panloob na enerhiya sa pamamagitan ng paggawa ng trabaho ay nailalarawan sa dami ng trabaho, i.e. ang trabaho ay isang sukatan ng pagbabago sa panloob na enerhiya sa isang naibigay na proseso. Ang pagbabago sa panloob na enerhiya ng isang katawan sa panahon ng paglipat ng init ay nailalarawan sa pamamagitan ng isang dami na tinatawag na dami ng init.
ay ang pagbabago sa panloob na enerhiya ng katawan sa proseso ng paglipat ng init nang hindi gumagawa ng trabaho. Ang dami ng init ay tinutukoy ng titik Q .
Ang trabaho, panloob na enerhiya at ang dami ng init ay sinusukat sa parehong mga yunit - joules ( J), tulad ng anumang iba pang anyo ng enerhiya.
Sa mga thermal measurements, isang espesyal na yunit ng enerhiya, ang calorie ( dumi), katumbas ng ang halaga ng init na kinakailangan upang itaas ang temperatura ng 1 gramo ng tubig ng 1 degree Celsius (mas tiyak, mula 19.5 hanggang 20.5 ° C). Ang yunit na ito, sa partikular, ay kasalukuyang ginagamit sa pagkalkula ng pagkonsumo ng init (thermal energy) sa mga gusali ng apartment. Empirically, ang mekanikal na katumbas ng init ay naitatag - ang ratio sa pagitan ng mga calorie at joules: 1 cal = 4.2 J.

Kapag ang isang katawan ay naglilipat ng isang tiyak na halaga ng init nang hindi gumagawa ng trabaho, ang panloob na enerhiya nito ay tumataas, kung ang isang katawan ay naglalabas ng isang tiyak na halaga ng init, ang panloob na enerhiya nito ay bumababa.
Kung ibubuhos mo ang 100 g ng tubig sa dalawang magkatulad na sisidlan, at 400 g sa isa pa sa parehong temperatura at ilagay ang mga ito sa parehong mga burner, kung gayon ang tubig sa unang sisidlan ay kumukulo nang mas maaga. Kaya, mas malaki ang masa ng katawan, mas malaki ang dami ng init na kailangan nito upang uminit. Ang parehong napupunta para sa paglamig.

Ang dami ng init na kinakailangan upang magpainit ng katawan ay depende rin sa uri ng sangkap kung saan ginawa ang katawan na ito. Ang pag-asa na ito ng dami ng init na kinakailangan upang mapainit ang katawan sa uri ng sangkap ay nailalarawan sa pamamagitan ng pisikal na dami na tinatawag na tiyak na kapasidad ng init mga sangkap.
- ito ay isang pisikal na dami na katumbas ng dami ng init na dapat iulat sa 1 kg ng isang sangkap upang mapainit ito ng 1 ° C (o 1 K). Ang parehong dami ng init ay ibinibigay ng 1 kg ng isang sangkap kapag pinalamig ng 1 °C.
Ang tiyak na kapasidad ng init ay tinutukoy ng titik Sa. Ang yunit ng tiyak na kapasidad ng init ay 1 J/kg °C o 1 J/kg °K.
Ang mga halaga ng tiyak na kapasidad ng init ng mga sangkap ay tinutukoy sa eksperimento. Ang mga likido ay may mas mataas na tiyak na kapasidad ng init kaysa sa mga metal; Ang tubig ay may pinakamataas na tiyak na kapasidad ng init, ang ginto ay may napakaliit na tiyak na kapasidad ng init.
Dahil ang halaga ng init ay katumbas ng pagbabago sa panloob na enerhiya ng katawan, maaari nating sabihin na ang tiyak na kapasidad ng init ay nagpapakita kung gaano kalaki ang pagbabago ng panloob na enerhiya. 1 kg sangkap kapag nagbabago ang temperatura nito 1 °C. Sa partikular, ang panloob na enerhiya ng 1 kg ng tingga, kapag pinainit ito ng 1 °C, ay tumataas ng 140 J, at kapag ito ay pinalamig, bumababa ito ng 140 J.
Q kinakailangan upang mapainit ang masa ng katawan m temperatura t 1 °С hanggang sa temperatura t 2 °С, ay katumbas ng produkto ng tiyak na kapasidad ng init ng sangkap, mass ng katawan at ang pagkakaiba sa pagitan ng pangwakas at paunang temperatura, i.e.Q \u003d c ∙ m (t 2 - t 1)
Ayon sa parehong formula, ang dami ng init na ibinibigay ng katawan kapag pinalamig ay kinakalkula din. Sa kasong ito lamang dapat ibawas ang panghuling temperatura mula sa paunang temperatura, i.e. Ibawas ang mas maliit na temperatura mula sa mas malaking temperatura.

Ito ay isang buod sa paksa. "Ang dami ng init. Tiyak na init". Piliin ang mga susunod na hakbang:
- Pumunta sa susunod na abstract:
« Physics - Grade 10"
Sa anong mga proseso nangyayari ang pinagsama-samang pagbabago ng bagay?
Paano mababago ang estado ng bagay?
Maaari mong baguhin ang panloob na enerhiya ng anumang katawan sa pamamagitan ng paggawa, pag-init o, kabaligtaran, paglamig nito.
Kaya, kapag nagpapanday ng isang metal, ang trabaho ay tapos na at ito ay pinainit, habang sa parehong oras ang metal ay maaaring pinainit sa isang nasusunog na apoy.
Gayundin, kung ang piston ay naayos (Larawan 13.5), kung gayon ang dami ng gas ay hindi nagbabago kapag pinainit at walang gawaing ginagawa. Ngunit ang temperatura ng gas, at samakatuwid ang panloob na enerhiya nito, ay tumataas.
Ang panloob na enerhiya ay maaaring tumaas at bumaba, kaya ang dami ng init ay maaaring maging positibo o negatibo.
Ang proseso ng paglilipat ng enerhiya mula sa isang katawan patungo sa isa pa nang hindi gumagawa ng trabaho ay tinatawag pagpapalitan ng init.
Ang quantitative measure ng pagbabago sa panloob na enerhiya sa panahon ng paglipat ng init ay tinatawag dami ng init.
Molekular na larawan ng paglipat ng init.
Sa panahon ng pagpapalitan ng init sa hangganan sa pagitan ng mga katawan, ang dahan-dahang gumagalaw na mga molekula ng isang malamig na katawan ay nakikipag-ugnayan sa mabilis na gumagalaw na mga molekula ng isang mainit na katawan. Bilang resulta, ang mga kinetic energies ng mga molekula ay equalized at ang mga bilis ng mga molekula ng isang malamig na katawan ay tumataas, habang ang mga sa isang mainit na katawan ay bumababa.
Sa panahon ng pagpapalitan ng init, walang pagbabago ng enerhiya mula sa isang anyo patungo sa isa pa; bahagi ng panloob na enerhiya ng isang mas mainit na katawan ay inililipat sa isang hindi gaanong pinainit na katawan.
Ang dami ng init at kapasidad ng init.
Alam mo na upang mapainit ang isang katawan na may mass m mula sa temperatura t 1 hanggang sa temperatura t 2, kinakailangang ilipat dito ang dami ng init:
Q \u003d cm (t 2 - t 1) \u003d cm Δt. (13.5)
Kapag ang katawan ay lumamig, ang huling temperatura nito t 2 ay lumalabas na mas mababa sa paunang temperatura t 1 at ang dami ng init na ibinibigay ng katawan ay negatibo.
Ang coefficient c sa formula (13.5) ay tinatawag tiyak na kapasidad ng init mga sangkap.
Tiyak na init- ito ay isang halaga ayon sa numero na katumbas ng dami ng init na natatanggap o ibinibigay ng isang substance na may mass na 1 kg kapag nagbago ang temperatura nito ng 1 K.
Ang tiyak na kapasidad ng init ng mga gas ay nakasalalay sa proseso kung saan inililipat ang init. Kung magpapainit ka ng gas sa pare-parehong presyon, lalawak ito at gagana. Upang magpainit ng gas ng 1 °C sa pare-parehong presyon, kailangan nitong maglipat ng mas maraming init kaysa sa painitin ito sa pare-parehong volume, kapag ang gas ay magpapainit lamang.
Ang mga likido at solid ay bahagyang lumalawak kapag pinainit. Ang kanilang mga tiyak na kapasidad ng init sa pare-pareho ang dami at pare-pareho ang presyon ay naiiba nang kaunti.
Tiyak na init ng singaw.
Upang i-convert ang isang likido sa singaw sa panahon ng proseso ng kumukulo, kinakailangan upang ilipat ang isang tiyak na halaga ng init dito. Ang temperatura ng isang likido ay hindi nagbabago kapag kumukulo ito. Ang pagbabagong-anyo ng likido sa singaw sa isang pare-parehong temperatura ay hindi humantong sa isang pagtaas sa kinetic energy ng mga molekula, ngunit sinamahan ng isang pagtaas sa potensyal na enerhiya ng kanilang pakikipag-ugnayan. Pagkatapos ng lahat, ang average na distansya sa pagitan ng mga molekula ng gas ay mas malaki kaysa sa pagitan ng mga likidong molekula.
Ang halaga na katumbas ng numero sa dami ng init na kinakailangan upang mai-convert ang isang 1 kg na likido sa singaw sa isang pare-parehong temperatura ay tinatawag tiyak na init ng singaw.
Ang proseso ng pagsingaw ng likido ay nangyayari sa anumang temperatura, habang ang pinakamabilis na molekula ay umalis sa likido, at ito ay lumalamig sa panahon ng pagsingaw. Ang tiyak na init ng singaw ay katumbas ng tiyak na init ng singaw.
Ang halagang ito ay tinutukoy ng letrang r at ipinahayag sa joules bawat kilo (J / kg).
Ang tiyak na init ng singaw ng tubig ay napakataas: r H20 = 2.256 10 6 J/kg sa temperatura na 100 °C. Sa iba pang mga likido, tulad ng alkohol, eter, mercury, kerosene, ang tiyak na init ng singaw ay 3-10 beses na mas mababa kaysa sa tubig.
Upang i-convert ang isang likido na mass m sa singaw, ang halaga ng init ay kinakailangan katumbas ng:
Q p \u003d rm. (13.6)
Kapag ang singaw ay namumuo, ang parehong dami ng init ay inilabas:
Q k \u003d -rm. (13.7)
Tiyak na init ng pagsasanib.
Kapag ang isang mala-kristal na katawan ay natutunaw, ang lahat ng init na ibinibigay dito ay napupunta upang mapataas ang potensyal na enerhiya ng pakikipag-ugnayan ng mga molekula. Ang kinetic energy ng mga molekula ay hindi nagbabago, dahil ang pagkatunaw ay nangyayari sa isang pare-parehong temperatura.
Ang halaga na katumbas ng numero sa dami ng init na kinakailangan upang baguhin ang isang mala-kristal na substansiya na tumitimbang ng 1 kg sa isang punto ng pagkatunaw sa isang likido ay tinatawag tiyak na init ng pagsasanib at ipinapahiwatig ng titik λ.
Sa panahon ng pagkikristal ng isang sangkap na may mass na 1 kg, eksaktong kaparehong dami ng init na inilalabas bilang nasisipsip sa panahon ng pagkatunaw.
Ang tiyak na init ng pagkatunaw ng yelo ay medyo mataas: 3.34 10 5 J/kg.
"Kung ang yelo ay walang mataas na init ng pagsasanib, kung gayon sa tagsibol ang buong masa ng yelo ay kailangang matunaw sa loob ng ilang minuto o segundo, dahil ang init ay patuloy na inililipat sa yelo mula sa hangin. Ang mga kahihinatnan nito ay magiging kakila-kilabot; sapagkat kahit sa ilalim ng kasalukuyang sitwasyon ay nagmumula ang malalaking baha at malalaking agos ng tubig mula sa pagkatunaw ng malalaking masa ng yelo o niyebe.” R. Black, ika-18 siglo
Upang matunaw ang isang mala-kristal na katawan ng mass m, isang halaga ng init ay kinakailangan katumbas ng:
Qpl \u003d λm. (13.8)
Ang dami ng init na inilabas sa panahon ng crystallization ng katawan ay katumbas ng:
Q cr = -λm (13.9)
Equation ng balanse ng init.
Isaalang-alang ang pagpapalitan ng init sa loob ng isang sistema na binubuo ng ilang katawan na sa simula ay may magkakaibang temperatura, halimbawa, pagpapalitan ng init sa pagitan ng tubig sa isang sisidlan at isang mainit na bolang bakal na ibinaba sa tubig. Ayon sa batas ng konserbasyon ng enerhiya, ang dami ng init na ibinibigay ng isang katawan ay ayon sa bilang na katumbas ng dami ng init na natanggap ng isa pa.
Ang ibinigay na halaga ng init ay itinuturing na negatibo, ang natanggap na halaga ng init ay itinuturing na positibo. Samakatuwid, ang kabuuang halaga ng init Q1 + Q2 = 0.
Kung ang pagpapalitan ng init ay nangyayari sa pagitan ng ilang mga katawan sa isang nakahiwalay na sistema, kung gayon
Q 1 + Q 2 + Q 3 + ... = 0. (13.10)
Ang equation (13.10) ay tinatawag equation ng balanse ng init.
Dito Q 1 Q 2 , Q 3 - ang dami ng init na natanggap o binigay ng mga katawan. Ang mga dami ng init na ito ay ipinahayag sa pamamagitan ng formula (13.5) o mga formula (13.6) - (13.9), kung ang iba't ibang mga pagbabagong bahagi ng sangkap ay nangyayari sa proseso ng paglipat ng init (pagtunaw, pagkikristal, singaw, paghalay).
Maaari mong baguhin ang panloob na enerhiya ng gas sa silindro hindi lamang sa pamamagitan ng paggawa, kundi pati na rin sa pag-init ng gas (Larawan 43). Kung ang piston ay naayos, kung gayon ang dami ng gas ay hindi magbabago, ngunit ang temperatura, at samakatuwid ang panloob na enerhiya, ay tataas.
Ang proseso ng paglilipat ng enerhiya mula sa isang katawan patungo sa isa pa nang hindi gumagawa ng trabaho ay tinatawag na heat transfer o heat transfer.
Ang enerhiya na inilipat sa katawan bilang resulta ng paglipat ng init ay tinatawag na dami ng init. Ang dami ng init ay tinatawag ding enerhiya na ibinibigay ng katawan sa proseso ng paglipat ng init.
Molekular na larawan ng paglipat ng init. Sa panahon ng pagpapalitan ng init sa hangganan sa pagitan ng mga katawan, ang dahan-dahang gumagalaw na mga molekula ng isang malamig na katawan ay nakikipag-ugnayan sa mas mabilis na gumagalaw na mga molekula ng isang mainit na katawan. Bilang isang resulta, ang kinetic energies
ang mga molekula ay nakahanay at ang mga bilis ng mga molekula ng isang malamig na katawan ay tumataas, at ang mga sa isang mainit ay bumababa.
Sa panahon ng pagpapalitan ng init, walang pagbabago ng enerhiya mula sa isang anyo patungo sa isa pa: bahagi ng panloob na enerhiya ng isang mainit na katawan ay inililipat sa isang malamig na katawan.
Ang dami ng init at kapasidad ng init. Mula sa kursong pisika ng klase VII, alam na upang mapainit ang isang katawan na may masa mula sa temperatura hanggang sa temperatura, kinakailangang ipaalam ito sa dami ng init.
![]()
Kapag ang katawan ay lumalamig, ang huling temperatura nito ay mas mababa kaysa sa una at ang dami ng init na ibinibigay ng katawan ay negatibo.
Ang coefficient c sa formula (4.5) ay tinatawag na tiyak na kapasidad ng init. Ang tiyak na kapasidad ng init ay ang dami ng init na natatanggap o ibinibigay ng 1 kg ng isang sangkap kapag nagbago ang temperatura nito ng 1 K -
Ang partikular na kapasidad ng init ay ipinahayag sa joules bawat kilo beses ng kelvin. Ang iba't ibang mga katawan ay nangangailangan ng hindi pantay na dami ng enerhiya upang mapataas ang temperatura ng I K. Kaya, ang tiyak na kapasidad ng init ng tubig at tanso
Ang tiyak na kapasidad ng init ay nakasalalay hindi lamang sa mga katangian ng sangkap, kundi pati na rin sa proseso kung saan nagaganap ang paglipat ng init. Upang magpainit ng gas ng 1 °C sa pare-parehong presyon, kakailanganin nitong maglipat ng mas maraming init kaysa sa painitin ito sa pare-parehong volume.
Ang mga likido at solid ay lumalawak nang bahagya kapag pinainit, at ang kanilang mga tiyak na kapasidad ng init sa pare-parehong dami at pare-parehong presyon ay bahagyang naiiba.
Tiyak na init ng singaw. Upang ma-convert ang isang likido sa singaw, ang isang tiyak na halaga ng init ay dapat ilipat dito. Ang temperatura ng likido ay hindi nagbabago sa panahon ng pagbabagong ito. Ang pagbabagong-anyo ng likido sa singaw sa isang pare-parehong temperatura ay hindi humantong sa isang pagtaas sa kinetic energy ng mga molekula, ngunit sinamahan ng isang pagtaas sa kanilang potensyal na enerhiya. Pagkatapos ng lahat, ang average na distansya sa pagitan ng mga molekula ng gas ay maraming beses na mas malaki kaysa sa pagitan ng mga likidong molekula. Bilang karagdagan, ang pagtaas ng lakas ng tunog sa panahon ng paglipat ng isang sangkap mula sa isang likido patungo sa isang gas na estado ay nangangailangan ng trabaho upang maisagawa laban sa mga puwersa ng panlabas na presyon.
Ang halaga ng init na kinakailangan upang gawing singaw ang 1 kg ng likido sa pare-parehong temperatura ay tinatawag
tiyak na init ng singaw. Ang halagang ito ay tinutukoy ng isang titik at ipinahayag sa joules bawat kilo.
Ang tiyak na init ng singaw ng tubig ay napakataas: sa temperatura na 100°C. Para sa iba pang mga likido (alkohol, eter, mercury, kerosene, atbp.), ang tiyak na init ng singaw ay 3-10 beses na mas mababa.
Upang gawing singaw ang isang likidong masa ay nangangailangan ng halaga ng init na katumbas ng:
Kapag ang singaw ay namumuo, ang parehong dami ng init ay inilabas:
Tiyak na init ng pagsasanib. Kapag ang isang mala-kristal na katawan ay natutunaw, ang lahat ng init na ibinibigay dito ay napupunta upang mapataas ang potensyal na enerhiya ng mga molekula. Ang kinetic energy ng mga molekula ay hindi nagbabago, dahil ang pagkatunaw ay nangyayari sa isang pare-parehong temperatura.
Ang halaga ng init A na kinakailangan upang ma-convert ang 1 kg ng isang mala-kristal na substansiya sa punto ng pagkatunaw sa isang likido ng parehong temperatura ay tinatawag na tiyak na init ng pagsasanib.
Sa panahon ng pagkikristal ng 1 kg ng isang sangkap, eksaktong kaparehong dami ng init ang inilalabas. Ang tiyak na init ng pagkatunaw ng yelo ay medyo mataas:
Upang matunaw ang isang mala-kristal na katawan na may masa, isang halaga ng init ay kinakailangan katumbas ng:
Ang dami ng init na inilabas sa panahon ng crystallization ng katawan ay katumbas ng:
1. Ano ang tinatawag na dami ng init? 2. Ano ang tumutukoy sa tiyak na kapasidad ng init ng mga sangkap? 3. Ano ang tinatawag na tiyak na init ng singaw? 4. Ano ang tinatawag na tiyak na init ng pagsasanib? 5. Sa anong mga kaso negatibo ang dami ng inilipat na init?
