យើងធ្វើបទបង្ហាញជូនលោកអ្នកនូវមេរៀនវីដេអូមួយស្តីពីប្រធានបទ "លក្ខណៈសម្បត្តិគីមីនៃ benzene"។ ដោយប្រើវីដេអូនេះ អ្នកអាចទទួលបានគំនិតអំពីលក្ខណៈសម្បត្តិគីមីនៃ benzene ក៏ដូចជាលក្ខខណ្ឌដ៏អាក្រក់ដែលតម្រូវឱ្យ benzene ប្រតិកម្មជាមួយសារធាតុផ្សេងទៀត។
ប្រធានបទ៖អ៊ីដ្រូកាបូនក្រអូប
មេរៀន៖លក្ខណៈសម្បត្តិគីមីនៃ benzene
អង្ករ។ 1. ម៉ូលេគុល Benzene
ការបំបែកពពក p-electron នៅក្នុងម៉ូលេគុល benzene គឺពិបាកណាស់។ ដូច្នេះ benzene ចូលទៅក្នុងប្រតិកម្មគីមីតិចជាងយ៉ាងសកម្មជាងសមាសធាតុ unsaturated ។


ដើម្បីឱ្យ benzene ចូលទៅក្នុងប្រតិកម្មគីមី លក្ខខណ្ឌដ៏អាក្រក់គឺចាំបាច់: សីតុណ្ហភាពកើនឡើង ហើយក្នុងករណីជាច្រើនមានកាតាលីករ។ នៅក្នុងប្រតិកម្មភាគច្រើន ចិញ្ចៀន benzene ស្ថេរភាពត្រូវបានរក្សាទុក។
1. ប្រូមូន។

កាតាលីករ (ដែក (III) ឬអាលុយមីញ៉ូមប្រូម) ត្រូវបានទាមទារ ហើយសូម្បីតែបរិមាណទឹកតិចតួចក៏មិនត្រូវអនុញ្ញាតឱ្យចូលដែរ។ តួនាទីរបស់កាតាលីករគឺថាម៉ូលេគុល bromine ត្រូវបានទាក់ទាញដោយអាតូម bromine មួយទៅកាន់អាតូមដែក។ ជាលទ្ធផលវា polarizes - គូនៃចំណងអេឡិចត្រុងឆ្លងកាត់ទៅអាតូម bromine ដែលត្រូវបានផ្សារភ្ជាប់ជាមួយនឹងជាតិដែក:
Br+…. Br - FeBr 3 ។
Br+ គឺជាអេឡិចត្រូហ្វីលដ៏រឹងមាំ។ វាត្រូវបានទាក់ទាញទៅពពកអេឡិចត្រុងប្រាំមួយនៃចិញ្ចៀន benzene ហើយបំបែកវាបង្កើតជាចំណង covalent ជាមួយអាតូមកាបូន៖
សារធាតុ bromine anion អាចចូលរួមជាមួយ cation លទ្ធផល។ ប៉ុន្តែការកាត់បន្ថយប្រព័ន្ធក្លិនបិដោរនៃចិញ្ចៀន benzene មានថាមពលអំណោយផលជាងការបន្ថែមនៃ bromine anion ។ ដូច្នេះ ម៉ូលេគុលចូលទៅក្នុងស្ថានភាពស្ថិរភាព ដោយបញ្ចេញអ៊ីយ៉ុងអ៊ីដ្រូសែន៖
រាល់ប្រតិកម្មជំនួសអេឡិចត្រូហ្វីលីកនៅក្នុងរង្វង់ benzene ដំណើរការទៅតាមយន្តការស្រដៀងគ្នា។
2. នីត្រាត

Benzene និងលក្ខណៈដូចគ្នារបស់វាមានប្រតិកម្មជាមួយនឹងល្បាយនៃអាស៊ីតស៊ុលហ្វួរិក និងអាស៊ីតនីទ្រីក (ល្បាយនីត្រាត)។ នៅក្នុងល្បាយនីត្រាត ក្នុងលំនឹង មាននីត្រូនីញ៉ូមអ៊ីយ៉ុង NO 2 + ដែលជាអេឡិចត្រូហ្វីល៖

3. ស៊ុលហ្វាន។
Benzene និង arenes ផ្សេងទៀត នៅពេលដែលកំដៅ ប្រតិកម្មជាមួយនឹងអាស៊ីតស៊ុលហ្វួរីក ឬ oleum ប្រមូលផ្តុំ - ដំណោះស្រាយនៃ SO 3 នៅក្នុងអាស៊ីតស៊ុលហ្វួរីក៖

4 . Friedel-Crafts Alkylation
5. Alkylation ជាមួយ alkenes

ប្រតិកម្មទាំងនេះមិនអំណោយផលខ្លាំងទេ ដូច្នេះវាដំណើរការតែនៅពេលដែលត្រូវកម្ដៅ ឬបញ្ចេញកាំរស្មី។
1. អ៊ីដ្រូសែន។
នៅពេលដែលកំដៅ សម្ពាធកើនឡើង និងនៅក្នុងវត្តមាននៃកាតាលីករ Ni, Pt, ឬ Pd, benzene និង arenes ផ្សេងទៀតបន្ថែមអ៊ីដ្រូសែនដើម្បីបង្កើតជា cyclohexane:

2. chlorination នៃ benzene ។
នៅក្រោមសកម្មភាពនៃវិទ្យុសកម្មអ៊ុលត្រាវីយូឡេ benzene បន្ថែមក្លរីន។ ប្រសិនបើដបកែវរ៉ែថ្មខៀវដែលមានដំណោះស្រាយក្លរីននៅក្នុង benzene ត្រូវបានប៉ះពាល់នឹងពន្លឺព្រះអាទិត្យ ដំណោះស្រាយនឹងប្រែពណ៌យ៉ាងឆាប់រហ័ស ក្លរីននឹងផ្សំជាមួយ benzene ដើម្បីបង្កើតជា 1,2,3,4,5,6-hexachlorocyclohexane ដែលត្រូវបានគេស្គាល់ថាជា hexachlorane(ពីមុនប្រើជាថ្នាំសំលាប់មេរោគ)៖

3. ការដុត benzene.
មិនដូចអាល់កានទេ អណ្ដាតភ្លើងនៃ benzene និងអ៊ីដ្រូកាបូនក្រអូបផ្សេងទៀតគឺភ្លឺ និងមានផ្សែង។
សង្ខេបមេរៀន
នៅក្នុងមេរៀននេះ អ្នកបានសិក្សាលើប្រធានបទ "លក្ខណៈសម្បត្តិគីមីនៃ Benzene" ។ ដោយប្រើសម្ភារៈនេះ អ្នកអាចទទួលបានគំនិតអំពីលក្ខណៈសម្បត្តិគីមីនៃ benzene ក៏ដូចជាលក្ខខណ្ឌដ៏អាក្រក់ដែលតម្រូវឱ្យ benzene ធ្វើប្រតិកម្មជាមួយសារធាតុផ្សេងទៀត។
គន្ថនិទ្ទេស
1. Rudzitis G.E. គីមីវិទ្យា។ មូលដ្ឋានគ្រឹះនៃគីមីវិទ្យាទូទៅ។ ថ្នាក់ទី១០៖ សៀវភៅសិក្សាសម្រាប់ស្ថាប័នអប់រំ៖ កម្រិតមូលដ្ឋាន / G.E. Rudzitis, F.G. Feldman ។ - បោះពុម្ពលើកទី ១៤ ។ - M. : ការអប់រំ, 2012 ។
2. គីមីវិទ្យា។ ថ្នាក់ទី 10 ។ កម្រិតប្រវត្តិរូប៖ សៀវភៅសិក្សា។ សម្រាប់ការអប់រំទូទៅ ស្ថាប័ន / V.V. Eremin, N.E. Kuzmenko, V.V. Lunin និងអ្នកផ្សេងទៀត - M.: Drofa, 2008. - 463 ទំ។
3. គីមីវិទ្យា។ ថ្នាក់ទី 11 ។ កម្រិតប្រវត្តិរូប៖ សៀវភៅសិក្សា។ សម្រាប់ការអប់រំទូទៅ ស្ថាប័ន / V.V. Eremin, N.E. Kuzmenko, V.V. Lunin និងអ្នកផ្សេងទៀត - M.: Drofa, 2010. - 462 ទំ។
4. Khomchenko G.P., Khomchenko I.G. ការប្រមូលបញ្ហាក្នុងគីមីវិទ្យាសម្រាប់អ្នកចូលសាកលវិទ្យាល័យ។ - ទី 4 ed ។ - M.: RIA "រលកថ្មី": អ្នកបោះពុម្ព Umerenkov, 2012. - 278 ទំ។
កិច្ចការផ្ទះ
1. លេខ 13, 14 (ទំ. 62) Rudzitis G.E., Feldman F.G. គីមីវិទ្យា៖ គីមីវិទ្យាសរីរាង្គ។ ថ្នាក់ទី១០៖ សៀវភៅសិក្សាសម្រាប់ស្ថាប័នអប់រំ៖ កម្រិតមូលដ្ឋាន / G.E. Rudzitis, F.G. Feldman ។ - បោះពុម្ពលើកទី ១៤ ។ - M. : ការអប់រំ, 2012 ។
2. ហេតុអ្វីបានជាសមាសធាតុក្រអូបមានលក្ខណៈសម្បត្តិគីមីខុសគ្នាពីអ៊ីដ្រូកាបូនឆ្អែត និងមិនឆ្អែត?
3. សរសេរសមីការសម្រាប់ប្រតិកម្មចំហេះនៃ ethylbenzene និង xylene ។
Aromatic HCs (សង្វៀន)គឺជាអ៊ីដ្រូកាបូនដែលម៉ូលេគុលមានចិញ្ចៀន benzene មួយ ឬច្រើន។
ឧទាហរណ៍នៃអ៊ីដ្រូកាបូនក្រអូប៖

សង្វៀនជួរ Benzene (សង្វៀន monocyclic)
រូបមន្តទូទៅ៖C n H 2n-6 , n≥6
អ្នកតំណាងសាមញ្ញបំផុតនៃអ៊ីដ្រូកាបូនក្រអូបគឺ benzene រូបមន្តជាក់ស្តែងរបស់វាគឺ C 6 H 6 ។
រចនាសម្ព័ន្ធអេឡិចត្រូនិចនៃម៉ូលេគុល benzene
រូបមន្តទូទៅនៃ C n H 2 n -6 monocyclic arenes បង្ហាញថាវាជាសមាសធាតុមិនឆ្អែត។
នៅឆ្នាំ 1856 អ្នកគីមីវិទ្យាអាល្លឺម៉ង់ A.F. Kekule បានស្នើរូបមន្តស៊ីក្លូសម្រាប់ benzene ជាមួយនឹងចំណងភ្ជាប់គ្នា (ចំណងតែមួយ និងទ្វេរជំនួស) - cyclohexatriene-1,3,5: 
រចនាសម្ព័ន្ធនៃម៉ូលេគុល benzene នេះមិនបានពន្យល់ពីលក្ខណៈសម្បត្តិជាច្រើនរបស់ benzene ទេ៖
- សម្រាប់ benzene ប្រតិកម្មជំនួសគឺជាលក្ខណៈ ហើយមិនមែនជាប្រតិកម្មបន្ថែមលក្ខណៈនៃសមាសធាតុ unsaturated ។ ប្រតិកម្មបន្ថែមគឺអាចធ្វើទៅបាន ប៉ុន្តែពួកគេពិបាកជាងសម្រាប់;
- benzene មិនចូលទៅក្នុងប្រតិកម្មដែលជាប្រតិកម្មគុណភាពទៅនឹងអ៊ីដ្រូកាបូនមិនឆ្អែត (ជាមួយនឹងទឹក bromine និងដំណោះស្រាយនៃ KMnO 4) ។
ការសិក្សាពីការបំភាយអេឡិចត្រុងក្រោយៗមកបានបង្ហាញថាចំណងទាំងអស់រវាងអាតូមកាបូននៅក្នុងម៉ូលេគុល benzene មានប្រវែងដូចគ្នានៃ 0.140 nm (តម្លៃជាមធ្យមរវាងប្រវែងនៃចំណង C-C តែមួយនៃ 0.154 nm និងចំណង C = C ទ្វេរដងនៃ 0.134 nm) ។ មុំរវាងចំណងនៅអាតូមកាបូននីមួយៗគឺ 120°។ ម៉ូលេគុលគឺជាឆកោនសំប៉ែតធម្មតា។
ទ្រឹស្តីទំនើបដើម្បីពន្យល់ពីរចនាសម្ព័ន្ធនៃម៉ូលេគុល C 6 H 6 ប្រើគំនិតនៃការបង្កាត់នៃគន្លងអាតូមិច។
អាតូមកាបូននៅក្នុង benzene ស្ថិតក្នុងស្ថានភាពនៃ sp 2 hybridization ។ អាតូម "C" នីមួយៗបង្កើតជាចំណង σ-bonds (ពីរជាមួយអាតូមកាបូន និងមួយជាមួយអាតូមអ៊ីដ្រូសែន) ។ ចំណង σ ទាំងអស់ស្ថិតនៅក្នុងប្លង់តែមួយ៖
អាតូមកាបូននីមួយៗមាន p-electron មួយដែលមិនចូលរួមក្នុងការបង្កាត់។ គន្លង p-orbitals ដែលមិនបង្កាត់នៃអាតូមកាបូនគឺស្ថិតនៅក្នុងប្លង់កាត់កែងទៅនឹងយន្តហោះនៃ σ-bonds ។ p-cloud នីមួយៗត្រួតលើគ្នាជាមួយ p-clouds ជិតខាងពីរ ហើយជាលទ្ធផលប្រព័ន្ធ π-conjugated តែមួយត្រូវបានបង្កើតឡើង (ចងចាំពីឥទ្ធិពលនៃការភ្ជាប់ p-electrons នៅក្នុងម៉ូលេគុល 1,3-butadiene ដែលបានពិភាក្សាក្នុងប្រធានបទ "Diene hydrocarbons ”):
ការរួមបញ្ចូលគ្នានៃ σ-bonds ប្រាំមួយជាមួយនឹងប្រព័ន្ធ π តែមួយត្រូវបានគេហៅថា ចំណងក្លិនក្រអូប។
ចិញ្ចៀននៃអាតូមកាបូនចំនួនប្រាំមួយដែលត្រូវបានតភ្ជាប់ដោយចំណងក្លិនក្រអូបត្រូវបានគេហៅថា ចិញ្ចៀន benzene,ឬ ស្នូល benzene.
អនុលោមតាមគំនិតទំនើបអំពីរចនាសម្ព័ន្ធអេឡិចត្រូនិចនៃ benzene ម៉ូលេគុល C 6 H 6 ត្រូវបានបង្ហាញដូចខាងក្រោម:

លក្ខណៈសម្បត្តិរូបវិទ្យានៃ benzene
Benzene នៅក្រោមលក្ខខណ្ឌធម្មតាគឺជារាវគ្មានពណ៌; t o pl = 5.5 o C; t o គីប។ = 80 អំពី C; មានក្លិនលក្ខណៈ; immiscible ជាមួយទឹក, សារធាតុរំលាយល្អ, ពុលខ្ពស់។
លក្ខណៈសម្បត្តិគីមីនៃ benzene
ចំណងក្លិនក្រអូបកំណត់លក្ខណៈគីមីនៃ benzene និងអ៊ីដ្រូកាបូនក្រអូបផ្សេងទៀត។
ប្រព័ន្ធ 6π-electron មានស្ថេរភាពជាង π-bonds ធម្មតា។ ដូច្នេះ ប្រតិកម្មបន្ថែមគឺមិនសូវធម្មតាសម្រាប់អ៊ីដ្រូកាបូនក្រអូបជាងអ៊ីដ្រូកាបូនដែលមិនឆ្អែត។ ធម្មតាបំផុតសម្រាប់ arenes គឺប្រតិកម្មជំនួស។
I. ប្រតិកម្មជំនួស
1. Halogenation

2. នីត្រាត
ប្រតិកម្មត្រូវបានអនុវត្តជាមួយនឹងល្បាយនៃនិងអាស៊ីត (ល្បាយ nitrating): 
3. ស៊ុលហ្វាន

4. Alkylation (ការជំនួសអាតូម "H" ដោយក្រុមអាល់គីល) - ប្រតិកម្មរបស់ Friedel-Crafts, homologues នៃ benzene ត្រូវបានបង្កើតឡើង:

ជំនួសឱ្យ haloalkanes អាល់ខេនអាចត្រូវបានប្រើ (នៅក្នុងវត្តមាននៃកាតាលីករ - AlCl 3 ឬអាស៊ីតអសរីរាង្គ):

II. ប្រតិកម្មបន្ថែម
1. អ៊ីដ្រូសែន

2. ការបន្ថែមក្លរីន

III.ប្រតិកម្មអុកស៊ីតកម្ម
1. ការដុត
2C 6 H 6 + 15O 2 → 12CO 2 + 6H 2 O
2. អុកស៊ីតកម្មមិនពេញលេញ (KMnO 4 ឬ K 2 Cr 2 O 7 ក្នុងបរិយាកាសអាសុីត) ។ ចិញ្ចៀន benzene មានភាពធន់នឹងភ្នាក់ងារអុកស៊ីតកម្ម។ ប្រតិកម្មមិនកើតឡើងទេ។
ការទទួលបាន benzene
នៅក្នុងឧស្សាហកម្ម៖
1) ដំណើរការប្រេងនិងធ្យូងថ្ម;
2) dehydrogenation នៃ cyclohexane:

3) dehydrocyclization (aromatization) នៃ hexane:

នៅក្នុងមន្ទីរពិសោធន៍៖
ការលាយអំបិលអាស៊ីត benzoic ជាមួយ៖

Isomerism និង nomenclature នៃ benzene homologues
ភាពដូចគ្នានៃ benzene ណាមួយមានខ្សែសង្វាក់ចំហៀង, i.e. រ៉ាឌីកាល់អាល់គីលភ្ជាប់ទៅនឹងចិញ្ចៀន benzene ។ ភាពដូចគ្នាដំបូងនៃ benzene គឺជាស្នូល benzene ដែលភ្ជាប់ទៅនឹងរ៉ាឌីកាល់មេទីល៖ 
Toluene មិនមាន isomers ទេ ចាប់តាំងពីមុខតំណែងទាំងអស់នៅក្នុង benzene ring គឺសមមូល។
សម្រាប់ភាពដូចគ្នាជាបន្តបន្ទាប់នៃ benzene ប្រភេទមួយនៃ isomerism គឺអាចធ្វើទៅបាន - isomerism ខ្សែសង្វាក់ចំហៀង ដែលអាចមានពីរប្រភេទ៖
1) isomerism នៃចំនួននិងរចនាសម្ព័ន្ធនៃសារធាតុជំនួស;
2) isomerism នៃទីតាំងនៃសារធាតុជំនួស។



លក្ខណៈសម្បត្តិរូបវន្តនៃសារធាតុ Toluene
តូលូអ៊ីន- វត្ថុរាវគ្មានពណ៌ មានក្លិនលក្ខណៈ មិនរលាយក្នុងទឹក រលាយក្នុងសារធាតុរំលាយសរីរាង្គ។ Toluene មានជាតិពុលតិចជាង benzene ។
លក្ខណៈគីមីនៃសារធាតុ Toluene
I. ប្រតិកម្មជំនួស
1. ប្រតិកម្មដែលទាក់ទងនឹងចិញ្ចៀន benzene
Methylbenzene ចូលទៅក្នុងប្រតិកម្មជំនួសទាំងអស់ដែល benzene ជាប់ពាក់ព័ន្ធ ហើយក្នុងពេលជាមួយគ្នានេះបង្ហាញពីប្រតិកម្មខ្ពស់ ប្រតិកម្មដំណើរការក្នុងអត្រាលឿនជាងមុន។
រ៉ាឌីកាល់មេទីលដែលមាននៅក្នុងម៉ូលេគុល toluene គឺជាសារធាតុជំនួសនៃហ្សែន ដូច្នេះជាលទ្ធផលនៃប្រតិកម្មជំនួសនៅក្នុងស្នូល benzene, ortho- និង para-derivatives នៃ toluene ត្រូវបានទទួល ឬជាមួយនឹងសារធាតុលើសនៃ reagent, tri-derivatives នៃរូបមន្តទូទៅ:

ក) halogenation


ជាមួយនឹងក្លរីនបន្ថែម dichloromethylbenzene និង trichloromethylbenzene អាចទទួលបាន:

II. ប្រតិកម្មបន្ថែម
អ៊ីដ្រូសែន

III.ប្រតិកម្មអុកស៊ីតកម្ម
1. ការដុត
C 6 H 5 CH 3 + 9O 2 → 7CO 2 + 4H 2 O
2. អុកស៊ីតកម្មមិនពេញលេញ
មិនដូច benzene, homologues របស់វាត្រូវបានកត់សុីដោយភ្នាក់ងារអុកស៊ីតកម្មមួយចំនួន; ក្នុងករណីនេះ ខ្សែសង្វាក់ចំហៀងឆ្លងកាត់ការកត់សុី នៅក្នុងករណីនៃ toluene ដែលជាក្រុមមេទីល។ ភ្នាក់ងារអុកស៊ីតកម្មកម្រិតស្រាលដូចជា MnO 2 កត់សុីវាទៅជាក្រុម aldehyde ភ្នាក់ងារអុកស៊ីតកម្មខ្លាំងជាង (KMnO 4) បណ្តាលឱ្យអុកស៊ីតកម្មបន្ថែមទៀតទៅជាអាស៊ីតមួយ៖ 
ភាពដូចគ្នាណាមួយនៃ benzene ដែលមានសង្វាក់ម្ខាងត្រូវបានកត់សុីដោយភ្នាក់ងារអុកស៊ីតកម្មដ៏ខ្លាំងដូចជា KMnO4 ទៅអាស៊ីត benzoic ពោលគឺឧ។ មានការបំបែកនៅក្នុងខ្សែសង្វាក់ចំហៀងជាមួយនឹងការកត់សុីនៃផ្នែកដែលបានបំបែករបស់វាទៅជា CO 2; ឧទាហរណ៍: 
នៅក្នុងវត្តមាននៃច្រវាក់ចំហៀងជាច្រើនពួកវានីមួយៗត្រូវបានកត់សុីទៅជាក្រុម carboxyl ហើយជាលទ្ធផលអាស៊ីត polybasic ត្រូវបានបង្កើតឡើងឧទាហរណ៍:

ការទទួលបានសារធាតុ Toluene៖
នៅក្នុងឧស្សាហកម្ម៖
1) ដំណើរការប្រេងនិងធ្យូងថ្ម;
2) dehydrogenation នៃ methylcyclohexane:

3) dehydrocyclization នៃ heptane:
នៅក្នុងមន្ទីរពិសោធន៍៖
1) Friedel-Crafts alkylation;
2) ប្រតិកម្ម Wurtz-Fittig(ប្រតិកម្មនៃសូដ្យូមជាមួយល្បាយនៃ halobenzene និង haloalkane) ។
PRTSVSH (F) FGBOU VPO
នាយកដ្ឋាន "សុវត្ថិភាពអគ្គីភ័យ"
សាកល្បង
នៅក្នុងវិន័យ "ទ្រឹស្តីនៃការឆេះនិងការផ្ទុះ"
លេខកិច្ចការ 1
កំណត់បរិមាណទ្រឹស្តីជាក់លាក់ និងបរិមាណនៃខ្យល់ដែលត្រូវការសម្រាប់ការឆេះពេញលេញនៃចំហាយ benzene ។ លក្ខខណ្ឌដែលខ្យល់ស្ថិតនៅត្រូវបានកំណត់លក្ខណៈដោយសីតុណ្ហភាព Tv និងសម្ពាធ Pv និងចំហាយ benzene - សីតុណ្ហភាព Tg និងសម្ពាធ Pg ។ បង្ហាញលទ្ធផលគណនាក្នុងឯកតាខាងក្រោម៖ ; ;;;
ទិន្នន័យដំបូង (N - លេខក្រុម, n - លេខយោងទៅតាមបញ្ជីសិស្ស:
ទូរទស្សន៍=300+(-1) N *2*N-(-1) n *0.2*n= 277.6 K
Pv \u003d? 10 3 \u003d 95900 ប៉ា;
Тg=300?(?1) N?2?N?(?1) n?0.2?n= 321.6 K;
Pr \u003d? 10 3 \u003d 79400 ប៉ា។
С6Н6+7.5О2+7.5?3.76N2=6CO2+3pO+7.5?3.76N2+Qp (1),
ដែល Qp គឺជាកំដៅនៃប្រតិកម្មគីមី។ ពីសមីការនេះ គេអាចកំណត់មេគុណ stoichiometric នៃ benzene និង molecular oxygen: Vg = 1, V0 = 7.5
2. បរិមាណខ្យល់តាមទ្រឹស្តីជាក់លាក់ - ចំនួនគីឡូម៉ែត្រនៃខ្យល់ដែលចាំបាច់សម្រាប់ការចំហេះពេញលេញនៃ 1 គីឡូម៉ុលនៃ benzene ត្រូវបានគណនាតាមរូបមន្ត៖
ដែល 4.76 គឺជាបរិមាណខ្យល់ដែលមានឯកតានៃអុកស៊ីសែន \u003d គឺជាសមាមាត្រនៃមេគុណ stoichiometric នៃអុកស៊ីសែនម៉ូលេគុល (Vo) និង benzene (Vg)
ការជំនួសក្នុង (d) តម្លៃនៃ Vo និង Vg យើងទទួលបាន៖
3. បរិមាណខ្យល់ដែលត្រូវការសម្រាប់ការចំហេះពេញលេញនៃ benzene មួយគីឡូម៉ែតត្រូវបានកំណត់ដូចខាងក្រោម:
តើបរិមាណនៃខ្យល់មួយគីឡូម៉ែត្រនៅសីតុណ្ហភាពទូរទស្សន៍ និងសម្ពាធ Pv នៅឯណា។ តម្លៃត្រូវបានគណនាដោយប្រើរូបមន្ត
ដែល 22.4 គឺជាបរិមាណម៉ូលេគុលនៃឧស្ម័ននៅក្រោមលក្ខខណ្ឌធម្មតា Po = 101325 Pa គឺជាសម្ពាធធម្មតា To = 273 K គឺជាសីតុណ្ហភាពធម្មតា។
ការជំនួសទូរទស្សន៍ To, Pv, Po ក្នុង (5) យើងទទួលបាន
បរិមាណខ្យល់តាមទ្រឹស្តីជាក់លាក់ត្រូវបានគណនាដោយរូបមន្ត (4)៖
4. បរិមាណខ្យល់ដែលត្រូវការសម្រាប់ការឆេះពេញលេញនៃបរិមាណឯកតានៃឥន្ធនៈឧស្ម័នត្រូវបានកំណត់ដូចខាងក្រោមៈ
តើបរិមាណឥន្ធនៈមួយគីឡូម៉ែលនៅឯណា - ចំហាយ benzene នៅសីតុណ្ហភាព Tg និងសម្ពាធ Pg ។ បានផ្តល់ឱ្យនោះ។
ហើយការជំនួស (8) និង (5) ទៅជា (7) យើងទទួលបានកន្សោមខាងក្រោមសម្រាប់បរិមាណខ្យល់តាមទ្រឹស្តីជាក់លាក់៖
យើងគណនាតម្លៃនៃប៉ារ៉ាម៉ែត្រនេះនៃដំណើរការចំហេះ៖
បរិមាណខ្យល់ដែលត្រូវការសម្រាប់ការឆេះពេញលេញនៃ benzene មួយគីឡូក្រាមត្រូវបានកំណត់ដូចខាងក្រោម:
ដែលជាកន្លែងដែល - ម៉ាស់ម៉ូលនៃឥន្ធនៈគឺជាម៉ាស់នៃ 1 គីឡូម៉ុលនៃ benzene ដែលបង្ហាញជាគីឡូក្រាម។ ម៉ាស់ម៉ូលេគុលនៃ benzene មានចំនួនស្មើនឹងទម្ងន់ម៉ូលេគុលរបស់វា ត្រូវបានរកឃើញដោយរូបមន្ត៖
Ac?nc + An?nn, UiAi?ni (11)
ដែល Ac និង An គឺជាទម្ងន់អាតូមិកនៃកាបូន និងអ៊ីដ្រូសែន nc និង nn គឺជាចំនួនអាតូមកាបូននៅក្នុងម៉ូលេគុល benzene ។ ការជំនួសតម្លៃ Ac = 12, nc = 6, An = 1, nn = 6 យើងទទួលបាន៖
យើងរកឃើញបរិមាណទ្រឹស្តីជាក់លាក់នៃខ្យល់ដោយជំនួសតម្លៃនៃ n ចូលទៅក្នុងនិងទៅជារូបមន្ត (10):
លទ្ធផលគណនា៖
លេខកិច្ចការ 2
កំណត់បរិមាណទ្រឹស្តីជាក់លាក់ បរិមាណ និងសមាសភាពនៃផលិតផលចំហេះ benzene ប្រសិនបើមេគុណនៃខ្យល់លើស c សីតុណ្ហភាព Tp និងសម្ពាធ Pp នៃផលិតផលចំហេះ សីតុណ្ហភាព Tg និងសម្ពាធ Pg នៃចំហាយ benzene ត្រូវបានគេស្គាល់។ បង្ហាញលទ្ធផលគណនាជាប្រភាគម៉ូល (គិតជាភាគរយ) និងក្នុងឯកតាខាងក្រោម៖ ; ;;
ទិន្នន័យដំបូង៖
c=1.5+(?1) N?0.1?N?(?1) n?0.01?n = 0.2;
Rp \u003d? 10 3 \u003d 68400 ប៉ា;
Tp=1600?(?1) N?20?N?(?1) n?2?n=1816 K;
Тg=273?(?1) N?2?N+(?1) n?0.2?n = 295.4 K;
Rg \u003d? 10 3 \u003d 111600 ប៉ា;
ដំណោះស្រាយ (N=11, n=2) ។
1. យើងសរសេរសមីការ stoichiometric សម្រាប់ប្រតិកម្មនៃចំហេះ benzene នៅក្នុងខ្យល់៖
C 6 H 6 +7.5O 2 +7.5? 3.76N 2 \u003d 6CO 2 + 3H 2 O + 7.5? 3.76N 2 + Qp, (1)
ដែល Qp គឺជាកំដៅនៃប្រតិកម្មគីមី។ ពីសមីការនេះ យើងកំណត់មេគុណ stoichiometric ខាងក្រោម៖
V CO2 \u003d 6, V pO \u003d 3, V C6H6 \u003d 1, V O2 \u003d 7.5, V N2 \u003d 7.5? 3.76
2. កំណត់បរិមាណប៉ាន់ស្មាននៃផលិតផលចំហេះនៃប្រេងឥន្ធនៈមួយគីឡូម៉ែត្រ៖
ការជំនួសនៅក្នុង (2) តម្លៃនៃមេគុណ stoichiometric នៃផលិតផលចំហេះ និងឥន្ធនៈ យើងទទួលបាន៖
3. បរិមាណខ្យល់តាមទ្រឹស្តីជាក់លាក់ - ចំនួនគីឡូម៉ែត្រនៃខ្យល់ដែលចាំបាច់សម្រាប់ការឆេះពេញលេញនៃប្រេងឥន្ធនៈមួយគីឡូម៉ុល យើងកំណត់ដោយប្រើរូបមន្ត៖
ដែលជាកន្លែងដែល 4.76 គឺជាបរិមាណនៃខ្យល់ដែលមានឯកតានៃអុកស៊ីសែន,
សមាមាត្រនៃមេគុណ stoichiometric នៃអុកស៊ីសែនម៉ូលេគុលនិង benzene ។
ការជំនួសក្នុង (4) តម្លៃ V O2 = 7.5 និង V C6H6 = 1 យើងទទួលបាន៖
4. បរិមាណលើសនៃខ្យល់ដែលធ្លាក់លើប្រេងឥន្ធនៈ 1 Kmol ត្រូវបានកំណត់ដោយកន្សោម៖
ឧស្ម័នចំហុយ benzene ខ្យល់
ការជំនួសនៅក្នុងកន្សោមនេះតម្លៃ
37,7(0,2-1)=30,16(7)
5. បរិមាណសរុបនៃផលិតផលចំហេះក្នុងមួយឯកតានៃបរិមាណសារធាតុឥន្ធនៈត្រូវបានកំណត់ដោយផលបូក៖
បន្ទាប់ពីជំនួសតម្លៃហើយយើងទទួលបាន៖
6. ប្រភាគ Mole នៃផលិតផលចំហេះ ដែលបង្ហាញជាភាគរយ ត្រូវបានកំណត់ដូចខាងក្រោម៖
នៅក្នុងរូបមន្ត (9) សម្រាប់ប្រភាគម៉ូលនៃអាសូត និងអុកស៊ីហ៊្សែននៅក្នុងផលិតផលចំហេះ 0.79 និង 0.21 គឺជាប្រភាគម៉ូលនៃសារធាតុទាំងនេះនៅក្នុងខ្យល់ ដែលលើសពីនេះនាំឱ្យមានការកើនឡើងនៃសមាមាត្រនៃអាសូត និងរូបរាងនៃអុកស៊ីសែន។ នៅក្នុងផលិតផលចំហេះ។
7. ដើម្បីកំណត់បរិមាណជាក់លាក់ និងផលិតផលនៃចំហេះ ចាំបាច់ត្រូវគណនាបរិមាណម៉ូលេគុលរបស់ពួកគេ - បរិមាណឧស្ម័នមួយគីឡូម៉ែល ក្រោមលក្ខខណ្ឌដែលផលិតផលស្ថិតនៅ៖
ដែល 22.4 គឺជាបរិមាណនៃឧស្ម័នមួយគីឡូម៉ែតក្រោមលក្ខខណ្ឌធម្មតា T 0 \u003d 273K - សីតុណ្ហភាពធម្មតា Po \u003d 101325 Pa - សម្ពាធធម្មតា។
ការជំនួសក្នុង (10) តម្លៃ Po, To យើងទទួលបាន៖
បរិមាណនៃផលិតផលដែលត្រូវបានបង្កើតឡើងកំឡុងពេលចំហេះនៃប្រេងឥន្ធនៈមួយគីឡូក្រាមដោយមិនរាប់បញ្ចូលខ្យល់លើសត្រូវបានគណនាដូចខាងក្រោម:
ដែលជាកន្លែងដែល - ម៉ាសឥន្ធនៈគឺជាម៉ាស់នៃ benzene មួយគីឡូម៉ែល ដែលបង្ហាញជាគីឡូក្រាម។ ម៉ាស់ម៉ូលេគុលនៃ benzene ត្រូវបានរកឃើញដោយរូបមន្ត៖
ដែល Ac និង An គឺជាទម្ងន់អាតូមនៃកាបូន (12) និងអ៊ីដ្រូសែន (1), n c និង n n គឺជាលេខនៃកាបូន (6) និងអ៊ីដ្រូសែន (6) អាតូមនៅក្នុងម៉ូលេគុល benzene (C 6 H 6) ។
ការជំនួសតម្លៃ ហើយនៅក្នុង (12) យើងទទួលបាន
បរិមាណលើសនៃខ្យល់ក្នុង 1 គីឡូក្រាមនៃឥន្ធនៈត្រូវបានកំណត់ដូចខាងក្រោម:
តើបរិមាណនៃខ្យល់លើសពីមួយគីឡូម៉ែល ដែលជាផ្នែកនៃផលិតផលចំហេះ។ ចាប់តាំងពីសីតុណ្ហភាពនិងសម្ពាធនៃខ្យល់លើសត្រូវគ្នាទៅនឹងសីតុណ្ហភាពនិងសម្ពាធនៃផលិតផលចំហេះបន្ទាប់មក \u003d \u003d 220.7 ។
ការជំនួសតម្លៃនេះ ក៏ដូចជានៅក្នុង (14) យើងទទួលបាន៖
ដើម្បីគណនាបរិមាណជាក់លាក់នៃផលិតផលនៃការចំហេះពេញលេញនៃឥន្ធនៈ យើងសន្មត់ថាចំហាយទឹក benzene មានសីតុណ្ហភាព Tg នៅសម្ពាធ៖
តើបរិមាណនៃចំហាយ benzene មួយគីឡូម៉ែលនៅសីតុណ្ហភាព Tg និងសម្ពាធ Pg នៅឯណា។ បរិមាណម៉ូលេគុលនៃឥន្ធនៈត្រូវបានគណនាដោយរូបមន្ត៖
ការជំនួសតម្លៃដែលទទួលបាន និងតម្លៃបែបនេះនៅក្នុង (17) យើងទទួលបាន៖
បរិមាណលើសនៃខ្យល់ក្នុងមួយម៉ែត្រគូបនៃចំហាយ benzene ត្រូវបានកំណត់ដូចខាងក្រោម:
ការជំនួសនៅក្នុងតម្លៃ (20) \u003d 30.16 , \u003d និង
ផ្តល់លទ្ធផលដូចខាងក្រោមៈ
បរិមាណជាក់លាក់សរុបនៃផលិតផលចំហេះដោយគិតគូរពីខ្យល់លើសត្រូវបានកំណត់ដោយផលបូក
លទ្ធផលគណនា៖
X CO2 \u003d%; X H2O \u003d 4.4%; X N2 =%; X O2 \u003d 11.7%
ឯកសារស្រដៀងគ្នា
ការគណនាមេគុណងាយឆេះនៃ nitrobenzene C6H5NO2 និង carbon disulfide CS2 ។ សមីការសម្រាប់ប្រតិកម្មចំហេះនៃ propyl acetate នៅក្នុងខ្យល់។ ការគណនាបរិមាណខ្យល់ និងផលិតផលចំហេះ កំឡុងពេលចំហេះឧស្ម័នដែលអាចឆេះបាន។ ការកំណត់ចំណុចពន្លឺនៃ toluene យោងតាមរូបមន្តរបស់ V. Blinov ។
ការធ្វើតេស្តបន្ថែម 04/08/2017
ការគណនាបរិមាណខ្យល់ និងផលិតផលចំហេះដែលបានបង្កើតឡើងកំឡុងពេលចំហេះនៃសារធាតុមួយ។ សមីការសម្រាប់ប្រតិកម្មចំហេះនៃអេទីឡែន glycol នៅក្នុងខ្យល់។ ចំហេះនៃល្បាយនៃឧស្ម័នដែលអាចឆេះបាន។ ការគណនាសីតុណ្ហភាពចំហេះ adiabatic សម្រាប់ល្បាយ stoichiometric ។ ការដុត propanol ។
ការធ្វើតេស្តបន្ថែម 10/17/2012
ប្រភេទនៃការឆេះ និងប៉ារ៉ាម៉ែត្រចំបងរបស់វា។ ការបំប្លែងគីមីនៃឥន្ធនៈ និងអុកស៊ីតកម្មទៅជាផលិតផលចំហេះ។ សមីការនៃសម្ភារៈ និងតុល្យភាពកម្ដៅនៃប្រតិកម្មចំហេះ។ ឥទ្ធិពលនៃមេគុណខ្យល់លើសលើសមាសភាពនៃផលិតផលចំហេះ និងសីតុណ្ហភាពចំហេះ។
សាកល្បង, បានបន្ថែម 01/17/2013
ការកំណត់បរិមាណខ្យល់ដែលត្រូវការសម្រាប់ការឆេះពេញលេញនៃម៉ាស់ឯកតានៃសារធាតុដែលអាចឆេះបាន។ សមាសភាពនៃផលិតផលចំហេះនៃម៉ាស់ឯកតានៃសារធាតុដែលអាចឆេះបាន។ ដែនកំណត់នៃការសាយភាយអណ្តាតភ្លើងនៃឧស្ម័ន ចំហាយទឹក ល្បាយធូលី-ខ្យល់។ សម្ពាធនៃការបំបែកបំផ្ទុះ។
ក្រដាសពាក្យបន្ថែម 12/23/2013
ការអភិវឌ្ឍវិធានការទប់ស្កាត់ការកើតឡើងនៃអគ្គីភ័យនិងការផ្ទុះការវាយតម្លៃលក្ខខណ្ឌសម្រាប់ការអភិវឌ្ឍនិងការបង្ក្រាបរបស់ពួកគេ។ គំនិតនៃអត្រាដុត វិធីសាស្រ្តនៃនិយមន័យរបស់វា។ នីតិវិធីសម្រាប់ការចងក្រងសមីការប្រតិកម្មចំហេះ។ ការគណនាបរិមាណខ្យល់ដែលត្រូវការសម្រាប់ការបញ្ឆេះ។
ក្រដាសពាក្យបន្ថែមថ្ងៃទី 07/10/2014
ការកំណត់សមាសភាពនៃផលិតផលនៃការឆេះពេញលេញនៃឧស្ម័ន។ ការគណនាសីតុណ្ហភាពចំហេះ adiabatic នៃល្បាយឧស្ម័នក្នុងបរិមាណថេរ និងសម្ពាធថេរ។ ប្រតិកម្ម Kinetic ថេរនៃការបញ្ឆេះដោយខ្លួនឯងនៃឧស្ម័នធម្មជាតិ។ ដែនកំណត់នៃការបញ្ឆេះនៃល្បាយឧស្ម័ន។
ក្រដាសពាក្យបន្ថែមថ្ងៃទី ០២/១៩/២០១៤
លក្ខណៈនៃវិធីសាស្រ្តឧស្សាហកម្មសម្រាប់ការ alkylation នៃ benzene ជាមួយ propylene ។ គោលការណ៍នៃការ alkylation នៃ benzene ជាមួយ olefins នៅក្នុងបច្ចេកវិទ្យាគីមី។ បញ្ហានៃការរចនាការដំឡើងបច្ចេកវិទ្យាសម្រាប់ benzene alkylation ។ ការពិពណ៌នាអំពីបច្ចេកវិទ្យានៃដំណើរការផលិត។
និក្ខេបបទបន្ថែម ១១/១៥/២០១០
ការដុតគឺជាដំណើរការអុកស៊ីតកម្មដ៏មានឥទ្ធិពល។ ប្រភេទនៃការឆេះ៖ ឆេះ និងឆេះដោយអណ្តាតភ្លើង។ ការផ្ទុះជាករណីពិសេសនៃការឆេះ។ លក្ខណៈសម្បត្តិអគ្គិសនីនៃអណ្តាតភ្លើង។ ភាពខុសគ្នានៃផលិតផលចំហេះដែលជាលទ្ធផលនៃការឆេះមិនពេញលេញនៃឥន្ធនៈ។ ការច្រោះផ្សែងតាមរយៈទឹក។
ការងារវិទ្យាសាស្ត្របន្ថែម ០៧/២៩/២០០៩
ការកំណត់បរិមាណនៃខ្យល់ដែលត្រូវការសម្រាប់ការឆេះពេញលេញនៃបរិមាណដែលបានផ្តល់ឱ្យនៃ propane ។ ការគណនានៃការផ្លាស់ប្តូរនៅក្នុងថាមពល enthalpy, entropy និង Gibbs ដោយប្រើផលវិបាកនៃច្បាប់របស់ Hess ។ ការកំណត់នៃសមមូលម៉ាស់ម៉ូលេគុលនៃសារធាតុអុកស៊ីតកម្ម និងភ្នាក់ងារកាត់បន្ថយ។
សាកល្បង, បានបន្ថែម 02/08/2012
វិធីសាស្រ្តសម្រាប់កំណត់ការប្រើប្រាស់ប្រេងស្រូបយក ការប្រមូលផ្តុំនៃ benzene នៅក្នុងប្រេងដែលស្រូបយកដោយបន្សល់ទុកឧបករណ៍ស្រូបយក។ ការគណនាអង្កត់ផ្ចិតនិងកម្ពស់របស់ឧបករណ៍ស្រូបយកខ្ចប់។ ការកំណត់ផ្ទៃកំដៅដែលត្រូវការនៅក្នុងគូបនៃជួរឈរនិងការប្រើប្រាស់ចំហាយកំដៅ។
ក្រុមទីមួយនៃប្រតិកម្មគឺ ប្រតិកម្មជំនួស។ យើងបាននិយាយថា អារ៉ែងមិនមានចំណងច្រើននៅក្នុងរចនាសម្ព័ន្ធម៉ូលេគុលទេ ប៉ុន្តែមានប្រព័ន្ធភ្ជាប់នៃអេឡិចត្រុងប្រាំមួយ ដែលមានស្ថេរភាពខ្លាំង និងផ្តល់កម្លាំងបន្ថែមដល់ចិញ្ចៀន បេហ្សេន។ ដូច្នេះនៅក្នុងប្រតិកម្មគីមី ជាដំបូងនៃការជំនួសអាតូមអ៊ីដ្រូសែនកើតឡើង ហើយមិនមែនជាការបំផ្លិចបំផ្លាញនៃចិញ្ចៀន benzene នោះទេ។
យើងបានជួបប្រទះប្រតិកម្មជំនួសរួចហើយនៅពេលនិយាយអំពីអាល់កាន ប៉ុន្តែសម្រាប់ពួកគេ ប្រតិកម្មទាំងនេះបានដំណើរការទៅតាមយន្តការរ៉ាឌីកាល់ ហើយសម្រាប់អារ៉េន យន្តការអ៊ីយ៉ុងនៃប្រតិកម្មជំនួសគឺជាលក្ខណៈ។
ទីមួយលក្ខណៈសម្បត្តិគីមី halogenation ។ ការជំនួសអាតូមអ៊ីដ្រូសែនសម្រាប់អាតូម halogen chlorine ឬ bromine ។
ប្រតិកម្មកើតឡើងនៅពេលដែលកម្តៅ ហើយតែងតែមានការចូលរួមពីកាតាលីករ។ ក្នុងករណីក្លរីនវាអាចជាអាលុយមីញ៉ូក្លរីតឬជាតិដែកក្លរួបី។ កាតាលីករ polarizes ម៉ូលេគុល halogen ដែលបណ្តាលឱ្យមានការបំបែកចំណង heterolytic ហើយអ៊ីយ៉ុងត្រូវបានទទួល។
អ៊ីយ៉ុងក្លរួដែលមានបន្ទុកវិជ្ជមានមានប្រតិកម្មជាមួយ benzene ។
ប្រសិនបើប្រតិកម្មកើតឡើងជាមួយ bromine បន្ទាប់មកជាតិដែក tribromide ឬអាលុយមីញ៉ូម bromide ដើរតួជាកាតាលីករ។

វាជាការសំខាន់ក្នុងការកត់សម្គាល់ថាប្រតិកម្មកើតឡើងជាមួយនឹងម៉ូលេគុល bromine និងមិនមែនជាមួយនឹងទឹក bromine ទេ។ Benzene មិនមានប្រតិកម្មជាមួយនឹងទឹក bromine ទេ។
halogenation នៃ benzene homologues មានលក្ខណៈផ្ទាល់ខ្លួនរបស់វា។ នៅក្នុងម៉ូលេគុល toluene ក្រុម methyl ជួយសម្រួលដល់ការជំនួសនៅក្នុងសង្វៀន ប្រតិកម្មកើនឡើង ហើយប្រតិកម្មកើតឡើងក្រោមលក្ខខណ្ឌស្រាលជាងមុន ពោលគឺនៅសីតុណ្ហភាពបន្ទប់រួចហើយ។

វាជាការសំខាន់ក្នុងការកត់សម្គាល់ថាការជំនួសតែងតែកើតឡើងនៅក្នុងទីតាំង ortho និង para ដូច្នេះល្បាយនៃ isomers ត្រូវបានទទួល។
ទីពីរនីត្រាតទ្រព្យសម្បត្តិនៃ benzene ការណែនាំនៃក្រុម nitro ចូលទៅក្នុងចិញ្ចៀន benzene ។
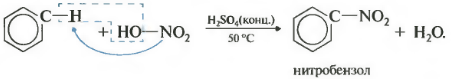
អង្គធាតុរាវពណ៌លឿងធ្ងន់ដែលមានក្លិនអាល់ម៉ុនជូរចត់ nitrobenzene ត្រូវបានបង្កើតឡើង ដូច្នេះប្រតិកម្មអាចមានគុណភាពសម្រាប់ benzene ។ សម្រាប់ nitration ល្បាយ nitrating នៃអាស៊ីត nitric និង sulfuric ប្រមូលផ្តុំត្រូវបានប្រើ។ ប្រតិកម្មត្រូវបានអនុវត្តដោយកំដៅ។
ខ្ញុំសូមរំលឹកអ្នកថាសម្រាប់ nitration នៃ alkanes នៅក្នុងប្រតិកម្ម Konovalov ទឹកអាស៊ីតនីទ្រីកពនឺត្រូវបានគេប្រើដោយគ្មានការបន្ថែមអាស៊ីតស៊ុលហ្វួរី។
នៅក្នុង nitration នៃ toluene ក៏ដូចជានៅក្នុង halogenation ល្បាយនៃ ortho- និង para-isomers ត្រូវបានបង្កើតឡើង។
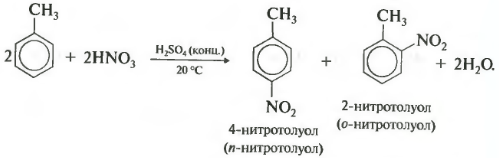
ទីបី alkylation ទ្រព្យសម្បត្តិនៃ benzene ជាមួយ haloalkanes ។

ប្រតិកម្មនេះអនុញ្ញាតឱ្យមានការបញ្ចូលរ៉ាឌីកាល់អ៊ីដ្រូកាបូនទៅក្នុងរង្វង់ benzene ហើយអាចត្រូវបានចាត់ទុកថាជាវិធីសាស្រ្តសម្រាប់ការទទួលបាន benzene homologues ។ អាលុយមីញ៉ូក្លរីតត្រូវបានគេប្រើជាកាតាលីករដែលជំរុញការរលួយនៃម៉ូលេគុល haloalkane ទៅជាអ៊ីយ៉ុង។ វាក៏ត្រូវការកំដៅផងដែរ។
ទីបួនទ្រព្យសម្បត្តិ alkylation នៃ benzene ជាមួយ alkenes ។
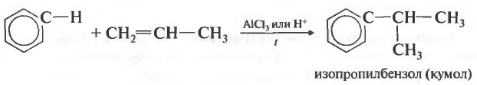
តាមរបៀបនេះឧទាហរណ៍ cumene ឬ ethylbenzene អាចត្រូវបានទទួល។ កាតាលីករអាលុយមីញ៉ូមក្លរួ។
2. ប្រតិកម្មនៃការបន្ថែមទៅ benzene
ក្រុមទីពីរនៃប្រតិកម្មគឺ ប្រតិកម្មបន្ថែម។ យើងបាននិយាយថា ប្រតិកម្មទាំងនេះមិនមែនជាលក្ខណៈទេ ប៉ុន្តែវាអាចធ្វើទៅបាននៅក្រោមលក្ខខណ្ឌដ៏អាក្រក់ជាមួយនឹងការបំផ្លិចបំផ្លាញនៃ pi-electron cloud និងការបង្កើតចំណងប្រាំមួយ sigma ។
ទីប្រាំទ្រព្យសម្បត្តិនៅក្នុងបញ្ជីទូទៅ អ៊ីដ្រូសែន ការបន្ថែមអ៊ីដ្រូសែន។
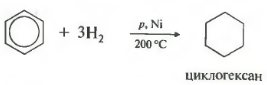
សីតុណ្ហភាព សម្ពាធ នីកែលកាតាលីករ ឬផ្លាទីន។ Toluene អាចមានប្រតិកម្មដូចគ្នា។
ទីប្រាំមួយ។ chlorination ទ្រព្យសម្បត្តិ។ សូមចំណាំថាយើងកំពុងនិយាយជាពិសេសអំពីអន្តរកម្មជាមួយក្លរីនចាប់តាំងពី bromine មិនចូលទៅក្នុងប្រតិកម្មនេះទេ។

ប្រតិកម្មដំណើរការក្រោមវិទ្យុសកម្មអ៊ុលត្រាវីយូឡេរឹង។ Hexachlorocyclohexane, ឈ្មោះផ្សេងទៀតសម្រាប់ hexachlorane, ត្រូវបានបង្កើតឡើង, រឹង។
វាជាការសំខាន់ក្នុងការចងចាំថាសម្រាប់ benzene មិនអាចទៅរួចប្រតិកម្មបន្ថែមនៃអ៊ីដ្រូសែន halides (hydrohalogenation) និងការបន្ថែមទឹក (ជាតិទឹក) ។
3. ការជំនួសនៅក្នុងខ្សែសង្វាក់ចំហៀងនៃ benzene homologues
ក្រុមទី 3 នៃប្រតិកម្មទាក់ទងនឹងតែ benzene homologues - នេះគឺជាការជំនួសនៅក្នុងខ្សែសង្វាក់ចំហៀង។
ទីប្រាំពីរទ្រព្យសម្បត្តិនៅក្នុងបញ្ជីទូទៅ halogenation នៅអាតូមកាបូនអាល់ហ្វានៅក្នុងខ្សែសង្វាក់ចំហៀង។

ប្រតិកម្មកើតឡើងនៅពេលត្រូវកម្ដៅ ឬបញ្ចេញកាំរស្មី ហើយតែងតែនៅអាល់ហ្វាកាបូន។ នៅពេលដែល halogenation បន្ត អាតូម halogen ទីពីរនឹងត្រលប់ទៅទីតាំងអាល់ហ្វាវិញ។
4. អុកស៊ីតកម្មនៃ benzene homologues
ក្រុមទីបួននៃប្រតិកម្មគឺអុកស៊ីតកម្ម។
ចិញ្ចៀន benzene គឺខ្លាំងពេក, ដូច្នេះ benzene មិនកត់សុីប៉ូតាស្យូម permanganate មិនធ្វើឱ្យសូលុយស្យុងរបស់វាប្រែពណ៌ទេ។ នេះគឺសំខាន់ណាស់ក្នុងការចងចាំ។
ម្យ៉ាងវិញទៀត សារធាតុ benzene homologues ត្រូវបានកត់សុីជាមួយនឹងដំណោះស្រាយអាស៊ីតនៃប៉ូតាស្យូម permanganate នៅពេលកំដៅ។ ហើយនេះគឺជាទ្រព្យសម្បត្តិគីមីទីប្រាំបី។

វាប្រែចេញអាស៊ីត benzoic ។ ការប្រែពណ៌នៃដំណោះស្រាយត្រូវបានអង្កេត។ ក្នុងករណីនេះ មិនថាខ្សែសង្វាក់កាបូននៃសារធាតុជំនួសមានរយៈពេលយូរប៉ុណ្ណានោះទេ វាតែងតែបំបែកបន្ទាប់ពីអាតូមកាបូនទីមួយ ហើយអាតូមអាល់ហ្វាត្រូវបានកត់សុីទៅជាក្រុម carboxyl ជាមួយនឹងការបង្កើតអាស៊ីត benzoic ។ ម៉ូលេគុលដែលនៅសល់ត្រូវបានកត់សុីទៅជាអាស៊ីតដែលត្រូវគ្នា ឬប្រសិនបើវាជាអាតូមកាបូនតែមួយ ទៅជាកាបូនឌីអុកស៊ីត។
ប្រសិនបើ benzene homologue មានសារធាតុជំនួសអ៊ីដ្រូកាបូនច្រើនជាងមួយនៅលើសង្វៀនក្រអូប នោះការកត់សុីកើតឡើងតាមក្បួនដូចគ្នា - កាបូននៅក្នុងទីតាំងអាល់ហ្វាត្រូវបានកត់សុី។
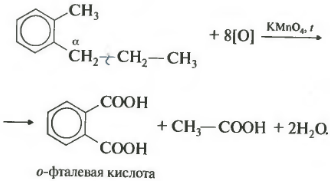
ក្នុងឧទាហរណ៍នេះ អាស៊ីតអាសេទិកឌីបាស៊ីកត្រូវបានទទួល ដែលត្រូវបានគេហៅថាអាស៊ីត phthalic ។
នៅក្នុងវិធីពិសេសមួយខ្ញុំកត់សម្គាល់ការកត់សុីនៃ cumene, isopropylbenzene ជាមួយនឹងអុកស៊ីសែនបរិយាកាសនៅក្នុងវត្តមាននៃអាស៊ីត sulfuric ។

នេះគឺជាអ្វីដែលគេហៅថា វិធីសាស្ត្រ cumene សម្រាប់ផលិត phenol ។ តាមក្បួនមួយមនុស្សម្នាក់ត្រូវតែដោះស្រាយជាមួយនឹងប្រតិកម្មនេះនៅក្នុងបញ្ហាទាក់ទងនឹងការផលិត phenol ។ នេះគឺជាវិធីឧស្សាហកម្ម។
ទីប្រាំបួនការឆេះទ្រព្យសម្បត្តិ ការកត់សុីពេញលេញជាមួយនឹងអុកស៊ីសែន។ Benzene និងលក្ខណៈដូចគ្នារបស់វាឆេះទៅជាកាបូនឌីអុកស៊ីត និងទឹក។
ចូរយើងសរសេរសមីការសម្រាប់ការឆេះនៃ benzene ក្នុងទម្រង់ទូទៅមួយ។
យោងតាមច្បាប់នៃការអភិរក្សម៉ាស់ គួរតែមានអាតូមច្រើននៅខាងឆ្វេង ព្រោះថាមានអាតូមនៅខាងស្តាំ។ ដោយសារតែនៅក្នុងប្រតិកម្មគីមី អាតូមមិនទៅណាទេ ប៉ុន្តែលំដាប់នៃចំណងរវាងពួកវាគ្រាន់តែផ្លាស់ប្តូរ។ ដូច្នេះវានឹងមានម៉ូលេគុលកាបូនឌីអុកស៊ីតច្រើនដូចដែលមានអាតូមកាបូននៅក្នុងម៉ូលេគុល Arene ព្រោះម៉ូលេគុលមានអាតូមកាបូនមួយ។ នោះគឺជាម៉ូលេគុល n CO 2 ។ វានឹងមានពាក់កណ្តាលនៃម៉ូលេគុលទឹកច្រើនដូចអាតូមអ៊ីដ្រូសែន ពោលគឺ (2n-6) / 2 ដែលមានន័យថា n-3 ។
មានអាតូមអុកស៊ីសែនដូចគ្នានៅខាងឆ្វេង និងខាងស្តាំ។ នៅខាងស្តាំមាន 2n ពីកាបូនឌីអុកស៊ីត ពីព្រោះមានអាតូមអុកស៊ីសែនពីរនៅក្នុងម៉ូលេគុលនីមួយៗ បូកនឹង n-3 ពីទឹកសម្រាប់សរុប 3n-3 ។ នៅខាងឆ្វេងមានអាតូមអុកស៊ីហ្សែន 3n-3 ដូចគ្នា ដែលមានន័យថាមានម៉ូលេគុលតិចជាងពីរដង ពីព្រោះម៉ូលេគុលមានអាតូមពីរ។ នោះគឺ (3n-3)/2 ម៉ូលេគុលអុកស៊ីសែន។
ដូច្នេះហើយ យើងបានចងក្រងសមីការសម្រាប់ការឆេះនៃ benzene homologues ក្នុងទម្រង់ទូទៅមួយ។
Arenes (អ៊ីដ្រូកាបូនក្រអូប) – ទាំងនេះគឺជាអ៊ីដ្រូកាបូនដែលមិនឆ្អែត (មិនឆ្អែត) ដែលម៉ូលេគុលមានក្រុមអាតូមដែលមានលំនឹង (នុយក្លេអ៊ែបេហ្សេន) ជាមួយនឹងប្រព័ន្ធបិទជិតនៃចំណងរួម។
រូបមន្តទូទៅ៖ C n H 2n–6សម្រាប់ n ≥ 6 ។
លក្ខណៈសម្បត្តិគីមីរបស់អារីន
សង្វៀន- អ៊ីដ្រូកាបូនមិនឆ្អែត ដែលជាម៉ូលេគុលដែលមានចំណងទ្វេបី និងវដ្តមួយ។ ប៉ុន្តែដោយសារឥទ្ធិពលនៃការផ្សំ លក្ខណៈសម្បត្តិរបស់អាណេខុសពីអ៊ីដ្រូកាបូនមិនឆ្អែតដទៃទៀត។
អ៊ីដ្រូកាបូនក្រអូបត្រូវបានកំណត់លក្ខណៈដោយប្រតិកម្ម៖
- ការចូលរួម,
- ការជំនួស,
- អុកស៊ីតកម្ម (សម្រាប់ benzene homologues) ។
ប្រព័ន្ធក្រអូបនៃ benzene មានភាពធន់នឹងភ្នាក់ងារអុកស៊ីតកម្ម។ ទោះជាយ៉ាងណាក៏ដោយ benzene homologs ត្រូវបានកត់សុីដោយសកម្មភាពនៃប៉ូតាស្យូម permanganate និងភ្នាក់ងារអុកស៊ីតកម្មផ្សេងទៀត។
1. ប្រតិកម្មបន្ថែម
Benzene បន្ថែមក្លរីននៅក្នុងពន្លឺ និងអ៊ីដ្រូសែននៅពេលដែលកំដៅនៅក្នុងវត្តមាននៃកាតាលីករ។
១.១. អ៊ីដ្រូសែន
Benzene បន្ថែមអ៊ីដ្រូសែននៅពេលដែលកំដៅនិងស្ថិតនៅក្រោមសម្ពាធនៅក្នុងវត្តមាននៃកាតាលីករដែក (Ni, Pt ។ ល។ ) ។
អ៊ីដ្រូសែននៃ benzene ផលិត cyclohexane:
អ៊ីដ្រូសែននៃភាពដូចគ្នាផ្តល់ឱ្យនិស្សន្ទវត្ថុ cycloalkane ។ នៅពេលដែល toluene ត្រូវបានកំដៅដោយអ៊ីដ្រូសែននៅក្រោមសម្ពាធ និងនៅក្នុងវត្តមាននៃកាតាលីករ methylcyclohexane ត្រូវបានបង្កើតឡើង:
១.២. chlorination នៃ arenes
ការបន្ថែមក្លរីនទៅ benzene ដំណើរការ ដោយយន្តការរ៉ាឌីកាល់នៅសីតុណ្ហភាពខ្ពស់។នៅក្រោមឥទ្ធិពលនៃវិទ្យុសកម្មអ៊ុលត្រាវីយូឡេ។
chlorination នៃ benzene នៅក្នុងវត្តមាននៃពន្លឺបង្កើត 1,2,3,4,5,6-hexachlorocyclohexane (hexachloran).
Hexachloran គឺជាថ្នាំសម្លាប់សត្វល្អិតដែលប្រើដើម្បីគ្រប់គ្រងសត្វល្អិតដែលបង្កគ្រោះថ្នាក់។ បច្ចុប្បន្ននេះការប្រើប្រាស់ hexachlorane ត្រូវបានហាមឃាត់។
Benzene ដូចគ្នាមិនបន្ថែមក្លរីនទេ។ ប្រសិនបើ benzene homologue មានប្រតិកម្មជាមួយនឹងក្លរីនឬ bromine ប៉ះពាល់នឹងពន្លឺ ឬសីតុណ្ហភាពខ្ពស់ (300°C)បន្ទាប់មកមានការជំនួសអាតូមអ៊ីដ្រូសែន នៅលើផ្នែកជំនួស alkyl មិនមែននៅលើចិញ្ចៀនក្រអូបទេ។
2. ប្រតិកម្មជំនួស
២.១. ហាឡូជីន
Benzene និងលក្ខណៈដូចគ្នារបស់វាចូលទៅក្នុងប្រតិកម្មជំនួសជាមួយ halogens (chlorine, bromine) នៅក្នុងវត្តមាននៃកាតាលីករ (AlCl 3, FeBr 3) .
នៅពេលធ្វើអន្តរកម្មជាមួយក្លរីនលើកាតាលីករ AlCl 3 ក្លរ៉ូបេហ្សេនត្រូវបានបង្កើតឡើង៖
អ៊ីដ្រូកាបូនក្រអូបមានអន្តរកម្មជាមួយ bromine នៅពេលដែលកំដៅ និងនៅក្នុងវត្តមាននៃកាតាលីករ - FeBr 3 ។ ដែកលោហធាតុក៏អាចត្រូវបានប្រើជាកាតាលីករផងដែរ។
ប្រូមីនមានប្រតិកម្មជាមួយជាតិដែកដើម្បីបង្កើតជាជាតិដែក (III) bromide ដែលជំរុញការបំប្លែងសារធាតុបេនហ្សេន៖
មេតា chlorotoluene ត្រូវបានបង្កើតឡើងក្នុងបរិមាណតិចតួច។
នៅក្នុងអន្តរកម្មនៃ benzene homologues ជាមួយ halogens នៅក្នុងពន្លឺឬនៅសីតុណ្ហភាពខ្ពស់។(300 o C) អ៊ីដ្រូសែនត្រូវបានជំនួសមិនមែននៅក្នុងរង្វង់ benzene ទេប៉ុន្តែនៅក្នុងរ៉ាឌីកាល់អ៊ីដ្រូកាបូន។
ឧទាហរណ៍នៅពេល chlorinating ethylbenzene:
២.២. នីត្រាត
Benzene មានប្រតិកម្មជាមួយនឹងអាស៊ីតនីទ្រីកប្រមូលផ្តុំនៅក្នុងវត្តមាននៃអាស៊ីតស៊ុលហ្វួរីកប្រមូលផ្តុំ (ល្បាយនីត្រាត) ។
ក្នុងករណីនេះ nitrobenzene ត្រូវបានបង្កើតឡើង:
Toluene មានប្រតិកម្មជាមួយនឹងអាស៊ីតនីទ្រីកប្រមូលផ្តុំនៅក្នុងវត្តមាននៃអាស៊ីតស៊ុលហ្វួរីកប្រមូលផ្តុំ។
នៅក្នុងផលិតផលប្រតិកម្ម យើងចង្អុលបង្ហាញផងដែរ។ អំពី- nitrotoluene៖
ឬ ទំ- nitrotoluene៖
nitration នៃ toluene ក៏អាចបន្តជាមួយនឹងការជំនួសអាតូមអ៊ីដ្រូសែនបី។ ក្នុងករណីនេះ 2,4,6-trinitrotoluene (trotyl, tol) ត្រូវបានបង្កើតឡើង:
២.៣. Alkylation នៃអ៊ីដ្រូកាបូនក្រអូប
- Arenes ធ្វើអន្តរកម្មជាមួយ haloalkanes នៅក្នុងវត្តមាននៃកាតាលីករ (AlCl 3, FeBr 3 ។
- អ៊ីដ្រូកាបូនក្រអូបមានអន្តរកម្មជាមួយអាល់ខេននៅក្នុងវត្តមាននៃក្លរួអាលុយមីញ៉ូម ជាតិដែក (III) bromide អាស៊ីតផូស្វ័រ។ល។
- Alkylation ជាមួយអាល់កុលដំណើរការនៅក្នុងវត្តមាននៃអាស៊ីតស៊ុលហ្វួរីកប្រមូលផ្តុំ។
២.៤. Sulfonation នៃអ៊ីដ្រូកាបូនក្រអូប
Benzene មានប្រតិកម្មនៅពេលដែលត្រូវបានកំដៅជាមួយនឹងអាស៊ីតស៊ុលហ្វួរីកកំហាប់ ឬដំណោះស្រាយនៃ SO 3 នៅក្នុងអាស៊ីតស៊ុលហ្វួរិក (oleum) ដើម្បីបង្កើតជាអាស៊ីត benzenesulfonic៖
3. អុកស៊ីតកម្មនៃ arenes
Benzene មានភាពធន់នឹងភ្នាក់ងារអុកស៊ីតកម្មខ្លាំង។ ប៉ុន្តែ benzene homologues ត្រូវបានកត់សុីក្រោមសកម្មភាពនៃភ្នាក់ងារអុកស៊ីតកម្មដ៏រឹងមាំ។ Benzene និង homologs របស់វាឆេះ។
3.1. អុកស៊ីតកម្មពេញលេញ - ចំហេះ
ចំហេះនៃ benzene និង homologues របស់វាផលិតកាបូនឌីអុកស៊ីត និងទឹក។ ប្រតិកម្មចំហេះរបស់ arenes ត្រូវបានអមដោយការបញ្ចេញកំដៅយ៉ាងច្រើន។
2C 6 H 6 + 15O 2 → 12CO 2 + 6H 2 O + Q
សមីការចំហេះទូទៅសម្រាប់ arenes គឺ៖
C n H 2n–6 + (3n–3)/2 O 2 → nCO 2 + (n–3)H 2 O + សំណួរ
នៅពេលដែលអ៊ីដ្រូកាបូនក្រអូបដុតដោយខ្វះអុកស៊ីសែន កាបូនម៉ូណូអុកស៊ីត CO ឬ soot C អាចត្រូវបានបង្កើតឡើង។
Benzene និងមនុស្សដូចគ្នារបស់វាឆេះនៅលើអាកាសជាមួយនឹងអណ្តាតភ្លើងដែលមានផ្សែង។ Benzene និងលក្ខណៈដូចគ្នារបស់វាបង្កើតជាល្បាយផ្ទុះជាមួយខ្យល់ និងអុកស៊ីសែន។
៣.២. អូការកត់សុីនៃ benzene homologues
ភាពដូចគ្នានៃ Benzene ត្រូវបានកត់សុីយ៉ាងងាយដោយ permanganate និងប៉ូតាស្យូម dichromate នៅក្នុងឧបករណ៍ផ្ទុកអាសុីត ឬអព្យាក្រឹត នៅពេលដែលកំដៅ។
ក្នុងពេលជាមួយគ្នានេះវាកើតឡើង ការកត់សុីនៃចំណងទាំងអស់នៅអាតូមកាបូននៅជាប់នឹងចិញ្ចៀន benzene លើកលែងតែចំណងនៃអាតូមកាបូននេះទៅនឹងចិញ្ចៀន benzene ។
Toluene កត់សុី ប៉ូតាស្យូម permanganate នៅក្នុងអាស៊ីតស៊ុលហ្វួរីជាមួយនឹងការអប់រំ អាស៊ីត benzoic៖
ប្រសិនបើ toluene ត្រូវបានកត់សុី នៅក្នុងដំណោះស្រាយអព្យាក្រឹតនៅពេលដែលកំដៅបន្ទាប់មកវាត្រូវបានបង្កើតឡើង អំបិលអាស៊ីត benzoic - ប៉ូតាស្យូម benzoate៖
ដូច្នេះ toluene decolorizes ដំណោះស្រាយអាស៊ីតប៉ូតាស្យូម permanganateនៅពេលកំដៅ។
រ៉ាឌីកាល់វែងត្រូវបានកត់សុីទៅជាអាស៊ីត benzoic និងអាស៊ីត carboxylic៖
នៅពេលដែល propylbenzene ត្រូវបានកត់សុី អាស៊ីត benzoic និង acetic ត្រូវបានបង្កើតឡើង៖
Isopropylbenzene ត្រូវបានកត់សុីដោយប៉ូតាស្យូម permanganate ក្នុងបរិយាកាសអាសុីតទៅជាអាស៊ីត benzoic និងកាបូនឌីអុកស៊ីត៖
4. សកម្មភាពតម្រង់ទិសនៃសារធាតុជំនួសនៅក្នុងរង្វង់ benzene
ប្រសិនបើមានសារធាតុជំនួសនៅក្នុងសង្វៀន benzene មិនត្រឹមតែអាល់គីលប៉ុណ្ណោះទេ ថែមទាំងមានអាតូមផ្សេងទៀត (អ៊ីដ្រូសែន ក្រុមអាមីណូ ក្រុមនីត្រូ។ ស្របតាមធម្មជាតិ ឥទ្ធិពលនៃសារធាតុជំនួសនៅលើប្រព័ន្ធ π- ក្រអូប។
ប្រភេទនៃសារធាតុជំនួសនៅលើចិញ្ចៀន benzene
| សារធាតុជំនួសនៃប្រភេទទីមួយ | សារធាតុជំនួសនៃប្រភេទទីពីរ |
| អ័រថូ- និង គូ-ទីតាំង | ការជំនួសបន្ថែមទៀតកើតឡើងជាចម្បងនៅក្នុង មេតា-ទីតាំង |
| ម្ចាស់ជំនួយអេឡិចត្រុង បង្កើនដង់ស៊ីតេអេឡិចត្រុងនៅក្នុងរង្វង់ benzene | ការដកអេឡិចត្រុងកាត់បន្ថយដង់ស៊ីតេអេឡិចត្រុងនៅក្នុងប្រព័ន្ធភ្ជាប់។ |
|
|
