លោក Antoine Laurent LAVOISIER ( ) ( ) បានស៊ើបអង្កេតអុកស៊ីហ្សែន និងបង្កើតទ្រឹស្ដីអុកស៊ីហ្សែននៃការឆេះ ដែលជំនួសទ្រឹស្ដី phlogiston ។ គាត់បានសិក្សាអុកស៊ីហ្សែន និងបង្កើតទ្រឹស្ដីអុកស៊ីហ្សែននៃការឆេះ ដែលជំនួសទ្រឹស្ដី phlogiston ។

អុកស៊ីសែនគឺជាធាតុទូទៅបំផុតនៅលើផែនដី នៅលើអាកាស ២១% (តាមបរិមាណ) ក្នុងខ្យល់ ២១% (បរិមាណ) ក្នុងសំបកផែនដី ៤៩% (ដោយម៉ាស់) ក្នុងសំបកផែនដី ៤៩% (ដោយម៉ាស់) នៅក្នុងអ៊ីដ្រូស្វ៊ែរ 89% (ដោយម៉ាស់) នៅក្នុងអ៊ីដ្រូស្វ៊ែរ 89% (ដោយម៉ាស់) នៅក្នុងសារពាង្គកាយមានជីវិតរហូតដល់ 65% ដោយម៉ាស់។ នៅក្នុងសារពាង្គកាយមានជីវិតរហូតដល់ 65% នៃម៉ាស។

លក្ខណៈសម្បត្តិរូបវន្តរដ្ឋសរុប - ឧស្ម័ននៅក្រោមលក្ខខណ្ឌធម្មតា។ នៅសីតុណ្ហភាពទាបខ្លាំង (-183°C) វាប្រែទៅជាសភាពរាវនៃការប្រមូលផ្តុំ (រាវពណ៌ខៀវ) ហើយនៅសីតុណ្ហភាពទាបជាង (-219°C) វាក្លាយជារឹង (គ្រីស្តាល់ព្រិលពណ៌ខៀវ)។ ស្ថានភាពសរុប - ឧស្ម័ននៅក្រោមលក្ខខណ្ឌធម្មតា។ នៅសីតុណ្ហភាពទាបខ្លាំង (-183°C) វាប្រែទៅជាសភាពរាវនៃការប្រមូលផ្តុំ (រាវពណ៌ខៀវ) ហើយនៅសីតុណ្ហភាពទាបជាង (-219°C) វាក្លាយជារឹង (គ្រីស្តាល់ព្រិលពណ៌ខៀវ)។ ពណ៌ - គ្មានពណ៌។ ពណ៌ - គ្មានពណ៌។ ក្លិន - គ្មានក្លិន។ ក្លិន - គ្មានក្លិន។ ភាពរលាយក្នុងទឹក - រលាយតិចតួច។ ភាពរលាយក្នុងទឹក - រលាយតិចតួច។ ធ្ងន់ជាងខ្យល់ ( M ខ្យល់ = 29 ក្រាម / mol និង M O 2 = 32 ក្រាម / mol ។ ធ្ងន់ជាងខ្យល់ ( M ខ្យល់ = 29 ក្រាម / mol និង M O 2 = 32 ក្រាម / mol ។

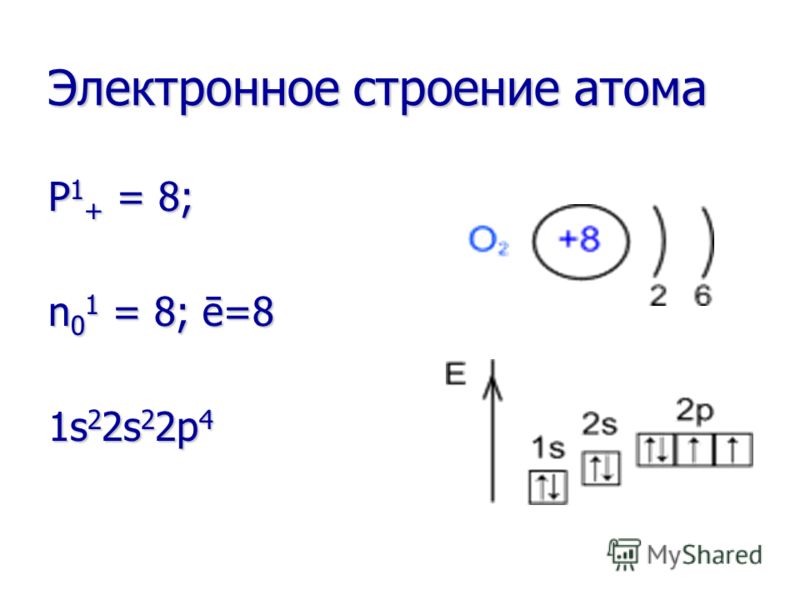
លក្ខណៈសម្បត្តិគីមី អុកស៊ីហ្សែនជាភ្នាក់ងារអុកស៊ីតកម្មខ្លាំង! វាធ្វើអុកស៊ីតកម្មសារធាតុជាច្រើនរួចហើយនៅសីតុណ្ហភាពបន្ទប់ (អុកស៊ីតកម្មយឺត) ហើយលើសពីនេះទៀតនៅពេលដែលសារធាតុត្រូវបានកំដៅ ឬដុត (អុកស៊ីតកម្មលឿន)។ អុកស៊ីហ្សែនជាភ្នាក់ងារអុកស៊ីតកម្មខ្លាំង! វាធ្វើអុកស៊ីតកម្មសារធាតុជាច្រើនរួចហើយនៅសីតុណ្ហភាពបន្ទប់ (អុកស៊ីតកម្មយឺត) ហើយលើសពីនេះទៀតនៅពេលដែលសារធាតុត្រូវបានកំដៅ ឬដុត (អុកស៊ីតកម្មលឿន)។ នៅក្នុងប្រតិកម្មជាមួយធាតុទាំងអស់ (លើកលែងតែហ្វ្លុយអូរីន) អុកស៊ីសែនតែងតែជាភ្នាក់ងារអុកស៊ីតកម្ម។ នៅក្នុងប្រតិកម្មជាមួយធាតុទាំងអស់ (លើកលែងតែហ្វ្លុយអូរីន) អុកស៊ីសែនតែងតែជាភ្នាក់ងារអុកស៊ីតកម្ម។

ប្រតិកម្មជាមួយលោហធាតុ ជាលទ្ធផលនៃប្រតិកម្មអុកស៊ីតនៃលោហៈនេះត្រូវបានបង្កើតឡើង។ ឧទាហរណ៍អាលុយមីញ៉ូមត្រូវបានកត់សុីដោយអុកស៊ីហ៊្សែនយោងទៅតាមសមីការ: ជាលទ្ធផលនៃប្រតិកម្មអុកស៊ីដនៃលោហៈនេះត្រូវបានបង្កើតឡើង។ ឧទាហរណ៍អាលុយមីញ៉ូមត្រូវបានកត់សុីដោយអុកស៊ីហ៊្សែនយោងទៅតាមសមីការ: t° 4Al + 3O 2 2Al 2 O 3 t° 4Al + 3O 2 2Al 2 O 3 ឧទាហរណ៍មួយទៀត។ នៅពេលទម្លាក់ខ្សែដែកក្តៅក្រហមចូលទៅក្នុងដបអុកស៊ីហ្សែន នោះខ្សែភ្លើងឆេះចេញ បាញ់ទៅសងខាង ធ្វើឱ្យមានផ្កាភ្លើង - ភាគល្អិតក្តៅនៃមាត្រដ្ឋានដែក Fe 3 O 4: t ° 3Fe + 2O 2 Fe 3 O 4 t ° 3Fe + 2O 2 Fe 3 O 4


ឧទាហរណ៍ផ្សេងទៀតនៃប្រតិកម្មជាមួយលោហធាតុ ្រំមហះនៃស្ពាន់ធ័រនៅក្នុងអុកស៊ីសែនដើម្បីបង្កើតជាស្ពាន់ធ័រឌីអុកស៊ីត SO 2: t ° S + O 2 SO 2 t ° S + O 2 SO 2 ការដុតធ្យូងថ្មនៅក្នុងអុកស៊ីសែនដើម្បីបង្កើតជាកាបូនឌីអុកស៊ីត: ការដុតធ្យូងថ្មនៅក្នុង អុកស៊ីសែនដើម្បីបង្កើតកាបូនឌីអុកស៊ីត: t ° C + O 2 CO 2 t ° C + O 2 CO 2
ប្រតិកម្មជាមួយសារធាតុស្មុគ្រស្មាញមួយចំនួន ក្នុងករណីនេះ អុកស៊ីដនៃធាតុដែលបង្កើតបានជាម៉ូលេគុលនៃសារធាតុស្មុគស្មាញមួយត្រូវបានបង្កើតឡើង។ ក្នុងករណីនេះអុកស៊ីដនៃធាតុដែលបង្កើតជាម៉ូលេគុលនៃសារធាតុស្មុគស្មាញមួយត្រូវបានបង្កើតឡើង។ ឧទាហរណ៍នៅពេលដុតទង់ដែង (II) ស៊ុលហ្វីត ឧទាហរណ៍នៅពេលដុតទង់ដែង (II) ស៊ុលហ្វីត t ° 2CuS + 3O 2 2CuO + 2SO 2 t ° 2CuS + 3O 2 2CuO + 2SO 2 អុកស៊ីដពីរត្រូវបានបង្កើតជាទង់ដែង (II) អុកស៊ីដ និងស្ពាន់ធ័រអុកស៊ីដ (IV) ។ អុកស៊ីដពីរត្រូវបានបង្កើតឡើង អុកស៊ីដទង់ដែង (II) និងអុកស៊ីដស្ពាន់ធ័រ (IV) ។ កំឡុងពេលអាំងស៊ុលហ្វីត អុកស៊ីដស្ពាន់ធ័រត្រូវបានបង្កើតឡើងជានិច្ច ដែលក្នុងនោះ វ៉ាល់ស៊ុលហ្វួគឺ IV ។ កំឡុងពេលអាំងស៊ុលហ្វីត អុកស៊ីដស្ពាន់ធ័រត្រូវបានបង្កើតឡើងជានិច្ច ដែលក្នុងនោះ វ៉ាល់ស៊ុលហ្វួគឺ IV ។ ឧទាហរណ៍មួយទៀតគឺការដុតមេតាន CH 4។ ដោយសារម៉ូលេគុលនេះមានអាតូមនៃធាតុកាបូន C និងអ៊ីដ្រូសែន H វាមានន័យថាអុកស៊ីដពីរត្រូវបានបង្កើតជាកាបូនម៉ូណូអុកស៊ីត (IV) CO 2 និងអ៊ីដ្រូសែនអុកស៊ីដ ពោលគឺទឹក - H 2 ។ O: t ° CH 4 + 2O 2 CO 2 + 2H 2 O t ° CH 4 + 2O 2 CO 2 + 2H 2 O

អន្តរកម្មគីមីនៃសារធាតុជាមួយអុកស៊ីសែនត្រូវបានគេហៅថាប្រតិកម្មអុកស៊ីតកម្ម។ ប្រតិកម្មអុកស៊ីតកម្មដែលអមដោយការបញ្ចេញកំដៅនិងពន្លឺត្រូវបានគេហៅថាប្រតិកម្មចំហេះ។ ប្រតិកម្មចំហេះនៃសារធាតុគឺជាឧទាហរណ៍នៃការកត់សុីយ៉ាងឆាប់រហ័ស ប៉ុន្តែការរលួយ ការច្រេះជាដើម។ ទាំងនេះគឺជាឧទាហរណ៍នៃការកត់សុីយឺតនៃសារធាតុជាមួយនឹងអុកស៊ីសែន។ ប្រតិកម្មចំហេះនៃសារធាតុគឺជាឧទាហរណ៍នៃការកត់សុីលឿន ប៉ុន្តែការរលួយ ការច្រេះជាដើម។ ទាំងនេះគឺជាឧទាហរណ៍នៃការកត់សុីយឺតនៃសារធាតុដោយអុកស៊ីសែន

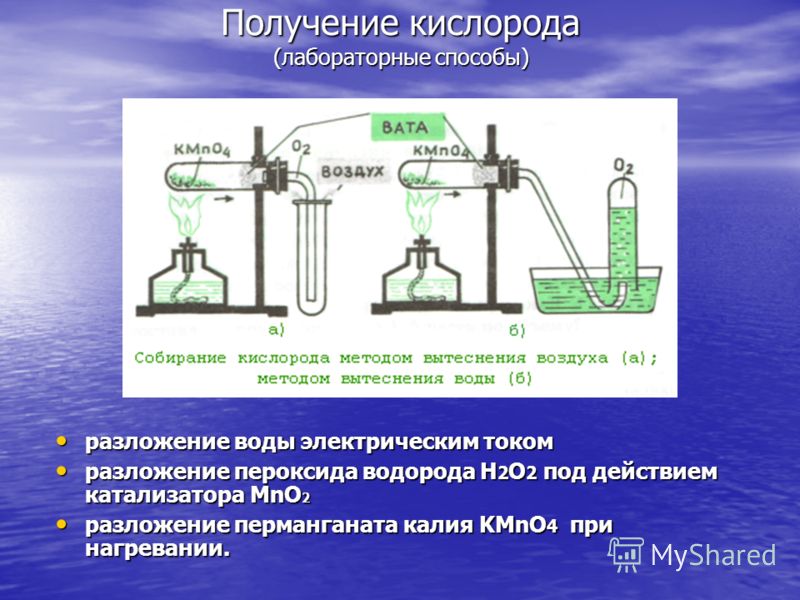
ការផលិតអុកស៊ីហ្សែន (វិធីសាស្ត្រមន្ទីរពិសោធន៍) ការបំបែកទឹកដោយចរន្តអគ្គិសនី ការបំផ្លិចបំផ្លាញដោយចរន្តអគ្គិសនីនៃអ៊ីដ្រូសែន peroxide H 2 O 2 ក្រោមសកម្មភាពនៃការបំផ្លិចបំផ្លាញកាតាលីករ MnO 2 នៃអ៊ីដ្រូសែន peroxide H 2 O 2 ក្រោមសកម្មភាពនៃ MnO 2 កាតាលីករ decomposition ប៉ូតាស្យូម permanganate KMnO 4 នៅពេលកំដៅ។ ការបំផ្លាញប៉ូតាស្យូម permanganate KMnO 4 នៅពេលកំដៅ។
ការទទួលបានអុកស៊ីសែន (វិធីសាស្ត្រឧស្សាហកម្ម) នៅក្នុងឧស្សាហកម្ម ដើម្បីទទួលបានអុកស៊ីហ្សែនសុទ្ធ ការចម្រោះនៃខ្យល់រាវត្រូវបានប្រើប្រាស់ ដោយផ្អែកលើសីតុណ្ហភាពពុះផ្សេងៗគ្នានៃសមាសធាតុខ្យល់។ ខ្យល់ត្រជាក់ដល់ -200°C ហើយបន្ទាប់មកឡើងកំដៅបន្តិចម្តងៗ។ នៅពេលដែលសីតុណ្ហភាពឡើងដល់ -183°C អុកស៊ីសែនរត់ចេញពីខ្យល់រាវ សមាសធាតុដែលនៅសល់នៃខ្យល់រាវនៅសីតុណ្ហភាពនេះនៅតែស្ថិតក្នុងសភាពរាវនៃការប្រមូលផ្តុំ។ នៅក្នុងឧស្សាហកម្ម ដើម្បីទទួលបានអុកស៊ីហ្សែនសុទ្ធ ការចម្រោះនៃខ្យល់រាវត្រូវបានប្រើ ដោយផ្អែកលើចំណុចរំពុះផ្សេងគ្នានៃសមាសធាតុខ្យល់។ ខ្យល់ត្រជាក់ដល់ -200°C ហើយបន្ទាប់មកឡើងកំដៅបន្តិចម្តងៗ។ នៅពេលដែលសីតុណ្ហភាពឡើងដល់ -183°C អុកស៊ីសែនរត់ចេញពីខ្យល់រាវ សមាសធាតុដែលនៅសល់នៃខ្យល់រាវនៅសីតុណ្ហភាពនេះនៅតែស្ថិតក្នុងសភាពរាវនៃការប្រមូលផ្តុំ។

ការប្រើប្រាស់អុកស៊ីហ្សែនក្នុងសំណង់ និងវិស្វកម្មមេកានិកក្នុងសំណង់ និងវិស្វកម្មមេកានិក - សម្រាប់ការផ្សារឧស្ម័នអុកស៊ីត-អាសេទីលីន និងការកាត់ឧស្ម័ននៃលោហធាតុ - សម្រាប់ការផ្សារឧស្ម័នអុកស៊ីតអាសេទីលីន និងការកាត់ឧស្ម័ននៃលោហធាតុ - សម្រាប់បាញ់ថ្នាំ និងលាបលោហៈក្នុងផលិតកម្មប្រេង ក្នុងការផលិតប្រេង។ - នៅពេលចាក់បញ្ចូលទៅក្នុងការបង្កើតដើម្បីបង្កើនថាមពលផ្លាស់ទីលំនៅក្នុងលោហធាតុ និងឧស្សាហកម្មរ៉ែក្នុងលោហធាតុ និងឧស្សាហកម្មរ៉ែ - នៅក្នុងការផលិតដែក convective ការបំផ្ទុះអុកស៊ីហ៊្សែននៅក្នុងឡដុត ការទាញយកមាស និងរ៉ែ ការផលិត ferroalloys ការរលាយនីកែល ស័ង្កសី សំណ។ , zirconium និងលោហៈដែលមិនមែនជាជាតិដែកផ្សេងទៀត - នៅក្នុងការផលិតដែក convective, ការផ្ទុះអុកស៊ីសែននៅក្នុង furnaces ការផ្ទុះ, ការទាញយកមាសនិងរ៉ែ, ការផលិតនៃ ferroalloys, smelting នីកែល, ស័ង្កសី, សំណ, zirconium និងលោហៈមិនមែនជាតិដែកផ្សេងទៀត - ជាមួយនឹងការកាត់បន្ថយដោយផ្ទាល់នៃ ជាតិដែក - ជាមួយនឹងការកាត់បន្ថយដោយផ្ទាល់នៃជាតិដែក - ជាមួយនឹងការសម្អាតភ្លើងនៅក្នុងការផលិតគ្រឹះ - ជាមួយនឹងការសម្អាតអគ្គីភ័យនៅក្នុងការផលិតគ្រឹះ - ជាមួយនឹងការខួងភ្លើង x ពូជ

ការប្រើប្រាស់អុកស៊ីហ៊្សែនក្នុងឱសថក្នុងឱសថ - នៅក្នុងបន្ទប់អុកស៊ីហ៊្សែន - នៅក្នុងបន្ទប់អុកស៊ីសែន - នៅពេលបំពេញរបាំងអុកស៊ីហ៊្សែន ខ្នើយ។ល។ - ពេលបំពេញរបាំងអុកស៊ីហ្សែន ខ្នើយ។ល។ - នៅក្នុងវួដដែលមាន microclimate ពិសេស - នៅក្នុងវួដដែលមាន microclimate ពិសេស - សម្រាប់ការផលិតស្រាក្រឡុកអុកស៊ីហ៊្សែន - សម្រាប់ការផលិតស្រាក្រឡុកអុកស៊ីហ៊្សែន - ក្នុងការដាំដុះមីក្រូសរីរាង្គ - ក្នុងការដាំដុះមីក្រូសរីរាង្គនៅក្នុងបរិស្ថានវិទ្យាក្នុងបរិស្ថានវិទ្យា - ក្នុងការបន្សុតនៃការផឹក។ ទឹក - ក្នុងការបន្សុតទឹកផឹក - ក្នុងការកែច្នៃលោហធាតុ - ពេលកែច្នៃលោហធាតុ - ពេលផ្លុំទឹកសំណល់ជាមួយអុកស៊ីហ្សែន - ពេលផ្លុំទឹកសំណល់ជាមួយអុកស៊ីសែន - ពេលបន្សាបកាកសំណល់សកម្មគីមីនៅក្នុងរោងចក្រប្រព្រឹត្តិកម្មក្នុងឡដុត - នៅពេលបន្សាបកាកសំណល់សកម្មគីមីនៅក្នុងរោងចក្រប្រព្រឹត្តិកម្ម។ នៅក្នុងឡដុត

ការប្រើប្រាស់អុកស៊ីសែននៅក្នុងឧស្សាហកម្មគីមីក្នុងឧស្សាហកម្មគីមី - ក្នុងការផលិតអាសេទីលលីន សែលុយឡូស ជាតិអាល់កុល មេទីល អាម៉ូញាក់ នីទ្រីក និងអាស៊ីតស៊ុលហ្វួរីក - ក្នុងការផលិតអាសេទីលីន សែលុយឡូស ជាតិអាល់កុលមេទីល អាម៉ូញាក់ នីទ្រីក និងអាស៊ីតស៊ុលហ្វួរីក - ក្នុង ការបំប្លែងកាតាលីករនៃឧស្ម័នធម្មជាតិ (ក្នុងការផលិតអាម៉ូញាក់សំយោគ) - នៅក្នុងការបំប្លែងកាតាលីករនៃឧស្ម័នធម្មជាតិ (ក្នុងការផលិតអាម៉ូញាក់សំយោគ) - នៅក្នុងការបំប្លែងសីតុណ្ហភាពខ្ពស់នៃមេតាន - នៅក្នុងការបំប្លែងសីតុណ្ហភាពខ្ពស់នៃមេតាននៅក្នុង ឧស្សាហកម្មថាមពលនៅក្នុងឧស្សាហកម្មថាមពល - នៅក្នុងការបំប្លែងឧស្ម័ននៃឥន្ធនៈរឹង - នៅក្នុងការបំប្លែងឧស្ម័ននៃឥន្ធនៈរឹង - សម្រាប់ការបង្កើនខ្យល់សម្រាប់ឡចំហាយក្នុងស្រុកនិងឧស្សាហកម្ម - សម្រាប់បង្កើនខ្យល់សម្រាប់ឡចំហាយក្នុងស្រុកនិងឧស្សាហកម្ម - សម្រាប់ការបង្ហាប់ទឹក - ល្បាយធ្យូងថ្ម - សម្រាប់បង្ហាប់ទឹក - ល្បាយធ្យូងថ្ម

ការប្រើប្រាស់អុកស៊ីសែននៅក្នុងឧបករណ៍យោធា នៅក្នុងឧបករណ៍យោធា - នៅក្នុងបន្ទប់សម្ពាធ - នៅក្នុងបន្ទប់សម្ពាធ - សម្រាប់ប្រតិបត្តិការម៉ាស៊ីនម៉ាស៊ូតនៅក្រោមទឹក - សម្រាប់ប្រតិបត្តិការម៉ាស៊ីនម៉ាស៊ូតនៅក្រោមទឹក - ជាសារធាតុអុកស៊ីតកម្មឥន្ធនៈសម្រាប់ម៉ាស៊ីនរ៉ុក្កែត - ជាសារធាតុអុកស៊ីតកម្មឥន្ធនៈសម្រាប់ ម៉ាស៊ីនរ៉ុក្កែតក្នុងវិស័យកសិកម្មក្នុងវិស័យកសិកម្ម - សម្រាប់ពង្រឹងបរិយាកាសក្នុងទឹកជាមួយនឹងអុកស៊ីសែនក្នុងការនេសាទ - សម្រាប់ពង្រឹងបរិយាកាសក្នុងទឹកជាមួយនឹងអុកស៊ីហ្សែនក្នុងការនេសាទ - ក្នុងការផលិតស្រាក្រឡុកអុកស៊ីហ្សែន - ក្នុងការផលិតក្រឡុកអុកស៊ីហ្សែន - សម្រាប់ការឡើងទម្ងន់សត្វ - សម្រាប់ការឡើងទម្ងន់សត្វ។

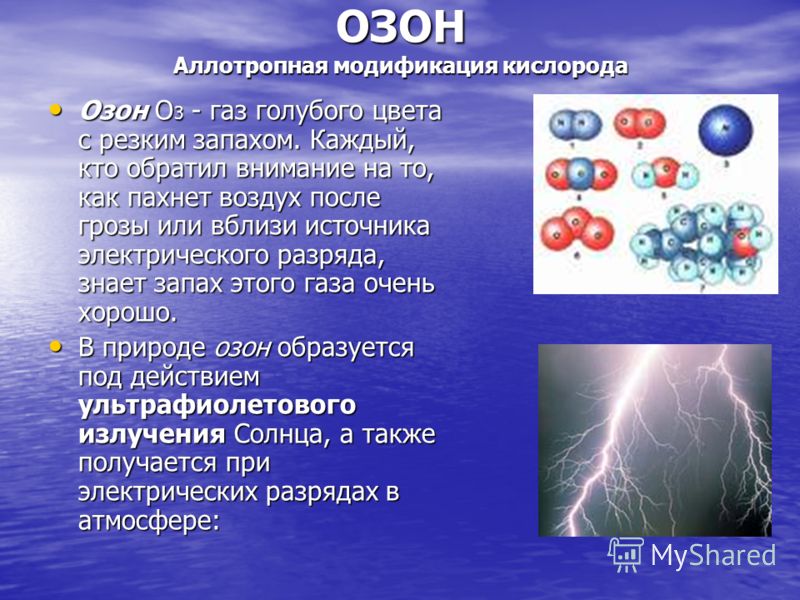
ការកែប្រែ OZONE Allotropic នៃអុកស៊ីសែន អូហ្សូន O 3 គឺជាឧស្ម័នពណ៌ខៀវដែលមានក្លិនស្អុយ។ អ្នកណាដែលបានយកចិត្តទុកដាក់ថាតើខ្យល់មានក្លិនយ៉ាងណាបន្ទាប់ពីមានខ្យល់ព្យុះផ្គររន្ទះ ឬនៅជិតប្រភពនៃការបញ្ចេញចរន្តអគ្គិសនីច្បាស់ជាស្គាល់ក្លិនឧស្ម័ននេះយ៉ាងច្បាស់។ អូហ្សូន O 3 គឺជាឧស្ម័នពណ៌ខៀវដែលមានក្លិនស្អុយ។ អ្នកណាដែលបានយកចិត្តទុកដាក់ថាតើខ្យល់មានក្លិនយ៉ាងណាបន្ទាប់ពីមានខ្យល់ព្យុះផ្គររន្ទះ ឬនៅជិតប្រភពនៃការបញ្ចេញចរន្តអគ្គិសនីច្បាស់ជាស្គាល់ក្លិនឧស្ម័ននេះយ៉ាងច្បាស់។ នៅក្នុងធម្មជាតិ អូហ្សូនត្រូវបានបង្កើតឡើងដោយសកម្មភាពនៃវិទ្យុសកម្មអ៊ុលត្រាវីយូឡេពីព្រះអាទិត្យ ហើយក៏ត្រូវបានផលិតដោយការឆក់អគ្គិសនីនៅក្នុងបរិយាកាស៖
អូហ្សូនគឺជាភ្នាក់ងារអុកស៊ីតកម្មដ៏រឹងមាំដូច្នេះវាត្រូវបានគេប្រើក្នុងការលាងចានទឹកផឹក។ នៅពេលទំនាក់ទំនងជាមួយសារធាតុដែលអាចកត់សុីបានភាគច្រើនការផ្ទុះកើតឡើង។ អូហ្សូនត្រូវបានបង្កើតឡើងនៅក្នុងបរិយាកាសផែនដីនៅកម្ពស់ 25 គីឡូម៉ែត្រក្រោមឥទ្ធិពលនៃវិទ្យុសកម្មព្រះអាទិត្យវាស្រូបយកវិទ្យុសកម្មដ៏គ្រោះថ្នាក់ពីព្រះអាទិត្យ។ ទោះជាយ៉ាងណាក៏ដោយនៅក្នុងអូហ្សូន "ឆ័ត្រ" នៃផែនដីមានកម្រាស់ត្រឹមតែ 30 ម៉ែត្រប៉ុណ្ណោះ "រន្ធ" លេចឡើងរាល់ពេល។ ឧស្ម័នកាន់តែច្រើនឡើងៗ "បង្កគ្រោះថ្នាក់" ដល់អូហ្សូន ដូចជា អាសូតម៉ូណូអុកស៊ីត NO ឬសារធាតុទាំងនោះដែលត្រូវបានប្រើដើម្បីបំពេញទូរទឹកកក និងកំប៉ុងអេរ៉ូសូល កំពុងចូលទៅក្នុងខ្យល់។ សូម្បីតែការបាត់ខ្លួនមួយផ្នែកនៃស្រទាប់អូហ្សូនពីលើផែនដី គំរាមកំហែងដល់ជីវិតទាំងអស់ជាមួយនឹងការស្លាប់… ទោះជាយ៉ាងណាក៏ដោយ នៅក្នុងអូហ្សូន "ឆ័ត្រ" នៃផែនដីមានកម្រាស់ត្រឹមតែ 30 ម៉ែត្រប៉ុណ្ណោះ "រន្ធ" លេចឡើងរាល់ពេល។ ឧស្ម័នកាន់តែច្រើនឡើងៗ "បង្កគ្រោះថ្នាក់" ដល់អូហ្សូន ដូចជា អាសូតម៉ូណូអុកស៊ីត NO ឬសារធាតុទាំងនោះដែលត្រូវបានប្រើដើម្បីបំពេញទូរទឹកកក និងកំប៉ុងអេរ៉ូសូល កំពុងចូលទៅក្នុងខ្យល់។ សូម្បីតែការបាត់ខ្លួនមួយផ្នែកនៃស្រទាប់អូហ្សូនពីលើផែនដី ក៏គំរាមកំហែងដល់ជីវិតទាំងអស់នឹងការស្លាប់...


