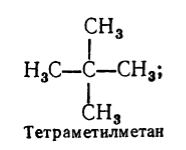
Alkane :
Alkane sind gesättigte Kohlenwasserstoffe, in deren Molekülen alle Atome durch Einfachbindungen verbunden sind. Formel -
Physikalische Eigenschaften :
- Schmelz- und Siedepunkte steigen mit dem Molekulargewicht und der Länge der Hauptkohlenstoffkette
- Unverzweigte Alkane von CH 4 bis C 4 H 10 sind unter Normalbedingungen Gase; von C 5 H 12 bis C 13 H 28 - Flüssigkeiten; nach C 14 H 30 - Feststoffe.
- Die Schmelz- und Siedepunkte nehmen von weniger verzweigt zu stärker verzweigt ab. So ist beispielsweise bei 20 °C n-Pentan eine Flüssigkeit und Neopentan ein Gas.
Chemische Eigenschaften:
· Halogenierung
dies ist eine der Substitutionsreaktionen. Das am wenigsten hydrierte Kohlenstoffatom wird zuerst halogeniert (tertiäres Atom, dann sekundäre, primäre Atome werden zuletzt halogeniert). Die Halogenierung von Alkanen erfolgt stufenweise – in einer Stufe wird nicht mehr als ein Wasserstoffatom ausgetauscht:
- CH 4 + Cl 2 → CH 3 Cl + HCl (Chlormethan)
- CH 3 Cl + Cl 2 → CH 2 Cl 2 + HCl (Dichlormethan)
- CH 2 Cl 2 + Cl 2 → CHCl 3 + HCl (Trichlormethan)
- CHCl 3 + Cl 2 → CCl 4 + HCl (Tetrachlormethan).
Unter Lichteinwirkung zerfällt das Chlormolekül in Radikale, dann greifen sie die Alkanmoleküle an und nehmen ihnen ein Wasserstoffatom ab, wodurch Methylradikale CH 3 entstehen, die mit Chlormolekülen kollidieren, sie zerstören und neu bilden Radikale.
· Verbrennung
Die wichtigste chemische Eigenschaft von gesättigten Kohlenwasserstoffen, die ihre Verwendung als Kraftstoff bestimmt, ist die Verbrennungsreaktion. Beispiel:
CH 4 + 2O 2 → CO 2 + 2H 2 O + Q
Bei Sauerstoffmangel entsteht statt Kohlendioxid Kohlenmonoxid oder Kohle (je nach Sauerstoffkonzentration).
Allgemein kann die Verbrennungsreaktion von Alkanen wie folgt geschrieben werden:
Mit n H2 n +2 +(1,5n+0,5) O 2 \u003d n CO 2 + ( n+1) H2O
· Zersetzung
Zersetzungsreaktionen treten nur unter dem Einfluss hoher Temperaturen auf. Eine Temperaturerhöhung führt zum Aufbrechen der Kohlenstoffbindung und zur Bildung freier Radikale.
Beispiele:
CH4 → C + 2H2 (t > 1000 °C)
C 2 H 6 → 2 C + 3 H 2
Alkene :
Alkene sind ungesättigte Kohlenwasserstoffe, die neben Einfachbindungen eine Kohlenstoff-Kohlenstoff-Doppelbindung im Molekül enthalten, die Formel lautet C n H 2n
Die Zugehörigkeit eines Kohlenwasserstoffs zur Klasse der Alkene spiegelt sich im generischen Suffix -en in seinem Namen wider.
Physikalische Eigenschaften :
- Die Schmelz- und Siedepunkte von Alkenen (vereinfacht) steigen mit dem Molekulargewicht und der Länge der Hauptkohlenstoffkette.
- Unter normalen Bedingungen sind Alkene von C 2 H 4 bis C 4 H 8 Gase; von C 5 H 10 bis C 17 H 34 - Flüssigkeiten, nach C 18 H 36 - Feststoffe. Alkene sind in Wasser unlöslich, aber gut löslich in organischen Lösungsmitteln.
Chemische Eigenschaften :
· Austrocknung ist der Prozess der Abspaltung eines Wassermoleküls von einem Molekül einer organischen Verbindung.
· Polymerisation- Dies ist ein chemischer Prozess, bei dem viele Ausgangsmoleküle einer Substanz mit niedrigem Molekulargewicht zu großen Polymermolekülen kombiniert werden.
Polymer ist eine hochmolekulare Verbindung, deren Moleküle aus vielen identischen Struktureinheiten bestehen.
Alkadiene :
Alkadiene sind ungesättigte Kohlenwasserstoffe, die neben Einfachbindungen zwei Kohlenstoff-Kohlenstoff-Doppelbindungen im Molekül enthalten
. Diene sind Strukturisomere von Alkinen.Physikalische Eigenschaften :
Butadien ist ein Gas (Siedepunkt –4,5 °C), Isopren ist eine bei 34 °C siedende Flüssigkeit, Dimethylbutadien ist eine bei 70 °C siedende Flüssigkeit. Isopren und andere Dien-Kohlenwasserstoffe können zu Kautschuk polymerisieren. Naturkautschuk in gereinigtem Zustand ist ein Polymer mit der allgemeinen Formel (C5H8)n und wird aus dem Latex bestimmter tropischer Pflanzen gewonnen.
Kautschuk ist sehr gut löslich in Benzol, Benzin, Schwefelkohlenstoff. Bei niedriger Temperatur wird es spröde, bei Erwärmung wird es klebrig. Um die mechanischen und chemischen Eigenschaften von Gummi zu verbessern, wird es durch Vulkanisation in Gummi umgewandelt. Um Gummiprodukte zu erhalten, werden sie zunächst aus einer Mischung von Gummi mit Schwefel sowie mit Füllstoffen geformt: Ruß, Kreide, Ton und einigen organischen Verbindungen, die zur Beschleunigung der Vulkanisation dienen. Dann werden die Produkte erhitzt - Heißvulkanisation. Während der Vulkanisation verbindet sich Schwefel chemisch mit Gummi. Außerdem ist in vulkanisiertem Gummi Schwefel in freiem Zustand in Form von winzigen Partikeln enthalten.
Dienkohlenwasserstoffe werden leicht polymerisiert. Die Polymerisationsreaktion von Dienkohlenwasserstoffen liegt der Kautschuksynthese zugrunde. Additionsreaktionen eingehen (Hydrierung, Halogenierung, Hydrohalogenierung):
H 2 C \u003d CH-CH \u003d CH 2 + H 2 -> H 3 C-CH \u003d CH-CH 3
Alkine :
Alkine sind ungesättigte Kohlenwasserstoffe, deren Moleküle neben Einfachbindungen eine Kohlenstoff-Kohlenstoff-Dreifachbindung enthalten Formel-C n H 2n-2
Physikalische Eigenschaften :
Alkine haben ähnliche physikalische Eigenschaften wie die entsprechenden Alkene. Niedriger (bis C 4) - Gase ohne Farbe und Geruch mit höheren Siedepunkten als ihre Gegenstücke in Alkenen.
Alkine sind in Wasser schlecht löslich, besser in organischen Lösungsmitteln.
Chemische Eigenschaften :
Halogenierungsreaktionen
Alkine sind in der Lage, ein oder zwei Halogenmoleküle zu addieren, um die entsprechenden Halogenderivate zu bilden:
Flüssigkeitszufuhr
In Gegenwart von Quecksilbersalzen fügen Alkine Wasser hinzu, um Acetaldehyd (für Acetylen) oder Keton (für andere Alkine) zu bilden.

DEFINITION
Alkane werden gesättigte Kohlenwasserstoffe genannt, deren Moleküle aus Kohlenstoff- und Wasserstoffatomen bestehen, die nur durch σ-Bindungen miteinander verbunden sind.
Unter normalen Bedingungen (bei 25 o C und atmosphärischem Druck) sind die ersten vier Mitglieder der homologen Reihe der Alkane (C 1 - C 4) Gase. Normale Alkane von Pentan bis Heptadecan (C 5 - C 17) sind Flüssigkeiten, ab C 18 und darüber sind sie Feststoffe. Mit zunehmendem relativen Molekulargewicht steigen die Siede- und Schmelzpunkte der Alkane. Bei gleicher Anzahl an Kohlenstoffatomen in einem Molekül haben verzweigte Alkane niedrigere Siedepunkte als normale Alkane. Die Struktur des Alkanmoleküls am Beispiel von Methan ist in Abb. 1 dargestellt. ein.
Reis. 1. Die Struktur des Methanmoleküls.
Alkane sind in Wasser praktisch unlöslich, da ihre Moleküle von geringer Polarität sind und nicht mit Wassermolekülen wechselwirken. Flüssige Alkane vermischen sich leicht miteinander. Sie lösen sich gut in unpolaren organischen Lösungsmitteln wie Benzol, Tetrachlorkohlenstoff, Diethylether usw.
Alkane erhalten
Die Hauptquellen verschiedener gesättigter Kohlenwasserstoffe mit bis zu 40 Kohlenstoffatomen sind Erdöl und Erdgas. Alkane mit einer geringen Anzahl von Kohlenstoffatomen (1 - 10) können durch fraktionierte Destillation von Erdgas oder Benzinfraktionen von Öl isoliert werden.
Es gibt industrielle (I) und Labormethoden (II), um Alkane zu erhalten.
C + H 2 → CH 4 (kat = Ni, t 0);
CO + 3H 2 → CH 4 + H 2 O (kat \u003d Ni, t 0 \u003d 200 - 300);
CO 2 + 4H 2 → CH 4 + 2H 2 O (kat, t 0).
— Hydrierung von ungesättigten Kohlenwasserstoffen
CH 3 -CH \u003d CH 2 + H 2 →CH 3 -CH 2 -CH 3 (kat \u003d Ni, t 0);
— Reduktion von Halogenalkanen
C 2 H 5 I + HI → C 2 H 6 + I 2 (t 0);
- alkalische Schmelzreaktionen von Salzen einbasiger organischer Säuren
C 2 H 5 -COONa + NaOH → C 2 H 6 + Na 2 CO 3 (t 0);
- Wechselwirkung von Halogenalkanen mit metallischem Natrium (Wurtz-Reaktion)
2C 2 H 5 Br + 2 Na → CH 3 -CH 2 -CH 2 -CH 3 + 2NaBr;
– Elektrolyse von Salzen einbasiger organischer Säuren
2C 2 H 5 COONa + 2 H 2 O → H 2 + 2 NaOH + C 4 H 10 + 2 CO 2;
K(–): 2H 2 O + 2e → H 2 + 2OH –;
A (+): 2C 2 H 5 COO - -2e → 2C 2 H 5 COO + → 2C 2 H 5 + + 2CO 2.
Chemische Eigenschaften von Alkanen
Alkane gehören zu den am wenigsten reaktiven organischen Verbindungen, was durch ihre Struktur erklärt wird.
Alkane reagieren unter normalen Bedingungen nicht mit konzentrierten Säuren, geschmolzenen und konzentrierten Laugen, Alkalimetallen, Halogenen (außer Fluor), Kaliumpermanganat und Kaliumdichromat in einer sauren Umgebung.
Am charakteristischsten für Alkane sind Reaktionen, die nach dem Radikalmechanismus ablaufen. Die homolytische Spaltung von C-H- und C-C-Bindungen ist energetisch günstiger als ihre heterolytische Spaltung.
Radikalische Substitutionsreaktionen laufen am leichtesten am tertiären, am sekundären und zuletzt am primären Kohlenstoffatom ab.
Alle chemischen Umwandlungen von Alkanen verlaufen unter Spaltung:
1) C-H-Bindungen
- Halogenierung (SR)
CH 4 + Cl 2 → CH 3 Cl + HCl ( hv);
CH 3 -CH 2 -CH 3 + Br 2 → CH 3 -CHBr-CH 3 + HBr ( hv).
- Nitrierung (S R)
CH 3 -C (CH 3) H-CH 3 + HONO 2 (verdünnt) → CH 3 -C (NO 2) H-CH 3 + H 2 O (t 0).
– Sulfochlorierung (S R)
R-H + SO 2 + Cl 2 → RSO 2 Cl + HCl ( hv).
– Dehydrierung
CH 3 -CH 3 → CH 2 \u003d CH 2 + H 2 (kat \u003d Ni, t 0).
— Dehydrocyclisierung
CH 3 (CH 2) 4 CH 3 → C 6 H 6 + 4 H 2 (kat = Cr 2 O 3, t 0).
2) C-H- und C-C-Bindungen
- Isomerisierung (intramolekulare Umlagerung)
CH 3 -CH 2 -CH 2 -CH 3 →CH 3 -C (CH 3) H-CH 3 (kat \u003d AlCl 3, t 0).
- Oxidation
2CH 3 -CH 2 -CH 2 -CH 3 + 5O 2 → 4CH 3 COOH + 2H 2 O (t 0, p);
C n H 2n + 2 + (1,5n + 0,5) O 2 → nCO 2 + (n + 1) H 2 O (t 0).
Anwendung von Alkanen
Alkane haben in verschiedenen Industrien Anwendung gefunden. Betrachten wir am Beispiel einiger Vertreter der homologen Reihe sowie Mischungen von Alkanen genauer.
Methan ist die Rohstoffbasis der wichtigsten chemischen Industrieprozesse zur Herstellung von Kohlenstoff und Wasserstoff, Acetylen, sauerstoffhaltigen organischen Verbindungen - Alkoholen, Aldehyden, Säuren. Propan wird als Kraftstoff für Autos verwendet. Butan wird zur Herstellung von Butadien verwendet, das ein Rohstoff für die Herstellung von synthetischem Kautschuk ist.
Ein Gemisch aus flüssigen und festen Alkanen bis C 25, Vaseline genannt, wird in der Medizin als Grundlage für Salben verwendet. Eine Mischung aus festen C 18 - C 25 -Alkanen (Paraffin) wird verwendet, um verschiedene Materialien (Papier, Stoffe, Holz) zu imprägnieren, um ihnen hydrophobe Eigenschaften zu verleihen, d.h. Wasserundurchlässigkeit. In der Medizin wird es für physiotherapeutische Verfahren (Paraffinbehandlung) verwendet.
Beispiele für Problemlösungen
BEISPIEL 1
| Die Übung | Beim Chlorieren von Methan wurden 1,54 g der Verbindung erhalten, deren Dampfdichte in Luft 5,31 beträgt. Berechnen Sie die Masse an Mangandioxid MnO 2 , die zur Herstellung von Chlor benötigt wird, wenn das Verhältnis der in die Reaktion eingebrachten Volumina von Methan und Chlor 1:2 beträgt. |
| Entscheidung | Das Verhältnis der Masse eines gegebenen Gases zur Masse eines anderen Gases im selben Volumen, bei derselben Temperatur und demselben Druck, wird als relative Dichte des ersten Gases gegenüber dem zweiten bezeichnet. Dieser Wert zeigt an, wie oft das erste Gas schwerer oder leichter ist als das zweite Gas. Das relative Molekulargewicht der Luft wird mit 29 angenommen (unter Berücksichtigung des Gehalts an Stickstoff, Sauerstoff und anderen Gasen in der Luft). Es sollte beachtet werden, dass das Konzept des "relativen Molekulargewichts von Luft" bedingt verwendet wird, da Luft ein Gasgemisch ist. Finden wir die Molmasse des Gases, das bei der Chlorierung von Methan entsteht: M Gas \u003d 29 × D Luft (Gas) \u003d 29 × 5,31 \u003d 154 g / mol. Dies ist Tetrachlorkohlenstoff-CCl 4 . Wir schreiben die Reaktionsgleichung und ordnen die stöchiometrischen Koeffizienten: CH 4 + 4Cl 2 \u003d CCl 4 + 4HCl. Berechnen Sie die Menge an Tetrachlorkohlenstoff: n(CCl 4) = m(CCl 4) / M(CCl 4); n (CCl 4) \u003d 1,54 / 154 \u003d 0,01 mol. Nach der Reaktionsgleichung ist dann n (CCl 4) : n (CH 4) = 1: 1 n (CH 4) \u003d n (CCl 4) \u003d 0,01 mol. Dann sollte die Menge an Chlorsubstanz gleich n(Cl 2) = 2 × 4 n(CH 4) sein, d.h. n(Cl 2) \u003d 8 × 0,01 \u003d 0,08 mol. Wir schreiben die Reaktionsgleichung für die Herstellung von Chlor: MnO 2 + 4HCl \u003d MnCl 2 + Cl 2 + 2H 2 O. Die Anzahl der Mole Mangandioxid beträgt 0,08 Mol, weil n (Cl 2) : n (MnO 2) = 1: 1. Finden Sie die Masse von Mangandioxid: m (MnO 2) \u003d n (MnO 2) × M (MnO 2); M (MnO 2) \u003d Ar (Mn) + 2 × Ar (O) \u003d 55 + 2 × 16 \u003d 87 g / mol; m (MnO 2) \u003d 0,08 × 87 \u003d 10,4 g. |
| Antworten | Die Masse an Mangandioxid beträgt 10,4 g. |
BEISPIEL 2
| Die Übung | Stellen Sie die Summenformel von Trichloralkan ein, dessen Massenanteil an Chlor 72,20 % beträgt. Bilden Sie die Strukturformeln aller möglichen Isomere und geben Sie die Stoffnamen gemäß der substitutionellen IUPAC-Nomenklatur an. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Antworten | Schreiben wir die allgemeine Formel von Trichloralken: C n H 2 n-1 Cl 3 . Nach der Formel ω(Cl) = 3×Ar(Cl) / Mr(C n H 2 n -1 Cl 3) × 100 % Berechnen Sie das Molekulargewicht von Trichloralkan: Mr(C n H 2 n-1 Cl 3) = 3 × 35,5 / 72,20 × 100 % = 147,5. Lassen Sie uns den Wert von n finden: 12n + 2n - 1 + 35,5 x 3 = 147,5; Daher ist die Formel von Trichloralkan C 3 H 5 Cl 3. Stellen wir die Strukturformeln der Isomere zusammen: 1,2,3-Trichlorpropan (1), 1,1,2-Trichlorpropan (2), 1,1,3-Trichlorpropan (3), 1,1,1-Trichlorpropan (4) und 1,2,2-Trichlorpropan (5). CH 2 Cl-CHCl-CH 2 Cl (1); CHCl 2 -CHCl-CH 3 (2); CHCl 2 -CH 2 -CH 2 Cl (3); CCl 3 -CH 2 -CH 3 (4); Alkane (Methan und seine Homologen) haben die allgemeine Formel C n H2 n+2. Die ersten vier Kohlenwasserstoffe heißen Methan, Ethan, Propan, Butan. Die Namen der höheren Mitglieder dieser Reihe bestehen aus der Wurzel - der griechischen Ziffer und dem Suffix -an. Die Namen der Alkane bilden die Grundlage der IUPAC-Nomenklatur.Regeln für die systematische Nomenklatur:
Der Hauptstromkreis wird nach folgenden Kriterien der Reihe nach ausgewählt:
Die Hauptkette ist von einem Ende zum anderen mit arabischen Ziffern nummeriert. Jeder Substituent erhält die Nummer des Kohlenstoffatoms der Hauptkette, an die er gebunden ist. Die Nummerierungsfolge ist so gewählt, dass die Summe der Substituentenzahlen (Lokanten) am kleinsten ist. Diese Regel gilt auch für die Numerierung monocyclischer Verbindungen.
Alle Kohlenwasserstoff-Seitengruppen werden als einwertige (einfach gebundene) Reste angesehen. Enthält der Seitenrest selbst Seitenketten, so wird darin nach den obigen Regeln eine zusätzliche Hauptkette ausgewählt, die ausgehend von dem an die Hauptkette gebundenen Kohlenstoffatom nummeriert wird.
Der Name der Verbindung beginnt mit einer Liste von Substituenten, die ihre Namen in alphabetischer Reihenfolge angeben. Dem Namen jedes Substituenten geht seine Nummer in der Hauptkette voraus. Das Vorhandensein mehrerer Substituenten wird durch Präfix-Zähler angezeigt: Di-, Tri-, Tetra- usw. Danach wird der der Hauptkette entsprechende Kohlenwasserstoff genannt. Im Tisch. 12.1 zeigt die Namen der ersten fünf Kohlenwasserstoffe, ihre Reste, mögliche Isomere und ihre entsprechenden Formeln. Die Namen von Radikalen enden mit dem Suffix -yl.
Beispiel. Nennen Sie alle Isomere von Hexan. Beispiel. Nennen Sie das Alkan der folgenden Struktur In diesem Beispiel wird von zwei zwölfatomigen Ketten diejenige gewählt, bei der die Summe der Zahlen am kleinsten ist (Regel 2). Unter Verwendung der in Tabelle angegebenen Namen verzweigter Reste. 12.2,
Der Name dieses Alkans ist etwas vereinfacht: 10-tert-Butyl-2,2-(dimethyl)-7-propyl-4-isopropyl-3-ethyldodecan. Schließt man die Kohlenwasserstoffkette in einem Kreislauf unter Verlust von zwei Wasserstoffatomen, entstehen Monocycloalkane mit der allgemeinen Formel C n H2 n. Die Cyclisierung beginnt bei C 3, Namen werden aus C gebildet n vorangestellt mit cyclo: polycyclische Alkane. Ihre Namen bilden sich aus der Vorsilbe bicyclo-, tricyclo- usw. Bicyclische und tricyclische Verbindungen enthalten zwei bzw. drei Zyklen im Molekül, zur Beschreibung ihrer Struktur geben eckige Klammern in absteigender Reihenfolge die Anzahl der Kohlenstoffatome in jedem an die Ketten, die die Knotenatome verbinden; unter der Formel der Name des Atoms: Dieser trizyklische Kohlenwasserstoff wird gemeinhin als Adamantan (vom tschechischen Adamant, Diamant) bezeichnet, da es sich um eine Kombination aus drei kondensierten Cyclohexanringen in einer Form handelt, die zu einer diamantähnlichen Anordnung von Kohlenstoffatomen im Kristallgitter führt. Cyclische Kohlenwasserstoffe mit einem gemeinsamen Kohlenstoffatom nennt man Spirane, zum Beispiel Spiro-5,5-Undecan: Planare zyklische Moleküle sind instabil, daher werden verschiedene Konformationsisomere gebildet. Im Gegensatz zu Konfigurationsisomeren (die räumliche Anordnung von Atomen in einem Molekül ohne Berücksichtigung der Orientierung) unterscheiden sich Konformationsisomere nur durch die Rotation von Atomen oder Radikalen um formal einfache Bindungen unter Beibehaltung der Konfiguration von Molekülen. Die Bildungsenergie eines stabilen Konformers wird genannt Konformation. Konformere befinden sich im dynamischen Gleichgewicht und werden durch instabile Formen ineinander umgewandelt. Die Instabilität planarer Zyklen wird durch eine signifikante Verformung der Bindungswinkel verursacht. Unter Beibehaltung der tetraedrischen Bindungswinkel für Cyclohexan C 6H 12 sind zwei stabile Konformationen möglich: in Form eines Sessels (a) und in Form eines Bades (b):
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||