Antoine Laurent LAVOISIER () () Menyelidiki oksigen dan menciptakan teori pembakaran oksigen, yang menggantikan teori flogiston. Dia mempelajari oksigen dan menciptakan teori pembakaran oksigen, yang menggantikan teori flogiston.

Oksigen adalah unsur yang paling umum di Bumi Di udara 21% (berdasarkan volume), Di udara 21% (berdasarkan volume), di kerak bumi 49% (berdasarkan massa), di kerak bumi 49% (berdasarkan massa), di hidrosfer 89% ( massa), di hidrosfer 89% (massa), pada organisme hidup hingga 65% massa. dalam organisme hidup hingga 65% dari massa.

Sifat fisik Keadaan agregat - gas dalam kondisi normal. Pada suhu yang sangat rendah (-183°C) berubah menjadi keadaan agregasi cair (cairan biru), dan bahkan pada suhu yang lebih rendah (-219°C) menjadi padat (kristal salju biru). Keadaan agregat - gas dalam kondisi normal. Pada suhu yang sangat rendah (-183°C) berubah menjadi keadaan agregasi cair (cairan biru), dan bahkan pada suhu yang lebih rendah (-219°C) menjadi padat (kristal salju biru). Warna - tidak berwarna. Warna - tidak berwarna. Bau - tidak berbau. Bau - tidak berbau. Kelarutan dalam air - sukar larut. Kelarutan dalam air - sukar larut. Lebih berat dari udara (M udara = 29 g / mol, dan M O 2 = 32 g / mol. Lebih berat dari udara (M udara = 29 g / mol, dan M O 2 = 32 g / mol.

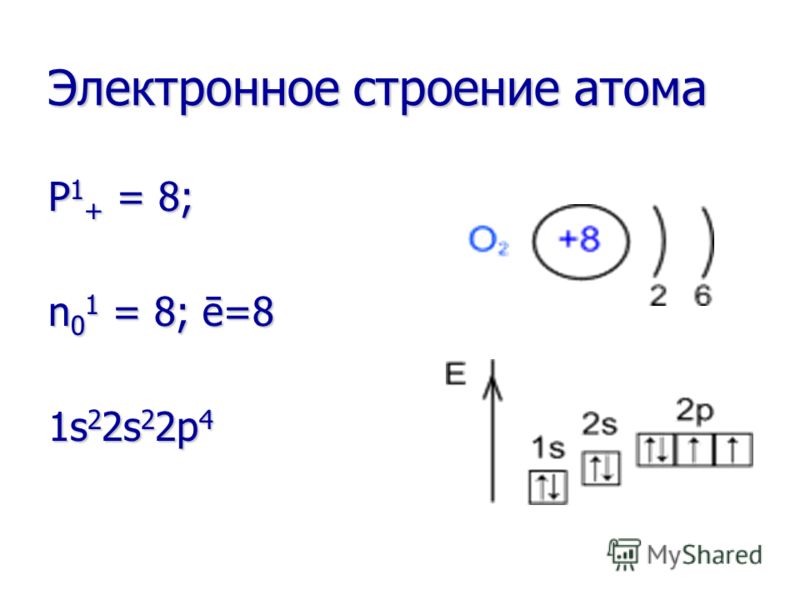
Sifat kimia Oksigen adalah zat pengoksidasi yang sangat kuat! Ini mengoksidasi banyak zat yang sudah pada suhu kamar (oksidasi lambat) dan terlebih lagi ketika zat tersebut dipanaskan atau dibakar (oksidasi cepat). Oksigen adalah oksidator yang sangat kuat! Ini mengoksidasi banyak zat yang sudah pada suhu kamar (oksidasi lambat) dan terlebih lagi ketika zat tersebut dipanaskan atau dibakar (oksidasi cepat). Dalam reaksi dengan semua elemen (kecuali fluor), oksigen selalu merupakan agen pengoksidasi. Dalam reaksi dengan semua elemen (kecuali fluor), oksigen selalu merupakan agen pengoksidasi.

Reaksi dengan logam Sebagai hasil dari reaksi, oksida logam ini terbentuk. Misalnya, aluminium dioksidasi oleh oksigen menurut persamaan: Sebagai hasil dari reaksi, oksida logam ini terbentuk. Misalnya, aluminium dioksidasi oleh oksigen menurut persamaan: t° 4Al + 3O 2 2Al 2 O 3 t° 4Al + 3O 2 2Al 2 O 3 Contoh lain. Saat menurunkan kawat besi merah-panas ke dalam botol oksigen, kawat terbakar, menyembur ke samping berkas bunga api - partikel panas skala besi Fe 3 O 4: t ° 3Fe + 2O 2 Fe 3 O 4 t ° 3Fe + 2O 2 Fe 3 O 4


Contoh lain dari reaksi dengan non-logam Pembakaran belerang dalam oksigen untuk membentuk belerang dioksida SO 2: t ° S + O 2 SO 2 t ° S + O 2 SO 2 Pembakaran batubara dalam oksigen untuk membentuk karbon dioksida: Pembakaran batubara dalam oksigen untuk membentuk karbon dioksida: t° C + O 2 CO 2 t° C + O 2 CO 2
Reaksi dengan beberapa zat kompleks Dalam hal ini, oksida dari unsur-unsur yang membentuk molekul zat kompleks terbentuk. Dalam hal ini, oksida dari unsur-unsur yang membentuk molekul zat kompleks terbentuk. Misalnya, saat membakar tembaga (II) sulfida Misalnya, saat membakar tembaga (II) sulfida t ° 2CuS + 3O 2 2CuO + 2SO 2 t ° 2CuS + 3O 2 2CuO + 2SO 2, terbentuk dua oksida tembaga (II) oksida dan sulfur oksida ( IV). dua oksida terbentuk, tembaga(II) oksida dan belerang(IV) oksida. Selama pemanggangan sulfida, oksida belerang selalu terbentuk, di mana valensi belerang adalah IV. Selama pemanggangan sulfida, oksida belerang selalu terbentuk, di mana valensi belerang adalah IV. Contoh lain adalah pembakaran metana CH 4. Karena molekul ini terdiri dari atom unsur karbon C dan hidrogen H, itu berarti bahwa dua oksida terbentuk karbon monoksida (IV) CO 2 dan hidrogen oksida, yaitu air - H 2 O: t ° CH 4 + 2O 2 CO 2 + 2H 2 O t ° CH 4 + 2O 2 CO 2 + 2H 2 O

Interaksi kimia suatu zat dengan oksigen disebut reaksi oksidasi. Reaksi oksidasi yang disertai pelepasan panas dan cahaya disebut reaksi pembakaran. Reaksi pembakaran zat adalah contoh oksidasi cepat, tetapi membusuk, berkarat, dll. ini adalah contoh oksidasi lambat zat dengan oksigen. Reaksi pembakaran zat adalah contoh oksidasi cepat, tetapi membusuk, berkarat, dll. ini adalah contoh oksidasi lambat zat oleh oksigen

Produksi oksigen (metode laboratorium) dekomposisi air dengan arus listrik dekomposisi air dengan arus listrik dekomposisi hidrogen peroksida H 2 O 2 di bawah aksi MnO 2 katalis dekomposisi hidrogen peroksida H 2 O 2 di bawah aksi MnO 2 katalis dekomposisi kalium permanganat KMnO4 saat dipanaskan. dekomposisi kalium permanganat KMnO 4 saat dipanaskan.
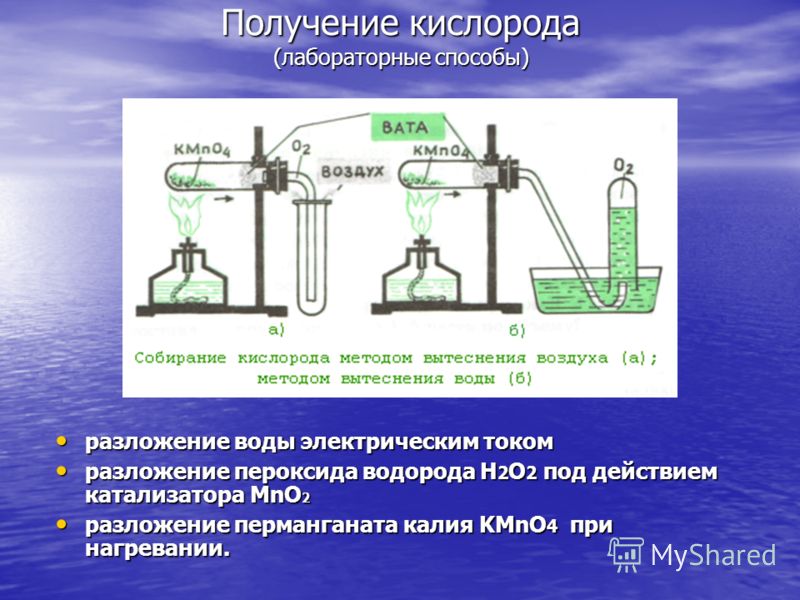
Pengambilan oksigen (metode industri) Dalam industri, untuk mendapatkan oksigen murni, digunakan destilasi udara cair, berdasarkan perbedaan suhu didih komponen udara. Udara didinginkan hingga sekitar -200 °C dan kemudian dipanaskan secara perlahan. Ketika suhu mencapai -183°C, oksigen keluar dari udara cair, komponen yang tersisa dari udara cair pada suhu ini tetap dalam keadaan agregasi cair. Dalam industri, untuk mendapatkan oksigen murni, digunakan distilasi udara cair, berdasarkan perbedaan suhu didih komponen udara. Udara didinginkan hingga sekitar -200 °C dan kemudian dipanaskan secara perlahan. Ketika suhu mencapai -183°C, oksigen keluar dari udara cair, komponen yang tersisa dari udara cair pada suhu ini tetap dalam keadaan agregasi cair.

Penggunaan oksigen dalam konstruksi dan teknik mesin dalam konstruksi dan teknik mesin - untuk pengelasan gas oxy-acetylene dan pemotongan gas logam - untuk pengelasan gas oxy-acetylene dan pemotongan gas logam - untuk penyemprotan dan pelapisan logam dalam produksi minyak dalam produksi minyak - ketika disuntikkan ke dalam formasi untuk meningkatkan energi perpindahan dalam metalurgi dan industri pertambangan di industri metalurgi dan pertambangan - dalam produksi baja konvektif, ledakan oksigen di tanur tinggi, ekstraksi emas dan bijih, produksi ferroalloy, peleburan nikel, seng, timbal , zirkonium dan logam non-ferro lainnya - dalam produksi baja konvektif, semburan oksigen dalam tanur tinggi , ekstraksi emas dan bijih, produksi ferroalloy, peleburan nikel, seng, timbal, zirkonium dan logam non-ferro lainnya - dengan reduksi langsung besi - dengan reduksi langsung besi - dengan pembersihan api dalam produksi pengecoran - dengan pembersihan api dalam produksi pengecoran - dengan pengeboran api x keturunan

Penggunaan oksigen dalam pengobatan dalam pengobatan - di ruang oksibarik - di ruang oksibarik - saat mengisi masker oksigen, bantal, dll. - saat mengisi masker oksigen, bantal, dll. - di bangsal dengan iklim mikro khusus - di bangsal dengan iklim mikro khusus - untuk produksi koktail oksigen - untuk produksi koktail oksigen - dalam budidaya mikroorganisme - dalam budidaya mikroorganisme dalam ekologi dalam ekologi - dalam pemurnian minum air - dalam pemurnian air minum - dalam daur ulang logam - saat mendaur ulang logam - saat meniup air limbah dengan oksigen - saat meniup air limbah dengan oksigen - saat menetralkan limbah kimia aktif di pabrik pengolahan di insinerator - saat menetralkan limbah kimia aktif di pabrik pengolahan di insinerator

Penggunaan oksigen dalam industri kimia dalam industri kimia - dalam produksi asetilena, selulosa, metil alkohol, amonia, asam nitrat dan sulfat - dalam produksi asetilena, selulosa, metil alkohol, amonia, asam nitrat dan sulfat - dalam konversi katalitik gas alam (dalam produksi amonia sintetis) - dalam konversi katalitik gas alam (dalam produksi amonia sintetis) - dalam konversi metana suhu tinggi - dalam konversi metana suhu tinggi di industri tenaga dalam industri tenaga - dalam gasifikasi bahan bakar padat - dalam gasifikasi bahan bakar padat - untuk pengayaan udara untuk boiler domestik dan industri - untuk pengayaan udara untuk boiler domestik dan industri - untuk mengompresi campuran air-batubara - untuk mengompresi air- campuran batubara

Penggunaan oksigen dalam peralatan militer di peralatan militer - di ruang bertekanan - di ruang bertekanan - untuk pengoperasian mesin diesel di bawah air - untuk pengoperasian mesin diesel di bawah air - sebagai pengoksidasi bahan bakar untuk mesin roket - sebagai pengoksidasi bahan bakar untuk mesin roket di bidang pertanian di bidang pertanian - untuk memperkaya lingkungan akuatik dengan oksigen dalam penangkapan ikan - untuk memperkaya lingkungan akuatik dengan oksigen dalam penangkapan ikan - dalam pembuatan koktail oksigen - dalam pembuatan koktail oksigen - untuk penambahan berat badan hewan - untuk penambahan berat badan hewan

OZON Modifikasi alotropik oksigen Ozon O 3 adalah gas berwarna biru dengan bau yang menyengat. Siapa pun yang telah memperhatikan bagaimana bau udara setelah badai petir atau di dekat sumber pelepasan listrik tahu betul bau gas ini. Ozon O 3 adalah gas berwarna biru dengan bau yang menyengat. Siapa pun yang telah memperhatikan bagaimana bau udara setelah badai petir atau di dekat sumber pelepasan listrik tahu betul bau gas ini. Di alam, ozon dibentuk oleh aksi radiasi ultraviolet dari Matahari, dan juga dihasilkan oleh pelepasan listrik di atmosfer:
Ozon adalah zat pengoksidasi yang sangat kuat, sehingga digunakan dalam desinfeksi air minum. Pada kontak dengan sebagian besar zat yang dapat teroksidasi, ledakan terjadi. Ozon terbentuk di atmosfer bumi pada ketinggian 25 km di bawah pengaruh radiasi matahari, menyerap radiasi berbahaya dari Matahari. Namun, di "payung" ozon Bumi, yang hanya setebal sekitar 30 meter, "lubang" muncul sesekali. Semakin banyak gas "berbahaya" bagi ozon, seperti nitrogen monoksida NO atau zat-zat yang digunakan untuk mengisi unit pendingin dan kaleng aerosol, yang masuk ke udara. Bahkan hilangnya sebagian lapisan ozon di atas Bumi mengancam semua makhluk hidup dengan kematian ... Namun, dalam "payung" ozon Bumi, hanya setebal sekitar 30 meter, "lubang" muncul sesekali. Semakin banyak gas "berbahaya" bagi ozon, seperti nitrogen monoksida NO atau zat-zat yang digunakan untuk mengisi unit pendingin dan kaleng aerosol, yang masuk ke udara. Bahkan hilangnya sebagian lapisan ozon di atas Bumi mengancam semua makhluk hidup dengan kematian...


