თქვენს ყურადღებას წარმოგიდგენთ ვიდეო გაკვეთილს თემაზე „ბენზოლის ქიმიური თვისებები“. ამ ვიდეოს გამოყენებით შეგიძლიათ მიიღოთ წარმოდგენა ბენზოლის ქიმიურ თვისებებზე, ასევე იმ მძიმე პირობებზე, რომლებიც საჭიროა ბენზოლის სხვა ნივთიერებებთან რეაგირებისთვის.
Თემა:არომატული ნახშირწყალბადები
გაკვეთილი:ბენზოლის ქიმიური თვისებები
ბრინჯი. 1. ბენზოლის მოლეკულა
ბენზოლის მოლეკულაში p-ელექტრონული ღრუბლის გატეხვა რთულია. ამრიგად, ბენზოლი ქიმიურ რეაქციებში გაცილებით ნაკლებად აქტიურად შედის, ვიდრე უჯერი ნაერთები.


იმისათვის, რომ ბენზოლი შევიდეს ქიმიურ რეაქციებში, საჭიროა საკმაოდ მკაცრი პირობები: ამაღლებული ტემპერატურა და ხშირ შემთხვევაში კატალიზატორი. უმეტეს რეაქციაში, სტაბილური ბენზოლის რგოლი შენარჩუნებულია.
1. ბრომირება.

საჭიროა კატალიზატორი (რკინა (III) ან ალუმინის ბრომიდი) და წყლის მცირე რაოდენობაც კი არ უნდა იყოს დაშვებული. კატალიზატორის როლი არის ის, რომ ბრომის მოლეკულა ბრომის ერთ-ერთი ატომით იზიდავს რკინის ატომს. შედეგად, ის პოლარიზდება - ბმული ელექტრონების წყვილი გადადის ბრომის ატომში, რომელიც დაკავშირებულია რკინასთან:
Br+…. ბრ - 3 თებერვალი .
Br+ არის ძლიერი ელექტროფილი. იგი იზიდავს ბენზოლის რგოლის ექვსელექტრონულ ღრუბელს და არღვევს მას, ქმნის კოვალენტურ კავშირს ნახშირბადის ატომთან:
ბრომის ანიონს შეუძლია შეუერთდეს მიღებულ კატიონს. მაგრამ ბენზოლის რგოლის არომატული სისტემის შემცირება ენერგიულად უფრო ხელსაყრელია, ვიდრე ბრომის ანიონის დამატება. ამრიგად, მოლეკულა გადადის სტაბილურ მდგომარეობაში წყალბადის იონის გამოდევნით:
ყველა ელექტროფილური ჩანაცვლების რეაქცია ბენზოლის რგოლში მიმდინარეობს მსგავსი მექანიზმის მიხედვით.
2. ნიტრაცია

ბენზოლი და მისი ჰომოლოგები რეაგირებენ კონცენტრირებული გოგირდის და აზოტის მჟავების ნარევთან (ნიტრატორული ნარევი). ნიტრატირების ნარევში, წონასწორობაში, არის ნიტრონიუმის იონი NO 2 +, რომელიც არის ელექტროფილი:

3. სულფონაცია.
ბენზოლი და სხვა არენები, გაცხელებისას, რეაგირებენ კონცენტრირებულ გოგირდმჟავასთან ან ოლეუმთან - SO 3 ხსნართან გოგირდმჟავაში:

4 . Friedel-Crafts Alkylation
5. ალკილაცია ალკენებით

ეს რეაქციები ენერგიულად არახელსაყრელია, ამიტომ ისინი მხოლოდ გაცხელების ან დასხივებისას მიმდინარეობს.
1. ჰიდროგენიზაცია.
როდესაც თბება, ამაღლებული წნევით და Ni, Pt ან Pd კატალიზატორის თანდასწრებით, ბენზოლი და სხვა არენები ამატებენ წყალბადს ციკლოჰექსანის წარმოქმნით:

2. ბენზოლის ქლორირება.
ულტრაიისფერი გამოსხივების ზემოქმედებით ბენზოლი ამატებს ქლორს. თუ კვარცის მინის კოლბა ბენზოლში ქლორის ხსნარით ექვემდებარება მზის სხივებს, ხსნარი სწრაფად გაუფერულდება, ქლორი გაერთიანდება ბენზოლთან და წარმოქმნის 1,2,3,4,5,6-ჰექსაქლოროციკლოჰექსანს, რომელიც ცნობილია როგორც. ჰექსაქლორანი(ადრე გამოიყენებოდა როგორც ინსექტიციდი):

3. იწვის ბენზოლი.
ალკანებისგან განსხვავებით, ბენზოლის და სხვა არომატული ნახშირწყალბადების ალი კაშკაშა და კვამლისფერია.
გაკვეთილის შეჯამება
ამ გაკვეთილზე თქვენ შეისწავლეთ თემა „ბენზოლის ქიმიური თვისებები“. ამ მასალის გამოყენებით თქვენ შეგეძლოთ წარმოდგენა შეგექმნათ ბენზოლის ქიმიურ თვისებებზე, ასევე იმ მძიმე პირობებზე, რომლებიც საჭიროა ბენზოლის სხვა ნივთიერებებთან რეაგირებისთვის.
ბიბლიოგრაფია
1. რუძიტის გ.ე. Ქიმია. ზოგადი ქიმიის საფუძვლები. მე-10 კლასი: სახელმძღვანელო საგანმანათლებლო დაწესებულებებისთვის: საბაზო დონე / გ.ე.რუძიტისი, ფ.გ. ფელდმანი. - მე-14 გამოცემა. - მ.: განათლება, 2012 წ.
2. ქიმია. მე-10 კლასი. პროფილის დონე: სახელმძღვანელო. ზოგადი განათლებისთვის დაწესებულებები / ვ.ვ. ერემინი, ნ.ე. კუზმენკო, ვ.ვ. ლუნინი და სხვები - მ.: დროფა, 2008. - 463 გვ.
3. ქიმია. მე-11 კლასი. პროფილის დონე: სახელმძღვანელო. ზოგადი განათლებისთვის დაწესებულებები / ვ.ვ. ერემინი, ნ.ე. კუზმენკო, ვ.ვ. ლუნინი და სხვები - მ.: დროფა, 2010. - 462 გვ.
4. ხომჩენკო გ.პ., ხომჩენკო ი.გ. ქიმიის პრობლემების კრებული უნივერსიტეტებში ჩასული პირებისთვის. - მე-4 გამოცემა. - M.: RIA "ახალი ტალღა": გამომცემელი უმერენკოვი, 2012. - 278 გვ.
Საშინაო დავალება
1. No13, 14 (გვ. 62) Rudzitis G.E., Feldman F.G. ქიმია: ორგანული ქიმია. მე-10 კლასი: სახელმძღვანელო საგანმანათლებლო დაწესებულებებისთვის: საბაზო დონე / გ.ე.რუძიტისი, ფ.გ. ფელდმანი. - მე-14 გამოცემა. - მ.: განათლება, 2012 წ.
2. რატომ განსხვავდება არომატული ნაერთები ქიმიური თვისებებით როგორც გაჯერებული, ისე უჯერი ნახშირწყალბადებისგან?
3. დაწერეთ ეთილბენზოლისა და ქსილენის წვის რეაქციების განტოლებები.
არომატული HCs (არენა)არის ნახშირწყალბადები, რომელთა მოლეკულები შეიცავს ერთ ან მეტ ბენზოლის რგოლს.
არომატული ნახშირწყალბადების მაგალითები:

ბენზოლის რიგის არენები (მონოციკლური არენები)
ზოგადი ფორმულა:C n H 2n-6, n≥6
არომატული ნახშირწყალბადების უმარტივესი წარმომადგენელია ბენზოლი, მისი ემპირიული ფორმულა არის C 6 H 6 .
ბენზოლის მოლეკულის ელექტრონული სტრუქტურა
C n H 2 n -6 მონოციკლური არენების ზოგადი ფორმულა აჩვენებს, რომ ისინი უჯერი ნაერთებია.
1856 წელს გერმანელმა ქიმიკოსმა ა.ფ. კეკულემ შემოგვთავაზა ბენზოლის ციკლური ფორმულა კონიუგირებული ბმებით (ერთჯერადი და ორმაგი ბმები ალტერნატიული) - ციკლოჰექსატრიენი-1,3,5: 
ბენზოლის მოლეკულის ეს სტრუქტურა არ ხსნის ბენზოლის ბევრ თვისებას:
- ბენზოლისთვის დამახასიათებელია ჩანაცვლების რეაქციები და არა უჯერი ნაერთებისთვის დამახასიათებელი დამატების რეაქციები. დამატების რეაქციები შესაძლებელია, მაგრამ ისინი უფრო რთულია, ვიდრე მათთვის;
- ბენზოლი არ შედის რეაქციებში, რომლებიც წარმოადგენს ხარისხობრივ რეაქციებს უჯერი ნახშირწყალბადებთან (ბრომით წყალთან და KMnO 4 ხსნართან ერთად).
მოგვიანებით ელექტრონის დიფრაქციულმა კვლევებმა აჩვენა, რომ ბენზოლის მოლეკულაში ნახშირბადის ატომებს შორის ყველა ბმას აქვს იგივე სიგრძე 0,140 ნმ (საშუალო მნიშვნელობა ერთი C-C ბმის სიგრძეს 0,154 ნმ და ორმაგ C=C კავშირს 0,134 ნმ შორის). ნახშირბადის თითოეულ ატომში ბმებს შორის კუთხე არის 120°. მოლეკულა არის ჩვეულებრივი ბრტყელი ექვსკუთხედი.
თანამედროვე თეორია C 6 H 6 მოლეკულის სტრუქტურის ასახსნელად იყენებს ატომური ორბიტალების ჰიბრიდიზაციის კონცეფციას.
ბენზოლში ნახშირბადის ატომები sp 2 ჰიბრიდიზაციის მდგომარეობაშია. თითოეული "C" ატომი აყალიბებს სამ σ-ბმას (ორი ნახშირბადის ატომთან და ერთი წყალბადის ატომთან). ყველა σ-ბმა ერთ სიბრტყეშია:
ნახშირბადის თითოეულ ატომს აქვს ერთი p-ელექტრონი, რომელიც არ მონაწილეობს ჰიბრიდიზაციაში. ნახშირბადის ატომების არაჰიბრიდირებული p-ორბიტალები განლაგებულია σ-ბმათა სიბრტყის პერპენდიკულარულ სიბრტყეში. თითოეული p-ღრუბელი გადაფარავს ორ მეზობელ p-ღრუბელს და შედეგად წარმოიქმნება ერთი კონიუგირებული π- სისტემა (გაიხსენეთ p-ელექტრონების შეერთების ეფექტი 1,3-ბუტადიენის მოლეკულაში, განხილული თემაში „დიენის ნახშირწყალბადები ”):
ექვსი σ-ბმის კომბინაციას ერთ π-სისტემასთან ე.წ არომატული ბმა.
ნახშირბადის ექვსი ატომისგან შემდგარი რგოლი, რომელსაც აკავშირებს არომატული ბმა ეწოდება ბენზოლის ბეჭედი,ან ბენზოლის ბირთვი.
ბენზოლის ელექტრონული სტრუქტურის შესახებ თანამედროვე იდეების შესაბამისად, C 6 H 6 მოლეკულა გამოსახულია შემდეგნაირად:

ბენზოლის ფიზიკური თვისებები
ბენზოლი ნორმალურ პირობებში არის უფერო სითხე; t o pl = 5,5 o C; ტო კიპ. = 80 დაახლოებით C; აქვს დამახასიათებელი სუნი; წყალთან შეურევა, კარგი გამხსნელი, ძალიან ტოქსიკური.
ბენზოლის ქიმიური თვისებები
არომატული ბმა განსაზღვრავს ბენზოლის და სხვა არომატული ნახშირწყალბადების ქიმიურ თვისებებს.
6π-ელექტრონული სისტემა უფრო სტაბილურია, ვიდრე ჩვეულებრივი ორელექტრონული π-ბმები. ამიტომ, დამატების რეაქციები ნაკლებად დამახასიათებელია არომატული ნახშირწყალბადებისთვის, ვიდრე უჯერი ნახშირწყალბადებისთვის. არენებისთვის ყველაზე დამახასიათებელია ჩანაცვლების რეაქციები.
მე. ჩანაცვლების რეაქციები
1.ჰალოგენაცია

2. ნიტრაცია
რეაქცია ხორციელდება მჟავებისა და მჟავების ნარევით (ნიტრატორული ნარევი): 
3. სულფონაცია

4. ალკილაცია ("H" ატომის ჩანაცვლება ალკილის ჯგუფით) - Friedel-Crafts-ის რეაქციებიწარმოიქმნება ბენზოლის ჰომოლოგები:

ჰალოალკანების ნაცვლად შეიძლება გამოყენებულ იქნას ალკენები (კატალიზატორის თანდასწრებით - AlCl 3 ან არაორგანული მჟავა):

II. დანამატის რეაქციები
1. ჰიდროგენიზაცია

2. ქლორის დამატება

III.ჟანგვის რეაქციები
1. წვა
2C 6 H 6 + 15O 2 → 12CO 2 + 6H 2 O
2. არასრული დაჟანგვა (KMnO 4 ან K 2 Cr 2 O 7 მჟავე გარემოში). ბენზოლის რგოლი მდგრადია ჟანგვის აგენტების მიმართ. რეაქცია არ ხდება.
ბენზოლის მიღება
ინდუსტრიაში:
1) ნავთობისა და ნახშირის გადამუშავება;
2) ციკლოჰექსანის დეჰიდროგენაცია:

3) ჰექსანის დეჰიდროციკლიზაცია (არომატიზაცია):

ლაბორატორიაში:
ბენზოის მჟავას მარილების შერწყმა:

ბენზოლის ჰომოლოგების იზომერიზმი და ნომენკლატურა
ბენზოლის ნებისმიერ ჰომოლოგს აქვს გვერდითი ჯაჭვი, ე.ი. ბენზოლის რგოლზე მიმაგრებული ალკილის რადიკალები. ბენზოლის პირველი ჰომოლოგი არის ბენზოლის ბირთვი, რომელიც დაკავშირებულია მეთილის რადიკალთან: 
ტოლუენს არ აქვს იზომერები, რადგან ბენზოლის რგოლში ყველა პოზიცია ექვივალენტურია.
ბენზოლის შემდგომი ჰომოლოგებისთვის შესაძლებელია იზომერიზმის ერთი ტიპი - გვერდითი ჯაჭვის იზომერიზმი, რომელიც შეიძლება იყოს ორი ტიპის:
1) შემცვლელთა რიცხვისა და სტრუქტურის იზომერიზმი;
2) შემცვლელების პოზიციის იზომერიზმი.



ტოლუოლის ფიზიკური თვისებები
ტოლუენი- უფერო სითხე დამახასიათებელი სუნით, წყალში უხსნადი, ორგანულ გამხსნელებში ხსნადი. ტოლუენი ნაკლებად ტოქსიკურია ვიდრე ბენზოლი.
ტოლუოლის ქიმიური თვისებები
მე. ჩანაცვლების რეაქციები
1. ბენზოლის რგოლთან დაკავშირებული რეაქციები
მეთილბენზოლი შედის ყველა ჩანაცვლების რეაქციაში, რომელშიც მონაწილეობს ბენზოლი და ამავდროულად ავლენს უფრო მაღალ რეაქტიულობას, რეაქციები უფრო სწრაფი ტემპით მიმდინარეობს.
ტოლუოლის მოლეკულაში შემავალი მეთილის რადიკალი არის გვარის შემცვლელი, ამიტომ, ბენზოლის ბირთვში ჩანაცვლებითი რეაქციების შედეგად მიიღება ტოლუოლის ორთო- და პარაწარმოებულები ან, რეაგენტის ჭარბი რაოდენობით, ტრი-წარმოებულები. ზოგადი ფორმულით:

ა) ჰალოგენაცია


შემდგომი ქლორირებით შესაძლებელია დიქლორმეთილბენზოლის და ტრიქლორმეთილბენზოლის მიღება:

II. დანამატის რეაქციები
ჰიდროგენიზაცია

III.ჟანგვის რეაქციები
1. წვა
C 6 H 5 CH 3 + 9O 2 → 7CO 2 + 4H 2 O
2. არასრული დაჟანგვა
ბენზოლისგან განსხვავებით, მისი ჰომოლოგები იჟანგება ზოგიერთი ჟანგვის აგენტებით; ამ შემთხვევაში გვერდითი ჯაჭვი განიცდის დაჟანგვას, ტოლუოლის შემთხვევაში მეთილის ჯგუფი. მსუბუქი ჟანგვის აგენტები, როგორიცაა MnO 2, აჟანგავს მას ალდეჰიდის ჯგუფში, უფრო ძლიერი ჟანგვის აგენტები (KMnO 4) იწვევს შემდგომ დაჟანგვას მჟავამდე: 
ბენზოლის ნებისმიერი ჰომოლოგი ერთი გვერდითი ჯაჭვით იჟანგება ძლიერი ჟანგვის აგენტით, როგორიცაა KMnO4 ბენზოინის მჟავად, ე.ი. ხდება გვერდითი ჯაჭვის წყვეტა მისი გაწყვეტილი ნაწილის CO 2-მდე დაჟანგვით; მაგალითად: 
რამდენიმე გვერდითი ჯაჭვის თანდასწრებით, თითოეული მათგანი იჟანგება კარბოქსილის ჯგუფში და შედეგად წარმოიქმნება პოლიბაზური მჟავები, მაგალითად:

ტოლუოლის მიღება:
ინდუსტრიაში:
1) ნავთობისა და ნახშირის გადამუშავება;
2) მეთილციკლოჰექსანის დეჰიდროგენაცია:

3) ჰეპტანის დეჰიდროციკლიზაცია:
ლაბორატორიაში:
1) Friedel-Crafts-ის ალკილაცია;
2) ვურც-ფიტიგის რეაქცია(ნატრიუმის რეაქცია ჰალობენზოლისა და ჰალოალკანის ნარევთან).
PRTSVSH (F) FGBOU VPO
სახანძრო უსაფრთხოების დეპარტამენტი
ტესტი
დისციპლინაში "წვის და აფეთქებების თეორია"
დავალება ნომერი 1
განსაზღვრეთ ბენზოლის ორთქლის სრული წვისთვის საჭირო ჰაერის სპეციფიკური თეორიული რაოდენობა და მოცულობა. პირობები, რომელშიც ჰაერი მდებარეობს, ხასიათდება ტემპერატურით Tv და წნევით Pv, ხოლო ბენზოლის ორთქლი - ტემპერატურა Tg და წნევა Pg. გამოთვალეთ გამოთვლების შედეგები შემდეგი ერთეულებით: ; ;;;
საწყისი მონაცემები (N - ჯგუფის ნომერი, n - ნომერი მოსწავლეთა სიის მიხედვით:
TV=300+(-1) N *2*N-(-1) n *0.2*n= 277.6 K
Pv \u003d? 10 3 \u003d 95900 Pa;
Тg=300?(?1) N?2?N?(?1) n?0.2?n= 321.6 K;
Pr \u003d? 10 3 \u003d 79400 Pa.
С6Н6+7.5О2+7.5?3.76N2=6CO2+3pO+7.5?3.76N2+Qp (1),
სადაც Qp არის ქიმიური რეაქციის სითბო. ამ განტოლებიდან შესაძლებელია ბენზოლისა და მოლეკულური ჟანგბადის სტოქიომეტრიული კოეფიციენტების დადგენა: Vg = 1, V0 = 7,5
2. ჰაერის სპეციფიკური თეორიული რაოდენობა – ჰაერის კილომოლთა რაოდენობა, რომელიც აუცილებელია ერთი კილომოლი ბენზოლის სრული წვისთვის, გამოითვლება ფორმულით:
სადაც 4.76 არის ჰაერის რაოდენობა, რომელიც შეიცავს ჟანგბადის ერთეულს, \u003d არის მოლეკულური ჟანგბადის (Vo) და ბენზოლის (Vg) სტექიომეტრიული კოეფიციენტების თანაფარდობა.
Vo და Vg მნიშვნელობების (დ) ჩანაცვლებით, მივიღებთ:
3. ერთი კილომოლი ბენზოლის სრული წვისთვის საჭირო ჰაერის მოცულობა განისაზღვრება შემდეგნაირად:
სად არის ერთი კილომოლი ჰაერის მოცულობა Tv ტემპერატურაზე და წნევა Pv. ღირებულება გამოითვლება ფორმულის გამოყენებით
სადაც 22.4 არის გაზის მოლური მოცულობა ნორმალურ პირობებში, Po = 101325 Pa არის ნორმალური წნევა, To = 273 K არის ნორმალური ტემპერატურა.
Tv, To, Pv, Po ჩანაცვლებით (5) ვიღებთ
ჰაერის სპეციფიკური თეორიული მოცულობა გამოითვლება ფორმულით (4):
4. აირისებრი საწვავის ერთეული მოცულობის სრული წვისთვის საჭირო ჰაერის მოცულობა განისაზღვრება შემდეგნაირად:
სად არის ერთი კილომოლი საწვავის მოცულობა - ბენზოლის ორთქლი ტემპერატურაზე Tg და წნევა Pg. Იმის გათვალისწინებით, რომ
და (8) და (5) (7) ჩანაცვლებით, მივიღებთ შემდეგ გამოხატულებას ჰაერის სპეციფიკური თეორიული მოცულობისთვის:
ჩვენ ვიანგარიშებთ წვის პროცესის ამ პარამეტრის მნიშვნელობას:
ერთი კილოგრამი ბენზოლის სრული წვისთვის საჭირო ჰაერის მოცულობა განისაზღვრება შემდეგნაირად:
სადაც - საწვავის მოლური მასა არის ბენზოლის ერთი კილომოლის მასა, გამოხატული კილოგრამებში. ბენზოლის მოლური მასა რიცხობრივად მისი მოლეკულური წონის ტოლია ფორმულით:
Ac?nc + An?nn, UiAi?ni (11)
სადაც Ac და An არის ნახშირბადის და წყალბადის ატომური წონა, nc და nn არის ნახშირბადის ატომების რიცხვი ბენზოლის მოლეკულაში. Ac = 12, nc = 6, An = 1, nn = 6 მნიშვნელობების ჩანაცვლებით, მივიღებთ:
ჩვენ ვპოულობთ ჰაერის სპეციფიკურ თეორიულ მოცულობას n-ის მნიშვნელობების ჩანაცვლებით ფორმულაში (10):
გაანგარიშების შედეგი:
დავალება ნომერი 2
განსაზღვრეთ ბენზოლის წვის პროდუქტების სპეციფიკური თეორიული რაოდენობა, მოცულობა და შემადგენლობა, თუ ცნობილია ჭარბი ჰაერის კოეფიციენტი c, ტემპერატურა Tp და წვის პროდუქტების წნევა Pp, ტემპერატურა Tg და ბენზოლის ორთქლის წნევა Pg. გამოთვალეთ გამოთვლის შედეგები მოლური წილადებით (პროცენტებში) და შემდეგ ერთეულებში: ; ;;
საწყისი მონაცემები:
c=1.5+(?1) N?0.1?N?(?1) n?0.01?n = 0.2;
Rp \u003d? 10 3 \u003d 68400 Pa;
Tp=1600?(?1) N?20?N?(?1) n?2?n = 1816 K;
Тg=273?(?1) N?2?N+(?1) n?0.2?n = 295.4 K;
Rg \u003d? 10 3 \u003d 111600 Pa;
ხსნარი (N=11, n=2).
1. ვწერთ სტოქიომეტრულ განტოლებას ჰაერში ბენზოლის წვის რეაქციისთვის:
C 6 H 6 +7.5O 2 +7.5? 3.76N 2 \u003d 6CO 2 + 3H 2 O + 7.5? 3.76N 2 + Qp, (1)
სადაც Qp არის ქიმიური რეაქციის სითბო. ამ განტოლებიდან ჩვენ ვადგენთ შემდეგ სტექიომეტრულ კოეფიციენტებს:
V CO2 \u003d 6, V pO \u003d 3, V C6H6 \u003d 1, V O2 \u003d 7.5, V N2 \u003d 7.5? 3.76
2. დაადგინეთ ერთი კილომოლი საწვავის წვის პროდუქტების სავარაუდო რაოდენობა:
წვის პროდუქტებისა და საწვავის სტოქიომეტრიული კოეფიციენტების (2) მნიშვნელობების ჩანაცვლებით, მივიღებთ:
3. ჰაერის სპეციფიკური თეორიული რაოდენობა - ერთი კილომოლი საწვავის სრული წვისთვის საჭირო კილომოლ ჰაერის რაოდენობას ვადგენთ ფორმულის გამოყენებით:
სადაც 4.76 არის ჰაერის რაოდენობა, რომელიც შეიცავს ჟანგბადის ერთეულს,
მოლეკულური ჟანგბადისა და ბენზოლის სტოქიომეტრიული კოეფიციენტების თანაფარდობა.
(4) V O2 =7.5 და V C6H6 =1 მნიშვნელობების ჩანაცვლებით, მივიღებთ:
4. ჰაერის ჭარბი რაოდენობა, რომელიც მოდის 1 კმოლ საწვავზე, განისაზღვრება გამოთქმით:
ბენზოლის ორთქლის წვის ჰაერი
ამ გამოსახულებაში მნიშვნელობების ჩანაცვლება
37,7(0,2-1)=30,16(7)
5. წვის პროდუქტების ჯამური რაოდენობა საწვავის ნივთიერების ერთეულ რაოდენობაზე განისაზღვრება ჯამით:
მნიშვნელობების ჩანაცვლების შემდეგ მივიღებთ:
6. წვის პროდუქტების მოლური ფრაქციები, გამოხატული პროცენტულად, განისაზღვრება შემდეგნაირად:
ფორმულებში (9) წვის პროდუქტებში აზოტისა და ჟანგბადის მოლური ფრაქციებისთვის 0,79 და 0,21 არის ამ ნივთიერებების მოლური ფრაქციები ჰაერში, რომელთა ჭარბი რაოდენობა იწვევს აზოტის პროპორციის ზრდას და ჟანგბადის გამოჩენას. წვის პროდუქტებში.
7. წვის სპეციფიკური მოცულობებისა და პროდუქტების დასადგენად საჭიროა მათი მოლური მოცულობის გამოთვლა - ერთი კილომოლის გაზის მოცულობა იმ პირობებში, რომელშიც პროდუქცია მდებარეობს:
სადაც 22.4 არის ერთი კილომოლი გაზის მოცულობა ნორმალურ პირობებში, T 0 \u003d 273K - ნორმალური ტემპერატურა, Po \u003d 101325 Pa - ნორმალური წნევა.
თუ შევცვლით (10) მნიშვნელობებს, Po, To, მივიღებთ:
პროდუქციის მოცულობა, რომელიც წარმოიქმნება ერთი კილოგრამი საწვავის წვის დროს, ზედმეტი ჰაერის გამოკლებით, გამოითვლება შემდეგნაირად:
სადაც - საწვავის მოლური მასა არის ბენზოლის ერთი კილომოლის მასა, გამოხატული კილოგრამებში. ბენზოლის მოლური მასა გვხვდება ფორმულით:
სადაც Ac და An არის ნახშირბადის (12) და წყალბადის (1) ატომური წონა, nc და n n არის ნახშირბადის (6) და წყალბადის (6) ატომების რაოდენობა ბენზოლის მოლეკულებში (C 6 H 6).
მნიშვნელობების ჩანაცვლება და (12)-ში ვიღებთ
ჰაერის ჭარბი მოცულობა 1 კილოგრამ საწვავზე განისაზღვრება შემდეგნაირად:
სად არის ერთი კილომოლის ჭარბი ჰაერის მოცულობა, რომელიც წვის პროდუქტების ნაწილია. ვინაიდან ჭარბი ჰაერის ტემპერატურა და წნევა შეესაბამება წვის პროდუქტების ტემპერატურასა და წნევას, მაშინ \u003d \u003d 220.7.
ამ მნიშვნელობის ჩანაცვლებით, ისევე როგორც (14-ში), მივიღებთ:
საწვავის სრული წვის პროდუქტების სპეციფიკური მოცულობის გამოსათვლელად, ჩვენ ვვარაუდობთ, რომ ბენზოლის ორთქლს აქვს ტემპერატურა Tg წნევაზე:
სად არის ერთი კილომოლი ბენზოლის ორთქლის მოცულობა Tg ტემპერატურაზე და წნევა Pg. საწვავის მოლური მოცულობა გამოითვლება ფორმულით:
მიღებული მნიშვნელობის ჩანაცვლებით და ასეთი მნიშვნელობებით (17), ვიღებთ:
ჰაერის ჭარბი მოცულობა ბენზოლის ორთქლის კუბურ მეტრზე განისაზღვრება შემდეგნაირად:
ჩანაცვლება (20) მნიშვნელობებში \u003d 30.16, \u003d და
იძლევა შემდეგ შედეგს:
წვის პროდუქტების საერთო სპეციფიკური მოცულობა, ჭარბი ჰაერის გათვალისწინებით, განისაზღვრება ჯამით
გაანგარიშების შედეგი:
X CO2 \u003d%; X H2O \u003d 4.4%; X N2 =%; X O2 \u003d 11,7%
მსგავსი დოკუმენტები
ნიტრობენზოლის C6H5NO2 და ნახშირბადის დისულფიდის CS2 წვადობის კოეფიციენტის გამოთვლა. ჰაერში პროპილაცეტატის წვის რეაქციის განტოლება. ჰაერისა და წვის პროდუქტების მოცულობის გაანგარიშება წვადი აირის წვის დროს. ტოლუოლის აალების წერტილის განსაზღვრა ვ.ბლინოვის ფორმულის მიხედვით.
ტესტი, დამატებულია 04/08/2017
ნივთიერების წვის დროს წარმოქმნილი ჰაერისა და წვის პროდუქტების მოცულობის გაანგარიშება. ჰაერში ეთილენგლიკოლის წვის რეაქციის განტოლება. აალებადი აირების ნარევის წვა. ადიაბატური წვის ტემპერატურის გაანგარიშება სტექიომეტრული ნარევისთვის. პროპანოლის წვა.
ტესტი, დამატებულია 17/10/2012
წვის ტიპი და მისი ძირითადი პარამეტრები. საწვავის და ოქსიდანტის ქიმიური გარდაქმნა წვის პროდუქტად. წვის რეაქციის მატერიალური და თერმული ბალანსის განტოლებები. ჭარბი ჰაერის კოეფიციენტის გავლენა წვის პროდუქტების შემადგენლობაზე და წვის ტემპერატურაზე.
ტესტი, დამატებულია 01/17/2013
წვადი ნივთიერების ერთეული მასის სრული წვისთვის საჭირო ჰაერის მოცულობის განსაზღვრა. წვადი ნივთიერების ერთეული მასის წვის პროდუქტების შემადგენლობა. აირის, ორთქლის, მტვერ-ჰაერის ნარევების ალი გავრცელების საზღვრები. ფეთქებადი დაშლის წნევა.
ნაშრომი, დამატებულია 23.12.2013
ხანძრისა და აფეთქების თავიდან აცილების ღონისძიებების შემუშავება, მათი განვითარებისა და ჩახშობის პირობების შეფასება. დამწვრობის სიჩქარის ცნება, მისი განსაზღვრის მეთოდი. წვის რეაქციის განტოლების შედგენის პროცედურა. ანთებისთვის საჭირო ჰაერის მოცულობის გაანგარიშება.
საკურსო ნაშრომი, დამატებულია 07/10/2014
გაზის სრული წვის პროდუქტების შემადგენლობის განსაზღვრა. გაზის ნარევის ადიაბატური წვის ტემპერატურის გამოთვლა მუდმივი მოცულობისა და მუდმივი წნევის დროს. ბუნებრივი აირის თვითაალების კინეტიკური რეაქციის მუდმივები. გაზის ნარევის აალების ლიმიტი.
საკურსო ნაშრომი, დამატებულია 19.02.2014
ბენზოლის პროპილენით ალკილირების სამრეწველო მეთოდების დახასიათება. ბენზოლის ალკილაციის პრინციპები ოლეფინებით ქიმიურ ტექნოლოგიაში. ბენზოლის ალკილირების ტექნოლოგიური დანადგარების დაპროექტების პრობლემები. წარმოების პროცესის ტექნოლოგიის აღწერა.
დისერტაცია, დამატებულია 15/11/2010
წვა არის ძლიერი დაჟანგვის პროცესი. წვის სახეები: დნება და წვა ალივით. აფეთქება, როგორც წვის განსაკუთრებული შემთხვევა. ცეცხლის ელექტრული თვისებები. წვის პროდუქტების მრავალფეროვნება საწვავის არასრული წვის შედეგად. კვამლის ფილტრაცია წყლის მეშვეობით.
სამეცნიერო ნაშრომი, დამატებულია 29.07.2009წ
პროპანის მოცემული რაოდენობის სრული წვისთვის საჭირო ჰაერის მოცულობის განსაზღვრა. ენთალპიის, ენტროპიისა და გიბსის ენერგიის ცვლილების გამოთვლა ჰესის კანონის შედეგების გამოყენებით. ჟანგვის და აღმდგენი აგენტის მოლური მასის ეკვივალენტების განსაზღვრა.
ტესტი, დამატებულია 02/08/2012
შთამნთქმელი ზეთის მოხმარების განსაზღვრის მეთოდები, შთამნთქმელ ზეთში ბენზოლის კონცენტრაცია, რომელიც ტოვებს შთამნთქმელს. შეფუთული შთანთქმის დიამეტრისა და სიმაღლის გაანგარიშება. სვეტის კუბში საჭირო გათბობის ზედაპირის განსაზღვრა და გათბობის ორთქლის მოხმარება.
რეაქციების პირველი ჯგუფი არის ჩანაცვლების რეაქციები. ჩვენ ვთქვით, რომ არენებს არ აქვთ მრავალჯერადი ბმა მოლეკულურ სტრუქტურაში, მაგრამ შეიცავს ექვსი ელექტრონის კონიუგირებულ სისტემას, რომელიც ძალიან სტაბილურია და დამატებით ძალას ანიჭებს ბენზოლის რგოლს. ამრიგად, ქიმიურ რეაქციებში, უპირველეს ყოვლისა, ხდება წყალბადის ატომების ჩანაცვლება და არა ბენზოლის რგოლის განადგურება.
ალკანებზე საუბრისას უკვე შეგვხვდა ჩანაცვლებითი რეაქციები, მაგრამ მათთვის ეს რეაქციები რადიკალური მექანიზმით მიმდინარეობდა, არენებისთვის კი დამახასიათებელია ჩანაცვლებითი რეაქციების იონური მექანიზმი.
Პირველიქიმიური თვისებების ჰალოგენაცია. წყალბადის ატომის ჩანაცვლება ჰალოგენის ატომით ქლორით ან ბრომით.
რეაქცია მიმდინარეობს გაცხელებისას და ყოველთვის კატალიზატორის მონაწილეობით. ქლორის შემთხვევაში, ეს შეიძლება იყოს ალუმინის ქლორიდი ან რკინის ქლორიდი სამი. კატალიზატორი ახდენს ჰალოგენის მოლეკულის პოლარიზებას, რის შედეგადაც ხდება ჰეტეროლიზური ბმის გაწყვეტა და იონების მიღება.
დადებითად დამუხტული ქლორიდის იონი რეაგირებს ბენზოლთან.
თუ რეაქცია ხდება ბრომთან, მაშინ რკინის ტრიბრომიდი ან ალუმინის ბრომიდი მოქმედებს როგორც კატალიზატორი.

მნიშვნელოვანია აღინიშნოს, რომ რეაქცია ხდება მოლეკულურ ბრომთან და არა ბრომიან წყალთან. ბენზოლი არ რეაგირებს ბრომიან წყალთან.
ბენზოლის ჰომოლოგების ჰალოგენიზაციას აქვს საკუთარი მახასიათებლები. ტოლუენის მოლეკულაში მეთილის ჯგუფი ხელს უწყობს ჩანაცვლებას რგოლში, რეაქტიულობა იზრდება და რეაქცია მიმდინარეობს უფრო რბილ პირობებში, ანუ უკვე ოთახის ტემპერატურაზე.

მნიშვნელოვანია აღინიშნოს, რომ ჩანაცვლება ყოველთვის ხდება ორთო და პარა პოზიციებზე, ამიტომ მიიღება იზომერების ნარევი.
მეორებენზოლის თვისება ნიტრირება, ბენზოლის რგოლში ნიტრო ჯგუფის შეყვანა.
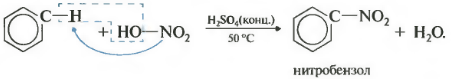
წარმოიქმნება მძიმე მოყვითალო სითხე მწარე ნუშის ნიტრობენზოლის სუნით, ამიტომ რეაქცია შეიძლება იყოს ხარისხობრივი ბენზოლისთვის. ნიტრატირებისთვის გამოიყენება კონცენტრირებული აზოტისა და გოგირდის მჟავების ნიტრატირების ნარევი. რეაქცია ხორციელდება გათბობით.
შეგახსენებთ, რომ კონოვალოვის რეაქციაში ალკანების ნიტრაციისთვის გამოიყენებოდა განზავებული აზოტის მჟავა გოგირდმჟავას დამატების გარეშე.
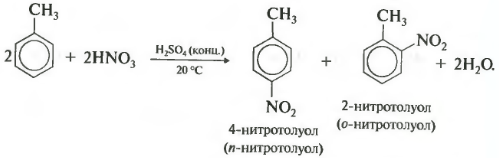
ტოლუოლის ნიტრაციისას, ასევე ჰალოგენიზაციისას წარმოიქმნება ორთო- და პარა-იზომერების ნარევი.
მესამებენზოლის ალკილაცია ჰალოალკანებით.

ეს რეაქცია იძლევა ბენზოლის რგოლში ნახშირწყალბადის რადიკალის შეყვანის საშუალებას და შეიძლება ჩაითვალოს ბენზოლის ჰომოლოგების მიღების მეთოდად. ალუმინის ქლორიდი გამოიყენება როგორც კატალიზატორი, რომელიც ხელს უწყობს ჰალოალკანის მოლეკულის იონებად დაშლას. მას ასევე სჭირდება გათბობა.
მეოთხებენზოლის ალკილიზაცია ალკენებით.
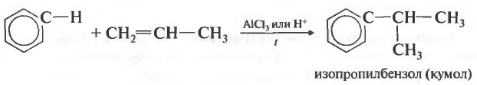
ამ გზით, მაგალითად, კუმენის ან ეთილბენზოლის მიღება შეიძლება. კატალიზატორი ალუმინის ქლორიდი.
2. ბენზოლთან დამატების რეაქციები
რეაქციების მეორე ჯგუფი არის დანამატის რეაქციები. ჩვენ ვთქვით, რომ ეს რეაქციები არ არის დამახასიათებელი, მაგრამ ისინი შესაძლებელია საკმაოდ მძიმე პირობებში პი-ელექტრონული ღრუბლის განადგურებით და ექვსი სიგმა ბმის წარმოქმნით.
მეხუთეთვისება ზოგად სიაში ჰიდროგენიზაცია, წყალბადის დამატება.
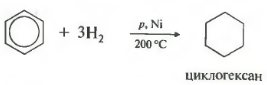
ტემპერატურა, წნევა, კატალიზატორი ნიკელი ან პლატინი. ტოლუენს შეუძლია ანალოგიურად რეაგირება.
მეექვსექონების ქლორირება. გთხოვთ გაითვალისწინოთ, რომ ჩვენ ვსაუბრობთ კონკრეტულად ქლორთან ურთიერთქმედების შესახებ, რადგან ბრომი არ შედის ამ რეაქციაში.

რეაქცია მიმდინარეობს მძიმე ულტრაიისფერი გამოსხივების ქვეშ. ჰექსაქლოროციკლოჰექსანი, ჰექსაქლორანის სხვა სახელი, წარმოიქმნება მყარი.
მნიშვნელოვანია გვახსოვდეს, რომ ბენზოლისთვის შეუძლებელიწყალბადის ჰალოგენების დამატების რეაქციები (ჰიდროჰალოგენაცია) და წყლის დამატება (ჰიდრატაცია).
3. ჩანაცვლება ბენზოლის ჰომოლოგების გვერდით ჯაჭვში
რეაქციების მესამე ჯგუფი ეხება მხოლოდ ბენზოლის ჰომოლოგებს - ეს არის ჩანაცვლება გვერდით ჯაჭვში.
მეშვიდეთვისება ზოგად სიაში ჰალოგენაცია ალფა ნახშირბადის ატომზე გვერდითა ჯაჭვში.

რეაქცია ხდება გაცხელების ან დასხივებისას და ყოველთვის მხოლოდ ალფა ნახშირბადზე. ჰალოგენაციის გაგრძელებისას მეორე ჰალოგენის ატომი უბრუნდება ალფა პოზიციას.
4. ბენზოლის ჰომოლოგების დაჟანგვა
რეაქციების მეოთხე ჯგუფი არის დაჟანგვა.
ბენზოლის რგოლი ძალიან ძლიერია, ამიტომ ბენზოლი არ იჟანგებაკალიუმის პერმანგანატი არ აფერხებს მის ხსნარს. ეს ძალიან მნიშვნელოვანია გახსოვდეთ.
მეორეს მხრივ, ბენზოლის ჰომოლოგები იჟანგება კალიუმის პერმანგანატის დამჟავებული ხსნარით გაცხელებისას. და ეს არის მერვე ქიმიური თვისება.

გამოდის ბენზოის მჟავა. შეინიშნება ხსნარის გაუფერულება. ამ შემთხვევაში, რაც არ უნდა გრძელი იყოს შემცვლელის ნახშირბადის ჯაჭვი, ის ყოველთვის წყდება ნახშირბადის პირველი ატომის შემდეგ და ალფა ატომი იჟანგება კარბოქსილის ჯგუფში ბენზოინის მჟავის წარმოქმნით. დანარჩენი მოლეკულა იჟანგება შესაბამის მჟავამდე ან, თუ ეს მხოლოდ ერთი ნახშირბადის ატომია, ნახშირორჟანგამდე.
თუ ბენზოლის ჰომოლოგს აქვს ერთზე მეტი ნახშირწყალბადის შემცვლელი არომატულ რგოლზე, მაშინ დაჟანგვა ხდება იგივე წესების მიხედვით - ალფა მდგომარეობაში მყოფი ნახშირბადი იჟანგება.
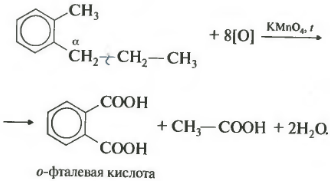
ამ მაგალითში მიიღება ორფუძიანი არომატული მჟავა, რომელსაც ფტალინის მჟავა ეწოდება.
განსაკუთრებულად აღვნიშნავ კუმენის, იზოპროპილბენზოლის დაჟანგვას ატმოსფერული ჟანგბადით გოგირდმჟავას თანდასწრებით.

ეს არის ეგრეთ წოდებული კუმენის მეთოდი ფენოლის წარმოებისთვის. როგორც წესი, ამ რეაქციას უნდა გაუმკლავდეთ ფენოლის წარმოებასთან დაკავშირებულ საკითხებში. ეს არის ინდუსტრიული გზა.
მეცხრექონების წვა, სრული დაჟანგვა ჟანგბადით. ბენზოლი და მისი ჰომოლოგები იწვება ნახშირორჟანგამდე და წყალში.
დავწეროთ ბენზოლის წვის განტოლება ზოგადი ფორმით.
მასის შენარჩუნების კანონის მიხედვით, მარცხნივ იმდენი ატომები უნდა იყოს, რამდენიც მარჯვნივ. იმიტომ რომ, ბოლოს და ბოლოს, ქიმიურ რეაქციებში ატომები არსად მიდიან, მაგრამ მათ შორის ობლიგაციების რიგი უბრალოდ იცვლება. ასე რომ, ნახშირორჟანგის იმდენი მოლეკულა იქნება, რამდენი ნახშირბადის ატომია არენის მოლეკულაში, ვინაიდან მოლეკულა შეიცავს ნახშირბადის ერთ ატომს. ეს არის n CO 2 მოლეკულები. იქნება წყალბადის ატომების ნახევარი წყლის მოლეკულა, ანუ (2n-6) / 2, რაც ნიშნავს n-3.
მარცხნივ და მარჯვნივ არის ჟანგბადის ატომების იგივე რაოდენობა. მარჯვნივ არის 2n ნახშირორჟანგიდან, რადგან თითოეულ მოლეკულაში არის ორი ჟანგბადის ატომი, პლუს n-3 წყლისგან, სულ 3n-3. მარცხნივ არის ჟანგბადის ატომების იგივე რაოდენობა 3n-3, რაც ნიშნავს, რომ ორჯერ ნაკლებია მოლეკულა, რადგან მოლეკულა შეიცავს ორ ატომს. ანუ (3n-3)/2 ჟანგბადის მოლეკულა.
ამრიგად, ჩვენ შევადგინეთ ბენზოლის ჰომოლოგების წვის განტოლება ზოგადი ფორმით.
არენები (არომატული ნახშირწყალბადები) – ეს არის უჯერი (უჯერი) ციკლური ნახშირწყალბადები, რომელთა მოლეკულები შეიცავს ატომების სტაბილურ ციკლურ ჯგუფებს (ბენზოლის ბირთვები) კონიუგირებული ბმების დახურული სისტემით.
ზოგადი ფორმულა: C n H 2n–6n ≥ 6-ისთვის.
არენების ქიმიური თვისებები
არენები- უჯერი ნახშირწყალბადები, რომელთა მოლეკულები შეიცავს სამ ორმაგ ბმას და ციკლს. მაგრამ კონიუგაციის ეფექტის გამო, არენების თვისებები განსხვავდება სხვა უჯერი ნახშირწყალბადების თვისებებისგან.
არომატული ნახშირწყალბადები ხასიათდება რეაქციებით:
- შეერთება,
- ცვლილება,
- დაჟანგვა (ბენზოლის ჰომოლოგებისთვის).
ბენზოლის არომატული სისტემა მდგრადია ჟანგვის აგენტების მიმართ. თუმცა, ბენზოლის ჰომოლოგები იჟანგება კალიუმის პერმანგანატის და სხვა ჟანგვის აგენტების მოქმედებით.
1. დანამატის რეაქციები
ბენზოლი ამატებს ქლორს სინათლეში და წყალბადს კატალიზატორის თანდასწრებით გაცხელებისას.
1.1. ჰიდროგენიზაცია
ბენზოლი ამატებს წყალბადს გაცხელებისას და წნევის ქვეშ ლითონის კატალიზატორების (Ni, Pt და ა.შ.) თანდასწრებით.
ბენზოლის ჰიდროგენაცია წარმოქმნის ციკლოჰექსანს:
ჰომოლოგების ჰიდროგენიზაცია იძლევა ციკლოალკანის წარმოებულებს. როდესაც ტოლუენი თბება წყალბადით წნევის ქვეშ და კატალიზატორის თანდასწრებით, წარმოიქმნება მეთილციკლოჰექსანი:
1.2. არენების ქლორირება
ბენზოლში ქლორის დამატება გრძელდება რადიკალური მექანიზმით მაღალ ტემპერატურაზე, ულტრაიისფერი გამოსხივების გავლენის ქვეშ.
სინათლის თანდასწრებით ბენზოლის ქლორირება წარმოებს 1,2,3,4,5,6-ჰექსაქლოროციკლოჰექსანი (ჰექსაქლორანი).
ჰექსაქლორანი არის პესტიციდი, რომელიც გამოიყენება მავნე მწერების გასაკონტროლებლად. ამჟამად ჰექსაქლორანის გამოყენება აკრძალულია.
ბენზოლის ჰომოლოგები არ ამატებენ ქლორს. თუ ბენზოლის ჰომოლოგი რეაგირებს ქლორთან ან ბრომთან სინათლის ან მაღალი ტემპერატურის ზემოქმედება (300°C), მაშინ ხდება წყალბადის ატომების ჩანაცვლება გვერდით ალკილის შემცვლელზე და არა არომატულ რგოლზე.
2. ჩანაცვლების რეაქციები
2.1. ჰალოგენაცია
ბენზოლი და მისი ჰომოლოგები შედიან ჩანაცვლების რეაქციებში ჰალოგენებთან (ქლორი, ბრომი) კატალიზატორების თანდასწრებით (AlCl3, FeBr3). .
AlCl 3 კატალიზატორზე ქლორთან ურთიერთობისას წარმოიქმნება ქლორბენზოლი:
არომატული ნახშირწყალბადები ურთიერთქმედებენ ბრომთან გაცხელებისას და კატალიზატორის - FeBr 3 თანდასწრებით. ლითონის რკინა ასევე შეიძლება გამოყენებულ იქნას როგორც კატალიზატორი.
ბრომი რეაგირებს რკინასთან და წარმოქმნის რკინას (III) ბრომიდს, რომელიც ახორციელებს ბენზოლის ბრომირებას:
მეტა- ქლოროტოლუენი წარმოიქმნება მცირე რაოდენობით.
ბენზოლის ჰომოლოგების ურთიერთქმედებისას ჰალოგენებით შუქზე ან მაღალ ტემპერატურაზე(300 o C), წყალბადი იცვლება არა ბენზოლის რგოლში, არამედ გვერდითი ნახშირწყალბადის რადიკალში.
მაგალითად, ეთილბენზოლის ქლორირებისას:
2.2. ნიტრაცია
ბენზოლი რეაგირებს კონცენტრირებულ აზოტმჟავასთან კონცენტრირებული გოგირდმჟავას (ნიტრატირების ნარევი) თანდასწრებით.
ამ შემთხვევაში წარმოიქმნება ნიტრობენზოლი:
ტოლუოლი რეაგირებს კონცენტრირებულ აზოტმჟავასთან კონცენტრირებული გოგირდმჟავას თანდასწრებით.
რეაქციის პროდუქტებში ჩვენ მივუთითებთ ან შესახებ-ნიტროტოლუენი:
ან პ-ნიტროტოლუენი:
ტოლუოლის ნიტრაცია ასევე შეიძლება გაგრძელდეს წყალბადის სამი ატომის ჩანაცვლებით. ამ შემთხვევაში წარმოიქმნება 2,4,6-ტრინიტროტოლუენი (ტროტილი, ტოლი):
2.3. არომატული ნახშირწყალბადების ალკილაცია
- არენები ურთიერთქმედებენ ჰალოალკანებთან კატალიზატორების (AlCl 3, FeBr 3 და სხვ.) თანდასწრებით ბენზოლის ჰომოლოგების წარმოქმნით.
- არომატული ნახშირწყალბადები ურთიერთქმედებენ ალკენებთან ალუმინის ქლორიდის, რკინის (III) ბრომიდის, ფოსფორის მჟავას და ა.შ.
- სპირტებთან ალკილაცია მიმდინარეობს კონცენტრირებული გოგირდმჟავას თანდასწრებით.
2.4. არომატული ნახშირწყალბადების სულფონაცია
ბენზოლი რეაქციაში შედის კონცენტრირებულ გოგირდმჟავასთან ან SO 3 ხსნარით გოგირდმჟავაში (ოლეუმი) გაცხელებისას ბენზოლის სულფონის მჟავის წარმოქმნით:
3. არენების დაჟანგვა
ბენზოლი მდგრადია ძლიერი ჟანგვის აგენტების მიმართაც კი. მაგრამ ბენზოლის ჰომოლოგები იჟანგება ძლიერი ჟანგვის აგენტების მოქმედებით. ბენზოლი და მისი ჰომოლოგები იწვის.
3.1. სრული დაჟანგვა - წვა
ბენზოლის და მისი ჰომოლოგების წვის შედეგად წარმოიქმნება ნახშირორჟანგი და წყალი. არენების წვის რეაქციას თან ახლავს დიდი რაოდენობით სითბოს გამოყოფა.
2C 6 H 6 + 15O 2 → 12CO 2 + 6H 2 O + Q
არენების წვის ზოგადი განტოლება არის:
C n H 2n–6 + (3n – 3)/2 O 2 → nCO 2 + (n – 3)H 2 O + ქ
როდესაც არომატული ნახშირწყალბადები იწვის ჟანგბადის ნაკლებობით, ნახშირბადის მონოქსიდი CO ან ჭვარტლი C შეიძლება წარმოიქმნას.
ბენზოლი და მისი ჰომოლოგები ჰაერში იწვის კვამლის ალით. ბენზოლი და მისი ჰომოლოგები ქმნიან ფეთქებად ნარევებს ჰაერთან და ჟანგბადთან.
3.2. ობენზოლის ჰომოლოგების დაჟანგვა
ბენზოლის ჰომოლოგები ადვილად იჟანგება პერმანგანატის და კალიუმის დიქრომატით მჟავე ან ნეიტრალურ გარემოში გაცხელებისას.
ამავე დროს, ხდება ნახშირბადის ატომში ყველა ბმის დაჟანგვაბენზოლის რგოლის მიმდებარედ, გარდა ამ ნახშირბადის ატომის ბენზოლის რგოლთან კავშირისა.
ტოლუენი იჟანგება კალიუმის პერმანგანატი გოგირდმჟავაშიგანათლებით ბენზოის მჟავა:
თუ ტოლუენი იჟანგება გაცხელებისას ნეიტრალურ ხსნარში, შემდეგ იქმნება ბენზოის მჟავას მარილი - კალიუმის ბენზოატი:
ასე რომ, ტოლუენი აფერადებს კალიუმის პერმანგანატის მჟავიან ხსნარსროცა თბება.
უფრო გრძელი რადიკალები იჟანგება ბენზოის მჟავად და კარბოქსილის მჟავად:
პროპილბენზოლის დაჟანგვისას წარმოიქმნება ბენზოური და ძმარმჟავები:
იზოპროპილბენზოლი იჟანგება კალიუმის პერმანგანატის მიერ მჟავე გარემოში ბენზოის მჟავასა და ნახშირორჟანგამდე:
4. შემცვლელების ორიენტირებული მოქმედება ბენზოლის რგოლში
თუ ბენზოლის რგოლში არის შემცვლელები, არა მხოლოდ ალკილი, არამედ სხვა ატომების შემცველი (ჰიდროქსილი, ამინო ჯგუფი, ნიტრო ჯგუფი და ა.შ.), მაშინ არომატულ სისტემაში წყალბადის ატომების შემცვლელი რეაქციები მიმდინარეობს მკაცრად განსაზღვრული გზით, ბუნების შესაბამისად შემცვლელის გავლენა არომატულ π- სისტემაზე.
შემცვლელების სახეები ბენზოლის რგოლზე
| პირველი სახის შემცვლელები | მეორე სახის შემცვლელები |
| ორთო- და წყვილი- პოზიცია | შემდგომი ჩანაცვლება ძირითადად ხდება მეტა- პოზიცია |
| ელექტრონის დონორი, გაზრდის ელექტრონის სიმკვრივეს ბენზოლის რგოლში | ელექტრონის ამოღება, ელექტრონის სიმკვრივის შემცირება კონიუგირებული სისტემაში. |
|
|
