अल्केन्स की विशेषता मुख्य रूप से प्रतिक्रियाएँ होती हैं परिग्रहणदोहरे बंधन द्वारा. मूलतः, ये प्रतिक्रियाएँ आयनिक तंत्र के अनुसार आगे बढ़ती हैं। पाई बांड टूट जाता है और दो नए सिग्मा बांड बनते हैं। मैं आपको याद दिला दूं कि प्रतिस्थापन प्रतिक्रियाएं अल्केन्स के लिए विशिष्ट थीं और वे मूल तंत्र के अनुसार आगे बढ़ती थीं। हाइड्रोजन के अणु एल्कीनों से जुड़ सकते हैं, इन प्रतिक्रियाओं को हाइड्रोजनीकरण, पानी के अणु, जलयोजन, हैलोजन - हैलोजनीकरण, हाइड्रोजन हैलाइड्स - हाइड्रोहैलोजनेशन कहा जाता है। लेकिन सबसे पहले चीज़ें.
डबल बॉन्ड जोड़ प्रतिक्रियाएं
इसलिए, पहलारासायनिक गुण, हाइड्रोजन हैलाइड, हाइड्रोहैलोजनीकरण को संलग्न करने की क्षमता।
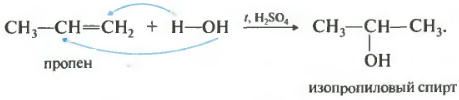
मार्कोवनिकोव के नियम के अनुसार प्रोपेन और अन्य एल्कीन हाइड्रोजन हैलाइड के साथ प्रतिक्रिया करते हैं।

हाइड्रोजन परमाणु सबसे अधिक हाइड्रोजनीकृत, या अधिक सही ढंग से हाइड्रोजनीकृत, कार्बन परमाणु से जुड़ा होता है।
दूसरागुणों की हमारी सूची में जलयोजन, पानी मिलाने का नंबर होगा।
प्रतिक्रिया तब होती है जब एसिड, आमतौर पर सल्फ्यूरिक या फॉस्फोरिक की उपस्थिति में गर्म किया जाता है। पानी का योग भी मार्कोवनिकोव के नियम के अनुसार होता है, अर्थात प्राथमिक अल्कोहल केवल एथिलीन के जलयोजन द्वारा प्राप्त किया जा सकता है, शेष अशाखित एल्केन्स द्वितीयक अल्कोहल देते हैं।
हाइड्रोहैलोजनेशन और हाइड्रेशन दोनों के लिए, मार्कोवनिकोव के नियम के अपवाद हैं। सबसे पहले, इस नियम के विरुद्ध, परिवर्धन पेरोक्साइड की उपस्थिति में होता है।
दूसरे, ऐल्कीनों के व्युत्पन्नों के लिए जिनमें इलेक्ट्रॉन निकालने वाले समूह मौजूद होते हैं। उदाहरण के लिए, 3,3,3-ट्राइफ्लोरोप्रोपीन-1 के लिए।
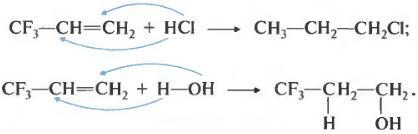
फ्लोरीन परमाणु, अपनी उच्च इलेक्ट्रोनगेटिविटी के कारण, सिग्मा बांड की श्रृंखला के साथ इलेक्ट्रॉन घनत्व को अपनी ओर खींचते हैं। इस घटना को नकारात्मक आगमनात्मक प्रभाव कहा जाता है।
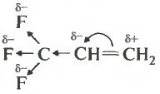
इसके कारण, दोहरे बंधन के मोबाइल पाई इलेक्ट्रॉन स्थानांतरित हो जाते हैं और सबसे बाहरी कार्बन परमाणु पर आंशिक सकारात्मक चार्ज होता है, जिसे आमतौर पर डेल्टा प्लस के रूप में दर्शाया जाता है। यह उसके लिए है कि नकारात्मक रूप से चार्ज किया गया ब्रोमीन आयन जाएगा, और हाइड्रोजन धनायन सबसे कम हाइड्रोजनीकृत कार्बन परमाणु में शामिल हो जाएगा।
उदाहरण के लिए, ट्राइफ्लोरोमेथाइल समूह के अलावा, ट्राइक्लोरोमेथाइल समूह, नाइट्रो समूह, कार्बोक्सिल समूह और कुछ अन्य का नकारात्मक प्रेरक प्रभाव होता है।
परीक्षा में मार्कोवनिकोव नियम के उल्लंघन का यह दूसरा मामला बहुत दुर्लभ है, लेकिन यदि आप अधिकतम अंक के लिए परीक्षा उत्तीर्ण करने की योजना बना रहे हैं तो इसे ध्यान में रखना अभी भी उचित है।
तीसराहैलोजन अणुओं का रासायनिक गुण योग।
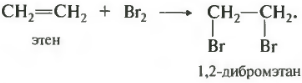
सबसे पहले, यह ब्रोमीन से संबंधित है, क्योंकि यह प्रतिक्रिया एकाधिक बंधन के लिए गुणात्मक है। उदाहरण के लिए, एथिलीन को ब्रोमीन पानी से गुजारते समय, यानी पानी में ब्रोमीन का घोल, जिसका रंग भूरा होता है, उसका मलिनकिरण होता है। यदि गैसों का मिश्रण, उदाहरण के लिए, ईथेन और ईथेन, ब्रोमीन पानी के माध्यम से पारित किया जाता है, तो ईथेन अशुद्धता के बिना शुद्ध ईथेन प्राप्त किया जा सकता है, क्योंकि यह डाइब्रोमोएथेन के रूप में प्रतिक्रिया फ्लास्क में रहेगा, जो एक तरल है।
विशेष रूप से ध्यान देने योग्य गैस चरण में तीव्र ताप के साथ एल्केन्स की प्रतिक्रिया है, उदाहरण के लिए, क्लोरीन के साथ।
ऐसी परिस्थितियों में, अतिरिक्त प्रतिक्रिया नहीं, बल्कि प्रतिस्थापन प्रतिक्रिया होती है। इसके अलावा, केवल अल्फा कार्बन परमाणु पर, यानी दोहरे बंधन से सटे परमाणु पर। इस स्थिति में, 3-क्लोरोप्रोपीन-1 प्राप्त होता है। परीक्षा में ये प्रतिक्रियाएँ आम नहीं हैं, इसलिए अधिकांश छात्र उन्हें याद नहीं रखते हैं और, एक नियम के रूप में, गलतियाँ करते हैं।
चौथीसंख्या हाइड्रोजनीकरण प्रतिक्रिया है, और इसके साथ निर्जलीकरण प्रतिक्रिया है। यानी हाइड्रोजन का जुड़ना या हटना।
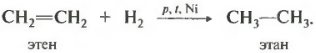
निकेल उत्प्रेरक पर हाइड्रोजनीकरण बहुत अधिक तापमान पर नहीं होता है। उच्च तापमान पर, एल्काइन बनाने के लिए डिहाइड्रोजनीकरण संभव है।
पांचवांएल्कीन का गुण पोलीमराइज़ करने की क्षमता है, जब पाई बंधन के टूटने और एक दूसरे के साथ सिग्मा बांड के निर्माण के कारण सैकड़ों और हजारों एल्कीन अणु बहुत लंबी और मजबूत श्रृंखला बनाते हैं।
इस मामले में, पॉलीथीन प्राप्त होता है। ध्यान दें कि परिणामी अणु में कोई एकाधिक बंधन नहीं हैं। ऐसे पदार्थों को पॉलिमर कहा जाता है, मूल अणुओं को मोनोमर्स कहा जाता है, दोहराए जाने वाला टुकड़ा बहुलक की प्राथमिक इकाई है, और संख्या n पोलीमराइजेशन की डिग्री है।
पॉलीप्रोपाइलीन जैसी अन्य महत्वपूर्ण पॉलिमर सामग्री के उत्पादन के लिए प्रतिक्रियाएं भी संभव हैं।
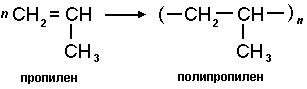

एक अन्य महत्वपूर्ण बहुलक पॉलीविनाइल क्लोराइड है।

इस पॉलिमर के उत्पादन के लिए प्रारंभिक सामग्री क्लोरोएथीन है, जिसका मामूली नाम विनाइल क्लोराइड है। चूँकि इस असंतृप्त पदार्थ को विनाइल कहा जाता है। प्लास्टिक उत्पादों के लिए एक सामान्य संक्षिप्त नाम पीवीसी का मतलब केवल पॉलीविनाइल क्लोराइड है।
हमने पाँच गुणों पर चर्चा की है जो दोहरे बंधन योगात्मक अभिक्रियाएँ हैं। अब आइये प्रतिक्रियाओं पर नजर डालते हैं. ऑक्सीकरण.
एल्कीन ऑक्सीकरण प्रतिक्रियाएं
छठाहमारी सामान्य सूची में रासायनिक गुण हल्का ऑक्सीकरण या वैगनर प्रतिक्रिया है। यह तब आगे बढ़ता है जब एल्कीन ठंड में पोटेशियम परमैंगनेट के जलीय घोल के संपर्क में आता है, इसलिए, अक्सर परीक्षा कार्यों में तापमान शून्य डिग्री होता है।
परिणाम एक डाइहाइड्रिक अल्कोहल है। इस मामले में, एथिलीन ग्लाइकॉल और सामान्य तौर पर ऐसे अल्कोहल को सामूहिक रूप से ग्लाइकोल कहा जाता है। प्रतिक्रिया के दौरान, परमैंगनेट का बैंगनी-गुलाबी घोल रंगहीन हो जाता है, इसलिए यह प्रतिक्रिया दोहरे बंधन के लिए भी गुणात्मक है। तटस्थ वातावरण में मैंगनीज +7 ऑक्सीकरण अवस्था से +4 ऑक्सीकरण अवस्था में कम हो जाता है। आइए कुछ और उदाहरण देखें. समीकरण
यहां हमें प्रोपेनेडियोल-1,2 मिलता है। हालाँकि, चक्रीय एल्केन्स उसी तरह से प्रतिक्रिया करेंगे। समीकरण
एक अन्य विकल्प तब होता है जब दोहरा बंधन, उदाहरण के लिए, सुगंधित हाइड्रोकार्बन की साइड चेन में होता है। नियमित रूप से परीक्षा कार्यों में स्टाइरीन से जुड़ी वैगनर प्रतिक्रिया होती है, इसका दूसरा नाम विनाइलबेंजीन है।
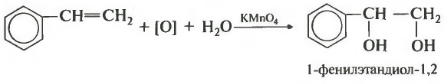
मुझे आशा है कि मैंने आपको यह समझने के लिए पर्याप्त उदाहरण प्रदान किए हैं कि दोहरे बंधन का हल्का ऑक्सीकरण हमेशा पाई बंधन को तोड़ने और प्रत्येक कार्बन परमाणु में एक हाइड्रॉक्सी समूह जोड़ने के सरल नियम का पालन करता है।
अब, कठोर ऑक्सीकरण के संबंध में। ये हमारा होगा सातवींसंपत्ति। यह ऑक्सीकरण तब होता है जब एक एल्कीन गर्म होने पर अम्लीय पोटेशियम परमैंगनेट समाधान के साथ प्रतिक्रिया करता है।
दोहरे बंधन पर अणु का विनाश होता है, अर्थात उसका विनाश होता है। ब्यूटेन-2 के मामले में, एसिटिक एसिड के दो अणु प्राप्त हुए। सामान्य तौर पर, कार्बन श्रृंखला में एकाधिक बंधन की स्थिति का अंदाजा ऑक्सीकरण उत्पादों से लगाया जा सकता है।
जब ब्यूटेन-1 का ऑक्सीकरण होता है, तो प्रोपियोनिक (प्रोपेनोइक) एसिड और कार्बन डाइऑक्साइड का एक अणु प्राप्त होता है।
एथिलीन के मामले में, कार्बन डाइऑक्साइड के दो अणु प्राप्त होंगे। सभी मामलों में, अम्लीय वातावरण में, मैंगनीज +7 ऑक्सीकरण अवस्था से +2 तक कम हो जाता है।
और अंत में आठवाँसंपत्ति पूर्ण ऑक्सीकरण या दहन.
एल्केन्स अन्य हाइड्रोकार्बन की तरह जलकर कार्बन डाइऑक्साइड और पानी में बदल जाते हैं। आइए हम एल्कीन के दहन के समीकरण को सामान्य रूप में लिखें।
वहाँ उतने ही कार्बन डाइऑक्साइड अणु होंगे जितने एक एल्कीन अणु में कार्बन परमाणु होते हैं, क्योंकि CO 2 अणु में एक कार्बन परमाणु होता है। वह n CO 2 अणु है। पानी के अणु हाइड्रोजन परमाणुओं से आधे होंगे, यानी 2n/2, यानी सिर्फ n।
बायीं और दायीं ओर ऑक्सीजन परमाणुओं की संख्या समान है। दाईं ओर, कार्बन डाइऑक्साइड से 2n प्लस पानी से n, कुल मिलाकर 3n है। बाईं ओर, ऑक्सीजन परमाणुओं की समान संख्या है, जिसका अर्थ है कि आधे अणु हैं, क्योंकि दो परमाणु अणु का हिस्सा हैं। वह 3n/2 ऑक्सीजन अणु है। आप 1.5n लिख सकते हैं.
हमने समीक्षा की है आठएल्केन्स के रासायनिक गुण।
सबसे सरल कार्बनिक यौगिक संतृप्त और असंतृप्त हाइड्रोकार्बन हैं। इनमें एल्केन्स, एल्केनीज़, एल्केनीज़ वर्ग के पदार्थ शामिल हैं।
उनके सूत्रों में एक निश्चित क्रम और मात्रा में हाइड्रोजन और कार्बन परमाणु शामिल होते हैं। ये अक्सर प्रकृति में पाए जाते हैं।
एल्केन्स की परिभाषा
इनका दूसरा नाम ओलेफिन या एथिलीन हाइड्रोकार्बन है। 18वीं शताब्दी में यौगिकों के इस वर्ग को यही कहा जाता था जब एक तैलीय तरल, एथिलीन क्लोराइड की खोज की गई थी।
एल्कीन हाइड्रोजन और कार्बन तत्वों से बने पदार्थ हैं। वे एसाइक्लिक हाइड्रोकार्बन से संबंधित हैं। उनके अणु में दो कार्बन परमाणुओं को एक दूसरे से जोड़ने वाला एक एकल दोहरा (असंतृप्त) बंधन होता है।
अल्कीन सूत्र
यौगिकों के प्रत्येक वर्ग का अपना रासायनिक पदनाम होता है। उनमें, आवधिक प्रणाली के तत्वों के प्रतीक प्रत्येक पदार्थ के बंधनों की संरचना और संरचना को दर्शाते हैं।

एल्केन्स का सामान्य सूत्र निम्नानुसार दर्शाया गया है: सी एन एच 2 एन, जहां संख्या एन 2 से अधिक या उसके बराबर है। इसे समझने पर, यह देखा जा सकता है कि प्रत्येक कार्बन परमाणु के लिए दो हाइड्रोजन परमाणु हैं।
सजातीय श्रृंखला के एल्कीनों के आणविक सूत्र निम्नलिखित संरचनाओं द्वारा दर्शाए गए हैं: सी 2 एच 4, सी 3 एच 6, सी 4 एच 8, सी 5 एच 10, सी 6 एच 12, सी 7 एच 14, सी 8 एच 16 , सी 9 एच 18, सी 10 एच 20। यह देखा जा सकता है कि प्रत्येक अगले हाइड्रोकार्बन में एक अधिक कार्बन और 2 अधिक हाइड्रोजन होते हैं।
एक अणु में परमाणुओं के बीच रासायनिक यौगिकों के स्थान और क्रम का एक ग्राफिक पदनाम है, जो एल्केन्स के संरचनात्मक सूत्र को दर्शाता है। वैलेंस लाइनों की मदद से, हाइड्रोजन के साथ कार्बन के बंधन को दर्शाया गया है।
एल्कीन के संरचनात्मक सूत्र को विस्तारित रूप में दिखाया जा सकता है, जब सभी रासायनिक तत्व और बंधन दिखाए जाते हैं। ओलेफ़िन की अधिक संक्षिप्त अभिव्यक्ति के साथ, संयोजकता रेखाओं की सहायता से कार्बन और हाइड्रोजन का संयोजन नहीं दिखाया गया है।
कंकाल सूत्र सबसे सरल संरचना को दर्शाता है। एक टूटी हुई रेखा अणु के आधार को दर्शाती है, जिसमें कार्बन परमाणुओं को उसके शीर्ष और सिरों द्वारा दर्शाया जाता है, और हाइड्रोजन को लिंक द्वारा दर्शाया जाता है।
ओलेफ़िन नाम कैसे बनते हैं
सीएच 3 -एचसी = सीएच 2 + एच 2 ओ → सीएच 3 -ओएचसीएच-सीएच 3।
सल्फ्यूरिक एसिड के साथ एल्केन्स के संपर्क में आने पर, सल्फोनेशन की प्रक्रिया होती है:
सीएच 3-एचसी = सीएच 2 + एचओ-ओएसओ-ओएच → सीएच 3-सीएच 3 सीएच-ओ-एसओ 2-ओएच।
प्रतिक्रिया एसिड एस्टर के निर्माण के साथ आगे बढ़ती है, उदाहरण के लिए, आइसोप्रोपिलसल्फ्यूरिक एसिड।
पानी और कार्बन डाइऑक्साइड गैस बनाने के लिए ऑक्सीजन की क्रिया के तहत दहन के दौरान अल्केन्स ऑक्सीकरण के अधीन होते हैं:
2CH 3 -HC \u003d CH 2 + 9O 2 → 6CO 2 + 6H 2 O।
घोल के रूप में ओलेफिनिक यौगिकों और तनु पोटेशियम परमैंगनेट की परस्पर क्रिया से ग्लाइकोल या डाइहाइड्रिक अल्कोहल का निर्माण होता है। यह प्रतिक्रिया एथिलीन ग्लाइकॉल के निर्माण और घोल के मलिनकिरण के साथ ऑक्सीडेटिव भी होती है:
3H 2 C = CH 2 + 4H 2 O + 2KMnO 4 → 3OHCH-CHOH + 2MnO 2 + 2KOH।
एल्कीन अणु एक मुक्त रेडिकल या धनायन-आयन तंत्र के साथ पोलीमराइजेशन प्रक्रिया में शामिल हो सकते हैं। पहले मामले में, पेरोक्साइड के प्रभाव में, पॉलीथीन जैसा बहुलक प्राप्त होता है।
दूसरे तंत्र के अनुसार, एसिड धनायनित उत्प्रेरक के रूप में कार्य करते हैं, और ऑर्गेनोमेटैलिक पदार्थ एक स्टीरियोसेलेक्टिव पॉलिमर की रिहाई के साथ आयनिक उत्प्रेरक होते हैं।
अल्केन्स क्या हैं
इन्हें पैराफिन या संतृप्त एसाइक्लिक हाइड्रोकार्बन भी कहा जाता है। उनके पास एक रैखिक या शाखित संरचना होती है, जिसमें केवल संतृप्त सरल बंधन होते हैं। इस वर्ग के सभी प्रतिनिधियों का सामान्य सूत्र C n H 2n+2 है।

इनमें केवल कार्बन और हाइड्रोजन परमाणु होते हैं। एल्केन्स का सामान्य सूत्र संतृप्त हाइड्रोकार्बन के पदनाम से बनता है।
अल्केन्स के नाम और उनकी विशेषताएँ
इस वर्ग का सबसे सरल प्रतिनिधि मीथेन है। इसके बाद ईथेन, प्रोपेन और ब्यूटेन जैसे पदार्थ आते हैं। उनका नाम ग्रीक में अंक की जड़ पर आधारित है, जिसमें प्रत्यय -an जोड़ा जाता है। अल्केन्स के नाम IUPAC नामकरण में सूचीबद्ध हैं।
एल्कीन, एल्कीन, एल्केन के सामान्य सूत्र में केवल दो प्रकार के परमाणु शामिल होते हैं। इनमें कार्बन और हाइड्रोजन तत्व शामिल हैं। तीनों वर्गों में कार्बन परमाणुओं की संख्या समान है, अंतर केवल हाइड्रोजन की संख्या में देखा जाता है, जिसे विभाजित या जोड़ा जा सकता है। से असंतृप्त यौगिक प्राप्त होते हैं। अणु में पैराफिन के प्रतिनिधियों में ओलेफिन की तुलना में 2 अधिक हाइड्रोजन परमाणु होते हैं, जिसकी पुष्टि अल्केन्स, अल्केन्स के सामान्य सूत्र से होती है। दोहरे बंधन की उपस्थिति के कारण एल्कीन संरचना को असंतृप्त माना जाता है।
यदि हम अल-का-ना में पानी-से-रो-डेनी और कार्बन-ले-रो-डेनी परमाणुओं की संख्या को सहसंबंधित करते हैं, तो कोयला-ले-वो के अन्य वर्गों की तुलना में मूल्य अधिकतम-सी-छोटा होगा। -टू -रो-डोव.
मीथेन से शुरू होकर ब्यूटेन (सी 1 से सी 4 तक) तक, पदार्थ गैसीय रूप में मौजूद होते हैं।
तरल रूप में, C 5 से C 16 तक समजात अंतराल के हाइड्रोकार्बन प्रस्तुत किए जाते हैं। एक अल्केन से शुरू होकर, जिसकी मुख्य श्रृंखला में 17 कार्बन परमाणु होते हैं, भौतिक अवस्था का एक ठोस रूप में संक्रमण होता है।
उन्हें कार्बन कंकाल में आइसोमेरिज्म और अणु के ऑप्टिकल संशोधनों की विशेषता है।

पैराफिन में, कार्बन वैलेंस को σ-प्रकार के बंधन के गठन के साथ पड़ोसी कार्बन-ले-रो-दा-मील या इन-डू-रो-दा-मील द्वारा पूरी तरह से व्याप्त माना जाता है। रासायनिक दृष्टिकोण से, यह उनके कमजोर गुणों का कारण बनता है, यही कारण है कि अल्केन्स को प्री-डेल-नी-एक्स या संतृप्त-शेन-नी-एक्स कोयला-ले-टू-डू-रो-डोव कहा जाता है, जो आत्मीयता से रहित है।
वे रेडिकल हैलोजनेशन, सल्फोक्लोरिनेशन या अणु के नाइट्रेशन से जुड़ी प्रतिस्थापन प्रतिक्रियाओं में प्रवेश करते हैं।
पैराफिन उच्च तापमान पर ऑक्सीकरण, दहन या अपघटन की प्रक्रिया से गुजरते हैं। प्रतिक्रिया त्वरक की क्रिया के तहत, हाइड्रोजन परमाणुओं का उन्मूलन या अल्केन्स का डिहाइड्रोजनीकरण होता है।
एल्केनीज़ क्या हैं
इन्हें एसिटाइलेनिक हाइड्रोकार्बन भी कहा जाता है, जिनमें कार्बन श्रृंखला में ट्रिपल बॉन्ड होता है। एल्केनीज़ की संरचना का वर्णन सामान्य सूत्र C n H 2 n-2 द्वारा किया गया है। इससे पता चलता है कि, अल्केन्स के विपरीत, एसिटाइलेनिक हाइड्रोकार्बन में चार हाइड्रोजन परमाणुओं की कमी होती है। उन्हें दो π-यौगिकों द्वारा गठित ट्रिपल बॉन्ड द्वारा प्रतिस्थापित किया जाता है।
यह संरचना इस वर्ग के रासायनिक गुणों को निर्धारित करती है। एल्कीन और एल्काइन का संरचनात्मक सूत्र स्पष्ट रूप से उनके अणुओं की असंतृप्ति, साथ ही एक डबल (H 2 C꞊CH 2) और ट्रिपल (HC≡CH) बंधन की उपस्थिति को दर्शाता है।
एल्काइनों के नाम और उनकी विशेषताएँ
सबसे सरल प्रतिनिधि एसिटिलीन या HC≡CH है। इसे एथिन भी कहा जाता है. यह एक संतृप्त हाइड्रोकार्बन के नाम से आता है, जिसमें प्रत्यय -an को हटा दिया जाता है और -in जोड़ा जाता है। लंबे एल्काइनों के नाम में, संख्या त्रिबंध के स्थान को दर्शाती है।
संतृप्त और असंतृप्त हाइड्रोकार्बन की संरचना को जानकर, यह निर्धारित करना संभव है कि एल्केनीज़ का सामान्य सूत्र किस अक्षर के अंतर्गत दर्शाया गया है: ए) सीएनएच2एन; ग) CnH2n+2; ग) CnH2n-2; घ) CnH2n-6। सही उत्तर तीसरा विकल्प है।
एसिटिलीन से शुरू होकर ब्यूटेन (सी 2 से सी 4 तक) तक, पदार्थ प्रकृति में गैसीय होते हैं।

तरल रूप में C5 से C17 तक समजातीय अंतराल के हाइड्रोकार्बन होते हैं। एल्काइन से शुरू होकर, जिसकी मुख्य श्रृंखला में 18 कार्बन परमाणु होते हैं, भौतिक अवस्था का ठोस रूप में संक्रमण होता है।
वे कार्बन कंकाल में आइसोमेरिज्म, ट्रिपल बॉन्ड की स्थिति के साथ-साथ अणु के इंटरक्लास संशोधनों की विशेषता रखते हैं।
एसिटिलीन हाइड्रोकार्बन रासायनिक रूप से एल्कीन के समान होते हैं।
यदि एल्काइनों में एक टर्मिनल ट्रिपल बॉन्ड होता है, तो वे एल्केनाइड लवण के निर्माण के साथ एक एसिड के रूप में कार्य करते हैं, उदाहरण के लिए, NaC≡CNa। दो π-बंधों की उपस्थिति सोडियम एसिटिल्डिन अणु को एक मजबूत न्यूक्लियोफाइल बनाती है जो प्रतिस्थापन प्रतिक्रियाओं में प्रवेश करती है।
डाइक्लोरोएसिटिलीन प्राप्त करने के लिए एसिटिलीन कॉपर क्लोराइड की उपस्थिति में क्लोरीनीकरण से गुजरता है, डायएसिटिलीन अणुओं की रिहाई के साथ हेलोअल्काइन की क्रिया के तहत संघनन होता है।
एल्काइन उन प्रतिक्रियाओं में शामिल होते हैं जिनका सिद्धांत हैलोजनेशन, हाइड्रोहैलोजनेशन, हाइड्रेशन और कार्बोनिलेशन पर आधारित है। हालाँकि, ऐसी प्रक्रियाएँ दोहरे बंधन वाले एल्केन्स की तुलना में अधिक कमजोर रूप से आगे बढ़ती हैं।
एसिटाइलेनिक हाइड्रोकार्बन के लिए, अल्कोहल अणु, प्राथमिक अमीन या हाइड्रोजन सल्फाइड के न्यूक्लियोफिलिक प्रकार की अतिरिक्त प्रतिक्रियाएं संभव हैं।
निरंतरता. शुरुआत के लिए देखें № 15, 16, 17, 18, 19/2004
पाठ 9
ऐल्कीनों के रासायनिक गुण
एल्केन्स (एथिलीन और उसके समजात) के रासायनिक गुण काफी हद तक उनके अणुओं में डी ... बांड की उपस्थिति से निर्धारित होते हैं। एल्केन्स तीनों प्रकार की प्रतिक्रियाओं में प्रवेश करते हैं, और उनमें से सबसे विशिष्ट प्रतिक्रियाएं पी हैं .... उदाहरण के तौर पर प्रोपलीन सी 3 एच 6 का उपयोग करके उन पर विचार करें।
सभी अतिरिक्त प्रतिक्रियाएं एक दोहरे बंधन के माध्यम से आगे बढ़ती हैं और इसमें एल्कीन के α-बंध का विभाजन होता है और टूटने के स्थान पर दो नए α-बंधों का निर्माण होता है।
हैलोजन का योग:

हाइड्रोजन का योग(हाइड्रोजनीकरण प्रतिक्रिया):
जल कनेक्शन(जलयोजन प्रतिक्रिया):

हाइड्रोजन हैलाइड्स (HHal) और पानी का योगअसममित ऐल्कीनों के लिए वी.वी. मार्कोवनिकोव के नियम के अनुसार (1869). हाइड्रोजन अम्लहहल दोहरे बंधन पर सबसे अधिक हाइड्रोजनीकृत कार्बन परमाणु से जुड़ जाता है।तदनुसार, हैल अवशेष सी परमाणु से बंधता है, जिसमें हाइड्रोजन परमाणुओं की संख्या कम होती है।

वायु में ऐल्कीनों का दहन।
प्रज्वलित होने पर, एल्केन्स हवा में जलते हैं:
2CH 2 = CHCH 3 + 9O 2 6CO 2 + 6H 2 O।
गैसीय एल्कीन वायुमंडलीय ऑक्सीजन के साथ विस्फोटक मिश्रण बनाते हैं।
जलीय माध्यम में पोटेशियम परमैंगनेट द्वारा एल्केन्स का ऑक्सीकरण होता है, जो KMnO 4 समाधान के मलिनकिरण और ग्लाइकोल (आसन्न सी परमाणुओं पर दो हाइड्रॉक्सिल समूहों के साथ यौगिक) के गठन के साथ होता है। यह प्रोसेस - ऐल्कीनों का हाइड्रॉक्सिलेशन:

एल्केन्स को वायुमंडलीय ऑक्सीजन द्वारा एपॉक्साइड में ऑक्सीकृत किया जाता है।चांदी उत्प्रेरक की उपस्थिति में गर्म करने पर:

ऐल्कीनों का पॉलिमराइजेशन- अनेक ऐल्कीन अणुओं का एक दूसरे से जुड़ना। प्रतिक्रिया की स्थिति: ताप, उत्प्रेरक की उपस्थिति। अणुओं का कनेक्शन इंट्रामोल्युलर-बंधों को विभाजित करने और नए अंतर-आणविक-बंधों के निर्माण से होता है:

इस प्रतिक्रिया में, मूल्यों की सीमा एन = 10 3 –10 4 .
व्यायाम.
1. ब्यूटेन-1 के लिए प्रतिक्रिया समीकरण लिखें: a) Br2; बी)एचबीआर; वी) H2O; जी)एच2. प्रतिक्रिया उत्पादों का नाम बताइए।
2.
ऐसी स्थितियाँ ज्ञात हैं जिनके तहत एल्केन्स के दोहरे बंधन में पानी और हाइड्रोजन हैलाइड का योग मार्कोवनिकोव नियम के विरुद्ध होता है। प्रतिक्रिया समीकरण लिखें
3-ब्रोमोप्रोपाइलीन एंटी-मार्कोवनिकोव के अनुसार: ए) पानी; बी) हाइड्रोजन ब्रोमाइड।
3.
पोलीमराइज़ेशन प्रतिक्रियाओं के लिए समीकरण लिखें: ए) ब्यूटेन-1; बी) विनाइल क्लोराइडसीएच 2 =सीएचसीएल;
ग) 1,2-डिफ्लुओरोएथिलीन।
4. निम्नलिखित प्रक्रियाओं के लिए एथिलीन की ऑक्सीजन के साथ प्रतिक्रियाओं के लिए समीकरण बनाएं: ए) हवा में दहन; बी) पानी के साथ हाइड्रॉक्सिलेशनकेएमएनओ4 ; ग) एपॉक्सीडेशन (250 डिग्री सेल्सियस,एजी ).
5. यह जानते हुए कि इस यौगिक के 0.21 ग्राम में 0.8 ग्राम ब्रोमीन मिलाया जा सकता है, एक एल्कीन का संरचनात्मक सूत्र लिखें।
6. 1 लीटर गैसीय हाइड्रोकार्बन जलाने पर, जो पोटेशियम परमैंगनेट के रास्पबेरी घोल को ख़राब कर देता है, 4.5 लीटर ऑक्सीजन की खपत होती है, और 3 लीटर प्राप्त होता है CO2. इस हाइड्रोकार्बन का संरचनात्मक सूत्र लिखिए।
पाठ 10
एल्केन्स प्राप्त करना और उनका उपयोग करना
एल्कीन प्राप्त करने के लिए प्रतिक्रियाओं को एल्कीन के रासायनिक गुणों का प्रतिनिधित्व करने वाली प्रतिक्रियाओं को उलटने तक कम कर दिया जाता है (उनका प्रवाह दाएं से बाएं, पाठ 9 देखें)। आपको बस सही परिस्थितियां ढूंढने की जरूरत है।
डायहैलोऐल्केन से दो हैलोजन परमाणुओं का विलोपनपड़ोसी C परमाणुओं में हैलोजन युक्त। प्रतिक्रिया धातुओं (Zn, आदि) की क्रिया के तहत आगे बढ़ती है:

संतृप्त हाइड्रोकार्बन का टूटना। तो, ईथेन के टूटने (पाठ 7 देखें) के दौरान, एथिलीन और हाइड्रोजन का मिश्रण बनता है:
अल्कोहल का निर्जलीकरण. जब अल्कोहल को पानी हटाने वाले एजेंटों (सांद्रित सल्फ्यूरिक एसिड) से उपचारित किया जाता है या उत्प्रेरक की उपस्थिति में 350 डिग्री सेल्सियस तक गर्म किया जाता है, तो पानी अलग हो जाता है और एल्कीन बनते हैं:
इस प्रकार प्रयोगशाला में एथिलीन प्राप्त किया जाता है।
प्रोपलीन के उत्पादन के लिए एक औद्योगिक विधि, क्रैकिंग के साथ, एल्यूमिना पर प्रोपेनॉल का निर्जलीकरण है:

अल्कोहल में क्षार घोल की क्रिया के तहत क्लोरोऐल्केन का डीहाइड्रोक्लोरिनेशन किया जाता है, क्योंकि पानी में, प्रतिक्रिया उत्पाद एल्केन्स नहीं, बल्कि अल्कोहल होते हैं।
एथिलीन और उसके समरूपों का उपयोगउनके रासायनिक गुणों के आधार पर, यानी, विभिन्न उपयोगी पदार्थों में बदलने की क्षमता।
मोटर ईंधन, उच्च ऑक्टेन संख्या के साथ, शाखित एल्कीन के हाइड्रोजनीकरण द्वारा प्राप्त किए जाते हैं:

एक अक्रिय विलायक (सीसीएल 4) में ब्रोमीन के पीले घोल का मलिनकिरण तब होता है जब एल्कीन की एक बूंद डाली जाती है या समाधान के माध्यम से एक गैसीय एल्कीन प्रवाहित किया जाता है। ब्रोमीन के साथ अंतःक्रिया - विशेषता दोहरे बंधन पर गुणात्मक प्रतिक्रिया:
एथिलीन हाइड्रोक्लोरिनेशन के उत्पाद क्लोरोइथेन का उपयोग किया जाता है रासायनिक संश्लेषणअणु में C 2 H 5 समूह का परिचय कराने के लिए:
क्लोरोइथेन में स्थानीय एनेस्थेटिक (दर्द निवारक) प्रभाव भी होता है, जिसका उपयोग सर्जिकल ऑपरेशन में किया जाता है।
ऐल्कीनों के जलयोजन से ऐल्कोहॉल प्राप्त होता है, उदाहरण के लिए, इथेनॉल:
अल्कोहल सी 2 एच 5 ओएच का उपयोग नए पदार्थों के संश्लेषण में, कीटाणुशोधन के लिए विलायक के रूप में किया जाता है।

ऑक्सीकरण एजेंट [O] की उपस्थिति में एथिलीन के जलयोजन से एथिलीन ग्लाइकॉल बनता है - एंटीफ्ऱीज़र और रासायनिक संश्लेषण का मध्यवर्ती उत्पाद:

एथिलीन का ऑक्सीकरण एथिलीन ऑक्साइड और एसीटैल्डिहाइड बनाने के लिए किया जाता है। रासायनिक उद्योग में कच्चा माल:
![]()
पॉलिमर और प्लास्टिक- एल्केन्स के पोलीमराइजेशन के उत्पाद, उदाहरण के लिए, पॉलीटेट्राफ्लुओरोएथिलीन (टेफ्लॉन):
व्यायाम.
1. उन्मूलन (विभाजन) की प्रतिक्रियाओं के लिए समीकरण पूरा करें, परिणामी ऐल्कीनों को नाम दें:
2.
हाइड्रोजनीकरण प्रतिक्रियाओं के लिए समीकरण बनाएं: ए) 3,3-डाइमिथाइलब्यूटीन-1;
बी) 2,3,3-ट्राइमेथिलब्यूटीन-1। इन प्रतिक्रियाओं से मोटर ईंधन के रूप में उपयोग किए जाने वाले अल्केन्स उत्पन्न होते हैं, उन्हें नाम दें।
3. गर्म एल्यूमिना से भरी एक ट्यूब के माध्यम से 100 ग्राम एथिल अल्कोहल प्रवाहित किया गया।सी 2 एच 5 ओएच। इसके परिणामस्वरूप 33.6 लीटर हाइड्रोकार्बन (n.o.s.) प्राप्त हुआ। कितनी शराब (% में) ने प्रतिक्रिया की?
4. 2.8 लीटर एथिलीन के साथ कितने ग्राम ब्रोमीन प्रतिक्रिया करेगा?
5. ट्राइफ्लोरोक्लोरोएथिलीन के पोलीमराइजेशन के लिए एक समीकरण लिखें। (परिणामस्वरूप प्लास्टिक गर्म सल्फ्यूरिक एसिड, धात्विक सोडियम, आदि के प्रति प्रतिरोधी है)
विषय 1 के अभ्यास के उत्तर
पाठ 9


5. एल्कीन सी की प्रतिक्रिया एनएच 2 एनसामान्यतः ब्रोमीन के साथ:
![]()
एल्कीन का दाढ़ द्रव्यमान एम(साथ एनएच 2 एन) = 0.21 160/0.8 = 42 ग्राम/मोल।
यह प्रोपलीन है.
उत्तर.
एल्कीन सूत्र सीएच 2 \u003d सीएचसीएच 3 (प्रोपलीन) है।
6. चूँकि प्रतिक्रिया में शामिल सभी पदार्थ गैसें हैं, प्रतिक्रिया समीकरण में स्टोइकोमेट्रिक गुणांक उनके आयतन अनुपात के समानुपाती होते हैं। आइए प्रतिक्रिया समीकरण लिखें:
साथ एएच वी+ 4.5O 2 3CO 2 + 3H 2 O.
पानी के अणुओं की संख्या प्रतिक्रिया समीकरण द्वारा निर्धारित की जाती है: 4.5 2 = 9 ओ परमाणुओं ने प्रतिक्रिया की, 6 ओ परमाणु सीओ 2 में बंधे हैं, शेष 3 ओ परमाणु तीन एच 2 ओ अणुओं का हिस्सा हैं। इसलिए, सूचकांक बराबर हैं: ए = 3, वी\u003d 6. वांछित हाइड्रोकार्बन प्रोपलीन सी 3 एच 6 है।
उत्तर.
प्रोपलीन का संरचनात्मक सूत्र CH 2 = CHCH 3 है।
पाठ 10
1. उन्मूलन (विभाजन) प्रतिक्रिया समीकरण - एल्कीन का संश्लेषण:

2. उत्प्रेरक की उपस्थिति में दबाव में गर्म करने पर एल्कीन की हाइड्रोजनीकरण प्रतिक्रियाएं:

3. एथिल अल्कोहल के निर्जलीकरण की प्रतिक्रिया का रूप है:
![]()
यहाँ के माध्यम से एक्सएथिलीन में परिवर्तित अल्कोहल का द्रव्यमान दर्शाया गया है।
आइए मूल्य ज्ञात करें एक्स: एक्स= 46 33.6 / 22.4 = 69 ग्राम।
प्रतिक्रियाशील अल्कोहल का अनुपात था: 69/100 = 0.69, या 69%।
उत्तर.
69% अल्कोहल ने प्रतिक्रिया की।
4.
![]()
चूंकि अभिकारकों (सी 2 एच 4 और बीआर 2) के सूत्रों के सामने स्टोइकोमेट्रिक गुणांक एक के बराबर हैं, संबंध मान्य है:
2,8/22,4 = एक्स/160. यहाँ से एक्स= 20 ग्राम बीआर 2.
उत्तर.
20 ग्राम Br 2.
एल्कीन एक या अधिक कार्बन-कार्बन दोहरे बंधन वाले असंतृप्त एलिफैटिक हाइड्रोकार्बन हैं। एक दोहरा बंधन दो कार्बन परमाणुओं को 120 डिग्री सेल्सियस के आसन्न बंधनों के बीच बंधन कोण के साथ एक समतल संरचना में बदल देता है:
एल्केन्स की सजातीय श्रृंखला का सामान्य सूत्र है; इसके पहले दो सदस्य एथीन (एथिलीन) और प्रोपेन (प्रोपलीन) हैं:

चार या अधिक कार्बन परमाणुओं वाले एल्कीन श्रृंखला के सदस्य बंधन स्थिति समावयवता प्रदर्शित करते हैं। उदाहरण के लिए, सूत्र वाले एक एल्केन में तीन आइसोमर्स होते हैं, जिनमें से दो बॉन्ड स्थिति आइसोमर्स होते हैं:
ध्यान दें कि एल्कीन श्रृंखला की नंबरिंग उसके उस सिरे से की जाती है, जो दोहरे बंधन के करीब है। एक दोहरे बंधन की स्थिति को दो संख्याओं में से छोटी संख्या से दर्शाया जाता है, जो एक दोहरे बंधन द्वारा एक साथ जुड़े दो कार्बन परमाणुओं के अनुरूप होती है। तीसरे आइसोमर में एक शाखित संरचना होती है:

किसी भी एल्कीन के आइसोमर्स की संख्या कार्बन परमाणुओं की संख्या के साथ बढ़ती है। उदाहरण के लिए, हेक्सेन में तीन बंधन स्थिति आइसोमर्स हैं:
डायन बूटा-1,3-डायन है, या सिर्फ ब्यूटाडीन है:
तीन दोहरे बंधन वाले यौगिकों को ट्राइएन्स कहा जाता है। एकाधिक दोहरे बंधन वाले यौगिकों को सामूहिक रूप से पॉलीएन्स कहा जाता है।
भौतिक गुण
ऐल्केनों का गलनांक और क्वथनांक उनके संगत ऐल्केनों की तुलना में थोड़ा कम होता है। उदाहरण के लिए, पेंटेन का क्वथनांक होता है। एथिलीन, प्रोपेन और ब्यूटेन के तीन आइसोमर्स कमरे के तापमान और सामान्य दबाव पर गैसीय अवस्था में होते हैं। 5 से 15 तक कार्बन परमाणुओं की संख्या वाले एल्कीन सामान्य परिस्थितियों में तरल अवस्था में होते हैं। उनकी अस्थिरता, अल्केन्स की तरह, कार्बन श्रृंखला में शाखाओं की उपस्थिति में बढ़ जाती है। 15 से अधिक कार्बन परमाणुओं वाले एल्कीन सामान्य परिस्थितियों में ठोस होते हैं।
प्रयोगशाला में प्राप्त करना
प्रयोगशाला में एल्कीन प्राप्त करने की दो मुख्य विधियाँ हैं अल्कोहल का निर्जलीकरण और हैलोऐल्केन का निर्जलीकरण। उदाहरण के लिए, 170 डिग्री सेल्सियस के तापमान पर सांद्र सल्फ्यूरिक एसिड की अधिकता की क्रिया के तहत इथेनॉल को निर्जलित करके एथिलीन प्राप्त किया जा सकता है (धारा 19.2 देखें):
गर्म एल्यूमिना की सतह पर इथेनॉल वाष्प प्रवाहित करके इथेनॉल से एथिलीन भी प्राप्त किया जा सकता है। इस प्रयोजन के लिए, सेटअप चित्र में योजनाबद्ध रूप से दिखाया गया है। 18.3.
एल्कीन प्राप्त करने की दूसरी सामान्य विधि बुनियादी उत्प्रेरण की शर्तों के तहत हेलोअल्केन्स के डीहाइड्रोहैलोजनेशन पर आधारित है।
इस प्रकार की उन्मूलन प्रतिक्रिया का तंत्र अनुभाग में वर्णित है। 17.3.
ऐल्कीनों की प्रतिक्रियाएँ
एल्केन्स, अल्केन्स की तुलना में बहुत अधिक प्रतिक्रियाशील होते हैं। यह इलेक्ट्रोफाइल को आकर्षित करने के लिए डबल बॉन्ड इलेक्ट्रॉनों की क्षमता के कारण है (धारा 17.3 देखें)। इसलिए, एल्केन्स की विशिष्ट प्रतिक्रियाएं मुख्य रूप से दोहरे बंधन में इलेक्ट्रोफिलिक जोड़ की प्रतिक्रियाएं हैं:

इनमें से कई प्रतिक्रियाओं में आयनिक तंत्र होते हैं (धारा 17.3 देखें)।
हाइड्रोजनीकरण
यदि किसी एल्कीन, जैसे एथिलीन, को हाइड्रोजन के साथ मिलाया जाता है और इस मिश्रण को कमरे के तापमान पर प्लैटिनम उत्प्रेरक या लगभग 150 डिग्री सेल्सियस के तापमान पर निकल उत्प्रेरक की सतह पर पारित किया जाता है, तो जोड़ घटित होगा
एल्केन के दोहरे बंधन पर हाइड्रोजन। इस स्थिति में, संबंधित अल्केन बनता है:

इस प्रकार की प्रतिक्रिया विषमांगी उत्प्रेरण का एक उदाहरण है। इसका तंत्र सेकंड में वर्णित है। 9.2 और चित्र में योजनाबद्ध रूप से दिखाया गया है। 9.20.
हैलोजन का जोड़
एल्कीन के दोहरे बंधन में क्लोरीन या ब्रोमीन आसानी से मिलाया जाता है; यह प्रतिक्रिया कार्बन टेट्राक्लोराइड या हेक्सेन जैसे गैर-ध्रुवीय सॉल्वैंट्स में होती है। प्रतिक्रिया आयनिक तंत्र के अनुसार आगे बढ़ती है, जिसमें कार्बोकेशन का निर्माण शामिल है। दोहरा बंधन हैलोजन अणु को ध्रुवीकृत करता है, इसे द्विध्रुव में बदल देता है:

इसलिए, हेक्सेन या टेट्राक्लोरोमेथेन में ब्रोमीन का घोल एल्कीन से हिलाने पर रंगहीन हो जाता है। यदि आप एल्कीन को ब्रोमीन जल के साथ हिलाते हैं तो भी यही होता है। ब्रोमीन जल, पानी में ब्रोमीन का एक घोल है। इस घोल में हाइपोब्रोमस एसिड होता है। हाइपोक्लोरस एसिड अणु एल्कीन के दोहरे बंधन से जुड़ा होता है, और परिणामस्वरूप, ब्रोमो-प्रतिस्थापित अल्कोहल बनता है। उदाहरण के लिए

हाइड्रोजन हैलाइडों का योग
इस प्रकार की प्रतिक्रिया का तंत्र अनुभाग में वर्णित है। 18.3. उदाहरण के तौर पर, प्रोपेन में हाइड्रोजन क्लोराइड मिलाने पर विचार करें:
ध्यान दें कि इस प्रतिक्रिया का उत्पाद 2-क्लोरोप्रोपेन है, 1-क्लोरो-प्रोपेन नहीं:
![]()
ऐसी अतिरिक्त प्रतिक्रियाओं में, सबसे अधिक विद्युत ऋणात्मक परमाणु या सबसे अधिक विद्युत ऋणात्मक समूह को हमेशा कार्बन परमाणु से जोड़ा जाता है
हाइड्रोजन परमाणुओं की सबसे छोटी संख्या. इस नियमितता को मार्कोवनिकोव का नियम कहा जाता है।
सबसे कम हाइड्रोजन परमाणुओं से जुड़े कार्बन परमाणु में एक इलेक्ट्रोनगेटिव परमाणु या समूह का पसंदीदा जोड़ कार्बोकेशन की स्थिरता में वृद्धि के कारण होता है क्योंकि कार्बन परमाणु पर एल्काइल प्रतिस्थापन की संख्या बढ़ जाती है। स्थिरता में यह वृद्धि, बदले में, एल्काइल समूहों में होने वाले आगमनात्मक प्रभाव द्वारा समझाया गया है, क्योंकि वे इलेक्ट्रॉन दाता हैं:

किसी भी कार्बनिक पेरोक्साइड की उपस्थिति में, प्रोपेन हाइड्रोजन ब्रोमाइड के साथ प्रतिक्रिया करता है, बनाता है, यानी, मार्कोवनिकोव के नियम के अनुसार नहीं। ऐसे उत्पाद को एंटी-मार्कोवनिकोव कहा जाता है। यह आयनिक तंत्र के बजाय रेडिकल के अनुसार आगे बढ़ने वाली प्रतिक्रिया के परिणामस्वरूप बनता है।
हाइड्रेशन
एल्केन्स ठंडे सांद्र सल्फ्यूरिक एसिड के साथ प्रतिक्रिया करके एल्काइल हाइड्रोजन सल्फेट बनाते हैं। उदाहरण के लिए

यह प्रतिक्रिया एक अतिरिक्त है क्योंकि यह दोहरे बंधन में एक एसिड जोड़ती है। एथिलीन के निर्माण के साथ इथेनॉल के निर्जलीकरण के संबंध में यह विपरीत प्रतिक्रिया है। इस प्रतिक्रिया का तंत्र दोहरे बंधन में हाइड्रोजन हैलाइडों को जोड़ने के तंत्र के समान है। इसमें एक मध्यवर्ती कार्बोकेशन का निर्माण शामिल है। यदि इस प्रतिक्रिया के उत्पाद को पानी से पतला किया जाता है और धीरे से गर्म किया जाता है, तो यह इथेनॉल बनाने के लिए हाइड्रोलाइज हो जाता है:
अल्केन्स में सल्फ्यूरिक एसिड की अतिरिक्त प्रतिक्रिया मार्कोवनिकोव नियम का पालन करती है:

पोटेशियम परमैंगनेट के अम्लीय घोल के साथ प्रतिक्रिया
पोटेशियम परमैंगनेट के अम्लीय घोल का बैंगनी रंग गायब हो जाता है यदि इस घोल को एल्कीन के साथ मिश्रण में हिलाया जाता है। एल्कीन का हाइड्रॉक्सिलेशन होता है (इसमें एक हाइड्रॉक्सी समूह का परिचय, जो ऑक्सीकरण के कारण बनता है), जिसके परिणामस्वरूप, एक डायोल में बदल जाता है। उदाहरण के लिए, जब एथिलीन की अधिक मात्रा को अम्लीय घोल में मिलाया जाता है, तो इथेन-1,2-डायोल (एथिलीन ग्लाइकॉल) बनता है।

यदि एल्कीन को -आयन विलयन की अधिकता से हिलाया जाता है, तो एल्कीन का ऑक्सीडेटिव विदलन होता है, जिससे एल्डिहाइड और कीटोन का निर्माण होता है:
इस प्रक्रिया में बनने वाले एल्डिहाइड कार्बोक्जिलिक एसिड बनाने के लिए आगे ऑक्सीकरण से गुजरते हैं।
पोटेशियम परमैंगनेट के क्षारीय घोल का उपयोग करके डायोल बनाने के लिए एल्केन्स का हाइड्रॉक्सिलेशन भी किया जा सकता है।
पेरबेंजोइक एसिड के साथ प्रतिक्रिया
एल्केन्स पेरोक्सी एसिड (पेरासिड्स), जैसे पेरबेंजोइक एसिड के साथ प्रतिक्रिया करके चक्रीय ईथर (एपॉक्सी यौगिक) बनाते हैं। उदाहरण के लिए

जब एपॉक्सीएथेन को किसी एसिड के पतले घोल के साथ धीरे से गर्म किया जाता है, तो ईथेन-1,2-डायोल बनता है:

ऑक्सीजन के साथ प्रतिक्रिया
अन्य सभी हाइड्रोकार्बन की तरह, एल्केन्स जलते हैं और प्रचुर मात्रा में हवा के साथ कार्बन डाइऑक्साइड और पानी बनाते हैं:
सीमित वायु पहुंच के साथ, एल्केन्स के दहन से कार्बन मोनोऑक्साइड और पानी का निर्माण होता है:
चूँकि एल्केन्स में संबंधित अल्केन्स की तुलना में सापेक्ष कार्बन की मात्रा अधिक होती है, इसलिए वे धुएँ वाली लौ के साथ जलते हैं। यह कार्बन कणों के निर्माण के कारण है:
यदि आप किसी एल्कीन को ऑक्सीजन के साथ मिलाते हैं और इस मिश्रण को लगभग 200 डिग्री सेल्सियस के तापमान पर सिल्वर उत्प्रेरक की सतह पर प्रवाहित करते हैं, तो एपॉक्सीथेन बनता है:
ओजोनोलिसिस
जब गैसीय ओजोन को 20 डिग्री सेल्सियस से नीचे के तापमान पर ट्राइक्लोरोमेथेन या टेट्राक्लोरोमेथेन में एक एल्कीन के घोल से गुजारा जाता है, तो संबंधित एल्कीन (ऑक्सिरेन) का ओजोनाइड बनता है।

ओजोनाइड्स अस्थिर यौगिक हैं और विस्फोटक हो सकते हैं। वे एल्डिहाइड या कीटोन बनाने के लिए हाइड्रोलिसिस से गुजरते हैं। उदाहरण के लिए

इस मामले में, मेथनॉल (फॉर्मेल्डिहाइड) का हिस्सा हाइड्रोजन पेरोक्साइड के साथ प्रतिक्रिया करता है, जिससे मीथेन (फॉर्मिक) एसिड बनता है:
बहुलकीकरण
सबसे सरल एल्कीन उच्च आणविक भार वाले यौगिकों को बनाने के लिए पोलीमराइज़ कर सकते हैं जिनका मूल एल्कीन के समान अनुभवजन्य सूत्र होता है:
यह प्रतिक्रिया उच्च दबाव, 120°C के तापमान और ऑक्सीजन की उपस्थिति में होती है, जो उत्प्रेरक की भूमिका निभाती है। हालाँकि, एथिलीन पोलीमराइजेशन को ज़िग्लर उत्प्रेरक का उपयोग करके कम दबाव पर भी किया जा सकता है। सबसे आम ज़िग्लर उत्प्रेरक में से एक ट्राइथाइलएल्यूमिनियम और टाइटेनियम टेट्राक्लोराइड का मिश्रण है।
ऐल्कीनों के पॉलिमरीकरण पर अनुभाग में अधिक विस्तार से चर्चा की गई है। 18.3.
जिनमें पाई बांड होता है वे असंतृप्त हाइड्रोकार्बन होते हैं। वे अल्केन्स के व्युत्पन्न हैं, जिनके अणुओं में दो हाइड्रोजन परमाणु विभाजित हो गए हैं। परिणामी मुक्त संयोजकताएं एक नए प्रकार का बंधन बनाती हैं, जो अणु के तल के लंबवत स्थित होता है। इस प्रकार यौगिकों का एक नया समूह उत्पन्न होता है - ऐल्कीन। हम इस लेख में रोजमर्रा की जिंदगी और उद्योग में इस वर्ग के पदार्थों के भौतिक गुणों, तैयारी और उपयोग पर विचार करेंगे।
एथिलीन की सजातीय श्रृंखला
एल्कीन कहे जाने वाले सभी यौगिकों का सामान्य सूत्र, जो उनकी गुणात्मक और मात्रात्मक संरचना को दर्शाता है, C n H 2 n है। व्यवस्थित नामकरण के अनुसार हाइड्रोकार्बन के नाम इस प्रकार हैं: संबंधित अल्केन के पद में, प्रत्यय -an से -ene में बदल जाता है, उदाहरण के लिए: ईथेन - एथीन, प्रोपेन - प्रोपेन, आदि। कुछ स्रोतों में, आप कर सकते हैं इस वर्ग के यौगिकों का दूसरा नाम खोजें - ओलेफ़िन। इसके बाद, हम दोहरे बंधन निर्माण की प्रक्रिया और एल्कीन के भौतिक गुणों का अध्ययन करेंगे, और अणु की संरचना पर उनकी निर्भरता भी निर्धारित करेंगे।
दोहरा बंधन कैसे बनता है?
एथिलीन के उदाहरण का उपयोग करके पाई बांड की इलेक्ट्रॉनिक प्रकृति को निम्नानुसार दर्शाया जा सकता है: इसके अणु में कार्बन परमाणु एसपी 2 संकरण के रूप में हैं। इस स्थिति में, एक सिग्मा बंधन बनता है। दो और हाइब्रिड ऑर्बिटल्स, प्रत्येक कार्बन परमाणु से, हाइड्रोजन परमाणुओं के साथ सरल सिग्मा बांड बनाते हैं। कार्बन परमाणुओं के दो शेष मुक्त संकर बादल अणु के तल के ऊपर और नीचे ओवरलैप होते हैं - एक पाई बंधन बनता है। यह वह है जो एल्केन्स के भौतिक और रासायनिक गुणों को निर्धारित करती है, जिस पर बाद में चर्चा की जाएगी।

स्थानिक समरूपता
ऐसे यौगिक जिनमें अणुओं की मात्रात्मक और गुणात्मक संरचना समान होती है, लेकिन एक अलग स्थानिक संरचना होती है, आइसोमर्स कहलाते हैं। आइसोमेरिज्म कार्बनिक नामक पदार्थों के समूह में होता है। ओलेफिन का लक्षण वर्णन ऑप्टिकल आइसोमेरिज्म की घटना से काफी प्रभावित होता है। यह इस तथ्य में व्यक्त किया गया है कि दोहरे बंधन में दो कार्बन परमाणुओं में से प्रत्येक में विभिन्न रेडिकल या प्रतिस्थापन वाले एथिलीन होमोलॉग दो ऑप्टिकल आइसोमर्स के रूप में हो सकते हैं। वे दोहरे बंधन के तल के सापेक्ष अंतरिक्ष में प्रतिस्थापकों की स्थिति के आधार पर एक दूसरे से भिन्न होते हैं। इस मामले में एल्कीन के भौतिक गुण भी भिन्न होंगे। उदाहरण के लिए, यह पदार्थों के क्वथनांक और गलनांक पर लागू होता है। इस प्रकार, सीधी श्रृंखला वाले ओलेफिन का क्वथनांक आइसोमर यौगिकों की तुलना में अधिक होता है। साथ ही, एल्कीन के सीआईएस आइसोमर्स का क्वथनांक ट्रांस आइसोमर्स की तुलना में अधिक होता है। पिघलने के तापमान के संबंध में, तस्वीर विपरीत है।
एथिलीन और उसके समरूपों के भौतिक गुणों की तुलनात्मक विशेषताएँ
ओलेफिन के पहले तीन प्रतिनिधि गैसीय यौगिक हैं, फिर, पेंटीन सी 5 एच 10 से शुरू होकर सूत्र सी 17 एच 34 के साथ एल्केन तक, वे तरल हैं, और फिर ठोस हैं। एथीन होमोलॉग्स निम्नलिखित प्रवृत्ति दिखाते हैं: यौगिकों के क्वथनांक कम हो जाते हैं। उदाहरण के लिए, एथिलीन के लिए यह संकेतक -169.1°C है, और प्रोपलीन के लिए -187.6°C है। लेकिन आणविक भार बढ़ने के साथ क्वथनांक बढ़ता है। तो, एथिलीन के लिए यह -103.7°C है, और प्रोपेन के लिए -47.7°C है। जो कहा गया है उसे सारांशित करते हुए, हम यह निष्कर्ष निकाल सकते हैं कि एल्कीन के भौतिक गुण उनके आणविक भार पर निर्भर करते हैं। इसकी वृद्धि के साथ, यौगिकों की समग्र स्थिति दिशा में बदल जाती है: गैस - तरल - ठोस, और पिघलने बिंदु भी कम हो जाता है, और क्वथनांक बढ़ जाता है।

एथीन के लक्षण
ऐल्कीनों की समजात श्रृंखला का पहला प्रतिनिधि एथिलीन है। यह एक रंगहीन गैस है, जो पानी में थोड़ा घुलनशील है, लेकिन कार्बनिक सॉल्वैंट्स में अत्यधिक घुलनशील है। आणविक भार - 28, एथीन हवा की तुलना में थोड़ा हल्का है, इसमें सूक्ष्म मीठी गंध है। यह आसानी से हैलोजन, हाइड्रोजन और हाइड्रोजन हैलाइड के साथ प्रतिक्रिया करता है। हालाँकि, एल्कीन और पैराफिन के भौतिक गुण काफी करीब हैं। उदाहरण के लिए, एकत्रीकरण की स्थिति, मीथेन और एथिलीन की गंभीर ऑक्सीकरण से गुजरने की क्षमता, आदि। एल्केन्स को कैसे अलग किया जा सकता है? ओलेफ़िन के असंतृप्त चरित्र को कैसे प्रकट करें? इसके लिए गुणात्मक प्रतिक्रियाएँ हैं, जिन पर हम अधिक विस्तार से ध्यान देंगे। याद रखें कि अणु की संरचना में एल्केन्स की क्या विशेषता है। इन पदार्थों के भौतिक और रासायनिक गुण उनकी संरचना में दोहरे बंधन की उपस्थिति से निर्धारित होते हैं। इसकी उपस्थिति साबित करने के लिए, गैसीय हाइड्रोकार्बन को पोटेशियम परमैंगनेट या ब्रोमीन पानी के बैंगनी घोल से गुजारा जाता है। यदि उनका रंग फीका पड़ जाता है, तो यौगिक में अणुओं की संरचना में पाई बांड होते हैं। एथिलीन ऑक्सीकरण प्रतिक्रिया में प्रवेश करता है और KMnO 4 और Br 2 के घोल को ख़राब कर देता है।
अतिरिक्त प्रतिक्रियाओं का तंत्र
दोहरे बंधन का टूटना कार्बन की मुक्त संयोजकता में अन्य रासायनिक तत्वों के परमाणुओं के जुड़ने के साथ समाप्त होता है। उदाहरण के लिए, एथिलीन की हाइड्रोजन के साथ प्रतिक्रिया, जिसे हाइड्रोजनीकरण कहा जाता है, ईथेन का उत्पादन करती है। एक उत्प्रेरक की आवश्यकता होती है, जैसे पाउडर निकल, पैलेडियम या प्लैटिनम। एचसीएल के साथ प्रतिक्रिया क्लोरोइथेन के निर्माण के साथ समाप्त होती है। वी. मार्कोवनिकोव के नियम को ध्यान में रखते हुए, अपने अणुओं में दो से अधिक कार्बन परमाणुओं वाले अल्केन्स हाइड्रोजन हेलाइड्स की अतिरिक्त प्रतिक्रिया से गुजरते हैं।

एथीन होमोलॉग्स हाइड्रोजन हैलाइड्स के साथ कैसे परस्पर क्रिया करते हैं
यदि हमारे सामने "एल्केन्स के भौतिक गुणों की विशेषताएँ और उनकी तैयारी" का कार्य है, तो हमें वी. मार्कोवनिकोव के नियम पर अधिक विस्तार से विचार करने की आवश्यकता है। यह व्यवहार में स्थापित किया गया है कि एथिलीन होमोलॉग एक निश्चित पैटर्न का पालन करते हुए, दोहरे बंधन टूटने के स्थल पर हाइड्रोजन क्लोराइड और अन्य यौगिकों के साथ प्रतिक्रिया करते हैं। इसमें यह तथ्य शामिल है कि हाइड्रोजन परमाणु सबसे अधिक हाइड्रोजनीकृत कार्बन परमाणु से जुड़ा होता है, और क्लोरीन, ब्रोमीन या आयोडीन आयन सबसे कम संख्या में हाइड्रोजन परमाणु वाले कार्बन परमाणु से जुड़ा होता है। योगात्मक प्रतिक्रियाओं के पाठ्यक्रम की इस विशेषता को वी. मार्कोवनिकोव का नियम कहा जाता है।
जलयोजन और पोलीमराइजेशन
आइए हम समजात श्रृंखला के पहले प्रतिनिधि - एथीन के उदाहरण का उपयोग करके एल्कीन के भौतिक गुणों और अनुप्रयोग पर विचार करना जारी रखें। पानी के साथ इसकी प्रतिक्रिया का उपयोग कार्बनिक संश्लेषण उद्योग में किया जाता है और इसका अत्यधिक व्यावहारिक महत्व है। यह प्रक्रिया पहली बार 19वीं सदी में ए.एम. द्वारा की गई थी। बटलरोव। प्रतिक्रिया के लिए कई शर्तों को पूरा करना आवश्यक है। यह, सबसे पहले, एथीन के लिए उत्प्रेरक और विलायक के रूप में केंद्रित सल्फ्यूरिक एसिड या ओलियम का उपयोग, लगभग 10 एटीएम का दबाव और 70 डिग्री के भीतर तापमान है। जलयोजन प्रक्रिया दो चरणों में होती है। सबसे पहले, पाई बांड के टूटने के बिंदु पर सल्फेट अणुओं को एथीन में जोड़ा जाता है, और एथिलसल्फ्यूरिक एसिड बनता है। फिर परिणामी पदार्थ पानी के साथ प्रतिक्रिया करता है, एथिल अल्कोहल प्राप्त होता है। इथेनॉल प्लास्टिक, सिंथेटिक रबर, वार्निश और अन्य कार्बनिक रसायनों के उत्पादन के लिए खाद्य उद्योग में उपयोग किया जाने वाला एक महत्वपूर्ण उत्पाद है।

ओलेफ़िन आधारित पॉलिमर
एल्केन्स के वर्ग से संबंधित पदार्थों के उपयोग के मुद्दे का अध्ययन जारी रखते हुए, हम उनके पोलीमराइजेशन की प्रक्रिया का अध्ययन करेंगे, जिसमें उनके अणुओं की संरचना में असंतृप्त रासायनिक बंधन वाले यौगिक भाग ले सकते हैं। कई प्रकार की पोलीमराइज़ेशन प्रतिक्रियाएं ज्ञात हैं, जिनके अनुसार उच्च-आणविक उत्पाद बनते हैं - पॉलिमर, उदाहरण के लिए, जैसे पॉलीइथाइलीन, पॉलीप्रोपाइलीन, पॉलीस्टाइनिन, आदि। मुक्त कण तंत्र उच्च दबाव पॉलीथीन के उत्पादन की ओर ले जाता है। यह उद्योग में सबसे व्यापक रूप से उपयोग किए जाने वाले यौगिकों में से एक है। धनायनित-आयनिक प्रकार एक बहुलक को पॉलीस्टायरीन जैसी स्टीरियोरेगुलर संरचना प्रदान करता है। इसे उपयोग करने के लिए सबसे सुरक्षित और सबसे सुविधाजनक पॉलिमर में से एक माना जाता है। पॉलीस्टाइनिन से बने उत्पाद आक्रामक पदार्थों के प्रति प्रतिरोधी होते हैं: एसिड और क्षार, गैर-ज्वलनशील, आसानी से रंगे हुए। एक अन्य प्रकार का पोलीमराइजेशन तंत्र डिमराइजेशन है, जो आइसोब्यूटीन के उत्पादन की ओर जाता है, जिसका उपयोग गैसोलीन के लिए एंटीनॉक एडिटिव के रूप में किया जाता है।
कैसे प्राप्त करें
अल्केन्स, जिनके भौतिक गुणों का हम अध्ययन करते हैं, प्रयोगशाला और उद्योग में विभिन्न तरीकों से प्राप्त किए जाते हैं। कार्बनिक रसायन विज्ञान के स्कूल पाठ्यक्रम में प्रयोगों में, एथिल अल्कोहल के निर्जलीकरण की प्रक्रिया का उपयोग पानी हटाने वाले एजेंटों, जैसे फॉस्फोरस पेंटोक्साइड या सल्फेट एसिड की मदद से किया जाता है। गर्म होने पर प्रतिक्रिया होती है और यह इथेनॉल प्राप्त करने की प्रक्रिया के विपरीत होती है। एल्केन्स प्राप्त करने की एक और सामान्य विधि ने उद्योग में अपना आवेदन पाया है, अर्थात्: संतृप्त हाइड्रोकार्बन के हैलोजन डेरिवेटिव को गर्म करना, जैसे कि क्लोरोप्रोपेन को क्षार के केंद्रित अल्कोहल समाधान - सोडियम या पोटेशियम हाइड्रॉक्साइड के साथ। प्रतिक्रिया में, एक हाइड्रोजन क्लोराइड अणु विभाजित हो जाता है, उस स्थान पर एक दोहरा बंधन बनता है जहां कार्बन परमाणुओं की मुक्त संयोजकता दिखाई देती है। रासायनिक प्रक्रिया का अंतिम उत्पाद ओलेफ़िन - प्रोपेन होगा। एल्केन्स के भौतिक गुणों पर विचार करना जारी रखते हुए, आइए हम ओलेफिन प्राप्त करने की मुख्य प्रक्रिया - पायरोलिसिस पर ध्यान दें।

एथिलीन श्रृंखला के असंतृप्त हाइड्रोकार्बन का औद्योगिक उत्पादन
सस्ते कच्चे माल - तेल के टूटने की प्रक्रिया में बनने वाली गैसें, रासायनिक उद्योग में ओलेफिन के स्रोत के रूप में काम करती हैं। इसके लिए, पायरोलिसिस की एक तकनीकी योजना का उपयोग किया जाता है - गैस मिश्रण का विभाजन, जो कार्बन बांड के टूटने और एथिलीन, प्रोपेन और अन्य एल्केन्स के निर्माण के साथ होता है। पायरोलिसिस विशेष भट्टियों में किया जाता है, जिसमें व्यक्तिगत पायरो-कॉइल्स शामिल होते हैं। वे लगभग 750-1150°C का तापमान बनाते हैं और इसमें मंदक के रूप में जलवाष्प होता है। प्रतिक्रियाएँ एक श्रृंखला तंत्र द्वारा आगे बढ़ती हैं जो मध्यवर्ती रेडिकल्स के निर्माण के साथ आगे बढ़ती हैं। अंतिम उत्पाद एथिलीन या प्रोपेन है, और इनका उत्पादन बड़ी मात्रा में होता है।

हमने भौतिक गुणों के साथ-साथ एल्कीन प्राप्त करने के अनुप्रयोग और विधियों का विस्तार से अध्ययन किया।
