730. Mengapa air digunakan untuk mendinginkan beberapa mekanisme?
Air memiliki kapasitas panas spesifik yang tinggi, yang berkontribusi pada penghilangan panas yang baik dari mekanisme.
731. Dalam hal apa lebih banyak energi harus dikeluarkan: untuk memanaskan satu liter air sebesar 1 °C atau untuk memanaskan seratus gram air sebesar 1 °C?
Untuk memanaskan satu liter air, karena semakin besar massanya, semakin banyak energi yang harus dikeluarkan.
732. Garpu tembaga dan perak dengan massa yang sama dicelupkan ke dalam air panas. Apakah mereka menerima jumlah panas yang sama dari air?
Garpu tembaga akan menerima lebih banyak panas, karena panas spesifik tembaga lebih besar daripada perak.
733. Sepotong timah dan sepotong besi tuang dengan massa yang sama dipukul tiga kali dengan palu godam. Bagian mana yang lebih panas?
Timbal akan lebih panas karena kapasitas panas spesifiknya lebih kecil daripada besi tuang, dan lebih sedikit energi yang dibutuhkan untuk memanaskan timah.
734. Satu labu berisi air, yang lain berisi minyak tanah dengan massa dan suhu yang sama. Sebuah kubus besi yang sama panasnya dilemparkan ke dalam masing-masing labu. Apa yang akan memanas hingga suhu yang lebih tinggi - air atau minyak tanah?
Minyak tanah.
735. Mengapa fluktuasi suhu kurang tajam di musim dingin dan musim panas di kota-kota di tepi pantai daripada di kota-kota yang terletak di pedalaman?
Air memanas dan mendingin lebih lambat daripada udara. Di musim dingin, ia mendingin dan menggerakkan massa udara hangat di darat, membuat iklim di pantai lebih hangat.
736. Kapasitas kalor jenis aluminium adalah 920 J/kg °C. Apa artinya ini?
Ini berarti dibutuhkan 920 J untuk memanaskan 1 kg aluminium sebesar 1 °C.
737. Batang aluminium dan tembaga dengan massa yang sama 1 kg didinginkan oleh 1 °C. Berapa perubahan energi internal setiap balok? Bilah mana yang akan berubah lebih banyak dan seberapa banyak?
738. Berapa jumlah kalor yang diperlukan untuk memanaskan satu kilogram billet besi sebesar 45 °C?

739. Berapa kalor yang diperlukan untuk memanaskan 0,25 kg air dari suhu 30°C menjadi 50°C?

740. Bagaimana energi dalam dari dua liter air berubah jika dipanaskan sebesar 5 °C?

741. Berapa kalor yang diperlukan untuk memanaskan 5 g air dari 20 °C menjadi 30 °C?
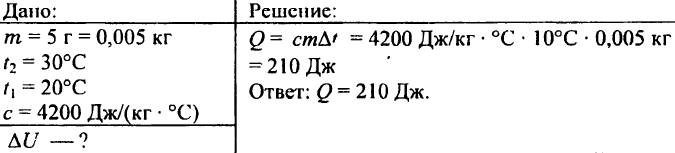
742. Berapa kalor yang diperlukan untuk memanaskan bola aluminium dengan berat 0,03 kg sebesar 72 °C?

743. Hitung jumlah kalor yang diperlukan untuk memanaskan 15 kg tembaga sebesar 80 °C.
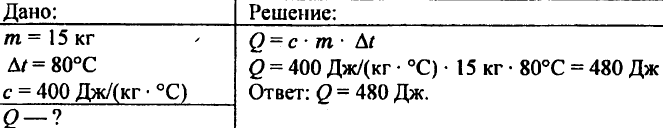
744. Hitung jumlah kalor yang diperlukan untuk memanaskan 5 kg tembaga dari 10 °C menjadi 200 °C.

745. Berapa kalor yang diperlukan untuk memanaskan 0,2 kg air dari 15 °C menjadi 20 °C?

746. Air seberat 0,3 kg telah mendingin sebesar 20 °C. Berapa banyak energi internal air berkurang?

747. Berapa kalor yang diperlukan untuk memanaskan 0,4 kg air pada suhu 20 °C hingga suhu 30 °C?

748. Berapa banyak panas yang dihabiskan untuk memanaskan 2,5 kg air pada 20 °C?
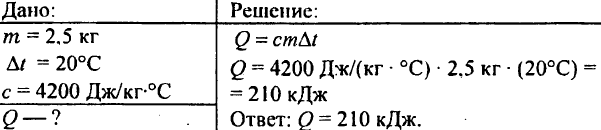
749. Berapa banyak kalor yang dilepaskan ketika 250 g air didinginkan dari 90 °C menjadi 40 °C?
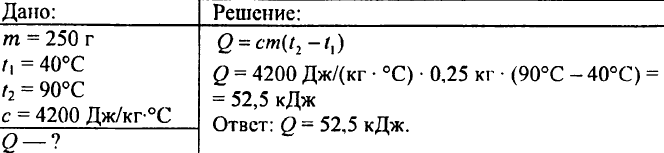
750. Berapa kalor yang diperlukan untuk memanaskan 0,015 liter air sebesar 1 °C?

751. Hitung jumlah kalor yang diperlukan untuk memanaskan sebuah kolam dengan volume 300 m3 sebesar 10 °C?
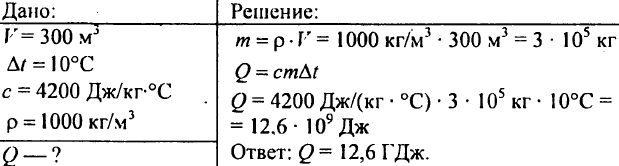
752. Berapa banyak kalor yang harus diberikan kepada 1 kg air untuk menaikkan suhunya dari 30°C menjadi 40°C?

753. Air dengan volume 10 liter telah mendingin dari suhu 100 °C menjadi suhu 40 °C. Berapa banyak panas yang dilepaskan dalam kasus ini?

754. Hitung jumlah kalor yang diperlukan untuk memanaskan 1 m3 pasir sebesar 60 °C.

755. Volume udara 60 m3, kapasitas panas spesifik 1000 J/kg °C, kerapatan udara 1,29 kg/m3. Berapa kalor yang diperlukan untuk menaikkan suhu menjadi 22°C?

756. Air dipanaskan 10 ° C, menghabiskan 4,20 103 J panas. Tentukan banyaknya air.
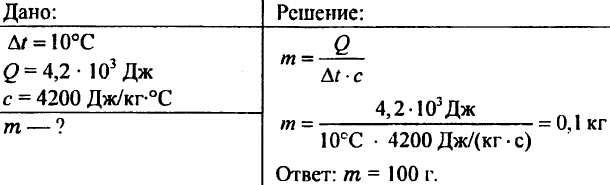
757. Air dengan berat 0,5 kg melaporkan panas sebesar 20,95 kJ. Berapa suhu air jika suhu awal air adalah 20°C?

758. 8 kg air pada 10 °C dituangkan ke dalam panci tembaga seberat 2,5 kg. Berapa banyak panas yang dibutuhkan untuk mendidihkan air dalam panci?

759. Satu liter air yang bersuhu 15 °C dituangkan ke dalam sendok tembaga yang beratnya 300 g. Berapa kalor yang diperlukan untuk memanaskan air dalam sendok sebesar 85 °C?

760. Sepotong granit yang dipanaskan dengan berat 3 kg ditempatkan di dalam air. Granit mentransfer 12,6 kJ panas ke air, mendingin sebesar 10 °C. Berapa kapasitas kalor jenis batu tersebut?

761. Air panas pada 50 °C ditambahkan ke 5 kg air pada 12 °C, memperoleh campuran dengan suhu 30 °C. Berapa banyak air yang ditambahkan?

762. Air pada 20 °C ditambahkan ke 3 liter air pada 60 °C untuk mendapatkan air pada 40 °C. Berapa banyak air yang ditambahkan?

763. Berapakah suhu campuran jika 600 g air pada 80 °C dicampur dengan 200 g air pada 20 °C?

764. Satu liter air bersuhu 90°C dituangkan ke dalam air bersuhu 10°C, dan suhu air menjadi 60°C. Berapa banyak air dingin di sana?

765. Tentukan berapa banyak air panas yang dipanaskan hingga 60°C yang harus dituangkan ke dalam bejana jika bejana tersebut telah berisi 20 liter air dingin pada suhu 15°C; suhu campuran harus 40 °C.

766. Tentukan berapa banyak kalor yang diperlukan untuk memanaskan 425 g air sebesar 20 °C.

767. Berapa derajat pemanasan 5 kg air jika air menerima 167,2 kJ?

768. Berapa kalor yang diperlukan untuk memanaskan m gram air pada suhu t1 sampai suhu t2?
769. 2 kg air dituangkan ke dalam kalorimeter pada suhu 15 °C. Sampai suhu berapa air dalam kalorimeter akan memanas jika berat kuningan 500 g yang dipanaskan hingga 100 °C diturunkan ke dalamnya? Kapasitas kalor jenis kuningan adalah 0,37 kJ/(kg °C).
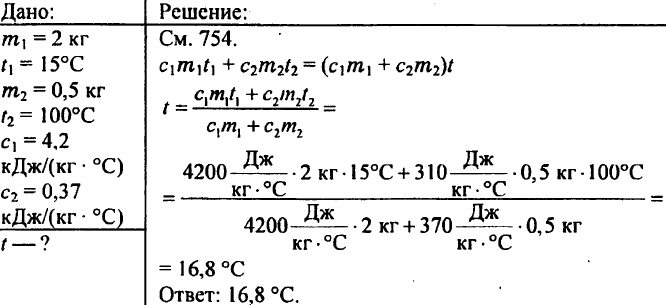
770. Ada potongan tembaga, timah dan aluminium dengan volume yang sama. Manakah dari potongan-potongan ini yang memiliki kapasitas panas terbesar dan terkecil?

771. 450 g air, yang suhunya 20 °C, dituangkan ke dalam kalorimeter. Ketika 200 g serbuk besi yang dipanaskan hingga 100 ° C direndam dalam air ini, suhu air menjadi 24 ° C. Tentukan kapasitas panas spesifik serbuk gergaji.

772. Sebuah kalorimeter tembaga dengan berat 100 g menampung 738 g air, yang suhunya 15 °C. 200 g tembaga diturunkan ke dalam kalorimeter ini pada suhu 100 °C, setelah itu suhu kalorimeter naik menjadi 17 °C. Berapa kapasitas panas spesifik tembaga?

773. Sebuah bola baja seberat 10 g dikeluarkan dari tungku dan diturunkan ke dalam air pada suhu 10 °C. Suhu air naik menjadi 25 ° C. Berapa suhu bola dalam oven jika massa air 50 g? Kapasitas panas spesifik baja adalah 0,5 kJ/(kg °C).

777. 50 g air pada 19 °C dituangkan ke dalam air seberat 150 g pada suhu 35 °C. Berapakah suhu campuran tersebut?

778. Air seberat 5 kg pada suhu 90 °C dituangkan ke dalam ketel besi seberat 2 kg pada suhu 10 °C. Berapa suhu airnya?

779. Sebuah pahat baja seberat 2 kg dipanaskan sampai suhu 800 °C dan kemudian diturunkan ke dalam bejana yang berisi 15 liter air pada suhu 10 °C. Sampai suhu berapa air dalam bejana akan dipanaskan?

(Indikasi. Untuk mengatasi masalah ini, perlu untuk membuat persamaan di mana suhu air yang diinginkan di kapal setelah pemotong diturunkan diambil sebagai tidak diketahui.)
780. Berapa suhu yang akan diperoleh air jika Anda mencampur 0,02 kg air pada 15 °C, 0,03 kg air pada 25 °C, dan 0,01 kg air pada 60 °C?
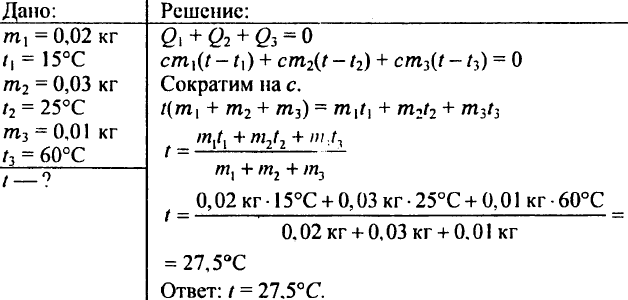
781. Pemanasan kelas yang berventilasi baik membutuhkan jumlah panas 4,19 MJ per jam. Air masuk ke radiator pemanas pada 80°C dan keluar pada 72°C. Berapa banyak air yang harus disuplai ke radiator setiap jam?

782. Timbal seberat 0,1 kg pada suhu 100 °C direndam dalam kalorimeter aluminium seberat 0,04 kg yang berisi 0,24 kg air pada suhu 15 °C. Setelah itu, suhu 16 °C ditetapkan dalam kalorimeter. Berapa kapasitas panas spesifik timah?

Apa yang lebih cepat panas di atas kompor - ketel atau seember air? Jawabannya jelas - ketel. Lalu pertanyaan kedua adalah mengapa?
Jawabannya tidak kalah jelas - karena massa air dalam ketel lebih sedikit. Bagus sekali. Dan sekarang Anda dapat melakukan sendiri pengalaman fisik paling nyata di rumah. Untuk melakukan ini, Anda memerlukan dua panci kecil yang identik, jumlah air dan minyak sayur yang sama, misalnya, masing-masing setengah liter dan kompor. Taruh panci berisi minyak dan air di atas api yang sama. Dan sekarang lihat saja apa yang akan memanas lebih cepat. Jika ada termometer untuk cairan, Anda dapat menggunakannya, jika tidak, Anda dapat mencoba suhu dari waktu ke waktu dengan jari Anda, berhati-hatilah agar tidak membakar diri sendiri. Bagaimanapun, Anda akan segera melihat bahwa minyak memanas secara signifikan lebih cepat daripada air. Dan satu pertanyaan lagi, yang juga bisa diimplementasikan dalam bentuk pengalaman. Mana yang lebih cepat mendidih - air hangat atau dingin? Semuanya jelas lagi - yang hangat akan menjadi yang pertama selesai. Mengapa semua pertanyaan dan eksperimen aneh ini? Untuk menentukan kuantitas fisik yang disebut "jumlah panas."
Kuantitas panas
Jumlah panas adalah energi yang hilang atau diperoleh tubuh selama perpindahan panas. Ini jelas dari namanya. Saat didinginkan, tubuh akan kehilangan sejumlah panas, dan ketika dipanaskan, ia akan menyerap. Dan jawaban atas pertanyaan kami menunjukkan kepada kami tergantung pada apa jumlah panasnya? Pertama, semakin besar massa tubuh, semakin besar jumlah panas yang harus dikeluarkan untuk mengubah suhunya satu derajat. Kedua, jumlah kalor yang diperlukan untuk memanaskan suatu benda bergantung pada zat penyusunnya, yaitu jenis zatnya. Dan ketiga, perbedaan suhu tubuh sebelum dan sesudah perpindahan panas juga penting untuk perhitungan kita. Berdasarkan hal tersebut di atas, kita dapat tentukan jumlah kalor dengan rumus :
Q=cm(t_2-t_1) ,
di mana Q adalah jumlah panas,
m - berat badan,
(t_2-t_1) - perbedaan antara suhu tubuh awal dan akhir,
c - kapasitas panas spesifik zat, ditemukan dari tabel yang relevan.
Dengan menggunakan rumus ini, Anda dapat menghitung jumlah panas yang diperlukan untuk memanaskan suatu benda atau yang akan dilepaskan oleh benda tersebut saat mendingin.
Jumlah panas diukur dalam joule (1 J), seperti bentuk energi lainnya. Namun, nilai ini diperkenalkan belum lama ini, dan orang-orang mulai mengukur jumlah panas jauh lebih awal. Dan mereka menggunakan unit yang banyak digunakan di zaman kita - kalori (1 kal). 1 kalori adalah jumlah kalor yang diperlukan untuk menaikkan suhu 1 gram air sebesar 1 derajat Celcius. Dipandu oleh data ini, pecinta menghitung kalori dalam makanan yang mereka makan dapat, demi kepentingan, menghitung berapa liter air yang dapat direbus dengan energi yang mereka konsumsi dengan makanan di siang hari.
Perubahan energi internal dengan melakukan pekerjaan ditandai dengan jumlah pekerjaan, yaitu. usaha adalah ukuran perubahan energi dalam dalam suatu proses tertentu. Perubahan energi internal suatu benda selama perpindahan panas ditandai dengan besaran yang disebut jumlah panas.
adalah perubahan energi dalam tubuh pada proses perpindahan panas tanpa melakukan usaha. Jumlah panas dilambangkan dengan huruf Q .
Kerja, energi internal, dan jumlah panas diukur dalam satuan yang sama - joule ( J), seperti bentuk energi lainnya.
Dalam pengukuran termal, satuan khusus energi, kalori ( kotoran), sama dengan banyaknya kalor yang diperlukan untuk menaikkan suhu 1 gram air sebesar 1 derajat celcius (lebih tepatnya, dari 19,5 hingga 20,5 ° C). Satuan ini, khususnya, saat ini digunakan untuk menghitung konsumsi panas (energi termal) di gedung apartemen. Secara empiris, ekuivalen mekanis panas telah ditetapkan - rasio antara kalori dan joule: 1 kal = 4,2 J.

Ketika suatu benda mentransfer sejumlah panas tertentu tanpa melakukan usaha, energi dalamnya meningkat, jika suatu benda melepaskan sejumlah panas tertentu, maka energi dalamnya berkurang.
Jika Anda menuangkan 100 g air ke dalam dua bejana yang identik, dan 400 g ke dalam bejana lain pada suhu yang sama dan meletakkannya di atas pembakar yang sama, maka air di bejana pertama akan mendidih lebih awal. Jadi, semakin besar massa tubuh, semakin besar jumlah panas yang dibutuhkan untuk memanaskan. Hal yang sama berlaku untuk pendinginan.

Jumlah panas yang dibutuhkan untuk memanaskan tubuh juga tergantung pada jenis zat dari mana tubuh ini dibuat. Ketergantungan jumlah panas yang dibutuhkan untuk memanaskan tubuh pada jenis zat ini ditandai dengan besaran fisika yang disebut kapasitas panas spesifik zat.
- ini adalah kuantitas fisik yang sama dengan jumlah panas yang harus dilaporkan ke 1 kg zat untuk memanaskannya sebesar 1 ° C (atau 1 K). Jumlah kalor yang sama dilepaskan oleh 1 kg zat ketika didinginkan oleh 1 °C.
Kapasitas panas spesifik dilambangkan dengan huruf Dengan. Satuan kapasitas kalor jenis adalah 1 J/kg °C atau 1 J/kg °K.
Nilai kapasitas panas spesifik zat ditentukan secara eksperimental. Cairan memiliki kapasitas panas spesifik yang lebih tinggi daripada logam; Air memiliki kapasitas panas spesifik tertinggi, emas memiliki kapasitas panas spesifik yang sangat kecil.
Karena jumlah panas sama dengan perubahan energi internal tubuh, kita dapat mengatakan bahwa kapasitas panas spesifik menunjukkan berapa banyak energi internal berubah. 1 kg zat ketika suhunya berubah 1 °C. Secara khusus, energi internal 1 kg timbal, ketika dipanaskan 1 °C, meningkat 140 J, dan ketika didinginkan, berkurang 140 J.
Q dibutuhkan untuk memanaskan massa tubuh m suhu t 1 °С hingga suhu t 2 °С, sama dengan produk dari kapasitas panas spesifik zat, massa tubuh dan perbedaan antara suhu akhir dan awal, mis.Q \u003d c m (t 2 - t 1)
Menurut rumus yang sama, jumlah panas yang dikeluarkan tubuh saat didinginkan juga dihitung. Hanya dalam kasus ini suhu akhir harus dikurangi dari suhu awal, mis. Kurangi suhu yang lebih kecil dari suhu yang lebih besar.

Ini adalah sinopsis tentang topik tersebut. "Jumlah panas. Panas spesifik". Pilih langkah selanjutnya:
- Pergi ke abstrak berikutnya:
« Fisika - Kelas 10 "
Dalam proses apa transformasi agregat materi terjadi?
Bagaimana keadaan materi dapat berubah?
Anda dapat mengubah energi internal benda apa pun dengan melakukan kerja, pemanasan atau, sebaliknya, pendinginan.
Jadi, ketika menempa logam, pekerjaan dilakukan dan itu dipanaskan, sementara pada saat yang sama logam dapat dipanaskan di atas nyala api yang menyala.
Juga, jika piston tetap (Gbr. 13.5), maka volume gas tidak berubah saat dipanaskan dan tidak ada kerja yang dilakukan. Tetapi suhu gas, dan karenanya energi internalnya, meningkat.
Energi internal dapat bertambah dan berkurang, sehingga jumlah kalor bisa positif atau negatif.
Proses perpindahan energi dari suatu benda ke benda lain tanpa melakukan usaha disebut pertukaran panas.
Ukuran kuantitatif perubahan energi dalam selama perpindahan panas disebut jumlah panas.
Gambar molekul perpindahan panas.
Selama pertukaran panas pada batas antara benda, molekul yang bergerak lambat dari benda dingin berinteraksi dengan molekul yang bergerak cepat dari benda panas. Akibatnya, energi kinetik molekul menjadi sama dan kecepatan molekul benda dingin meningkat, sedangkan benda panas berkurang.
Selama pertukaran panas, tidak ada konversi energi dari satu bentuk ke bentuk lain; bagian dari energi internal dari tubuh yang lebih panas ditransfer ke tubuh yang kurang panas.
Jumlah panas dan kapasitas panas.
Anda sudah tahu bahwa untuk memanaskan benda bermassa m dari suhu t 1 ke suhu t 2, perlu untuk mentransfer jumlah panas ke sana:
Q \u003d cm (t 2 - t 1) \u003d cm t. (13,5)
Ketika tubuh mendingin, suhu akhirnya t 2 ternyata lebih kecil dari suhu awal t 1 dan jumlah panas yang dilepaskan oleh tubuh adalah negatif.
Koefisien c dalam rumus (13,5) disebut kapasitas panas spesifik zat.
Panas spesifik- ini adalah nilai numerik yang sama dengan jumlah panas yang diterima atau dilepaskan oleh suatu zat dengan massa 1 kg ketika suhunya berubah sebesar 1 K.
Kapasitas panas spesifik gas tergantung pada proses perpindahan panas. Jika Anda memanaskan gas pada tekanan konstan, itu akan memuai dan melakukan pekerjaan. Untuk memanaskan gas sebesar 1 °C pada tekanan konstan, ia perlu mentransfer lebih banyak panas daripada memanaskannya pada volume konstan, ketika gas hanya akan memanas.
Zat cair dan zat padat memuai sedikit bila dipanaskan. Kapasitas panas spesifik mereka pada volume konstan dan tekanan konstan sedikit berbeda.
Panas spesifik penguapan.
Untuk mengubah cairan menjadi uap selama proses perebusan, perlu untuk mentransfer sejumlah panas ke dalamnya. Suhu zat cair tidak berubah ketika mendidih. Transformasi cairan menjadi uap pada suhu konstan tidak menyebabkan peningkatan energi kinetik molekul, tetapi disertai dengan peningkatan energi potensial interaksi mereka. Lagi pula, jarak rata-rata antara molekul gas jauh lebih besar daripada antara molekul cair.
Nilai numerik yang sama dengan jumlah panas yang dibutuhkan untuk mengubah 1 kg cairan menjadi uap pada suhu konstan disebut panas spesifik penguapan.
Proses penguapan cairan terjadi pada suhu berapa pun, sementara molekul tercepat meninggalkan cairan, dan mendingin selama penguapan. Panas spesifik penguapan sama dengan panas spesifik penguapan.
Nilai ini dilambangkan dengan huruf r dan dinyatakan dalam joule per kilogram (J / kg).
Panas spesifik penguapan air sangat tinggi: r H20 = 2,256 10 6 J/kg pada suhu 100 °C. Dalam cairan lain, seperti alkohol, eter, merkuri, minyak tanah, panas spesifik penguapan 3-10 kali lebih kecil daripada air.
Untuk mengubah cairan bermassa m menjadi uap, sejumlah panas diperlukan sama dengan:
Q p \u003d rm. (13.6)
Saat uap mengembun, jumlah panas yang sama dilepaskan:
Q k \u003d -rm. (13.7)
Panas spesifik fusi.
Ketika tubuh kristal meleleh, semua panas yang disuplai ke sana pergi untuk meningkatkan energi potensial interaksi molekul. Energi kinetik molekul tidak berubah, karena peleburan terjadi pada suhu konstan.
Nilai numerik yang sama dengan jumlah panas yang dibutuhkan untuk mengubah zat kristal dengan berat 1 kg pada titik leleh menjadi cairan disebut panas spesifik fusi dan dilambangkan dengan huruf .
Selama kristalisasi zat dengan massa 1 kg, jumlah kalor yang dilepaskan sama persis dengan yang diserap selama peleburan.
Kalor jenis peleburan es agak tinggi: 3,34 10 5 J/kg.
“Jika es tidak memiliki panas peleburan yang tinggi, maka pada musim semi seluruh massa es harus mencair dalam beberapa menit atau detik, karena panas terus-menerus ditransfer ke es dari udara. Konsekuensi dari ini akan mengerikan; karena bahkan di bawah situasi sekarang ini, banjir besar dan aliran air yang deras muncul dari pencairan es atau salju yang sangat banyak.” R. Black, abad ke-18
Untuk melelehkan benda kristal bermassa m, sejumlah panas yang diperlukan sama dengan:
Qpl \u003d m. (13.8)
Jumlah panas yang dilepaskan selama kristalisasi tubuh sama dengan:
Q cr = -λm (13,9)
persamaan keseimbangan panas.
Pertimbangkan pertukaran panas dalam suatu sistem yang terdiri dari beberapa benda yang awalnya memiliki suhu berbeda, misalnya, pertukaran panas antara air dalam bejana dan bola besi panas yang diturunkan ke dalam air. Menurut hukum kekekalan energi, jumlah panas yang dilepaskan oleh satu benda secara numerik sama dengan jumlah panas yang diterima oleh benda lain.
Jumlah panas yang diberikan dianggap negatif, jumlah panas yang diterima dianggap positif. Jadi, jumlah total kalor Q1 + Q2 = 0.
Jika pertukaran panas terjadi antara beberapa benda dalam sistem yang terisolasi, maka
Q 1 + Q 2 + Q 3 + ... = 0. (13.10)
Persamaan (13.10) disebut persamaan keseimbangan panas.
Di sini Q 1 Q 2 , Q 3 - jumlah panas yang diterima atau dilepaskan oleh tubuh. Jumlah panas ini dinyatakan dengan rumus (13,5) atau rumus (13,6) - (13,9), jika berbagai transformasi fase zat (pelelehan, kristalisasi, penguapan, pengembunan) terjadi dalam proses perpindahan panas.
Anda dapat mengubah energi internal gas di dalam silinder tidak hanya dengan melakukan kerja, tetapi juga dengan memanaskan gas (Gbr. 43). Jika piston tetap, maka volume gas tidak akan berubah, tetapi suhu, dan karenanya energi internal, akan meningkat.
Proses perpindahan energi dari satu benda ke benda lain tanpa melakukan usaha disebut perpindahan panas atau heat transfer.
Energi yang ditransfer ke tubuh sebagai akibat dari perpindahan panas disebut jumlah panas. Jumlah panas juga disebut energi yang dikeluarkan tubuh dalam proses perpindahan panas.
Gambar molekul perpindahan panas. Selama pertukaran panas pada batas antara benda, molekul yang bergerak perlahan dari benda dingin berinteraksi dengan molekul yang bergerak lebih cepat dari benda panas. Akibatnya, energi kinetik
molekul disejajarkan dan kecepatan molekul benda dingin meningkat, dan molekul benda panas berkurang.
Selama pertukaran panas, tidak ada konversi energi dari satu bentuk ke bentuk lain: bagian dari energi internal benda panas dipindahkan ke benda dingin.
Jumlah panas dan kapasitas panas. Dari mata kuliah fisika kelas VII diketahui bahwa untuk memanaskan suatu benda yang bermassa dari temperatur ke temperatur, perlu diketahui besaran kalornya.
![]()
Ketika tubuh mendingin, suhu akhirnya lebih rendah dari suhu awal dan jumlah panas yang dilepaskan oleh tubuh adalah negatif.
Koefisien c dalam rumus (4,5) disebut kapasitas panas spesifik. Kapasitas kalor jenis adalah jumlah kalor yang diterima atau dilepaskan oleh 1 kg suatu zat ketika suhunya berubah sebesar 1 K -
Kapasitas panas spesifik dinyatakan dalam joule per kilogram kali kelvin. Benda yang berbeda membutuhkan jumlah energi yang tidak sama untuk meningkatkan suhu sebesar I K. Jadi, kapasitas panas spesifik air dan tembaga
Kapasitas panas spesifik tidak hanya bergantung pada sifat-sifat zat, tetapi juga pada proses perpindahan panas terjadi.Jika Anda memanaskan gas pada tekanan konstan, ia akan memuai dan melakukan kerja. Untuk memanaskan gas sebesar 1 °C pada tekanan konstan, ia perlu mentransfer lebih banyak panas daripada memanaskannya pada volume konstan.
Cairan dan padatan memuai sedikit ketika dipanaskan, dan kapasitas panas spesifiknya pada volume konstan dan tekanan konstan sedikit berbeda.
Panas spesifik penguapan. Untuk mengubah cairan menjadi uap, sejumlah panas harus ditransfer ke sana. Suhu cairan tidak berubah selama transformasi ini. Transformasi cairan menjadi uap pada suhu konstan tidak menyebabkan peningkatan energi kinetik molekul, tetapi disertai dengan peningkatan energi potensial mereka. Lagi pula, jarak rata-rata antara molekul gas jauh lebih besar daripada jarak antara molekul cair. Selain itu, peningkatan volume selama transisi suatu zat dari cair ke keadaan gas membutuhkan pekerjaan yang harus dilakukan melawan gaya tekanan eksternal.
Banyaknya kalor yang diperlukan untuk mengubah 1 kg zat cair menjadi uap pada suhu tetap disebut
panas spesifik penguapan. Nilai ini dilambangkan dengan huruf dan dinyatakan dalam joule per kilogram.
Panas spesifik penguapan air sangat tinggi: pada suhu 100 °C. Untuk cairan lain (alkohol, eter, merkuri, minyak tanah, dll.), panas spesifik penguapan 3-10 kali lebih kecil.
Untuk mengubah massa cair menjadi uap membutuhkan jumlah panas yang sama dengan:
Saat uap mengembun, jumlah panas yang sama dilepaskan:
Panas spesifik fusi. Ketika tubuh kristal meleleh, semua panas yang disuplai ke sana pergi untuk meningkatkan energi potensial molekul. Energi kinetik molekul tidak berubah, karena peleburan terjadi pada suhu konstan.
Banyaknya kalor A yang diperlukan untuk mengubah 1 kg zat kristal pada titik leleh menjadi zat cair dengan suhu yang sama disebut kalor jenis peleburan.
Selama kristalisasi 1 kg suatu zat, jumlah kalor yang dilepaskan sama persis. Panas spesifik pencairan es cukup tinggi:
Untuk melelehkan benda kristal dengan massa, jumlah panas yang dibutuhkan sama dengan:
Jumlah panas yang dilepaskan selama kristalisasi tubuh sama dengan:
1. Apa yang disebut jumlah kalor? 2. Apa yang menentukan kapasitas panas spesifik zat? 3. Apa yang disebut panas spesifik penguapan? 4. Apa yang disebut panas spesifik peleburan? 5. Dalam kasus apa jumlah panas yang ditransfer negatif?
