Suriin ang impormasyon. Kinakailangang suriin ang katumpakan ng mga katotohanan at pagiging maaasahan ng impormasyong ipinakita sa artikulong ito. Sa pahina ng pag-uusap ay mayroong talakayan sa paksa: Mga pagdududa tungkol sa terminolohiya. Formula ng kemikal ... Wikipedia
Ang isang kemikal na formula ay sumasalamin sa impormasyon tungkol sa komposisyon at istraktura ng mga sangkap gamit ang mga kemikal na simbolo, mga numero at mga simbolo ng paghahati ng mga bracket. Sa kasalukuyan, ang mga sumusunod na uri ng mga formula ng kemikal ay nakikilala: Ang pinakasimpleng formula. Maaaring makuha ng karanasan... ... Wikipedia
Ang isang kemikal na formula ay sumasalamin sa impormasyon tungkol sa komposisyon at istraktura ng mga sangkap gamit ang mga kemikal na simbolo, mga numero at mga simbolo ng paghahati ng mga bracket. Sa kasalukuyan, ang mga sumusunod na uri ng mga formula ng kemikal ay nakikilala: Ang pinakasimpleng formula. Maaaring makuha ng karanasan... ... Wikipedia
Ang isang kemikal na formula ay sumasalamin sa impormasyon tungkol sa komposisyon at istraktura ng mga sangkap gamit ang mga kemikal na simbolo, mga numero at mga simbolo ng paghahati ng mga bracket. Sa kasalukuyan, ang mga sumusunod na uri ng mga formula ng kemikal ay nakikilala: Ang pinakasimpleng formula. Maaaring makuha ng karanasan... ... Wikipedia
Ang isang kemikal na formula ay sumasalamin sa impormasyon tungkol sa komposisyon at istraktura ng mga sangkap gamit ang mga kemikal na simbolo, mga numero at mga simbolo ng paghahati ng mga bracket. Sa kasalukuyan, ang mga sumusunod na uri ng mga formula ng kemikal ay nakikilala: Ang pinakasimpleng formula. Maaaring makuha ng karanasan... ... Wikipedia
Pangunahing artikulo: Mga inorganic na compound Listahan ng mga inorganic na compound ayon sa elemento Pang-impormasyon na listahan ng mga inorganic na compound na ipinakita sa alpabetikong pagkakasunud-sunod (ayon sa formula) para sa bawat sangkap, hydrogen acid ng mga elemento (kung ... ... Wikipedia
Ang artikulo o seksyong ito ay nangangailangan ng rebisyon. Mangyaring pagbutihin ang artikulo alinsunod sa mga tuntunin sa pagsulat ng mga artikulo... Wikipedia
Ang isang kemikal na equation (equation ng isang kemikal na reaksyon) ay isang kumbensyonal na representasyon ng isang kemikal na reaksyon gamit ang mga formula ng kemikal, mga numerical coefficient at mga simbolo ng matematika. Ang equation ng isang chemical reaction ay nagbibigay ng qualitative at quantitative... ... Wikipedia
Ang kemikal na software ay mga programa sa kompyuter na ginagamit sa larangan ng kimika. Mga Nilalaman 1 Mga editor ng kemikal 2 Mga Plataporma 3 Panitikan ... Wikipedia
Mga libro
- Isang maikling diksyunaryo ng mga terminong biochemical, Kunizhev S.M. , Ang diksyunaryo ay inilaan para sa mga mag-aaral ng chemical at biological specialty sa mga unibersidad na nag-aaral ng pangkalahatang biochemistry, ekolohiya at mga batayan ng biotechnology, at maaari ding gamitin sa ... Kategorya: Biology Publisher: VUZOVSKAYA KNIGA, Tagagawa:
Formula ng kemikal ay isang imahe na gumagamit ng mga simbolo.
Mga palatandaan ng elemento ng kemikal
Tanda ng kemikal o simbolo ng elemento ng kemikal– ito ang una o dalawang unang titik ng Latin na pangalan ng elementong ito.
Halimbawa: FerrumFe , Cuprum –Cu , OxygeniumO atbp.
Talahanayan 1: Impormasyong ibinigay ng isang simbolo ng kemikal
| Katalinuhan | Gamit ang halimbawa ng Cl |
| Pangalan ng item | Chlorine |
| Hindi metal, halogen | |
| Isang elemento | 1 chlorine atom |
| (Ar) ng elementong ito | Ar(Cl) = 35.5 |
| Absolute atomic mass ng isang kemikal na elemento
m = Ar 1.66 10 -24 g = Ar 1.66 10 -27 kg |
M (Cl) = 35.5 1.66 10 -24 = 58.9 10 -24 g |
Ang pangalan ng isang simbolo ng kemikal sa karamihan ng mga kaso ay binabasa bilang pangalan ng isang elemento ng kemikal. Halimbawa, K - potasa, Ca - kaltsyum, Mg - magnesiyo, Mn – mangganeso.
Ang mga kaso kapag ang pangalan ng isang simbolo ng kemikal ay binasa nang iba ay ibinibigay sa Talahanayan 2:
| Pangalan ng elemento ng kemikal | Tanda ng kemikal | Pangalan ng simbolo ng kemikal
(pagbigkas) |
| Nitrogen | N | Sinabi ni En |
| Hydrogen | H | Ash |
| bakal | Fe | Ferrum |
| ginto | Au | Aurum |
| Oxygen | O | TUNGKOL SA |
| Silicon | Si | Silicium |
| tanso | Cu | Cuprum |
| Tin | Si Sn | Stanum |
| Mercury | Hg | Hydrargium |
| Nangunguna | Pb | Plumbum |
| Sulfur | S | Es |
| pilak | Ag | Argentum |
| Carbon | C | Tse |
| Posporus | P | Sinabi ni Pe |
Mga formula ng kemikal ng mga simpleng sangkap
Ang mga pormula ng kemikal ng karamihan sa mga simpleng sangkap (lahat ng mga metal at maraming hindi metal) ay ang mga palatandaan ng mga kaukulang elemento ng kemikal.
Kaya sangkap na bakal At elementong kemikal na bakal ay itinalagang pareho - Fe .
Kung mayroon itong istrukturang molekular (umiiral sa anyo , pagkatapos ang formula nito ay ang kemikal na simbolo ng elementong may index kanang ibaba na nagpapahiwatig bilang ng mga atomo sa isang molekula: H 2, O2, O 3, N 2, F 2, Cl2, BR 2, P 4, S 8.
Talahanayan 3: Impormasyong ibinigay ng isang simbolo ng kemikal
| Katalinuhan | Gamit ang C bilang isang halimbawa |
| Pangalan ng sangkap | Carbon (brilyante, grapayt, graphene, carbyne) |
| Pag-aari ng isang elemento sa isang partikular na klase ng mga elemento ng kemikal | Hindi metal |
| Isang atom ng isang elemento | 1 carbon atom |
| Relatibong atomic mass (Ar) elemento na bumubuo ng isang sangkap | Ar(C) = 12 |
| Ganap na atomic mass | M(C) = 12 1.66 10-24 = 19.93 10 -24 g |
| Isang sangkap | 1 mole ng carbon, i.e. 6.02 10 23 mga atomo ng carbon |
| M (C) = Ar (C) = 12 g/mol |
Mga formula ng kemikal ng mga kumplikadong sangkap
Ang pormula ng isang kumplikadong sangkap ay inihanda sa pamamagitan ng pagsusulat ng mga palatandaan ng mga elemento ng kemikal kung saan ang sangkap ay binubuo, na nagpapahiwatig ng bilang ng mga atomo ng bawat elemento sa molekula. Sa kasong ito, bilang panuntunan, ang mga elemento ng kemikal ay nakasulat sa pagkakasunud-sunod ng pagtaas ng electronegativity alinsunod sa sumusunod na praktikal na serye:
Ako, Si, B, Te, H, P, As, I, Se, C, S, Br, Cl, N, O, F
Halimbawa, H2O , CaSO4 , Al2O3 , CS 2 , NG 2 , NaH.
Ang mga pagbubukod ay:
- ilang mga compound ng nitrogen na may hydrogen (halimbawa, ammonia NH 3 , hydrazine N 2H 4 );
- mga asin ng mga organikong acid (halimbawa, sodium formate HCOONa , calcium acetate (CH 3COO) 2Ca) ;
- hydrocarbon ( CH 4 , C2H4 , C2H2 ).
Mga kemikal na formula ng mga sangkap na umiiral sa anyo dimer (HINDI 2 , P2O 3 , P2O5, mga asin ng monovalent mercury, halimbawa: HgCl , HgNO3 atbp.), nakasulat sa form N 2 O4,P 4 O6,P 4 O 10Hg 2 Cl2,Hg 2 ( HINDI 3) 2 .
Ang bilang ng mga atom ng isang elemento ng kemikal sa isang molekula at isang kumplikadong ion ay tinutukoy batay sa konsepto valency o mga estado ng oksihenasyon at naitala index sa kanang ibaba mula sa tanda ng bawat elemento (inalis ang index 1). Sa kasong ito, nagpapatuloy sila mula sa panuntunan:
ang algebraic na kabuuan ng mga estado ng oksihenasyon ng lahat ng mga atomo sa isang molekula ay dapat na katumbas ng zero (ang mga molekula ay neutral sa kuryente), at sa isang kumplikadong ion - ang singil ng ion.
Halimbawa:
2Al 3 + +3SO 4 2- =Al 2 (SO 4) 3
Ang parehong panuntunan ay ginagamit kapag tinutukoy ang estado ng oksihenasyon ng isang elemento ng kemikal gamit ang formula ng isang sangkap o kumplikado. Ito ay karaniwang isang elemento na may ilang mga estado ng oksihenasyon. Ang mga estado ng oksihenasyon ng natitirang mga elemento na bumubuo ng molekula o ion ay dapat malaman.
Ang singil ng isang kumplikadong ion ay ang algebraic na kabuuan ng mga estado ng oksihenasyon ng lahat ng mga atomo na bumubuo sa ion. Samakatuwid, kapag tinutukoy ang estado ng oksihenasyon ng isang elemento ng kemikal sa isang kumplikadong ion, ang ion mismo ay inilalagay sa mga bracket, at ang singil nito ay tinanggal mula sa mga bracket.
Kapag nag-compile ng mga formula para sa valence ang isang sangkap ay kinakatawan bilang isang tambalan na binubuo ng dalawang particle ng iba't ibang uri, ang mga valencies nito ay kilala. Sunod nilang gamitin tuntunin:
sa isang molekula, ang produkto ng valence sa pamamagitan ng bilang ng mga particle ng isang uri ay dapat na katumbas ng produkto ng valence sa pamamagitan ng bilang ng mga particle ng isa pang uri.
Halimbawa:
Ang numero bago ang formula sa isang equation ng reaksyon ay tinatawag koepisyent. Siya ay nagpapahiwatig ng alinman bilang ng mga molekula, o bilang ng mga moles ng substance.
Ang koepisyent bago ang simbolo ng kemikal, ay nagpapahiwatig bilang ng mga atom ng isang ibinigay na elemento ng kemikal, at sa kaso kapag ang sign ay ang formula ng isang simpleng substance, ang coefficient ay nagpapahiwatig ng alinman bilang ng mga atomo, o ang bilang ng mga moles ng sangkap na ito.
Halimbawa:
- 3 Fe– tatlong iron atoms, 3 moles ng iron atoms,
- 2 H– dalawang hydrogen atoms, 2 moles ng hydrogen atoms,
- H 2– isang molekula ng hydrogen, 1 mole ng hydrogen.
Ang mga pormula ng kemikal ng maraming mga sangkap ay natukoy nang eksperimento, kaya naman tinawag ang mga ito "empirical".
Talahanayan 4: Impormasyong ibinibigay ng chemical formula ng isang komplikadong substance
| Katalinuhan | Halimbawa C aCO3 |
| Pangalan ng sangkap | Kaltsyum carbonate |
| Pag-aari ng isang elemento sa isang tiyak na klase ng mga sangkap | Katamtamang (normal) na asin |
| Isang molekula ng sangkap | 1 molekula ng calcium carbonate |
| Isang nunal ng substance | 6.02 10 23 mga molekula CaCO3 |
| Relatibong molecular mass ng substance (Mr) | Мr (CaCO3) = Ar (Ca) +Ar (C) +3Ar (O) =100 |
| Molar mass ng substance (M) | M (CaCO3) = 100 g/mol |
| Ganap na molekular na masa ng sangkap (m) | M (CaCO3) = Mr (CaCO3) 1.66 10 -24 g = 1.66 10 -22 g |
| Qualitative composition (anong mga kemikal na elemento ang bumubuo sa substance) | calcium, carbon, oxygen |
| Dami ng komposisyon ng sangkap: | |
| Ang bilang ng mga atomo ng bawat elemento sa isang molekula ng isang sangkap: | isang molekula ng calcium carbonate ay binubuo ng 1 atom kaltsyum, 1 atom carbon at 3 mga atomo oxygen. |
| Ang bilang ng mga moles ng bawat elemento sa 1 mole ng substance: | Sa 1 nunal CaCO 3(6.02 · 10 23 molekula) na nilalaman 1 nunal(6.02 · 10 23 atoms) calcium, 1 nunal(6.02 10 23 atoms) ng carbon at 3 mol(3 6.02 10 23 atoms) ng kemikal na elementong oxygen) |
| Mass na komposisyon ng sangkap: | |
| Mass ng bawat elemento sa 1 mole ng substance: | Ang 1 mole ng calcium carbonate (100g) ay naglalaman ng mga sumusunod na elemento ng kemikal: 40g kaltsyum, 12g carbon, 48g oxygen. |
| Mga mass fraction ng mga elemento ng kemikal sa sangkap (komposisyon ng sangkap bilang isang porsyento ng timbang):
|
Komposisyon ng calcium carbonate ayon sa timbang:
W (Ca) = (n (Ca) Ar (Ca))/Mr (CaCO3) = (1·40)/100= 0.4 (40%) W (C) = (n (Ca) Ar (Ca))/Mr (CaCO3) = (1 12)/100 = 0.12 (12%) W (O) = (n (Ca) Ar (Ca))/Mr (CaCO3) = (3 16)/100 = 0.48 (48%) |
| Para sa isang sangkap na may isang ionic na istraktura (asin, acid, base), ang pormula ng sangkap ay nagbibigay ng impormasyon tungkol sa bilang ng mga ion ng bawat uri sa molekula, ang kanilang dami at ang masa ng mga ion bawat 1 mole ng sangkap:
|
Molecule CaCO 3 binubuo ng isang ion Ca 2+ at ion CO 3 2-
1 mol ( 6.02 10 23 mga molekula) CaCO 3 naglalaman ng 1 mol Ca 2+ ion At 1 taling ng mga ion CO 3 2-; Naglalaman ang 1 mole (100g) ng calcium carbonate 40g ion Ca 2+ At 60g ion CO 3 2- |
| Dami ng molar ng isang sangkap sa mga karaniwang kondisyon (para sa mga gas lamang) | |
Mga graphic na formula
Upang makakuha ng mas kumpletong impormasyon tungkol sa isang sangkap, gamitin mga graphic na formula , na nagpapahiwatig pagkakasunud-sunod ng koneksyon ng mga atomo sa isang molekula At valence ng bawat elemento.
Ang mga graphic na formula ng mga sangkap na binubuo ng mga molekula kung minsan, sa isang antas o iba pa, ay sumasalamin sa istraktura (istraktura) ng mga molekula na ito; sa mga kasong ito maaari silang tawaging istruktural .
Upang mag-compile ng graphical (structural) formula ng isang substance, kailangan mong:
- Tukuyin ang valence ng lahat ng elemento ng kemikal na bumubuo sa substance.
- Isulat ang mga palatandaan ng lahat ng elemento ng kemikal na bumubuo sa sangkap, bawat isa sa halagang katumbas ng bilang ng mga atomo ng isang partikular na elemento sa molekula.
- Ikonekta ang mga palatandaan ng mga elemento ng kemikal sa mga gitling. Ang bawat gitling ay tumutukoy sa isang pares na nakikipag-ugnayan sa pagitan ng mga elemento ng kemikal at samakatuwid ay pantay na kabilang sa parehong mga elemento.
- Ang bilang ng mga linya na nakapalibot sa tanda ng isang kemikal na elemento ay dapat tumugma sa valency ng kemikal na elementong ito.
- Kapag bumubuo ng mga acid na naglalaman ng oxygen at kanilang mga asing-gamot, ang mga atomo ng hydrogen at mga atom ng metal ay nakagapos sa elementong bumubuo ng acid sa pamamagitan ng isang atom ng oxygen.
- Ang mga atomo ng oxygen ay pinagsama sa isa't isa lamang kapag bumubuo ng mga peroxide.
Mga halimbawa ng mga graphic na formula:
Ang pormula para sa batayan ng buhay - tubig - ay kilala. Ang molekula nito ay binubuo ng dalawang hydrogen atoms at isang oxygen, na nakasulat bilang H2O. Kung mayroong dalawang beses na mas maraming oxygen, kung gayon ang isang ganap na magkakaibang sangkap ay makukuha - H2O2. Ano ito at paano mag-iiba ang nagreresultang sangkap sa "kamag-anak" na tubig nito?
H2O2 - ano ang sangkap na ito?
Tingnan natin ito nang mas detalyado. Ang H2O2 ay ang formula ng hydrogen peroxide, Oo, ang parehong ginagamit sa paggamot sa mga gasgas, puti. Hydrogen peroxide H2O2 - siyentipiko.
Para sa pagdidisimpekta, gumamit ng tatlong porsyento na solusyon ng peroxide. Sa dalisay o puro anyo, nagdudulot ito ng mga kemikal na paso sa balat. Ang tatlumpung porsyentong solusyon ng peroxide ay tinatawag na perhydrol; Dati, ito ay ginagamit sa mga tagapag-ayos ng buhok sa pagpapaputi ng buhok. Ang balat na nasunog nito ay nagiging puti din.
Mga kemikal na katangian ng H2O2
Ang hydrogen peroxide ay isang walang kulay na likido na may "metal" na lasa. Ito ay isang mahusay na solvent at madaling natutunaw sa tubig, eter, at alkohol.
Ang tatlo at anim na porsyentong peroxide solution ay kadalasang inihahanda sa pamamagitan ng pagtunaw ng tatlumpung porsyentong solusyon. Kapag nag-iimbak ng puro H2O2, ang sangkap ay nabubulok sa paglabas ng oxygen, kaya hindi ito dapat na nakaimbak sa mahigpit na selyadong mga lalagyan upang maiwasan ang pagsabog. Habang bumababa ang konsentrasyon ng peroxide, tumataas ang katatagan nito. Gayundin, upang pabagalin ang agnas ng H2O2, maaari kang magdagdag ng iba't ibang mga sangkap dito, halimbawa, phosphoric o salicylic acid. Upang mag-imbak ng mga solusyon ng mataas na konsentrasyon (higit sa 90 porsiyento), ang sodium pyrophosphate ay idinagdag sa peroxide, na nagpapatatag sa estado ng sangkap, at ginagamit din ang mga sisidlan ng aluminyo.

Ang H2O2 ay maaaring parehong oxidizing agent at reducing agent sa mga kemikal na reaksyon. Gayunpaman, mas madalas ang peroxide ay nagpapakita ng mga katangian ng oxidizing. Ang peroxide ay itinuturing na isang acid, ngunit isang napakahina; ang mga asin ng hydrogen peroxide ay tinatawag na peroxide.
bilang isang paraan ng paggawa ng oxygen
Ang decomposition reaction ng H2O2 ay nangyayari kapag ang substance ay nalantad sa mataas na temperatura (higit sa 150 degrees Celsius). Bilang resulta, nabuo ang tubig at oxygen.
Formula ng reaksyon - 2 H2O2 + t -> 2 H2O + O2
Ang estado ng oksihenasyon ng H sa H 2 O 2 at H 2 O = +1.
Katayuan ng oksihenasyon ng O: sa H 2 O 2 = -1, sa H 2 O = -2, sa O 2 = 0
2 O -1 - 2e -> O2 0
O -1 + e -> O -2
2 H2O2 = 2 H2O + O2
Ang hydrogen peroxide ay maaari ding mabulok sa temperatura ng silid kung gumamit ng isang katalista (isang kemikal na nagpapabilis sa reaksyon).
Sa mga laboratoryo, ang isa sa mga pamamaraan para sa paggawa ng oxygen, kasama ang decomposition ng berthollet salt o potassium permanganate, ay ang decomposition reaction ng peroxide. Sa kasong ito, ang manganese (IV) oxide ay ginagamit bilang isang katalista. Ang iba pang mga sangkap na nagpapabilis sa pagkabulok ng H2O2 ay tanso, platinum, at sodium hydroxide.
Kasaysayan ng pagtuklas ng peroxide
Ang mga unang hakbang patungo sa pagtuklas ng peroxide ay ginawa noong 1790 ng German Alexander Humboldt, nang matuklasan niya ang pagbabago ng barium oxide sa peroxide kapag pinainit. Ang prosesong iyon ay sinamahan ng pagsipsip ng oxygen mula sa hangin. Makalipas ang labindalawang taon, ang mga siyentipiko na sina Tenard at Gay-Lussac ay nagsagawa ng isang eksperimento sa pagsunog ng mga alkali metal na may labis na oxygen, na nagreresulta sa sodium peroxide. Ngunit ang hydrogen peroxide ay nakuha nang maglaon, noong 1818 lamang, nang pag-aralan ni Louis Thénard ang epekto ng mga acid sa mga metal; isang mababang halaga ng oxygen ay kinakailangan para sa kanilang matatag na pakikipag-ugnayan. Ang pagsasagawa ng confirmatory experiment na may barium peroxide at sulfuric acid, ang siyentipiko ay nagdagdag ng tubig, hydrogen chloride at yelo sa kanila. Pagkaraan ng maikling panahon, natuklasan ni Tenar ang maliliit na patak ng frozen sa mga dingding ng lalagyan na may barium peroxide. Ito ay naging malinaw na ito ay H2O2. Pagkatapos ay binigyan nila ang nagresultang H2O2 ng pangalang "oxidized water." Ito ay hydrogen peroxide - isang walang kulay, walang amoy, mahirap na sumingaw na likido na mahusay na natutunaw ang iba pang mga sangkap. Ang resulta ng pakikipag-ugnayan ng H2O2 at H2O2 ay isang reaksyon ng dissociation, ang peroxide ay natutunaw sa tubig.

Ang isang kagiliw-giliw na katotohanan ay ang mga katangian ng bagong sangkap ay mabilis na natuklasan, na nagpapahintulot na magamit ito sa gawaing pagpapanumbalik. Si Tenar mismo, gamit ang peroxide, ay nagpanumbalik ng isang pagpipinta ni Raphael na nagdilim sa paglipas ng panahon.
Hydrogen peroxide noong ika-20 siglo
Pagkatapos ng maingat na pag-aaral ng nagresultang sangkap, nagsimula itong gawin sa isang pang-industriya na sukat. Sa simula ng ikadalawampu siglo, ang teknolohiyang electrochemical para sa paggawa ng peroxide, batay sa proseso ng electrolysis, ay ipinakilala. Ngunit ang buhay ng istante ng sangkap na nakuha sa pamamaraang ito ay maikli, mga ilang linggo. Ang purong peroxide ay hindi matatag, at sa karamihan ay ginawa ito sa tatlumpung porsyentong konsentrasyon para sa pagpapaputi ng mga tela at sa tatlo o anim na porsyentong konsentrasyon para sa mga pangangailangan sa sambahayan.
Ang mga siyentipiko sa Nazi Germany ay gumamit ng peroxide upang lumikha ng isang likidong gasolina na rocket engine, na ginamit para sa mga layunin ng pagtatanggol noong Ikalawang Digmaang Pandaigdig. Bilang resulta ng pakikipag-ugnayan ng H2O2 at methanol/hydrazine, nakuha ang malakas na gasolina, kung saan ang sasakyang panghimpapawid ay umabot sa bilis na higit sa 950 km/h.
Saan ginagamit ngayon ang H2O2?
- sa gamot - para sa pagpapagamot ng mga sugat;
- sa industriya ng pulp at papel ang mga katangian ng pagpapaputi ng sangkap ay ginagamit;
- sa industriya ng tela, ang natural at sintetikong tela, balahibo, at lana ay pinaputi ng peroxide;
- bilang rocket fuel o oxidizer nito;
- sa kimika - upang makabuo ng oxygen, bilang isang foaming agent para sa produksyon ng mga porous na materyales, bilang isang catalyst o hydrogenating agent;
- para sa paggawa ng mga disinfectant o mga ahente ng paglilinis, mga pampaputi;
- para sa pagpapaputi ng buhok (ito ay isang hindi napapanahong paraan, dahil ang buhok ay malubhang napinsala ng peroxide);

Ang hydrogen peroxide ay maaaring matagumpay na magamit upang malutas ang iba't ibang mga problema sa sambahayan. Ngunit tatlong porsyento lamang ng hydrogen peroxide ang maaaring gamitin para sa mga layuning ito. Narito ang ilang paraan:
- Upang linisin ang mga ibabaw, kailangan mong ibuhos ang peroxide sa isang lalagyan na may spray bottle at i-spray ito sa mga kontaminadong lugar.
- Upang disimpektahin ang mga bagay, kailangan itong punasan ng isang undiluted H2O2 solution. Makakatulong ito na linisin sila ng mga nakakapinsalang mikroorganismo. Ang paghuhugas ng mga espongha ay maaaring ibabad sa tubig na may peroxide (1:1 ratio).
- Upang paputiin ang mga tela, magdagdag ng isang baso ng peroxide kapag naghuhugas ng mga puting bagay. Maaari mo ring banlawan ang mga puting tela sa tubig na hinaluan ng isang baso ng H2O2. Ang pamamaraang ito ay nagpapanumbalik ng kaputian, pinoprotektahan ang mga tela mula sa pag-yellowing at tumutulong sa pag-alis ng mga matigas na mantsa.
- Upang labanan ang amag at amag, paghaluin ang peroxide at tubig sa isang 1:2 ratio sa isang lalagyan na may spray bottle. I-spray ang nagresultang timpla sa mga kontaminadong ibabaw at pagkatapos ng 10 minuto linisin ang mga ito gamit ang isang brush o espongha.
- Maaari mong i-renew ang madilim na grawt sa mga tile sa pamamagitan ng pag-spray ng peroxide sa mga nais na lugar. Pagkatapos ng 30 minuto, kailangan mong lubusan na kuskusin ang mga ito gamit ang isang matigas na brush.
- Upang maghugas ng mga pinggan, magdagdag ng kalahating baso ng H2O2 sa isang buong palanggana ng tubig (o isang lababo na may saradong kanal). Ang mga tasa at plato na hinugasan sa solusyon na ito ay magniningning nang malinis.
- Upang linisin ang iyong toothbrush, kailangan mong isawsaw ito sa isang undiluted na tatlong porsyento na solusyon ng peroxide. Pagkatapos ay banlawan sa ilalim ng malakas na tubig na tumatakbo. Ang pamamaraang ito ay mahusay na nagdidisimpekta ng mga bagay sa kalinisan.
- Upang disimpektahin ang mga biniling gulay at prutas, dapat mong i-spray ang isang solusyon ng 1 bahagi ng peroxide at 1 bahagi ng tubig sa kanila, pagkatapos ay banlawan ang mga ito nang lubusan ng tubig (maaaring malamig).
- Sa iyong summer cottage, gamit ang H2O2 maaari mong labanan ang mga sakit ng halaman. Kailangan mong i-spray ang mga ito ng isang solusyon ng peroxide o ibabad ang mga buto sa ilang sandali bago itanim sa 4.5 litro ng tubig na may halong 30 ML ng apatnapung porsyento na hydrogen peroxide.
- Upang buhayin ang aquarium fish, kung sila ay nalason ng ammonia, na-suffocate kapag ang aeration ay naka-off, o para sa ibang dahilan, maaari mong subukang ilagay ang mga ito sa tubig na may hydrogen peroxide. Kailangan mong paghaluin ang tatlong porsyento na peroxide sa tubig sa rate na 30 ml bawat 100 litro at ilagay ang walang buhay na isda sa nagresultang timpla sa loob ng 15-20 minuto. Kung hindi sila nabuhay sa panahong ito, kung gayon ang lunas ay hindi nakatulong.

Kahit na bilang isang resulta ng masiglang pag-alog ng isang bote ng tubig, ang isang tiyak na halaga ng peroxide ay nabuo sa loob nito, dahil ang tubig ay puspos ng oxygen sa panahon ng pagkilos na ito.
Ang mga sariwang prutas at gulay ay naglalaman din ng H2O2 hanggang sa maluto. Kapag ang pag-init, pagluluto, pagprito at iba pang mga proseso na may kasamang mataas na temperatura, isang malaking halaga ng oxygen ay nawasak. Ito ang dahilan kung bakit ang mga lutong pagkain ay itinuturing na hindi gaanong malusog, bagaman ang ilang mga bitamina ay nananatili sa kanila. Ang mga sariwang kinatas na juice o oxygen cocktail na inihahain sa mga sanatorium ay kapaki-pakinabang para sa parehong dahilan - dahil sa saturation na may oxygen, na nagbibigay sa katawan ng bagong lakas at nililinis ito.
Panganib ng peroxide kapag kinain
Pagkatapos ng itaas, maaaring mukhang ang peroxide ay maaaring partikular na kunin nang pasalita, at ito ay makikinabang sa katawan. Ngunit ito ay hindi totoo sa lahat. Sa tubig o juice, ang tambalan ay matatagpuan sa kaunting dami at malapit na nauugnay sa iba pang mga sangkap. Ang pagkuha ng "hindi natural" na hydrogen peroxide sa loob (at lahat ng peroxide na binili sa isang tindahan o ginawa bilang resulta ng mga eksperimento sa kemikal ay hindi maaaring ituring na natural, at mayroon ding masyadong mataas na konsentrasyon kumpara sa natural) ay maaaring humantong sa mga panganib sa buhay at kalusugan na kahihinatnan. Upang maunawaan kung bakit, kailangan nating bumaling muli sa kimika.
Tulad ng nabanggit na, sa ilalim ng ilang mga kundisyon, ang hydrogen peroxide ay nasisira at naglalabas ng oxygen, na isang aktibong oxidizing agent. maaaring mangyari kapag ang H2O2 ay bumangga sa peroxidase, isang intracellular enzyme. Ang paggamit ng peroxide para sa pagdidisimpekta ay batay sa mga katangian ng oxidizing nito. Kaya, kapag ang isang sugat ay ginagamot ng H2O2, ang inilabas na oxygen ay sumisira sa mga nabubuhay na pathogenic microorganism na nakapasok dito. Ito ay may parehong epekto sa iba pang mga buhay na selula. Kung tinatrato mo ang buo na balat na may peroxide at pagkatapos ay punasan ang ginagamot na lugar na may alkohol, makakaramdam ka ng nasusunog na pandamdam, na nagpapatunay sa pagkakaroon ng microscopic na pinsala pagkatapos ng peroxide. Ngunit kapag ang mababang konsentrasyon ng peroxide ay ginagamit sa labas, walang kapansin-pansing pinsala sa katawan.

Isa pang bagay kung susubukan mong dalhin ito nang pasalita. Ang sangkap na iyon, na maaaring makapinsala kahit na medyo makapal na balat sa labas, ay napupunta sa mauhog lamad ng digestive tract. Iyon ay, nangyayari ang mga kemikal na mini-burn. Siyempre, ang inilabas na ahente ng oxidizing - oxygen - ay maaari ring pumatay ng mga nakakapinsalang mikrobyo. Ngunit ang parehong proseso ay mangyayari sa mga selula ng lagay ng pagkain. Kung ang pagkasunog bilang isang resulta ng pagkilos ng ahente ng oxidizing ay paulit-ulit, pagkatapos ay ang pagkasayang ng mauhog lamad ay posible, at ito ang unang hakbang sa landas sa kanser. Ang pagkamatay ng mga selula ng bituka ay humahantong sa kawalan ng kakayahan ng katawan na sumipsip ng mga sustansya, na nagpapaliwanag, halimbawa, pagbaba ng timbang at pagkawala ng paninigas ng dumi sa ilang mga tao na nagsasagawa ng "paggamot" na may peroxide.
Hiwalay, kinakailangang sabihin ang tungkol sa pamamaraang ito ng paggamit ng peroxide, tulad ng mga intravenous injection. Kahit na sa ilang kadahilanan ay inireseta sila ng isang doktor (maaari lamang itong bigyang katwiran sa kaso ng pagkalason sa dugo, kapag walang iba pang angkop na gamot na magagamit), pagkatapos ay sa ilalim ng pangangasiwa ng medikal at may mahigpit na pagkalkula ng dosis, mayroon pa ring mga panganib. Ngunit sa ganitong matinding sitwasyon, ito ay isang pagkakataon para sa pagbawi. Sa anumang pagkakataon dapat kang magreseta ng mga iniksyon ng hydrogen peroxide sa iyong sarili. Ang H2O2 ay nagdudulot ng malaking panganib sa mga selula ng dugo - mga pulang selula ng dugo at mga platelet, dahil sinisira nito ang mga ito kapag ito ay pumasok sa daluyan ng dugo. Bilang karagdagan, ang isang nakamamatay na pagbara ng mga daluyan ng dugo ng inilabas na oxygen ay maaaring mangyari - isang gas embolism.
Mga pag-iingat sa kaligtasan para sa paghawak ng H2O2
- Iwasang maabot ng mga bata at mga taong may kapansanan. Ang kakulangan ng amoy at kakaibang lasa ay ginagawang mas mapanganib para sa kanila ang peroxide, dahil ang malalaking dosis ay maaaring inumin. Kung ang solusyon ay nakapasok sa loob, ang mga kahihinatnan ng paggamit ay maaaring hindi mahuhulaan. Dapat kang kumunsulta kaagad sa isang doktor.
- Ang mga solusyon sa peroxide na may konsentrasyon na higit sa tatlong porsyento ay nagdudulot ng paso kung sila ay nadikit sa balat. Ang lugar ng paso ay dapat hugasan ng maraming tubig.

- Huwag hayaang makapasok ang peroxide solution sa iyong mga mata, dahil magdudulot ito ng pamamaga, pamumula, pangangati, at kung minsan ay pananakit. Ang pangunang lunas bago makipag-ugnay sa isang doktor ay ang paghuhugas ng mata nang sagana sa tubig.
- Itago ang sangkap sa paraang malinaw na ito ay H2O2, iyon ay, sa isang lalagyan na may sticker upang maiwasan ang hindi sinasadyang paggamit para sa iba pang mga layunin.
- Ang mga kondisyon ng imbakan na nagpapahaba ng buhay nito ay isang madilim, tuyo, malamig na lugar.
- Ang hydrogen peroxide ay hindi dapat ihalo sa anumang likido maliban sa malinis na tubig, kabilang ang chlorinated tap water.
- Ang lahat ng nasa itaas ay nalalapat hindi lamang sa H2O2, kundi pati na rin sa lahat ng mga paghahanda na naglalaman nito.
2.1. Wikang kimikal at mga bahagi nito
Gumagamit ang sangkatauhan ng maraming iba't ibang wika. Maliban sa natural na mga wika(Japanese, English, Russian - higit sa 2.5 thousand sa kabuuan), mayroon din mga artipisyal na wika, halimbawa, Esperanto. Kabilang sa mga artipisyal na wika ay mayroong mga wika iba-iba mga agham. Kaya, sa kimika ginagamit nila ang kanilang sarili, kemikal na wika.
Wikang kimikal– isang sistema ng mga simbolo at konsepto na idinisenyo para sa isang maikli, maikli at nakikitang pagtatala at paghahatid ng impormasyong kemikal.
Ang isang mensahe na nakasulat sa karamihan ng mga natural na wika ay nahahati sa mga pangungusap, mga pangungusap sa mga salita, at mga salita sa mga titik. Kung tinatawag nating mga bahagi ng wika ang mga pangungusap, salita at letra, matutukoy natin ang magkatulad na bahagi sa wikang kemikal (Talahanayan 2).
Talahanayan 2.Mga bahagi ng wikang kemikal
Imposibleng makabisado kaagad ang anumang wika; naaangkop din ito sa isang kemikal na wika. Samakatuwid, sa ngayon ay makikilala mo lamang ang mga pangunahing kaalaman ng wikang ito: matuto ng ilang "mga titik", matutong maunawaan ang kahulugan ng "mga salita" at "mga pangungusap". Sa dulo ng kabanatang ito ay ipapakilala sa iyo mga pangalan ang mga kemikal na sangkap ay isang mahalagang bahagi ng wikang kemikal. Habang nag-aaral ka ng chemistry, lalawak at lalalim ang iyong kaalaman sa chemical language.
KEMIKAL NA WIKA.
1. Anong mga artipisyal na wika ang alam mo (maliban sa mga nabanggit sa teksto ng aklat-aralin)?
2. Paano naiiba ang mga natural na wika sa mga artipisyal?
3. Sa iyong palagay, posible bang ilarawan ang mga phenomena ng kemikal nang hindi gumagamit ng wikang kemikal? Kung hindi, bakit hindi? Kung gayon, ano ang mga pakinabang at disadvantage ng naturang paglalarawan?
2.2. Mga simbolo ng elemento ng kemikal
Ang simbolo para sa isang kemikal na elemento ay kumakatawan sa elemento mismo o isang atom ng elementong iyon.
Ang bawat naturang simbolo ay isang pinaikling pangalan ng Latin ng isang elemento ng kemikal, na binubuo ng isa o dalawang titik ng alpabetong Latin (para sa alpabetong Latin, tingnan ang Apendise 1). Ang simbolo ay nakasulat na may malaking titik. Ang mga simbolo, gayundin ang mga pangalan ng Ruso at Latin ng ilang elemento, ay ibinibigay sa Talahanayan 3. Ang impormasyon tungkol sa pinagmulan ng mga pangalang Latin ay ibinigay din doon. Walang pangkalahatang tuntunin para sa pagbigkas ng mga simbolo, samakatuwid ang Talahanayan 3 ay nagpapakita rin ng "pagbasa" ng simbolo, iyon ay, kung paano binabasa ang simbolong ito sa formula ng kemikal.
Imposibleng palitan ang pangalan ng isang elemento ng isang simbolo sa oral speech, ngunit sa sulat-kamay o naka-print na mga teksto ito ay pinahihintulutan, ngunit hindi inirerekomenda. Union of Pure and Applied Chemistry (IUPAC).
Ang talahanayan 3 ay nagbibigay ng impormasyon sa 33 elemento lamang. Ito ang mga elemento na una mong makakaharap kapag nag-aaral ng chemistry. Ang mga pangalang Ruso (sa alpabetikong pagkakasunud-sunod) at mga simbolo ng lahat ng elemento ay ibinibigay sa Appendix 2.
Talahanayan 3.Mga pangalan at simbolo ng ilang elemento ng kemikal
Pangalan |
||||
Latin |
Pagsusulat |
|||
| - | Pagsusulat |
Pinagmulan |
- | - |
| Nitrogen | N itrogenium | Mula sa Griyego "nagsilang ng saltpeter" | "en" | |
| aluminyo | Sinabi ni Al uminium | Mula sa lat. "tawas" | "aluminyo" | |
| Argon | Ar gon | Mula sa Griyego "hindi aktibo" | "argon" | |
| Barium | Ba rium | Mula sa Griyego "mabigat" | "barium" | |
| Bor | B orum | Mula sa Arabic "puting mineral" | "boron" | |
| Bromine | Sinabi ni Br omum | Mula sa Griyego "mabango" | "bromine" | |
| Hydrogen | H hydrogenium | Mula sa Griyego "nagsilang ng tubig" | "abo" | |
| Helium | Siya lium | Mula sa Griyego "Araw" | "helium" | |
| bakal | Fe rrum | Mula sa lat. "tabak" | "ferrum" | |
| ginto | Au rum | Mula sa lat. "nasusunog" | "aurum" | |
| yodo | ako odum | Mula sa Griyego "lila" | "yodo" | |
| Potassium | K alium | Mula sa Arabic "lihiya" | "potassium" | |
| Kaltsyum | Ca lcium | Mula sa lat. "apog" | "calcium" | |
| Oxygen | O xygenium | Mula sa Griyego "pagbuo ng acid" | "O" | |
| Silicon | Si licium | Mula sa lat. "flint" | "silicium" | |
| Krypton | Kr ypton | Mula sa Griyego "nakatago" | "krypton" | |
| Magnesium | M a g nesium | Mula sa pangalan Tangway ng Magnesia | "magnesium" | |
| Manganese | M a n ganum | Mula sa Griyego "paglilinis" | "mangganeso" | |
| tanso | Cu prum | Mula sa Griyego pangalan O. Cyprus | "cuprum" | |
| Sosa | Na trium | Mula sa Arabic, "detergent" | "sodium" | |
| Neon | Ne sa | Mula sa Griyego "bago" | "neon" | |
| Nikel | Ni ccolum | Galing sa kanya. "St. Nicholas Copper" | "nickel" | |
| Mercury | H ydrar g yrum | Lat. "likidong pilak" | "hydrargyrum" | |
| Nangunguna | P lum b um | Mula sa lat. mga pangalan ng isang haluang metal ng tingga at lata. | "plumbum" | |
| Sulfur | S ulfur | Mula sa Sanskrit "nasusunog na pulbos" | "es" | |
| pilak | A r g entum | Mula sa Griyego "liwanag" | "argentum" | |
| Carbon | C arboneum | Mula sa lat. "uling" | "tse" | |
| Posporus | P hosporus | Mula sa Griyego "tagapagdala ng liwanag" | "peh" | |
| Fluorine | F luorum | Mula sa lat. pandiwa "daloy" | "fluorine" | |
| Chlorine | Cl orum | Mula sa Griyego "berde" | "chlorine" | |
| Chromium | C h r omium | Mula sa Griyego "kulay" | "chrome" | |
| Cesium | C ae s ium | Mula sa lat. "asul na langit" | "cesium" | |
| Sink | Z i n cum | Galing sa kanya. "lata" | "sink" | |
2.3. Mga formula ng kemikal
Ginagamit upang italaga ang mga kemikal na sangkap mga pormula ng kemikal.
Para sa mga molekular na sangkap, ang isang kemikal na formula ay maaaring magpahiwatig ng isang molekula ng sangkap na ito.
Maaaring mag-iba ang impormasyon tungkol sa isang substance, kaya may iba mga uri ng mga formula ng kemikal.
Depende sa pagkakumpleto ng impormasyon, ang mga formula ng kemikal ay nahahati sa apat na pangunahing uri: protozoa,
molekular, istruktural At spatial.
Ang mga subscript sa pinakasimpleng formula ay walang karaniwang divisor.
Ang index na "1" ay hindi ginagamit sa mga formula.
Mga halimbawa ng pinakasimpleng formula: tubig - H 2 O, oxygen - O, sulfur - S, phosphorus oxide - P 2 O 5, butane - C 2 H 5, phosphoric acid - H 3 PO 4, sodium chloride (table salt) - NaCl.
Ang pinakasimpleng formula ng tubig (H 2 O) ay nagpapakita na ang komposisyon ng tubig ay kinabibilangan ng elemento hydrogen(H) at elemento oxygen(O), at sa anumang bahagi (isang bahagi ay isang bahagi ng isang bagay na maaaring hatiin nang hindi nawawala ang mga katangian nito.) ng tubig, ang bilang ng mga atomo ng hydrogen ay dalawang beses sa bilang ng mga atomo ng oxygen.
Bilang ng mga particle, kasama ang bilang ng mga atomo, na tinutukoy ng isang Latin na titik N. Tinutukoy ang bilang ng mga atomo ng hydrogen - N H, at ang bilang ng mga atomo ng oxygen ay N O, kaya nating isulat iyan
O kaya N H: N O=2:1.
Ang pinakasimpleng formula ng phosphoric acid (H 3 PO 4) ay nagpapakita na ang phosphoric acid ay naglalaman ng mga atomo hydrogen, mga atomo posporus at mga atomo oxygen, at ang ratio ng mga bilang ng mga atom ng mga elementong ito sa anumang bahagi ng phosphoric acid ay 3:1:4, iyon ay
NH: N P: N O=3:1:4.

Ang pinakasimpleng formula ay maaaring i-compile para sa anumang indibidwal na kemikal na sangkap, at para sa isang molekular na sangkap, bilang karagdagan, maaari itong i-compile. molekular na formula.
Mga halimbawa ng molecular formula: tubig - H 2 O, oxygen - O 2, sulfur - S 8, phosphorus oxide - P 4 O 10, butane - C 4 H 10, phosphoric acid - H 3 PO 4.
Ang mga non-molecular substance ay walang molecular formula.
Ang pagkakasunud-sunod ng pagsulat ng mga simbolo ng elemento sa simple at molekular na mga formula ay tinutukoy ng mga tuntunin ng kemikal na wika, na magiging pamilyar ka sa iyong pag-aaral ng kimika. Ang impormasyong ipinadala ng mga formula na ito ay hindi apektado ng pagkakasunud-sunod ng mga simbolo.
Sa mga palatandaan na sumasalamin sa istraktura ng mga sangkap, gagamitin lamang natin sa ngayon valence stroke("gitling"). Ang tanda na ito ay nagpapakita ng presensya sa pagitan ng mga atomo ng tinatawag na covalent bond(kung anong uri ng koneksyon ito at kung ano ang mga tampok nito, malalaman mo sa lalong madaling panahon).

Sa isang molekula ng tubig, ang isang atom ng oxygen ay konektado sa pamamagitan ng simpleng (iisang) mga bono sa dalawang atomo ng hydrogen, ngunit ang mga atomo ng hydrogen ay hindi konektado sa isa't isa. Ito ay tiyak kung ano ang malinaw na ipinapakita ng structural formula ng tubig. ![]()
Isa pang halimbawa: ang sulfur molecule S8. Sa molekula na ito, 8 sulfur atoms ang bumubuo ng isang walong miyembro na singsing, kung saan ang bawat sulfur atom ay konektado sa dalawa pang atom sa pamamagitan ng simpleng mga bono. Ihambing ang structural formula ng sulfur sa three-dimensional na modelo ng molekula nito na ipinapakita sa Fig. 3. Pakitandaan na ang pormula ng istruktura ng asupre ay hindi nagbibigay ng hugis ng molekula nito, ngunit nagpapakita lamang ng pagkakasunod-sunod ng koneksyon ng mga atomo sa pamamagitan ng mga covalent bond.

Ang pormula ng istruktura ng phosphoric acid ay nagpapakita na sa molekula ng sangkap na ito ang isa sa apat na oxygen atoms ay konektado lamang sa phosphorus atom sa pamamagitan ng isang double bond, at ang phosphorus atom, naman, ay konektado sa tatlong higit pang oxygen atoms sa pamamagitan ng mga single bond. . Ang bawat isa sa tatlong mga atomo ng oxygen na ito ay konektado din sa pamamagitan ng isang simpleng bono sa isa sa tatlong mga atomo ng hydrogen na nasa molekula.
Ihambing ang sumusunod na three-dimensional na modelo ng isang methane molecule sa spatial, structural at molecular formula nito:
|
|
|
Sa spatial formula ng methane, ang mga valence stroke na hugis wedge, na parang sa pananaw, ay nagpapakita kung alin sa mga hydrogen atoms ang "mas malapit sa atin" at kung alin ang "mas malayo sa atin".
Minsan ang spatial formula ay nagpapahiwatig ng mga haba ng bono at mga anggulo sa pagitan ng mga bono sa isang molekula, tulad ng ipinapakita sa halimbawa ng isang molekula ng tubig.

Ang mga non-molecular substance ay hindi naglalaman ng mga molecule. Para sa kaginhawahan ng mga kalkulasyon ng kemikal sa isang non-molecular substance, ang tinatawag na yunit ng formula.
Mga halimbawa ng komposisyon ng mga formula unit ng ilang substance: 1) silicon dioxide (quartz sand, quartz) SiO 2 – isang formula unit ay binubuo ng isang silicon atom at dalawang oxygen atoms; 2) sodium chloride (table salt) NaCl – ang formula unit ay binubuo ng isang sodium atom at isang chlorine atom; 3) iron Fe - isang formula unit ay binubuo ng isang iron atom. Tulad ng isang molekula, ang isang formula unit ay ang pinakamaliit na bahagi ng isang substance na nagpapanatili ng mga kemikal na katangian nito.
Talahanayan 4
Impormasyong inihahatid ng iba't ibang uri ng mga formula
Uri ng formula |
Ang impormasyong inihatid ng formula. |
|
| Ang pinakasimple Molekular Structural Spatial |
|
|
Isaalang-alang natin ngayon, gamit ang mga halimbawa, kung anong impormasyon ang ibinibigay sa atin ng iba't ibang uri ng mga formula.
1. Substansya: acetic acid. Ang pinakasimpleng formula ay CH 2 O, ang molecular formula ay C 2 H 4 O 2, structural formula

Ang pinakasimpleng formula nagsasabi sa amin na
1) ang acetic acid ay naglalaman ng carbon, hydrogen at oxygen;
2) sa sangkap na ito ang bilang ng mga carbon atom ay nauugnay sa bilang ng mga atomo ng hydrogen at ang bilang ng mga atomo ng oxygen, bilang 1: 2: 1, iyon ay N H: N C: N O = 1:2:1.
Molecular formula dagdag niyan
3) sa isang molekula ng acetic acid mayroong 2 carbon atoms, 4 hydrogen atoms at 2 oxygen atoms.
Pormula sa istruktura dagdag niyan
4, 5) sa isang molekula dalawang carbon atoms ay konektado sa isa't isa sa pamamagitan ng isang simpleng bono; ang isa sa kanila, bilang karagdagan, ay konektado sa tatlong atomo ng hydrogen, bawat isa ay may isang solong bono, at ang isa pa sa dalawang atomo ng oxygen, ang isa ay may dobleng bono at ang isa ay may isang solong bono; ang huling oxygen atom ay konektado pa rin sa pamamagitan ng isang simpleng bono sa ikaapat na hydrogen atom.
2. Substansya: sodium chloride.
Ang pinakasimpleng formula ay NaCl.
1) Ang sodium chloride ay naglalaman ng sodium at chlorine.
2) Sa sangkap na ito, ang bilang ng sodium atoms ay katumbas ng bilang ng chlorine atoms.
3. Substansya: bakal.
Ang pinakasimpleng formula ay Fe.
1) Ang sangkap na ito ay naglalaman lamang ng bakal, iyon ay, ito ay isang simpleng sangkap.
4. Substansya: trimetaphosphoric acid . Ang pinakasimpleng formula ay HPO 3, molecular formula ay H 3 P 3 O 9, structural formula
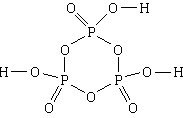
1) Ang trimetaphosphoric acid ay naglalaman ng hydrogen, phosphorus at oxygen.
2) N H: N P: N O = 1:1:3.
3) Ang molekula ay binubuo ng tatlong hydrogen atoms, tatlong phosphorus atoms at siyam na oxygen atoms.
4, 5) Tatlong phosphorus atoms at tatlong oxygen atoms, alternating, ay bumubuo ng anim na miyembro na cycle. Ang lahat ng mga koneksyon sa cycle ay simple. Ang bawat phosphorus atom ay, bilang karagdagan, ay konektado sa dalawa pang oxygen atoms, ang isa ay may double bond at ang isa ay may isang solong bond. Ang bawat isa sa tatlong mga atomo ng oxygen na konektado sa pamamagitan ng simpleng mga bono sa mga atomo ng posporus ay konektado din ng isang simpleng bono sa isang atom ng hydrogen.
| Phosphoric acid – H 3 PO 4(isa pang pangalan ay orthophosphoric acid) ay isang transparent, walang kulay, mala-kristal na sangkap ng molekular na istraktura na natutunaw sa 42 o C. Ang sangkap na ito ay natutunaw nang mahusay sa tubig at kahit na sumisipsip ng singaw ng tubig mula sa hangin (hygroscopic). Ang phosphoric acid ay ginawa sa maraming dami at pangunahing ginagamit sa paggawa ng mga phosphate fertilizers, ngunit din sa industriya ng kemikal, sa paggawa ng mga posporo at maging sa konstruksyon. Bilang karagdagan, ang phosphoric acid ay ginagamit sa paggawa ng semento sa teknolohiya ng ngipin at kasama sa maraming mga gamot. Ang acid na ito ay medyo mura, kaya sa ilang mga bansa, tulad ng Estados Unidos, ang napakadalisay na phosphoric acid, na lubos na natunaw ng tubig, ay idinagdag sa mga nakakapreskong inumin upang palitan ang mahal na sitriko acid. |
| Methane - CH 4. Kung mayroon kang gas stove sa bahay, pagkatapos ay nakatagpo ka ng sangkap na ito araw-araw: ang natural na gas na nasusunog sa mga burner ng iyong kalan ay binubuo ng 95% methane. Ang methane ay isang walang kulay at walang amoy na gas na may boiling point na –161 o C. Kapag inihalo sa hangin, ito ay sumasabog, na nagpapaliwanag sa mga pagsabog at sunog na kung minsan ay nangyayari sa mga minahan ng karbon (isa pang pangalan para sa methane ay firedamp). Ang ikatlong pangalan para sa methane - swamp gas - ay dahil sa ang katunayan na ang mga bula ng partikular na gas na ito ay tumaas mula sa ilalim ng mga swamp, kung saan ito ay nabuo bilang isang resulta ng aktibidad ng ilang mga bakterya. Sa industriya, ang methane ay ginagamit bilang panggatong at hilaw na materyal para sa paggawa ng iba pang mga sangkap. Ang methane ay ang pinakasimpleng haydrokarbon. Kasama rin sa klase ng mga substance ang ethane (C 2 H 6), propane (C 3 H 8), ethylene (C 2 H 4), acetylene (C 2 H 2) at marami pang ibang substance. |
Talahanayan 5.Mga halimbawa ng iba't ibang uri ng mga formula para sa ilang mga sangkap-



