बेंजीन की चक्रीय संरचना सबसे पहले एफ.ए. द्वारा प्रस्तावित की गई थी। 1865 में केकुले

फ्रेडरिक ऑगस्ट केकुले वॉन स्ट्राडोनिट्ज़ 19वीं सदी के एक उत्कृष्ट जर्मन रसायनज्ञ थे। 1854 में, उन्होंने सल्फर युक्त पहले कार्बनिक यौगिक की खोज की - थियोएसेटिक एसिड (थियोएथेनोइक एसिड)। इसके अलावा, उन्होंने डायज़ो यौगिकों की संरचना की स्थापना की। हालांकि, रसायन विज्ञान के विकास में उनका सबसे प्रसिद्ध योगदान बेंजीन (1866) की संरचना की स्थापना है। केकुले ने दिखाया कि बेंजीन के दोहरे बंधन रिंग के चारों ओर वैकल्पिक होते हैं (यह विचार पहली बार उन्हें एक सपने में आया था)। बाद में उन्होंने दिखाया कि दो संभावित दोहरे बंधन व्यवस्था समान हैं और बेंजीन की अंगूठी दो संरचनाओं के बीच एक संकर है। इस प्रकार, उन्होंने प्रतिध्वनि (मेसोमेरिज़्म) की अवधारणा का अनुमान लगाया, जो 1930 के दशक की शुरुआत में रासायनिक बंधन के सिद्धांत में दिखाई दी।
यदि बेंजीन में वास्तव में ऐसी संरचना होती है, तो इसके 1,2-प्रतिस्थापित डेरिवेटिव में प्रत्येक में दो आइसोमर होने चाहिए। उदाहरण के लिए,

हालांकि, 1,2-प्रतिस्थापित बेंजीन में से कोई भी दो आइसोमर्स को अलग नहीं कर सकता है।
इसलिए, केकुले ने बाद में सुझाव दिया कि बेंजीन अणु दो संरचनाओं के रूप में मौजूद है जो तेजी से एक दूसरे में गुजरते हैं:

ध्यान दें कि बेंजीन अणुओं और उनके डेरिवेटिव के इस तरह के योजनाबद्ध प्रतिनिधित्व आमतौर पर बेंजीन रिंग के कार्बन परमाणुओं से जुड़े हाइड्रोजन परमाणुओं को नहीं दर्शाते हैं।
आधुनिक रसायन विज्ञान में, बेंजीन अणु को इन दो सीमित गुंजयमान रूपों के गुंजयमान संकर के रूप में माना जाता है (देखें खंड 2.1)। बेंजीन अणु का एक अन्य विवरण इसके आणविक कक्षकों के विचार पर आधारित है। सेकंड में। 3.1, यह संकेत दिया गया था कि -बंधन कक्षकों में स्थित -इलेक्ट्रॉन बेंजीन रिंग के सभी कार्बन परमाणुओं के बीच स्थित होते हैं और एक -इलेक्ट्रॉन बादल बनाते हैं। इस प्रतिनिधित्व के अनुसार, बेंजीन अणु को पारंपरिक रूप से निम्नानुसार दर्शाया जा सकता है:
प्रायोगिक डेटा बेंजीन में ऐसी ही एक संरचना की उपस्थिति की पुष्टि करता है। यदि बेंजीन में तीन संयुग्मित दोहरे बंधनों के साथ मूल रूप से प्रस्तावित केकुले की संरचना थी, तो बेंजीन को एल्केन्स जैसी अतिरिक्त प्रतिक्रियाओं में प्रवेश करना होगा। हालांकि, जैसा कि ऊपर उल्लेख किया गया है, बेंजीन अतिरिक्त प्रतिक्रियाओं में प्रवेश नहीं करता है। इसके अलावा, बेंजीन तीन अलग-अलग दोहरे बंधनों की तुलना में अधिक स्थिर है। सेकंड में। 5.3 यह संकेत दिया गया था कि साइक्लोहेक्सेन के निर्माण के साथ बेंजीन के हाइड्रोजनीकरण की एन्थैल्पी का एक बड़ा नकारात्मक है
तालिका 18.3। विभिन्न कार्बन-कार्बन बंधों की लंबाई


चावल। 18.6. बेंजीन अणु की ज्यामितीय संरचना।
साइक्लोहेक्सिन के हाइड्रोजनीकरण की थैलीपी से तीन गुना अधिक मूल्य। इन मूल्यों के बीच के अंतर को आमतौर पर डेलोकलाइज़ेशन थैलेपी, गुंजयमान ऊर्जा या बेंजीन स्थिरीकरण ऊर्जा कहा जाता है।
बेंजीन रिंग में सभी कार्बन-कार्बन बॉन्ड की लंबाई समान होती है, जो अल्केन्स में CC बॉन्ड की लंबाई से कम होती है, लेकिन एल्केन्स में C=C बॉन्ड की लंबाई से लंबी होती है (सारणी 18.3)। यह पुष्टि करता है कि बेंजीन में कार्बन-कार्बन बॉन्ड सिंगल और डबल बॉन्ड के बीच एक हाइब्रिड हैं।
बेंजीन अणु की एक सपाट संरचना होती है, जिसे अंजीर में दिखाया गया है। 18.6.
भौतिक गुण
सामान्य परिस्थितियों में, बेंजीन एक रंगहीन तरल होता है जो 5.5 डिग्री सेल्सियस पर जम जाता है और 80 डिग्री सेल्सियस पर उबलता है। इसकी एक विशिष्ट सुखद गंध है, लेकिन, जैसा कि ऊपर उल्लेख किया गया है, अत्यधिक विषैला होता है। बेंजीन पानी के साथ अमिश्रणीय है, और बेंजीन प्रणाली में, पानी दो परतों के ऊपर बनता है। हालांकि, यह गैर-ध्रुवीय कार्बनिक सॉल्वैंट्स में घुलनशील है और स्वयं अन्य कार्बनिक यौगिकों के लिए एक अच्छा विलायक है।
रासायनिक गुण
यद्यपि बेंजीन कुछ अतिरिक्त अभिक्रियाओं में प्रवेश करता है (नीचे देखें), यह उनमें एल्केन्स की विशिष्ट प्रतिक्रियाशीलता प्रदर्शित नहीं करता है। उदाहरण के लिए, यह ब्रोमीन जल या α-आयन विलयन को रंगहीन नहीं करता है। इसके अलावा, बेंजीन
हाइड्रोक्लोरिक या सल्फ्यूरिक एसिड जैसे मजबूत एसिड के साथ अतिरिक्त प्रतिक्रियाओं में प्रवेश करता है।
उसी समय, बेंजीन कई इलेक्ट्रोफिलिक प्रतिस्थापन प्रतिक्रियाओं में भाग लेता है। सुगंधित यौगिक इस प्रकार की प्रतिक्रियाओं के उत्पाद हैं, क्योंकि इन प्रतिक्रियाओं में बेंजीन का डेलोकाइज्ड-इलेक्ट्रॉन सिस्टम संरक्षित है। बेंजीन रिंग पर हाइड्रोजन परमाणु के कुछ इलेक्ट्रोफाइल द्वारा प्रतिस्थापन की सामान्य क्रियाविधि का वर्णन भाग में किया गया है। 17.3. बेंजीन के इलेक्ट्रोफिलिक प्रतिस्थापन के उदाहरण इसके नाइट्रेशन, हैलोजनेशन, सल्फोनेशन और फ्रीडेल-क्राफ्ट्स प्रतिक्रियाएं हैं।
नाइट्रेशन। बेंजीन को सांद्र नाइट्रिक और सल्फ्यूरिक एसिड के मिश्रण के साथ इलाज करके नाइट्रेट किया जा सकता है (इसमें एक समूह का परिचय):

nitrobenzene
इस प्रतिक्रिया की शर्तें और इसके तंत्र को भाग में वर्णित किया गया है। 17.3.
नाइट्रोबेंजीन एक हल्के पीले रंग का तरल है जिसमें बादाम की विशिष्ट गंध होती है। बेंजीन के नाइट्रेशन के दौरान, नाइट्रोबेंजीन के अलावा, 1,3-डाइनिट्रोबेंजीन के क्रिस्टल भी बनते हैं, जो निम्नलिखित प्रतिक्रिया का उत्पाद है:

हैलोजनीकरण। यदि आप अंधेरे में बेंजीन को क्लोरीन या ब्रोमीन के साथ मिलाते हैं, तो कैंसर नहीं होगा। हालांकि, लुईस एसिड के गुणों वाले उत्प्रेरक की उपस्थिति में, ऐसे मिश्रणों में इलेक्ट्रोफिलिक प्रतिस्थापन प्रतिक्रियाएं होती हैं। इन प्रतिक्रियाओं के लिए विशिष्ट उत्प्रेरक लोहा (III) ब्रोमाइड और एल्यूमीनियम क्लोराइड हैं। इन उत्प्रेरकों की क्रिया यह है कि वे हलोजन अणुओं में ध्रुवीकरण पैदा करते हैं, जो तब उत्प्रेरक के साथ एक जटिल बनाते हैं:
हालांकि इस बात का कोई प्रत्यक्ष प्रमाण नहीं है कि इस मामले में मुक्त आयन बनते हैं। आयन वाहक के रूप में आयरन (III) ब्रोमाइड का उपयोग करते हुए बेंजीन ब्रोमिनेशन की क्रियाविधि को निम्नानुसार दर्शाया जा सकता है:

सल्फोनेशन। कई घंटों के लिए केंद्रित सल्फ्यूरिक एसिड के साथ अपने मिश्रण को रिफ्लक्स करके बेंजीन को सल्फोनेट किया जा सकता है (इसमें एक हाइड्रोजन परमाणु को एक सल्फो समूह के साथ बदल दिया जाता है)। इसके बजाय, बेंजीन को फ्यूमिंग सल्फ्यूरिक एसिड के साथ मिलाकर धीरे से गर्म किया जा सकता है। फ्यूमिंग सल्फ्यूरिक एसिड में सल्फर ट्राइऑक्साइड होता है। इस प्रतिक्रिया के तंत्र को योजना द्वारा दर्शाया जा सकता है

फ्राइडल-शिल्प प्रतिक्रियाएं। फ्राइडल-शिल्प प्रतिक्रियाओं को मूल रूप से निर्जल एल्यूमीनियम क्लोराइड उत्प्रेरक की उपस्थिति में सुगंधित यौगिकों और एल्काइल हैलाइड्स के बीच संक्षेपण प्रतिक्रिया कहा जाता था।
संघनन प्रतिक्रियाओं में, अभिकारकों के दो अणु (या एक अभिकारक) एक दूसरे के साथ संयुक्त होते हैं, एक नए यौगिक के अणु का निर्माण करते हैं, जबकि कुछ सरल यौगिक, जैसे पानी या हाइड्रोजन क्लोराइड का एक अणु, उनसे अलग (समाप्त) हो जाता है। .
वर्तमान में, फ्राइडल-शिल्प प्रतिक्रिया एक सुगंधित यौगिक का कोई इलेक्ट्रोफिलिक प्रतिस्थापन है जिसमें एक कार्बोकेशन या एक सकारात्मक चार्ज कार्बन परमाणु के साथ एक अत्यधिक ध्रुवीकृत परिसर एक इलेक्ट्रोफाइल की भूमिका निभाता है। इलेक्ट्रोफिलिक एजेंट आमतौर पर एक कार्बोक्जिलिक एसिड का एल्काइल हैलाइड या क्लोराइड होता है, हालांकि यह भी हो सकता है, उदाहरण के लिए, एक एल्केन या अल्कोहल। इन प्रतिक्रियाओं के लिए आमतौर पर निर्जल एल्यूमीनियम क्लोराइड उत्प्रेरक के रूप में उपयोग किया जाता है। फ्राइडल-शिल्प प्रतिक्रियाओं को आमतौर पर दो प्रकारों में विभाजित किया जाता है: क्षारीकरण और एसाइलेशन।
क्षारीकरण। इस प्रकार की फ्राइडल-क्राफ्ट्स प्रतिक्रियाओं में, बेंजीन रिंग में एक या एक से अधिक हाइड्रोजन परमाणुओं को अल्काइल समूहों द्वारा प्रतिस्थापित किया जाता है। उदाहरण के लिए, जब बेंजीन और क्लोरोमेथेन के मिश्रण को निर्जल एल्युमिनियम क्लोराइड की उपस्थिति में सावधानी से गर्म किया जाता है, तो मिथाइलबेन्जीन बनता है। इस प्रतिक्रिया में क्लोरोमेथेन एक इलेक्ट्रोफिलिक एजेंट की भूमिका निभाता है। यह एल्यूमीनियम क्लोराइड द्वारा उसी तरह ध्रुवीकृत होता है जैसे हलोजन अणुओं के साथ होता है:
विचाराधीन प्रतिक्रिया के तंत्र को निम्नानुसार दर्शाया जा सकता है:

यह ध्यान दिया जाना चाहिए कि बेंजीन और क्लोरोमेथेन के बीच इस संक्षेपण प्रतिक्रिया में, एक हाइड्रोजन क्लोराइड अणु अलग हो जाता है। हम यह भी नोट करते हैं कि मुक्त आयन के रूप में धातु कार्बोकेशन का वास्तविक अस्तित्व संदिग्ध है।
उत्प्रेरक की उपस्थिति में क्लोरोमेथेन के साथ बेंजीन का क्षारीकरण - निर्जल एल्यूमीनियम क्लोराइड मिथाइलबेनज़ीन के गठन के साथ समाप्त नहीं होता है। इस प्रतिक्रिया में, बेंजीन रिंग का और क्षारीकरण होता है, जिससे 1,2-डाइमिथाइलबेंजीन का निर्माण होता है:

एसाइलेशन। इस प्रकार की फ्राइडल-क्राफ्ट्स प्रतिक्रियाओं में, बेंजीन रिंग में एक हाइड्रोजन परमाणु को एक एसाइल समूह द्वारा प्रतिस्थापित किया जाता है, जिसके परिणामस्वरूप एक सुगंधित कीटोन बनता है।
एसाइल समूह का सामान्य सूत्र है
एक एसाइल यौगिक का व्यवस्थित नाम प्रत्यय और अंत -ओवा को संबंधित कार्बोक्जिलिक एसिड के नाम से बदलकर बनाया जाता है, जिसमें से दिया गया एसाइल यौगिक प्रत्यय -(o)yl के साथ एक व्युत्पन्न है। उदाहरण के लिए

एक निर्जल एल्यूमीनियम क्लोराइड उत्प्रेरक की उपस्थिति में एक कार्बोक्जिलिक एसिड के क्लोराइड या एनहाइड्राइड का उपयोग करके बेंजीन का एसाइलेशन किया जाता है। उदाहरण के लिए

यह प्रतिक्रिया एक संघनन है जिसमें हाइड्रोजन क्लोराइड अणु का उन्मूलन होता है। यह भी ध्यान दें कि "फिनाइल" नाम का प्रयोग अक्सर उन यौगिकों में बेंजीन की अंगूठी को दर्शाने के लिए किया जाता है जहां बेंजीन मुख्य समूह नहीं है:

जोड़ प्रतिक्रियाएं। यद्यपि बेंजीन इलेक्ट्रोफिलिक प्रतिस्थापन प्रतिक्रियाओं की सबसे विशेषता है, यह कुछ अतिरिक्त प्रतिक्रियाओं में भी प्रवेश करता है। हम उनमें से एक से पहले ही मिल चुके हैं। हम बेंजीन के हाइड्रोजनीकरण के बारे में बात कर रहे हैं (देखें खंड 5.3)। जब बेंजीन और हाइड्रोजन का मिश्रण 150-160 डिग्री सेल्सियस के तापमान पर बारीक पिसे निकल उत्प्रेरक की सतह पर पारित किया जाता है, तो प्रतिक्रियाओं का एक पूरा क्रम होता है, जो साइक्लोहेक्सेन के गठन के साथ समाप्त होता है। इस प्रतिक्रिया के लिए समग्र स्टोइकोमेट्रिक समीकरण को निम्नानुसार दर्शाया जा सकता है:

पराबैंगनी विकिरण या प्रत्यक्ष सूर्य के प्रकाश की क्रिया के तहत, बेंजीन भी क्लोरीन के साथ प्रतिक्रिया करता है। यह प्रतिक्रिया एक जटिल कट्टरपंथी तंत्र द्वारा की जाती है। इसका अंतिम उत्पाद 1,2,3,4,5,6-हेक्साक्लोरोसाइक्लोहेक्सेन है:

इसी तरह की प्रतिक्रिया पराबैंगनी विकिरण या सूर्य के प्रकाश की क्रिया के तहत बेंजीन और ब्रोमीन के बीच होती है।
ऑक्सीकरण। अन्य सुगंधित यौगिकों में बेंजीन और बेंजीन रिंग आमतौर पर पोटेशियम परमैंगनेट के अम्लीय या क्षारीय घोल जैसे मजबूत ऑक्सीकरण एजेंटों द्वारा भी ऑक्सीकरण के लिए प्रतिरोधी होते हैं। हालांकि, बेंजीन और अन्य एरोमेटिक्स हवा या ऑक्सीजन में जलकर एक बहुत ही धुँआदार लौ बनाते हैं, जो उच्च सापेक्ष कार्बन सामग्री वाले हाइड्रोकार्बन की विशेषता है।

प्रतिक्रियाओं का पहला समूह प्रतिस्थापन प्रतिक्रियाएं हैं। हमने कहा कि आण्विक संरचना में एरेन्स के कई बंधन नहीं होते हैं, लेकिन इसमें छह इलेक्ट्रॉनों की एक संयुग्मित प्रणाली होती है, जो बहुत स्थिर होती है और बेंजीन की अंगूठी को अतिरिक्त ताकत देती है। इसलिए, रासायनिक प्रतिक्रियाओं में, सबसे पहले, हाइड्रोजन परमाणुओं का प्रतिस्थापन होता है, न कि बेंजीन की अंगूठी का विनाश।
अल्केन्स के बारे में बात करते समय हम पहले ही प्रतिस्थापन प्रतिक्रियाओं का सामना कर चुके हैं, लेकिन उनके लिए ये प्रतिक्रियाएं एक कट्टरपंथी तंत्र के अनुसार आगे बढ़ीं, जबकि एरेन्स को प्रतिस्थापन प्रतिक्रियाओं के एक आयनिक तंत्र की विशेषता है।
प्रथमरासायनिक गुण - हलोजन। हैलोजन परमाणु के लिए हाइड्रोजन परमाणु का प्रतिस्थापन - क्लोरीन या ब्रोमीन।
गर्म होने पर और हमेशा उत्प्रेरक की भागीदारी के साथ प्रतिक्रिया आगे बढ़ती है। क्लोरीन के मामले में, यह एल्यूमीनियम क्लोराइड या आयरन क्लोराइड तीन हो सकता है। उत्प्रेरक हलोजन अणु का ध्रुवीकरण करता है, जिसके परिणामस्वरूप हेटेरोलाइटिक बंधन टूटता है और आयन प्राप्त होते हैं।
धनावेशित क्लोराइड आयन बेंजीन के साथ अभिक्रिया करता है।
यदि ब्रोमीन के साथ अभिक्रिया होती है, तो आयरन ट्राइब्रोमाइड या एल्युमिनियम ब्रोमाइड उत्प्रेरक का कार्य करता है।

यह ध्यान रखना महत्वपूर्ण है कि प्रतिक्रिया आणविक ब्रोमीन के साथ होती है न कि ब्रोमीन पानी के साथ। बेंजीन ब्रोमीन के पानी के साथ प्रतिक्रिया नहीं करता है।
बेंजीन होमोलॉग के हलोजन की अपनी विशेषताएं हैं। टोल्यूनि अणु में, मिथाइल समूह रिंग में प्रतिस्थापन की सुविधा देता है, प्रतिक्रियाशीलता बढ़ जाती है, और प्रतिक्रिया मामूली परिस्थितियों में होती है, यानी पहले से ही कमरे के तापमान पर।

यह ध्यान रखना महत्वपूर्ण है कि प्रतिस्थापन हमेशा ऑर्थो और पैरा स्थितियों में होता है, इसलिए आइसोमर्स का मिश्रण प्राप्त होता है।
दूसरासंपत्ति - बेंजीन का नाइट्रेशन, बेंजीन रिंग में नाइट्रो समूह की शुरूआत।
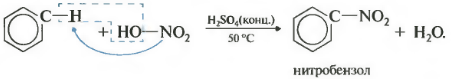
कड़वे बादाम की गंध के साथ एक भारी पीला तरल बनता है - नाइट्रोबेंजीन, इसलिए बेंजीन के लिए प्रतिक्रिया गुणात्मक हो सकती है। नाइट्रेशन के लिए, सांद्र नाइट्रिक और सल्फ्यूरिक एसिड के नाइट्रेटिंग मिश्रण का उपयोग किया जाता है। अभिक्रिया गर्म करके की जाती है।
आपको याद दिला दूं कि कोनोवलोव प्रतिक्रिया में अल्केन्स के नाइट्रेशन के लिए सल्फ्यूरिक एसिड को मिलाए बिना तनु नाइट्रिक एसिड का उपयोग किया गया था।
टोल्यूनि के नाइट्रेशन में, साथ ही हैलोजन में, ऑर्थो- और पैरा-आइसोमर्स का मिश्रण बनता है।
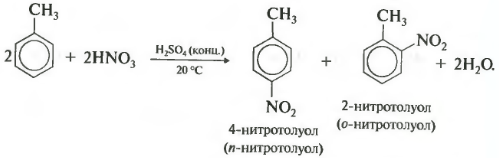
तीसरागुण - बेंजीन का हैलोऐल्केन के साथ क्षारीकरण।

यह प्रतिक्रिया बेंजीन रिंग में एक हाइड्रोकार्बन रेडिकल की शुरूआत की अनुमति देती है और इसे बेंजीन होमोलॉग प्राप्त करने की एक विधि माना जा सकता है। एल्युमिनियम क्लोराइड का उपयोग उत्प्रेरक के रूप में किया जाता है, जो हैलोकेन अणु के आयनों में अपघटन को बढ़ावा देता है। इसे गर्म करने की भी जरूरत है।
चौथीगुण - बेंजीन का एल्कीन के साथ क्षारीकरण।
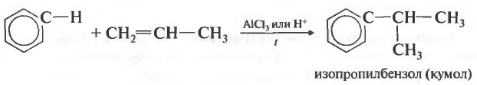
इस तरह, उदाहरण के लिए, कमीन या एथिलबेन्जीन प्राप्त किया जा सकता है। उत्प्रेरक एल्यूमीनियम क्लोराइड है।
2. बेंजीन के अलावा की प्रतिक्रियाएं
प्रतिक्रियाओं का दूसरा समूह जोड़ प्रतिक्रियाएं हैं। हमने कहा कि ये प्रतिक्रियाएं विशेषता नहीं हैं, लेकिन वे पाई-इलेक्ट्रॉन बादल के विनाश और छह सिग्मा बांडों के गठन के साथ कठोर परिस्थितियों में संभव हैं।
पांचवांसामान्य सूची में संपत्ति - हाइड्रोजनीकरण, हाइड्रोजन का जोड़।
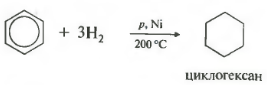
तापमान, दबाव, उत्प्रेरक निकल या प्लैटिनम। टोल्यूनि उसी तरह प्रतिक्रिया करने में सक्षम है।
छठासंपत्ति - क्लोरीनीकरण। कृपया ध्यान दें कि हम विशेष रूप से क्लोरीन के साथ बातचीत के बारे में बात कर रहे हैं, क्योंकि ब्रोमीन इस प्रतिक्रिया में प्रवेश नहीं करता है।
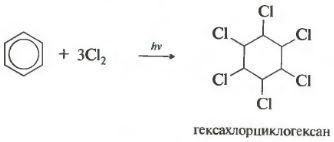
प्रतिक्रिया कठोर पराबैंगनी विकिरण के तहत आगे बढ़ती है। हेक्साक्लोरोसायक्लोहेक्सेन, हेक्साक्लोरेन का दूसरा नाम, बनता है, एक ठोस।
यह याद रखना महत्वपूर्ण है कि बेंजीन के लिए संभव नहींहाइड्रोजन हैलाइड्स (हाइड्रोहैलोजनेशन) और पानी (हाइड्रेशन) की जोड़ प्रतिक्रियाएँ।
3. बेंजीन होमोलॉग्स की साइड चेन में प्रतिस्थापन
प्रतिक्रियाओं का तीसरा समूह केवल बेंजीन होमोलॉग्स की चिंता करता है - यह साइड चेन में एक प्रतिस्थापन है।
सातवींसामान्य सूची में एक संपत्ति पार्श्व श्रृंखला में अल्फा कार्बन परमाणु पर हलोजन है।
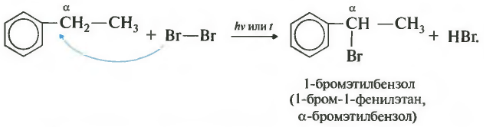
प्रतिक्रिया तब होती है जब गर्म या विकिरणित होता है, और हमेशा केवल अल्फा कार्बन पर। जैसे ही हलोजन जारी रहता है, दूसरा हलोजन परमाणु अल्फा स्थिति में वापस आ जाएगा।
4. बेंजीन समरूपों का ऑक्सीकरण
प्रतिक्रियाओं का चौथा समूह ऑक्सीकरण है।
बेंजीन की अंगूठी बहुत मजबूत है, इसलिए बेंजीन ऑक्सीकरण नहीं करता हैपोटैशियम परमैंगनेट - इसके विलयन का रंग नहीं बदलता है। यह याद रखना बहुत जरूरी है।
दूसरी ओर, बेंजीन समरूपों को गर्म करने पर पोटेशियम परमैंगनेट के अम्लीकृत घोल से ऑक्सीकृत किया जाता है। और यह आठवां रासायनिक गुण है।
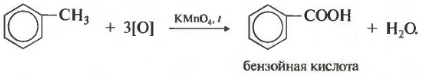
यह बेंजोइक एसिड निकलता है। समाधान का मलिनकिरण मनाया जाता है। इस मामले में, प्रतिस्थापक की कार्बन श्रृंखला कितनी भी लंबी क्यों न हो, यह हमेशा पहले कार्बन परमाणु के बाद टूट जाती है और अल्फा परमाणु बेंजोइक एसिड के गठन के साथ एक कार्बोक्सिल समूह में ऑक्सीकृत हो जाता है। शेष अणु संबंधित एसिड में ऑक्सीकृत हो जाता है या, यदि यह केवल एक कार्बन परमाणु है, तो कार्बन डाइऑक्साइड में।
यदि बेंजीन होमोलॉग में सुगंधित वलय पर एक से अधिक हाइड्रोकार्बन पदार्थ होते हैं, तो ऑक्सीकरण समान नियमों के अनुसार होता है - अल्फा स्थिति में कार्बन ऑक्सीकृत होता है।
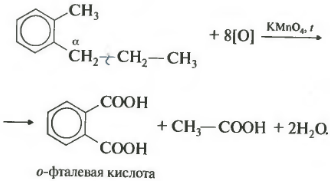
इस उदाहरण में, एक द्विक्षारकीय ऐरोमैटिक अम्ल प्राप्त होता है, जिसे phthalic अम्ल कहा जाता है।
एक विशेष तरीके से, मैं सल्फ्यूरिक एसिड की उपस्थिति में वायुमंडलीय ऑक्सीजन के साथ, क्यूमिन, आइसोप्रोपिलबेन्जीन के ऑक्सीकरण को नोट करता हूं।

यह फिनोल के उत्पादन के लिए तथाकथित कमीन विधि है। एक नियम के रूप में, फिनोल के उत्पादन से संबंधित मामलों में इस प्रतिक्रिया से निपटना पड़ता है। यह औद्योगिक तरीका है।
नौवांगुण - दहन, ऑक्सीजन के साथ पूर्ण ऑक्सीकरण। बेंजीन और उसके समरूप कार्बन डाइऑक्साइड और पानी को जलाते हैं।
आइए हम बेंजीन के दहन के समीकरण को सामान्य रूप में लिखें।
द्रव्यमान के संरक्षण के नियम के अनुसार, बाईं ओर उतने ही परमाणु होने चाहिए जितने दाईं ओर परमाणु हैं। क्योंकि रासायनिक प्रतिक्रियाओं में परमाणु कहीं नहीं जाते, लेकिन उनके बीच बंधनों का क्रम बस बदल जाता है। तो उतने ही कार्बन डाइऑक्साइड अणु होंगे जितने कि एक एरीन अणु में कार्बन परमाणु होते हैं, क्योंकि अणु में एक कार्बन परमाणु होता है। वह n CO2 अणु है। हाइड्रोजन परमाणुओं की तुलना में पानी के अणु दो गुना कम होंगे, यानी (2n-6) / 2, जिसका अर्थ है n-3।
बाईं ओर और दाईं ओर समान संख्या में ऑक्सीजन परमाणु होते हैं। दाईं ओर, कार्बन डाइऑक्साइड से 2n हैं, क्योंकि प्रत्येक अणु में दो ऑक्सीजन परमाणु होते हैं, साथ ही पानी से n-3, कुल 3n-3 के लिए। बाईं ओर, ऑक्सीजन परमाणुओं की संख्या समान है - 3n-3, जिसका अर्थ है कि आधे अणु हैं, क्योंकि अणु में दो परमाणु होते हैं। यानी (3n-3)/2 ऑक्सीजन अणु।
इस प्रकार, हमने सामान्य रूप में बेंजीन होमोलॉग के दहन के लिए समीकरण संकलित किया है।
अभिकर्मक की प्रकृति के आधार पर बेंजीन होमोलॉग एक सुगंधित नाभिक और एक साइड चेन (एल्काइल समूह) की भागीदारी के साथ दो दिशाओं में प्रतिक्रिया करने में सक्षम हैं।
1. सुगंधित नाभिक पर प्रतिक्रियाएं
एल्काइल समूह के दाता प्रभाव के कारण, प्रतिक्रियाएं S E ArH जाती हैं ऑर्थो- और जोड़ा- सुगंधित नाभिक की स्थिति, जबकि बेंजीन की तुलना में स्थितियां हल्की होती हैं।
ए) हलोजन

बी) नाइट्रेशन


ध्यान दें कि जैसे-जैसे स्वीकर्ता समूहों (-NO 2) की संख्या बढ़ती है, नाइट्रेशन प्रतिक्रियाओं का तापमान कैसे बढ़ता है।
सी) सल्फोनेशन

प्रतिक्रिया मुख्य रूप से उत्पन्न करती है पी-आइसोमर।
डी) क्षारीकरण

ई) एसाइलेशन

2. साइड चेन रिएक्शन
बेंजीन अणु का एल्काइल टुकड़ा कार्बन परमाणु की भागीदारी के साथ एस आर प्रतिक्रियाओं में प्रवेश करता है α -स्थिति (बेंज़िल स्थिति)।


बेंजीन केएमएनओ 4/100 डिग्री सेल्सियस के सभी समरूपों के ऑक्सीकरण से बेंजोइक एसिड बनता है।
संघनित अखाड़ा

संघनित एरेनास सुगंधित प्रणालियां हैं (एन = 2 और 3)। बेंजीन की तुलना में संघनित एरेन्स की सुगंध की डिग्री कम होती है। वे बेंजीन की तुलना में हल्के परिस्थितियों में होने वाली इलेक्ट्रोफिलिक प्रतिस्थापन प्रतिक्रियाओं, जोड़ और ऑक्सीकरण प्रतिक्रियाओं की विशेषता है।
नेफ़थलीन की प्रतिक्रियाशीलता
नेफ़थलीन के लिए एस ई एआरएच प्रतिक्रियाएं मुख्य रूप से आगे बढ़ती हैं α -स्थिति, सल्फोनेशन को छोड़कर। Ad E का इलेक्ट्रोफिलिक जोड़ 1,4 की स्थिति में आगे बढ़ता है, जबकि नेफ़थलीन संयुग्मित डायन के गुणों को प्रदर्शित करता है।
1. इलेक्ट्रोफिलिक प्रतिस्थापन प्रतिक्रियाएं,एस इ एआरएच


2. इलेक्ट्रोफिलिक जोड़, कमी और ऑक्सीकरण की प्रतिक्रियाएं।


एन्थ्रेसीन और फेनेंथ्रीन की प्रतिक्रियाशीलता
एन्थ्रेसीन के लिए इलेक्ट्रोफिलिक प्रतिस्थापन, एस ई एआरएच और इलेक्ट्रोफिलिक जोड़, विज्ञापन ई की प्रतिक्रियाएं मुख्य रूप से 9 और 10 पदों पर आगे बढ़ती हैं (नीचे दी गई योजना देखें)।

फेनेंथ्रीन के लिए इलेक्ट्रोफिलिक प्रतिस्थापन, एस ई एआरएच और इलेक्ट्रोफिलिक जोड़, विज्ञापन ई की प्रतिक्रियाएं मुख्य रूप से एंथ्रेसीन के लिए 9 और 10 पदों पर आगे बढ़ती हैं (नीचे चित्र देखें)।

एन्थ्रेसीन और फेनेंथ्रीन के लिए ऑक्सीकरण और कमी प्रतिक्रियाएं।


नेफ़थलीन पर आधारित कुछ दवाओं की संरचना, एन्थ्रेसीन और फेनेंथ्रीन
नेफ्थिज़िन(नाफ़ाज़ोलिन, सैनोरिन)

वाहिकासंकीर्णक क्रिया(राइनाइटिस, साइनसाइटिस का इलाज)
(शीर्षक में मूल संरचना को रेखांकित किया गया है, क्रमांकन पर ध्यान दें)
नैफ्टीफिन

ऐंटिफंगलक्रिया (त्वचा रोग का उपचार)
नबुमेटोन

विरोधी भड़काऊ, ज्वरनाशक, एनाल्जेसिक कार्रवाई(ऑस्टियोआर्थराइटिस, रुमेटीइड गठिया का उपचार)।
नादोलोल

(शब्द सीआईएस, इस मामले में, हाइड्रॉक्सिल समूहों की पारस्परिक व्यवस्था को दर्शाता है)
रक्तचाप(रक्तचाप कम करता है) और अतालतारोधी क्रिया
मॉर्फिन, कोडीन

अध्याय "एरिना" के लिए सुरक्षा प्रश्न
1. बेंजीन के कौन से गुण इसे अन्य असंतृप्त यौगिकों से अलग करते हैं - एल्केन्स, एल्काइन्स? "सुगंधित यौगिक" शब्द का क्या अर्थ है?
2. यौगिकों के संरचनात्मक सूत्र लिखिए: क) एथिलबेन्जीन; बी) 1,3-डाइमिथाइलबेंजीन ( एम -ज़ाइलीन); सी) 1,3,5-ट्राइमेथिलबेंजीन (मेसिटिलीन); डी) आइसोप्रोपिलबेंजीन (क्यूमिन); ई) 3-फेनिलपेंटेन; च) विनाइलबेंजीन (स्टाइरीन); छ) फेनिलएसिटिलीन; एच) ट्रांस -डिपेनाइलथिलीन ( ट्रांस -स्टिलबेन)।
3. सुगंधितता प्रदर्शित करने वाले यौगिकों की संरचनात्मक विशेषताओं का वर्णन करें। हुकेल का नियम लिखिए। निम्नलिखित में से कौन से यौगिक सुगंधित हैं?

4. संकेतित परिस्थितियों में साइक्लोहेक्सिन और बेंजीन के अनुपात की तुलना निम्नलिखित अभिकर्मकों से करें: : ए) भाई 2 (एच 2 ओ.20 सी); बी) केएमएनओ 4 (एच 2 ओह, 0 सी); सी) एच 2 इसलिए 4 (संक्षिप्त), 20 सी; घ) एच 2 (पीडी, 30 सी); इससे पहले 3 , फिर H 2 ओ (जेडएन); ई) एचबीआर।
5. निम्नलिखित अभिकर्मकों के साथ बेंजीन की प्रतिक्रियाओं में बनने वाले मोनोप्रतिस्थापित बेंजीन के संरचनात्मक सूत्र लिखें: ए) एच 2 इसलिए 4 (संक्षिप्त); बी) एचएनओ 3 ; एच 2 इसलिए 4 (संक्षिप्त); ग) भाई 2 / एफई; घ) क्लू 2 /AlCl 3 ; ई) सीएच 3 Br/AlBr 3 ; ई) सीएच 3 COCl/AlCl 3 . अभिक्रियाओं और उनके उत्पादों के नाम लिखिए। संकेत दें कि प्रत्येक विशिष्ट मामले में किस इलेक्ट्रोफाइल बेंजीन के साथ प्रतिक्रिया होती है।
6. इलेक्ट्रोफिलिक अभिकर्मक के साथ बेंजीन की बातचीत के लिए एक सामान्य योजना दें ( इ + ) मध्यवर्ती परिसरों का नाम बताइए। आमतौर पर कौन सा कदम प्रतिक्रिया की दर निर्धारित करता है? विचाराधीन अभिक्रिया की स्थितिज ऊर्जा में परिवर्तन का आलेख दीजिए।
7. निम्नलिखित अवधारणाओं को परिभाषित करें: क) संक्रमण अवस्था; बी) मध्यवर्ती कनेक्शन; ग) -जटिल; d) -कॉम्प्लेक्स। उनमें से कौन समान हैं? उत्प्रेरक की उपस्थिति में बेंजीन ब्रोमिनेशन के उदाहरण का उपयोग करके इन अवधारणाओं को स्पष्ट करें। फरवरी 3 .
8. ब्रोमीन के साथ एथीन और बेंजीन की प्रतिक्रियाओं के उदाहरण का उपयोग करते हुए, ऐल्कीन में इलेक्ट्रोफिलिक जोड़ के तंत्र की एरोमैटिक श्रृंखला में इलेक्ट्रोफिलिक प्रतिस्थापन के तंत्र के साथ तुलना करें। अंतर किस स्तर पर देखा जाता है और क्यों?
9. आगमनात्मक और मेसोमेरिक प्रभावों का उपयोग करते हुए, संकेतित यौगिकों में बेंजीन रिंग के साथ प्रतिस्थापक की बातचीत का वर्णन करें:

इलेक्ट्रॉन-दान (ईडी) और इलेक्ट्रॉन-निकासी (ईए) प्रतिस्थापन पर ध्यान दें।
10. निम्नलिखित यौगिकों के लिए मोनोनाइट्रेशन योजनाएं लिखें: ए) फिनोल; बी) बेंजीनसल्फोनिक एसिड; ग) आइसोप्रोपिलबेन्जीन; डी) क्लोरोबेंजीन। किस यौगिक के लिए आपेक्षिक प्रतिस्थापन दर सबसे अधिक होनी चाहिए और क्यों?
11. यौगिकों के मोनोसल्फ़ोनेशन के दौरान किन उत्पादों की अपेक्षा की जानी चाहिए: ए) टोल्यूनि; बी) नाइट्रोबेंजीन; ग) बेंजोइक एसिड; डी) ब्रोमोबेंजीन? कौन सा यौगिक सबसे आसान सल्फोनेट किया जाना चाहिए? क्यों?
12. निम्नलिखित यौगिकों को बेंजीन वलय में ब्रोमिनेट करने पर प्रतिक्रियाशीलता में वृद्धि के अनुसार एक पंक्ति में व्यवस्थित करें: ए) बेंजीन; बी) फिनोल; ग) बेंजाल्डिहाइड; डी) एथिलबेंजीन। स्पष्टीकरण दें।
13. निम्नलिखित हाइड्रोकार्बन के नाम लिखिए:

14. निम्नलिखित अभिकर्मकों के साथ बेंजीन की अभिक्रियाएँ लिखिए: : ए) क्ल 2 (फे); बी) 3Cl 2 (रोशनी); सी) एचएनओ 3 (एच 2 इसलिए 4 ); घ) ओह 2 (वायु) (वी 2 हे 5 , 450 सी); ई) 3O 3 , फिर H 2 ओ (जेडएन); च) एच 2 इसलिए 4 (ओलियम); छ) 3H 2 (नी, 200 सी,पी ). बेंजीन में जोड़ प्रतिक्रियाओं की विशेषता क्या है?
15. संकेतित अभिकर्मकों के साथ टोल्यूनि की अभिक्रियाएँ लिखिए : ए) 3H 2 (नी, 200 सी, 9806.7 केपीए); बी) केएमएनओ 4 में एच 2 के विषय में; सी*) l 2 , रोशनी; घ*) क्ल 2 (फे); ई*) सीएच 3 सीएल (AlCl 3 ); ई*) सीएच 3 COCl(AlCl .) 3 ); छ) एचएनओ 3 (एच 2 इसलिए 4 ). तारक से चिह्नित प्रतिक्रियाओं के लिए, तंत्र बताएं।
16. संकेतित परिस्थितियों में एथिलबेन्जीन के नाइट्रेशन की अभिक्रियाएँ लिखिए। क) 65% एचएनओ 3 + एच 2 इसलिए 4 (संक्षिप्त); बी) 10% एचएनओ 3 , ताप, दबाव। तंत्र लाओ।
17. isopropylbenzene के अनुपात की ब्रोमीन से तुलना करें: a) की उपस्थिति में अलब्रा 3 ; बी) जब रोशन और गरम किया जाता है। प्रतिक्रियाएं और उनके तंत्र दें।
18. एथिलबेन्जीन और से कौन-से यौगिक बनते हैं? पी -xylene संकेतित ऑक्सीकरण एजेंटों की कार्रवाई के तहत: ए) ओह 3 , फिर H 2 ओ (जेडएन); बी) केएमएनओ 4 एच में 2 के बारे में,टी ; वीके 2 करोड़ 2 हे 7 एच में 2 इसलिए 4 , टी ?
19. यौगिकों के निम्नलिखित युग्मों को किन अभिक्रियाओं की सहायता से पहचाना जा सकता है: a) एथिलबेन्जीन और एम -ज़ाइलीन; बी) एथिलबेंजीन और स्टाइरीन; ग) स्टाइरीन और फेनिलएसिटिलीन; जी) के बारे में - और पी -ज़ाइलीन?
20. निम्नलिखित प्रतिक्रियाओं के उत्पाद कौन से यौगिक हैं:

21. बेंजीन और किसी अन्य अभिकर्मक के आधार पर, निम्नलिखित यौगिक प्राप्त करें: a) पी -टर्टा -ब्यूटाइलटोल्यूनि; बी) एथिल- पी - टॉयल कीटोन; ग) ऐलिलबेन्जीन; जी) पी - ब्रोमोबेंजोइक एसिड।
22. निम्नलिखित अभिक्रियाओं में बनने वाले मुख्य यौगिकों के नाम लिखिए:

बेंजीन, श्रीमती रसायन शास्त्र के रूप में इस तरह के एक यौगिक ने अंततः और अपरिवर्तनीय रूप से केवल 1833 में अधिग्रहण किया। बेंजीन एक ऐसा यौगिक है जिसमें तेज-स्वभाव होता है, कोई कह सकता है, यहां तक कि विस्फोटक चरित्र भी। तुम्हें कैसे पता चला?
कहानी
1649 में जोहान ग्लौबर ने अपना ध्यान एक ऐसे यौगिक की ओर लगाया जो सफलतापूर्वक बनाया गया था जब रसायनज्ञ कोयला टार पर काम कर रहा था। लेकिन वह गुप्त रहना चाहता था।
लगभग 170 वर्षों के बाद, और अधिक सटीक होने के लिए, XIX सदी के मध्य-बीस के दशक में, संयोग से, बेंजीन को प्रकाश गैस से निकाला गया था, अर्थात् जारी घनीभूत से। मानव जाति इस तरह के प्रयासों का श्रेय इंग्लैंड के एक वैज्ञानिक माइकल फैराडे को देती है।
बेंजीन के अधिग्रहण के लिए बैटन को जर्मन इलगार्ड मित्शेरलिच ने रोक लिया था। यह बेंजोइक एसिड के निर्जल कैल्शियम लवण के प्रसंस्करण के दौरान हुआ। शायद इसीलिए यौगिक को ऐसा नाम दिया गया - बेंजीन। फिर भी, एक विकल्प के रूप में, वैज्ञानिक ने इसे गैसोलीन कहा। धूप, अगर अरबी से अनुवादित।
बेंजीन खूबसूरती और चमक से जलता है, इन अवलोकनों के संबंध में, ऑगस्टे लॉरेंट ने इसे "फेन" या "बेंजीन" कहने की सलाह दी। उज्ज्वल, चमकदार - यदि ग्रीक से अनुवादित किया गया है।
इलेक्ट्रॉनिक बांड की प्रकृति, बेंजीन के गुणों की अवधारणा के आधार पर, वैज्ञानिक ने निम्नलिखित छवि के रूप में यौगिक के अणु प्रदान किए। यह एक षट्भुज है। इसमें एक वृत्त अंकित है। पूर्वगामी से पता चलता है कि बेंजीन में एक अभिन्न इलेक्ट्रॉन बादल होता है, जिसमें चक्र के छह (अपवाद के बिना) कार्बन परमाणु सुरक्षित रूप से होते हैं। कोई निश्चित बाइनरी बॉन्ड नहीं हैं।
बेंजीन को पहले एक विलायक के रूप में माना जाता था। लेकिन मूल रूप से, जैसा कि वे कहते हैं, वह सदस्य नहीं थे, उन्होंने भाग नहीं लिया, शामिल नहीं थे। लेकिन बात 19वीं सदी की है। XX में महत्वपूर्ण परिवर्तन हुए। बेंजीन के गुण सबसे मूल्यवान गुण व्यक्त करते हैं जिससे उन्हें अधिक लोकप्रिय बनने में मदद मिली। ऑक्टेन संख्या, जो उच्च निकली, ने इसे ईंधन भरने वाली कारों के लिए ईंधन तत्व के रूप में उपयोग करना संभव बना दिया। यह क्रिया बेंजीन की व्यापक निकासी के लिए प्रेरणा थी, जिसका निष्कर्षण इस्पात उत्पादन के कोकिंग के उप-उत्पाद के रूप में किया जाता है।
चालीस के दशक तक, रासायनिक क्षेत्र में, उन पदार्थों के निर्माण में बेंजीन का सेवन किया जाने लगा, जो जल्दी से फट जाते हैं। 20वीं सदी ने खुद को इस तथ्य के साथ ताज पहनाया कि तेल शोधन उद्योग ने इतना बेंजीन का उत्पादन किया कि उसने रासायनिक उद्योग की आपूर्ति शुरू कर दी।
बेंजीन की विशेषता
असंतृप्त हाइड्रोकार्बन बेंजीन के समान होते हैं। उदाहरण के लिए, एथिलीन की हाइड्रोकार्बन श्रृंखला खुद को एक असंतृप्त हाइड्रोकार्बन के रूप में दर्शाती है। इसकी एक अतिरिक्त प्रतिक्रिया है। बेंजीन स्वेच्छा से एक ही विमान में मौजूद परमाणुओं के लिए यह सब धन्यवाद देता है। और एक तथ्य के रूप में - संयुग्मित इलेक्ट्रॉन बादल।

यदि सूत्र में बेंजीन की अंगूठी है, तो हम प्राथमिक निष्कर्ष पर आ सकते हैं कि यह बेंजीन है, जिसका संरचनात्मक सूत्र बिल्कुल इस तरह दिखता है।
भौतिक गुण
बेंजीन एक रंगहीन तरल है, लेकिन इसमें एक दुर्भाग्यपूर्ण गंध है। तापमान 5.52 डिग्री सेल्सियस तक पहुंचने पर बेंजीन पिघल जाता है। 80.1 पर उबलता है। घनत्व 0.879 ग्राम / सेमी 3 है, दाढ़ द्रव्यमान 78.11 ग्राम / मोल है। जलते समय, यह बहुत अधिक धूम्रपान करता है। वायु में प्रवेश करने पर विस्फोटक यौगिक बनाता है। चट्टानों (गैसोलीन, ईथर और अन्य) को बिना किसी समस्या के वर्णित पदार्थ के साथ जोड़ा जाता है। पानी के साथ एक एज़ोट्रोपिक यौगिक बनाता है। वाष्पीकरण की शुरुआत से पहले ताप 69.25 डिग्री (91% बेंजीन) पर होता है। 25 डिग्री सेल्सियस पर 1.79 ग्राम/लीटर पानी में घोला जा सकता है।
रासायनिक गुण
बेंजीन सल्फ्यूरिक और नाइट्रिक एसिड के साथ प्रतिक्रिया करता है। और अल्केन्स, हैलोजन, क्लोरोअल्केन्स के साथ भी। प्रतिस्थापन प्रतिक्रिया वह है जो उसकी विशेषता है। दबाव का तापमान बेंजीन रिंग की सफलता को प्रभावित करता है, जो कि कठोर परिस्थितियों में होता है।
हम प्रत्येक बेंजीन प्रतिक्रिया समीकरण पर अधिक विस्तार से विचार कर सकते हैं।
1. इलेक्ट्रोफिलिक प्रतिस्थापन। ब्रोमीन, उत्प्रेरक की उपस्थिति में, क्लोरीन के साथ परस्पर क्रिया करता है। परिणाम क्लोरोबेंजीन है:
С6H6+3Cl2 → C6H5Cl + HCl
2. फ्राइडल-शिल्प प्रतिक्रिया, या बेंजीन एल्किलेशन। एल्काइलबेंजीन की उपस्थिति अल्केन्स के साथ संयोजन के कारण होती है, जो हैलोजन डेरिवेटिव हैं:
C6H6 + C2H5Br → C6H5C2H5 + HBr
3. इलेक्ट्रोफिलिक प्रतिस्थापन। यहाँ नाइट्रेशन और सल्फोनेशन की प्रतिक्रिया है। बेंजीन समीकरण इस तरह दिखेगा:
C6H6 + H2SO4 → C6H5SO3H + H2O
C6H6 + HNO3 → C6H5NO2 + H2O
4. जलते समय बेंजीन:
2C6H6 + 15O2 → 12CO2 + 6H2O
कुछ शर्तों के तहत, यह संतृप्त हाइड्रोकार्बन की एक विशेषता विशेषता प्रदर्शित करता है। पी-इलेक्ट्रॉन बादल, जो विचाराधीन पदार्थ की संरचना में है, इन प्रतिक्रियाओं की व्याख्या करता है।
विभिन्न प्रकार के बेंजीन विशेष तकनीक पर निर्भर करते हैं। यहीं से पेट्रोलियम बेंजीन की लेबलिंग आती है। उदाहरण के लिए, शुद्ध और उच्च शुद्धि, संश्लेषण के लिए। मैं बेंजीन के समरूपों और विशेष रूप से उनके रासायनिक गुणों पर अलग से ध्यान देना चाहूंगा। ये एल्किलबेंजीन हैं।

बेंजीन होमोलॉग के प्रतिक्रिया करने की अधिक संभावना है। लेकिन बेंजीन की उपरोक्त प्रतिक्रियाएं, अर्थात् होमोलॉग्स, कुछ अंतर के साथ होती हैं।
एल्किलबेंजीन का हलोजनीकरण
समीकरण का रूप इस प्रकार है:
С6H5-CH3 + Br = C6H5-CH2Br + HBr।
बेंजीन रिंग में ब्रोमीन की आकांक्षा नहीं देखी जाती है। यह किनारे की चेन में चला जाता है। लेकिन अल (+3) नमक उत्प्रेरक के लिए धन्यवाद, ब्रोमीन साहसपूर्वक अंगूठी में प्रवेश करती है।
एल्किलबेंजीन का नाइट्रेशन
सल्फ्यूरिक और नाइट्रिक एसिड के लिए धन्यवाद, बेंजीन और अल्किलबेंजीन नाइट्रेटेड होते हैं। प्रतिक्रियाशील एल्किलबेंजीन। प्रस्तुत तीनों से दो उत्पाद प्राप्त होते हैं - ये पैरा- और ऑर्थो-आइसोमर हैं। आप इनमें से कोई एक सूत्र लिख सकते हैं:
C6H5 - CH3 + 3HNO3 → C6H2CH3 (NO2)3।
ऑक्सीकरण
बेंजीन के लिए, यह अस्वीकार्य है। लेकिन ऐल्किलबेंजीन स्वेच्छा से प्रतिक्रिया करते हैं। उदाहरण के लिए, बेंजोइक एसिड। सूत्र नीचे है:
C6H5CH3 + [O] → C6H5COOH।
एल्किलबेंजीन और बेंजीन, उनका हाइड्रोजनीकरण
एक एन्हांसर की उपस्थिति में, हाइड्रोजन बेंजीन के साथ प्रतिक्रिया करना शुरू कर देता है, जिसके परिणामस्वरूप साइक्लोहेक्सेन का निर्माण होता है, जैसा कि ऊपर चर्चा की गई है। इसी प्रकार, ऐल्किल बेंजीन आसानी से ऐल्किलसाइक्लोहेक्सेन में परिवर्तित हो जाते हैं। ऐल्किलसाइक्लोहेक्सेन प्राप्त करने के लिए वांछित ऐल्किल बेंजीन को हाइड्रोजनीकरण के अधीन करना आवश्यक है। मूल रूप से, यह शुद्ध उत्पाद के उत्पादन के लिए एक आवश्यक प्रक्रिया है। और यह सभी बेंजीन और एल्किलबेंजीन की प्रतिक्रियाएं नहीं हैं।
बेंजीन का उत्पादन। उद्योग
इस तरह के उत्पादन की नींव घटकों के प्रसंस्करण पर आधारित है: टोल्यूनि, नेफ्था, टार, जो कोयले के टूटने के दौरान निकलता है, और अन्य। इसलिए, पेट्रोकेमिकल, धातुकर्म उद्यमों में बेंजीन का उत्पादन किया जाता है। यह जानना महत्वपूर्ण है कि शुद्धिकरण की अलग-अलग डिग्री के बेंजीन कैसे प्राप्त करें, क्योंकि इस पदार्थ का ब्रांड सीधे निर्माण और उद्देश्य के सिद्धांत पर निर्भर है।
शेर का हिस्सा कास्टोबियोलाइट भाग के थर्मोकैटलिटिक सुधार द्वारा बनाया जाता है, जो 65 डिग्री पर उबलता है, जिसमें एक अर्क का प्रभाव होता है, डाइमिथाइलफॉर्मामाइड के साथ आसवन होता है।
एथिलीन और प्रोपलीन के उत्पादन के दौरान, तरल उत्पाद प्राप्त होते हैं, जो गर्मी के प्रभाव में अकार्बनिक और कार्बनिक यौगिकों के अपघटन के दौरान बनते हैं। इनमें से बेंजीन पृथक है। लेकिन, दुर्भाग्य से, इस बेंजीन उत्पादन विकल्प के लिए इतनी अधिक स्रोत सामग्री नहीं है। इसलिए, हमारे लिए रुचि का पदार्थ सुधार द्वारा निर्मित होता है। इस विधि से बेंजीन का आयतन बढ़ाया जाता है।

610-830 डिग्री के तापमान पर प्लस चिन्ह के साथ डीलकिलेशन द्वारा, पानी और हाइड्रोजन के उबलने के दौरान बनने वाली भाप की उपस्थिति में, टोल्यूनि से बेंजीन प्राप्त किया जाता है। एक और विकल्प है - उत्प्रेरक। जब जिओलाइट्स की उपस्थिति, या, वैकल्पिक रूप से, ऑक्साइड उत्प्रेरक, 227-627 डिग्री के तापमान शासन के अधीन मनाया जाता है।
बेंजीन विकसित करने का एक और पुराना तरीका है। कार्बनिक अवशोषक द्वारा अवशोषण की सहायता से इसे कोल कोकिंग के अंतिम परिणाम से पृथक किया जाता है। उत्पाद स्टीम-गैस है और इसे प्री-कूल्ड किया गया है। उदाहरण के लिए, तेल का उपयोग किया जाता है, जिसका स्रोत तेल या कोयला है। जब भाप से आसवन किया जाता है, तो मेहतर अलग हो जाता है। हाइड्रोट्रीटिंग कच्चे बेंजीन को अतिरिक्त पदार्थों से मुक्त करने में मदद करता है।
कोयला कच्चा माल
धातु विज्ञान में, जब कोयले का उपयोग किया जाता है, या, अधिक सटीक होने के लिए, इसका सूखा आसवन, कोक प्राप्त किया जाता है। इस प्रक्रिया के दौरान, हवा की आपूर्ति सीमित है। यह मत भूलो कि कोयले को 1200-1500 सेल्सियस के तापमान पर गर्म किया जाता है।
कोयला-रासायनिक बेंजीन को पूरी तरह से शुद्धिकरण की आवश्यकता होती है। बिना असफलता के मिथाइल साइक्लोहेक्सेन और उसके साथी एन-हेप्टेन से छुटकारा पाना आवश्यक है। भी हटाया जाना चाहिए। बेंजीन को पृथक्करण, शुद्धिकरण की प्रक्रिया से गुजरना है, जिसे एक से अधिक बार किया जाएगा।
ऊपर वर्णित विधि सबसे पुरानी है, लेकिन समय के बाद यह अपना उच्च स्थान खो देती है।
तेल अंश
0.3-1.2% - कच्चे तेल में हमारे नायक की संरचना के ऐसे संकेतक। वित्त और बलों के निवेश के लिए कम संकेतक। पेट्रोलियम अंशों के प्रसंस्करण के लिए औद्योगिक प्रक्रिया का उपयोग करना सबसे अच्छा है। वह उत्प्रेरक सुधार है। एल्यूमीनियम-प्लैटिनम-रेनियम एम्पलीफायर की उपस्थिति में, सुगंधित कार्बोहाइड्रेट के समावेश का प्रतिशत बढ़ जाता है, और संकेतक जो ईंधन की क्षमता को उसके संपीड़न के दौरान अनायास प्रज्वलित नहीं करने की क्षमता को निर्धारित करता है।
पायरोलिसिस रेजिन
यदि हमारे तेल उत्पाद को गैर-ठोस कच्चे माल से निकाला जाता है, अर्थात् निर्माण में उत्पन्न होने वाले प्रोपलीन और एथिलीन के पायरोलिसिस द्वारा, तो यह दृष्टिकोण सबसे स्वीकार्य होगा। सटीक होने के लिए, बेंजीन को पाइरोकॉन्डेनसेट से छोड़ा जाता है। कुछ अंशों के अपघटन के लिए हाइड्रोट्रीटमेंट की आवश्यकता होती है। सफाई के दौरान सल्फर और असंतृप्त मिश्रण हटा दिए जाते हैं। प्रारंभिक परिणाम में, xylene, टोल्यूनि, बेंजीन की सामग्री नोट की गई थी। आसवन की सहायता से, जो निष्कर्षण है, बीटीएक्स समूह को अलग किया जाता है और बेंजीन प्राप्त किया जाता है।

टोल्यूनि का हाइड्रोडीकेलाइलेशन
प्रक्रिया के नायक, हाइड्रोजन प्रवाह और टोल्यूनि का एक कॉकटेल, रिएक्टर में गरम किया जाता है। टोल्यूनि उत्प्रेरक बिस्तर से होकर गुजरता है। इस प्रक्रिया के दौरान, मिथाइल समूह को बेंजीन बनाने के लिए अलग किया जाता है। यहां शुद्धिकरण का एक निश्चित तरीका है। परिणाम एक अत्यधिक शुद्ध पदार्थ (नाइट्रेशन के लिए) है।
टोल्यूनि अनुपातहीनता
मिथाइल वर्ग की अस्वीकृति के परिणामस्वरूप, बेंजीन का निर्माण होता है, जाइलीन का ऑक्सीकरण होता है। इस प्रक्रिया में, transalkylation मनाया गया है। उत्प्रेरक क्रिया पैलेडियम, प्लैटिनम और नियोडिमियम के कारण होती है, जो एल्यूमीनियम ऑक्साइड पर होते हैं।
एक स्थिर उत्प्रेरक बिस्तर के साथ रिएक्टर को टोल्यूनि और हाइड्रोजन की आपूर्ति की जाती है। इसका उद्देश्य हाइड्रोकार्बन को उत्प्रेरक तल पर बसने से रोकना है। रिएक्टर से निकलने वाली धारा को ठंडा किया जाता है, और हाइड्रोजन को रीसायकल के लिए सुरक्षित रूप से पुनर्प्राप्त किया जाता है। जो बचा है उसे तीन बार आसुत किया जाता है। प्रारंभिक चरण में, गैर-सुगंधित यौगिकों को वापस ले लिया जाता है। बेंजीन को दूसरा निकाला जाता है, और अंतिम चरण जाइलीन का निष्कर्षण है।
एसिटिलीन ट्रिमराइजेशन
फ्रांसीसी भौतिक रसायनज्ञ मार्सेलिन बर्थेलॉट के काम के लिए धन्यवाद, एसिटिलीन से बेंजीन का उत्पादन शुरू हुआ। लेकिन एक ही समय में, कई अन्य तत्वों से एक भारी कॉकटेल बाहर खड़ा था। सवाल यह था कि प्रतिक्रिया तापमान को कैसे कम किया जाए। उत्तर केवल XX सदी के चालीसवें दशक के अंत में प्राप्त हुआ था। वी. रेप्पे को एक उपयुक्त उत्प्रेरक मिला, वह निकल निकला। एसिटिलीन से बेंजीन प्राप्त करने का एकमात्र तरीका ट्रिमराइजेशन है।

बेंजीन का निर्माण सक्रिय कार्बन की मदद से होता है। उच्च ताप दर पर, एसिटिलीन कोयले के ऊपर से गुजरती है। यदि तापमान कम से कम 410 डिग्री है तो बेंजीन निकलता है। इसी समय, विभिन्न प्रकार के सुगंधित हाइड्रोकार्बन अभी भी पैदा होते हैं। इसलिए अच्छे उपकरण की जरूरत है जो एसिटिलीन को गुणात्मक तरीके से शुद्ध करने में सक्षम हो। ट्रिमराइजेशन जैसी श्रमसाध्य विधि के साथ, बहुत अधिक एसिटिलीन का सेवन किया जाता है। 15 मिली बेंजीन प्राप्त करने के लिए 20 लीटर एसिटिलीन लिया जाता है। आप देख सकते हैं कि प्रतिक्रिया में यह कैसा दिखता है, इसमें अधिक समय नहीं लगेगा।
3C2H2 → C6H6 (ज़ेलिंस्की समीकरण)।
3CH → CH = (t, kat) = C6H6।
बेंजीन का उपयोग कहाँ किया जाता है
बेंजीन रसायन विज्ञान के काफी लोकप्रिय दिमाग की उपज है। विशेष रूप से अक्सर यह देखा गया कि कैसे बेंजीन का उपयोग क्यूमीन, साइक्लोहेक्सेन, एथिलबेन्जीन के निर्माण में किया जाता था। स्टाइरीन बनाने के लिए एथिलबेन्जीन अपरिहार्य है। कैप्रोलैक्टम के उत्पादन के लिए प्रारंभिक सामग्री साइक्लोहेक्सेन है। थर्माप्लास्टिक राल बनाते समय, यह कैप्रोलैक्टम होता है जिसका उपयोग किया जाता है। वर्णित पदार्थ विभिन्न पेंट और वार्निश के निर्माण में अपरिहार्य है।
कितना खतरनाक है बेंजीन
बेंजीन एक विषैला पदार्थ है। अस्वस्थता की भावना का प्रकट होना, जो मतली और गंभीर चक्कर आना के साथ है, विषाक्तता का संकेत है। यहां तक कि मौत से भी इंकार नहीं किया जा सकता है। बेंजीन विषाक्तता के मामले में अवर्णनीय आनंद की भावना कम परेशान करने वाली घंटी नहीं है।
लिक्विड बेंजीन त्वचा में जलन पैदा करता है। बेंजीन के वाष्प बरकरार त्वचा में भी आसानी से प्रवेश कर जाते हैं। एक छोटी खुराक में किसी पदार्थ के साथ सबसे अल्पकालिक संपर्क के साथ, लेकिन नियमित रूप से, अप्रिय परिणाम आने में लंबे समय तक नहीं होंगे। यह अस्थि मज्जा और विभिन्न प्रकार के तीव्र ल्यूकेमिया का घाव हो सकता है।

इसके अलावा, पदार्थ मनुष्यों में नशे की लत है। बेंजीन एक डोप की तरह काम करता है। तंबाकू का धुआं टार जैसा उत्पाद पैदा करता है। जब उन्होंने इसका अध्ययन किया, तो वे इस निष्कर्ष पर पहुंचे कि बाद की सामग्री मनुष्यों के लिए सुरक्षित नहीं है। निकोटिन की उपस्थिति के अलावा, बेंजपाइरीन प्रकार के सुगंधित कार्बोहाइड्रेट की उपस्थिति भी पाई गई। बेंज़पायरीन की एक विशिष्ट विशेषता कार्सिनोजेन्स हैं। इनका बहुत ही हानिकारक प्रभाव होता है। उदाहरण के लिए, वे कैंसर का कारण बनते हैं।
पूर्वगामी के बावजूद, बेंजीन विभिन्न दवाओं, प्लास्टिक, सिंथेटिक रबर और निश्चित रूप से, रंगों के उत्पादन के लिए एक प्रारंभिक सामग्री है। यह रसायन विज्ञान और सुगंधित यौगिक का सबसे आम दिमाग की उपज है।
