Alkenes ត្រូវបានកំណត់លក្ខណៈជាចម្បងដោយប្រតិកម្ម ការចូលដោយចំណងទ្វេ។ ជាទូទៅ ប្រតិកម្មទាំងនេះដំណើរការទៅតាមយន្តការអ៊ីយ៉ុង។ ចំណង pi ត្រូវបានខូច ហើយចំណង sigma ថ្មីពីរត្រូវបានបង្កើតឡើង។ ខ្ញុំសូមរំលឹកអ្នកថា ប្រតិកម្មជំនួសគឺជារឿងធម្មតាសម្រាប់ alkanes ហើយវាដំណើរការទៅតាមយន្តការរ៉ាឌីកាល់។ ម៉ូលេគុលអ៊ីដ្រូសែនអាចចូលរួមជាមួយ alkenes ប្រតិកម្មទាំងនេះត្រូវបានគេហៅថា hydrogenation ម៉ូលេគុលទឹក hydration halogens - halogenation អ៊ីដ្រូសែន halides - hydrohalogenation ។ ប៉ុន្តែរឿងដំបូង។
ប្រតិកម្មបន្ថែមចំណងទ្វេ
ដូច្នេះ ដំបូងទ្រព្យសម្បត្តិគីមី - សមត្ថភាពក្នុងការភ្ជាប់អ៊ីដ្រូសែន halides, hydrohalogenation ។
Propene និង alkenes ផ្សេងទៀតមានប្រតិកម្មជាមួយនឹងអ៊ីដ្រូសែន halides យោងទៅតាមច្បាប់របស់ Markovnikov ។

អាតូមអ៊ីដ្រូសែនត្រូវបានភ្ជាប់ទៅនឹងអាតូមកាបូនដែលមានអ៊ីដ្រូសែនច្រើនបំផុត ឬត្រឹមត្រូវជាងនេះ។
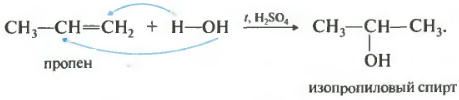
ទីពីរលេខនៅក្នុងបញ្ជីនៃលក្ខណៈសម្បត្តិរបស់យើងនឹងមានជាតិទឹក ការបន្ថែមទឹក។
ប្រតិកម្មកើតឡើងនៅពេលដែលកំដៅក្នុងវត្តមាននៃអាស៊ីត ជាធម្មតាស៊ុលហ្វួរី ឬផូស្វ័រ។ ការបន្ថែមទឹកក៏កើតឡើងផងដែរដោយយោងទៅតាមច្បាប់ Markovnikov ពោលគឺអាល់កុលបឋមអាចទទួលបានដោយជាតិទឹកនៃអេទីឡែនតែប៉ុណ្ណោះ alkenes ដែលនៅសល់ផ្តល់ជាតិអាល់កុលបន្ទាប់បន្សំ។
សម្រាប់ទាំង hydrohalogenation និង hydration មានករណីលើកលែងចំពោះច្បាប់របស់ Markovnikov ។ ទីមួយប្រឆាំងនឹងច្បាប់នេះការបន្ថែមដំណើរការនៅក្នុងវត្តមាននៃ peroxides ។
ទីពីរ សម្រាប់ដេរីវេនៃ alkenes ដែលក្រុមដកអេឡិចត្រុងមានវត្តមាន។ ឧទាហរណ៍សម្រាប់ 3,3,3-trifluoropropene-1 ។
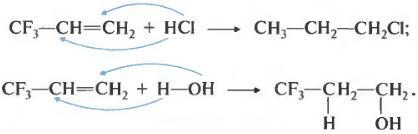
អាតូមហ្វ្លុយអូរីន ដោយសារតែការបញ្ជូនអេឡិចត្រុងខ្ពស់របស់វា ទាញដង់ស៊ីតេអេឡិចត្រុងមកលើខ្លួនវាតាមខ្សែសង្វាក់នៃចំណង sigma ។ បាតុភូតនេះត្រូវបានគេហៅថាឥទ្ធិពលអវិជ្ជមាន។
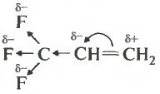
ដោយសារតែនេះ អេឡិចត្រុង pi ចល័តនៃចំណងទ្វេត្រូវបានផ្លាស់ប្តូរ ហើយអាតូមកាបូនខាងក្រៅបំផុតមានបន្ទុកវិជ្ជមានមួយផ្នែក ដែលជាធម្មតាត្រូវបានតំណាងថាជាដីសណ្តបូក។ វាគឺសម្រាប់គាត់ដែលអ៊ីយ៉ុង bromine ដែលត្រូវបានចោទប្រកាន់អវិជ្ជមាននឹងទៅ ហើយ cation អ៊ីដ្រូសែននឹងចូលរួមជាមួយអាតូមកាបូនអ៊ីដ្រូសែនតិចបំផុត។
បន្ថែមពីលើក្រុម trifluoromethyl ជាឧទាហរណ៍ ក្រុម trichloromethyl ក្រុម nitro ក្រុម carboxyl និងមួយចំនួនទៀតមានឥទ្ធិពលអវិជ្ជមាន។
ករណីទីពីរនៃការរំលោភលើច្បាប់ Markovnikov ក្នុងការប្រឡងគឺកម្រណាស់ ប៉ុន្តែវានៅតែគួរចងចាំទុកក្នុងចិត្ត ប្រសិនបើអ្នកមានគម្រោងប្រឡងជាប់ដើម្បីទទួលបានពិន្ទុអតិបរមា។
ទីបីទ្រព្យសម្បត្តិគីមី - ការបន្ថែមម៉ូលេគុល halogen ។
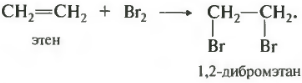
ដំបូងបង្អស់ នេះទាក់ទងនឹង bromine ចាប់តាំងពីប្រតិកម្មនេះមានគុណភាពសម្រាប់ចំណងច្រើន។ ឧទាហរណ៍ នៅពេលដែលឆ្លងកាត់ អេទីឡែន តាមរយៈទឹក bromine ដែលជាដំណោះស្រាយពណ៌ត្នោតនៃ bromine នៅក្នុងទឹក វាប្រែពណ៌។ ប្រសិនបើល្បាយនៃឧស្ម័ន ឧទាហរណ៍ អេតាន និងអេទីន ត្រូវបានឆ្លងកាត់ទឹកប្រូមីន នោះអេតានសុទ្ធអាចទទួលបានដោយគ្មានភាពមិនបរិសុទ្ធ អេធីន ព្រោះវានឹងនៅតែមាននៅក្នុងធុងប្រតិកម្មក្នុងទម្រង់ជាឌីប្រូម៉ូថេន ដែលជាអង្គធាតុរាវ។
ចំណាំជាពិសេសគឺប្រតិកម្មនៃអាល់ខេនក្នុងដំណាក់កាលឧស្ម័នជាមួយនឹងកំដៅខ្លាំងឧទាហរណ៍ជាមួយក្លរីន។
នៅក្រោមលក្ខខណ្ឌបែបនេះ មិនមែនប្រតិកម្មបន្ថែមកើតឡើងទេ ប៉ុន្តែប្រតិកម្មជំនួស។ លើសពីនេះទៅទៀត មានតែនៅលើអាតូមអាល់ហ្វាកាបូន ពោលគឺអាតូមដែលនៅជាប់នឹងចំណងទ្វេ។ ក្នុងករណីនេះ 3-chloropropene-1 ត្រូវបានទទួល។ ប្រតិកម្មទាំងនេះនៅលើការប្រឡងគឺមិនមែនជារឿងធម្មតាទេ ដូច្នេះសិស្សភាគច្រើនមិនចាំពួកគេទេ ហើយជាក្បួនធ្វើខុស។
ទីបួនលេខគឺជាប្រតិកម្មអ៊ីដ្រូសែន ហើយជាមួយវា ប្រតិកម្ម dehydrogenation ។ នោះគឺការបន្ថែមឬការដកអ៊ីដ្រូសែន។
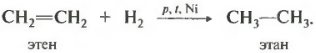
អ៊ីដ្រូសែនកើតឡើងនៅសីតុណ្ហភាពមិនខ្ពស់នៅលើកាតាលីករនីកែលមួយ។ នៅសីតុណ្ហភាពខ្ពស់ ការ dehydrogenation ដើម្បីបង្កើត alkynes គឺអាចធ្វើទៅបាន។
ទីប្រាំទ្រព្យសម្បត្តិនៃ alkenes គឺជាសមត្ថភាពក្នុងការធ្វើវត្ថុធាតុ polymerize នៅពេលដែលម៉ូលេគុលអាល់ខេនរាប់រយរាប់ពាន់បង្កើតជាខ្សែសង្វាក់ដ៏វែងនិងរឹងមាំដោយសារតែការបំបែកនៃចំណង pi និងការបង្កើតចំណង sigma ជាមួយគ្នា។
ក្នុងករណីនេះជ័រត្រូវបានទទួល។ ចំណាំថាមិនមានចំណងច្រើននៅក្នុងម៉ូលេគុលលទ្ធផលទេ។ សារធាតុបែបនេះត្រូវបានគេហៅថាប៉ូលីមែរ ម៉ូលេគុលដើមត្រូវបានគេហៅថាម៉ូណូមឺរ បំណែកដែលកើតឡើងដដែលៗគឺជាឯកតាបឋមនៃវត្ថុធាតុ polymer ហើយលេខ n គឺជាកម្រិតនៃវត្ថុធាតុ polymerization ។
ប្រតិកម្មដើម្បីផលិតវត្ថុធាតុ polymeric សំខាន់ៗផ្សេងទៀតដូចជា polypropylene ក៏អាចធ្វើទៅបានដែរ។
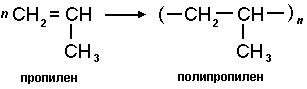

វត្ថុធាតុ polymer សំខាន់មួយទៀតគឺ polyvinyl chloride ។

សម្ភារៈចាប់ផ្តើមសម្រាប់ការផលិតវត្ថុធាតុ polymer នេះគឺ chloroethene ដែលជាឈ្មោះមិនសំខាន់នៃ vinyl chloride ។ ចាប់តាំងពីសារធាតុជំនួសមិនឆ្អែតនេះត្រូវបានគេហៅថា vinyl ។ អក្សរកាត់ទូទៅសម្រាប់ផលិតផលប្លាស្ទិក PVC គ្រាន់តែតំណាងឱ្យ polyvinyl chloride ។
យើងបានពិភាក្សាអំពីលក្ខណៈសម្បត្តិចំនួនប្រាំ ដែលជាប្រតិកម្មបន្ថែមចំណងទ្វេ។ ឥឡូវនេះសូមក្រឡេកមើលប្រតិកម្ម។ អុកស៊ីតកម្ម.
ប្រតិកម្មអុកស៊ីតកម្មអាល់ខេន
ទីប្រាំមួយ។ទ្រព្យសម្បត្តិគីមីនៅក្នុងបញ្ជីទូទៅរបស់យើងគឺអុកស៊ីតកម្មស្រាលឬប្រតិកម្ម Wagner ។ វាដំណើរការនៅពេលដែលអាល់ខេនត្រូវបានប៉ះពាល់ទៅនឹងដំណោះស្រាយ aqueous នៃ permanganate ប៉ូតាស្យូមក្នុងភាពត្រជាក់ ដូច្នេះជាញឹកញាប់នៅក្នុងកិច្ចការពិនិត្យ សីតុណ្ហភាពគឺសូន្យដឺក្រេ។
លទ្ធផលគឺអាល់កុល dihydric ។ ក្នុងករណីនេះអេទីឡែន glycol ហើយជាទូទៅអាល់កុលបែបនេះត្រូវបានគេហៅថាជាសមូហភាព glycols ។ កំឡុងពេលប្រតិកម្ម ដំណោះស្រាយ violet-pink នៃ permanganate ក្លាយទៅជាគ្មានពណ៌ ដូច្នេះប្រតិកម្មនេះក៏មានគុណភាពសម្រាប់ចំណងទ្វេរដងផងដែរ។ ម៉ង់ហ្គាណែសនៅក្នុងបរិយាកាសអព្យាក្រឹតពីស្ថានភាពអុកស៊ីតកម្ម +7 ត្រូវបានកាត់បន្ថយទៅជាស្ថានភាពអុកស៊ីតកម្ម +4 ។ សូមក្រឡេកមើលឧទាហរណ៍មួយចំនួនទៀត។ សមីការ
នៅទីនេះយើងទទួលបាន propanediol-1,2 ។ ទោះជាយ៉ាងណាក៏ដោយ cyclic alkenes នឹងមានប្រតិកម្មតាមរបៀបដូចគ្នា។ សមីការ
ជម្រើសមួយទៀតគឺនៅពេលដែលចំណងទ្វេរជាឧទាហរណ៍នៅក្នុងខ្សែសង្វាក់ចំហៀងនៃអ៊ីដ្រូកាបូនក្រអូប។ ជាទៀងទាត់នៅក្នុងភារកិច្ចប្រឡងមានប្រតិកម្ម Wagner ពាក់ព័ន្ធនឹង styrene ឈ្មោះទីពីររបស់វាគឺ vinylbenzene ។
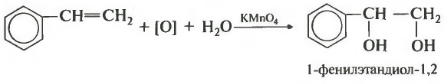
ខ្ញុំសង្ឃឹមថាខ្ញុំបានផ្តល់នូវឧទាហរណ៍គ្រប់គ្រាន់សម្រាប់អ្នកដើម្បីយល់ថាអុកស៊ីតកម្មស្រាលនៃចំណងទ្វេរដងតែងតែអនុវត្តតាមច្បាប់សាមញ្ញជាង - ចំណង pi ត្រូវបានខូច ហើយក្រុមអ៊ីដ្រូស៊ីត្រូវបានបន្ថែមទៅអាតូមកាបូននីមួយៗ។
ឥឡូវនេះទាក់ទងទៅនឹងអុកស៊ីតកម្មរឹង។ នេះនឹងជារបស់យើង។ ទីប្រាំពីរទ្រព្យសម្បត្តិ។ អុកស៊ីតកម្មនេះកើតឡើងនៅពេលដែលអាល់ខេនមានប្រតិកម្មជាមួយនឹងដំណោះស្រាយប៉ូតាស្យូម permanganate ដែលមានជាតិអាស៊ីតនៅពេលដែលកំដៅ។
មានការបំផ្លិចបំផ្លាញនៃម៉ូលេគុល ពោលគឺការបំផ្លាញរបស់វានៅចំណងទ្វេ។ ក្នុងករណី butene-2 ម៉ូលេគុលអាស៊ីតអាសេទិកពីរត្រូវបានទទួល។ ជាទូទៅទីតាំងនៃចំណងច្រើននៅក្នុងសង្វាក់កាបូនអាចត្រូវបានវិនិច្ឆ័យពីផលិតផលអុកស៊ីតកម្ម។
នៅពេលដែល butene-1 ត្រូវបានកត់សុី ម៉ូលេគុលនៃអាស៊ីត propionic (propanoic) និងកាបូនឌីអុកស៊ីតត្រូវបានទទួល។
ក្នុងករណីអេទីឡែន ម៉ូលេគុលកាបូនឌីអុកស៊ីតពីរនឹងត្រូវបានទទួល។ ក្នុងករណីទាំងអស់នៅក្នុងបរិយាកាសអាសុីតម៉ង់ហ្គាណែសត្រូវបានកាត់បន្ថយពីស្ថានភាពអុកស៊ីតកម្ម +7 ទៅ +2 ។
ជាចុងក្រោយ ទីប្រាំបីទ្រព្យសម្បត្តិ - អុកស៊ីតកម្មពេញលេញឬចំហេះ។
Alkenes ឆេះដូចអ៊ីដ្រូកាបូនផ្សេងទៀតទៅនឹងកាបូនឌីអុកស៊ីត និងទឹក។ ចូរយើងសរសេរសមីការសម្រាប់ការឆេះនៃ alkenes ក្នុងទម្រង់ទូទៅមួយ។
វានឹងមានម៉ូលេគុលកាបូនឌីអុកស៊ីតច្រើន ដូចដែលមានអាតូមកាបូននៅក្នុងម៉ូលេគុលអាល់ខេន ព្រោះម៉ូលេគុល CO 2 មានអាតូមកាបូនមួយ។ នោះគឺជាម៉ូលេគុល n CO 2 ។ វានឹងមានពាក់កណ្តាលនៃម៉ូលេគុលទឹកជាច្រើនដូចជាអាតូមអ៊ីដ្រូសែន ពោលគឺ 2n/2 ដែលមានន័យថាគ្រាន់តែ n ។
មានអាតូមអុកស៊ីសែនដូចគ្នានៅខាងឆ្វេង និងខាងស្តាំ។ នៅខាងស្តាំមាន 2n ពីកាបូនឌីអុកស៊ីតបូក n ពីទឹក សរុប 3n ។ នៅខាងឆ្វេង មានចំនួនអាតូមអុកស៊ីហ្សែនដូចគ្នា ដែលមានន័យថាមានពាក់កណ្តាលនៃម៉ូលេគុល ព្រោះអាតូមពីរជាផ្នែកនៃម៉ូលេគុល។ នោះគឺជាម៉ូលេគុលអុកស៊ីសែន 3n/2 ។ អ្នកអាចសរសេរ 1.5n ។
យើងបានពិនិត្យឡើងវិញ ប្រាំបីលក្ខណៈគីមីនៃអាល់ខេន។
សមាសធាតុសរីរាង្គសាមញ្ញបំផុតគឺអ៊ីដ្រូកាបូនឆ្អែតនិងមិនឆ្អែត។ ទាំងនេះរួមបញ្ចូលសារធាតុនៃថ្នាក់នៃ alkanes, alkynes, alkenes ។
រូបមន្តរបស់ពួកគេរួមមានអាតូមអ៊ីដ្រូសែន និងកាបូនក្នុងលំដាប់ និងបរិមាណជាក់លាក់មួយ។ ពួកគេត្រូវបានរកឃើញជាញឹកញាប់នៅក្នុងធម្មជាតិ។
និយមន័យនៃអាល់ខេន
ឈ្មោះផ្សេងទៀតរបស់ពួកគេគឺ olefins ឬ ethylene hydrocarbons ។ នោះហើយជាអ្វីដែលថ្នាក់នៃសមាសធាតុនេះត្រូវបានគេហៅថានៅក្នុងសតវត្សទី 18 នៅពេលដែលវត្ថុរាវដែលមានជាតិខ្លាញ់ អេទីឡែនក្លរ ត្រូវបានរកឃើញ។
Alkenes គឺជាសមាសធាតុផ្សំឡើងពីធាតុអ៊ីដ្រូសែន និងកាបូន។ ពួកវាជាកម្មសិទ្ធិរបស់អ៊ីដ្រូកាបូន acyclic ។ នៅក្នុងម៉ូលេគុលរបស់ពួកគេមានចំណងទ្វេ (មិនឆ្អែត) តែមួយតភ្ជាប់អាតូមកាបូនពីរទៅគ្នាទៅវិញទៅមក។
រូបមន្តអាល់ខេន
ថ្នាក់នីមួយៗនៃសមាសធាតុមានការកំណត់គីមីរបស់វា។ នៅក្នុងពួកវានិមិត្តសញ្ញានៃធាតុនៃប្រព័ន្ធតាមកាលកំណត់បង្ហាញពីសមាសភាពនិងរចនាសម្ព័ន្ធនៃចំណងនៃសារធាតុនីមួយៗ។

រូបមន្តទូទៅនៃ alkenes ត្រូវបានតាងដូចខាងក្រោមៈ C n H 2n ដែលលេខ n ធំជាង ឬស្មើ 2 ។ នៅពេលឌិគ្រីបវា វាអាចត្រូវបានគេមើលឃើញថាមានអាតូមអ៊ីដ្រូសែនពីរសម្រាប់អាតូមកាបូននីមួយៗ។
រូបមន្តម៉ូលេគុលនៃ alkenes ពីស៊េរី homologous ត្រូវបានតំណាងដោយរចនាសម្ព័ន្ធដូចខាងក្រោម: C 2 H 4, C 3 H 6, C 4 H 8, C 5 H 10, C 6 H 12, C 7 H 14, C 8 H 16 , C 9 H 18, C 10 H 20 ។ វាអាចត្រូវបានគេមើលឃើញថាអ៊ីដ្រូកាបូនជាបន្តបន្ទាប់នីមួយៗមានកាបូនមួយនិងអ៊ីដ្រូសែន 2 ទៀត។
មានការរចនាក្រាហ្វិកនៃទីតាំង និងលំដាប់នៃសមាសធាតុគីមីរវាងអាតូមក្នុងម៉ូលេគុល ដែលបង្ហាញរូបមន្តរចនាសម្ព័ន្ធនៃអាល់ខេន។ ដោយមានជំនួយពីបន្ទាត់ valence ចំណងនៃកាបូនជាមួយអ៊ីដ្រូសែនត្រូវបានចង្អុលបង្ហាញ។
រូបមន្តរចនាសម្ព័ន្ធនៃ alkenes អាចត្រូវបានបង្ហាញជាទម្រង់ពង្រីក នៅពេលដែលធាតុគីមី និងចំណងទាំងអស់ត្រូវបានបង្ហាញ។ ជាមួយនឹងការបញ្ចេញមតិសង្ខេបនៃ olefins ការរួមបញ្ចូលគ្នានៃកាបូន និងអ៊ីដ្រូសែន ដោយមានជំនួយពីបន្ទាត់ valence មិនត្រូវបានបង្ហាញទេ។
រូបមន្តគ្រោងឆ្អឹងតំណាងឱ្យរចនាសម្ព័ន្ធសាមញ្ញបំផុត។ បន្ទាត់ដែលខូចបង្ហាញពីមូលដ្ឋាននៃម៉ូលេគុល ដែលអាតូមកាបូនត្រូវបានតំណាងដោយកំពូល និងចុងរបស់វា ហើយអ៊ីដ្រូសែនត្រូវបានចង្អុលបង្ហាញដោយតំណភ្ជាប់។
របៀបដែលឈ្មោះ olefin ត្រូវបានបង្កើតឡើង
CH 3 -HC \u003d CH 2 + H 2 O → CH 3 -OHCH-CH 3 ។
នៅពេលដែលប៉ះពាល់នឹងអាល់ខេនជាមួយនឹងអាស៊ីតស៊ុលហ្វួរីក ដំណើរការនៃស៊ុលហ្វានកើតឡើង៖
CH 3 -HC \u003d CH 2 + HO-OSO-OH → CH 3 -CH 3 CH-O-SO 2 -OH ។
ប្រតិកម្មកើតឡើងជាមួយនឹងការបង្កើតអាស៊ីត esters ឧទាហរណ៍អាស៊ីត isopropylsulfuric ។
Alkenes ត្រូវបានទទួលរងការកត់សុីក្នុងអំឡុងពេលចំហេះរបស់ពួកគេក្រោមសកម្មភាពនៃអុកស៊ីសែនដើម្បីបង្កើតជាទឹកនិងឧស្ម័នកាបូនឌីអុកស៊ីត:
2CH 3 -HC \u003d CH 2 + 9O 2 → 6CO 2 + 6H 2 O ។
អន្តរកម្មនៃសមាសធាតុ olefinic និង dilute ប៉ូតាស្យូម permanganate ក្នុងទម្រង់ជាដំណោះស្រាយនាំទៅដល់ការបង្កើត glycols ឬជាតិអាល់កុល dihydric ។ ប្រតិកម្មនេះក៏ជាអុកស៊ីតកម្មជាមួយនឹងការបង្កើតអេទីឡែន glycol និងការប្រែពណ៌នៃដំណោះស្រាយ៖
3H 2 C \u003d CH 2 + 4H 2 O + 2KMnO 4 → 3OHCH-CHOH + 2MnO 2 + 2KOH ។
ម៉ូលេគុល Alkene អាចចូលរួមក្នុងដំណើរការ polymerization ជាមួយនឹងយន្តការរ៉ាឌីកាល់សេរី ឬ cation-anion ។ ក្នុងករណីដំបូងនៅក្រោមឥទ្ធិពលនៃ peroxides វត្ថុធាតុ polymer ដូចជា polyethylene ត្រូវបានទទួល។
យោងតាមយន្តការទី 2 អាស៊ីតដើរតួជាកាតាលីករ cationic ហើយសារធាតុសរីរាង្គគឺជាកាតាលីករ anionic ជាមួយនឹងការបញ្ចេញសារធាតុប៉ូលីម៊ែរស្តេរ៉េអូសេទិក។
តើអាល់កានជាអ្វី
ពួកវាត្រូវបានគេហៅថាប៉ារ៉ាហ្វីន ឬអ៊ីដ្រូកាបូនអ៊ីដ្រូកាបូនឆ្អែត។ ពួកវាមានរចនាសម្ព័ន្ធលីនេអ៊ែរឬសាខាដែលមានតែចំណងសាមញ្ញឆ្អែត។ អ្នកតំណាងទាំងអស់នៃថ្នាក់នេះមានរូបមន្តទូទៅ C n H 2n + 2 ។

ពួកវាផ្ទុកតែអាតូមកាបូន និងអ៊ីដ្រូសែនប៉ុណ្ណោះ។ រូបមន្តទូទៅនៃអាល់ខេនត្រូវបានបង្កើតឡើងពីការកំណត់នៃអ៊ីដ្រូកាបូនឆ្អែត។
ឈ្មោះរបស់ alkanes និងលក្ខណៈរបស់វា។
អ្នកតំណាងសាមញ្ញបំផុតនៃថ្នាក់នេះគឺមេតាន។ វាត្រូវបានបន្តដោយសារធាតុដូចជា ethane, propane និង butane ។ ឈ្មោះរបស់ពួកគេគឺផ្អែកលើឫសនៃលេខជាភាសាក្រិច ដែលបច្ច័យ -an ត្រូវបានបន្ថែម។ ឈ្មោះរបស់ alkanes ត្រូវបានរាយក្នុងបញ្ជីឈ្មោះ IUPAC ។
រូបមន្តទូទៅនៃ alkenes, alkynes, alkanes រួមបញ្ចូលតែអាតូមពីរប្រភេទប៉ុណ្ណោះ។ ទាំងនេះរួមបញ្ចូលធាតុកាបូន និងអ៊ីដ្រូសែន។ ចំនួនអាតូមកាបូននៅក្នុងថ្នាក់ទាំងបីគឺដូចគ្នា ភាពខុសគ្នាត្រូវបានគេសង្កេតឃើញតែនៅក្នុងចំនួនអ៊ីដ្រូសែនប៉ុណ្ណោះដែលអាចបំបែកចេញ ឬបន្ថែម។ ពីទទួលបានសមាសធាតុមិនឆ្អែត។ អ្នកតំណាងនៃប៉ារ៉ាហ្វីននៅក្នុងម៉ូលេគុលមានអាតូមអ៊ីដ្រូសែន 2 ច្រើនជាង olefins ដែលត្រូវបានបញ្ជាក់ដោយរូបមន្តទូទៅនៃ alkanes, alkenes ។ រចនាសម្ព័ន្ធអាល់ខេនត្រូវបានចាត់ទុកថាមិនឆ្អែតដោយសារតែវត្តមាននៃចំណងទ្វេ។
ប្រសិនបើយើងភ្ជាប់ចំនួនអាតូមទឹកទៅរ៉ូ-ឌីនី និងកាបូន-លេ-រ៉ូ-ឌីនី ក្នុងអាល់កា-ណា នោះតម្លៃនឹងមានចំនួនអតិបរមា-ស៊ី-តូច បើប្រៀបធៀបជាមួយថ្នាក់ផ្សេងទៀតនៃធ្យូងថ្ម-លេ-វ៉ូ - ទៅ -ro-dov ។
ចាប់ផ្តើមពីមេតាន និងបញ្ចប់ដោយ butane (ពី C 1 ដល់ C 4) សារធាតុមាននៅក្នុងទម្រង់ជាឧស្ម័ន។
នៅក្នុងទម្រង់រាវ អ៊ីដ្រូកាបូននៃចន្លោះពេលដូចគ្នាពី C 5 ដល់ C 16 ត្រូវបានបង្ហាញ។ ចាប់ផ្តើមជាមួយអាល់កានដែលមានអាតូមកាបូនចំនួន 17 នៅក្នុងខ្សែសង្វាក់សំខាន់ ការផ្លាស់ប្តូរនៃស្ថានភាពរូបវន្តទៅជាទម្រង់រឹងកើតឡើង។
ពួកវាត្រូវបានកំណត់លក្ខណៈដោយ isomerism នៅក្នុងគ្រោងកាបូន និងការកែប្រែអុបទិកនៃម៉ូលេគុល។

នៅក្នុងប៉ារ៉ាហ្វីន វ៉ាឡង់កាបូនត្រូវបានចាត់ទុកថាត្រូវបានកាន់កាប់ទាំងស្រុងដោយកាបូនជិតខាង-le-ro-da-mi ឬ in-do-ro-da-mi ជាមួយនឹងការបង្កើតចំណង σ-type ។ តាមទស្សនៈគីមី នេះបណ្តាលឱ្យមានលក្ខណៈសម្បត្តិខ្សោយរបស់ពួកគេ ដែលជាមូលហេតុដែលអាល់កានត្រូវបានគេហៅថា pre-del-ny-x ឬ saturated-schen-ny-x coal-le-to-do-ro-dov ដែលមិនមានទំនាក់ទំនង។
ពួកវាចូលទៅក្នុងប្រតិកម្មជំនួសដែលទាក់ទងនឹង halogenation រ៉ាឌីកាល់ sulfochlorination ឬ nitration នៃម៉ូលេគុល។
ប៉ារ៉ាហ្វីនឆ្លងកាត់ដំណើរការអុកស៊ីតកម្ម ចំហេះ ឬការរលួយនៅសីតុណ្ហភាពខ្ពស់។ នៅក្រោមសកម្មភាពរបស់ឧបករណ៍បង្កើនល្បឿនប្រតិកម្មការលុបបំបាត់អាតូមអ៊ីដ្រូសែនឬការខះជាតិទឹកនៃអាល់កានកើតឡើង។
តើអាល់គីនជាអ្វី
ពួកវាត្រូវបានគេហៅថាអ៊ីដ្រូកាបូនអាសេទីលិកផងដែរ ដែលមានចំណងបីដងនៅក្នុងខ្សែសង្វាក់កាបូន។ រចនាសម្ព័ន្ធនៃ alkynes ត្រូវបានពិពណ៌នាដោយរូបមន្តទូទៅ C n H 2 n-2 ។ វាបង្ហាញថាមិនដូចអាល់កានទេ អ៊ីដ្រូកាបូនអាសេទីលិកខ្វះអាតូមអ៊ីដ្រូសែនបួន។ ពួកវាត្រូវបានជំនួសដោយចំណងបីដងដែលបង្កើតឡើងដោយសមាសធាតុπពីរ។
រចនាសម្ព័ន្ធនេះកំណត់លក្ខណៈគីមីនៃថ្នាក់នេះ។ រូបមន្តរចនាសម្ព័ន្ធនៃ alkenes និង alkynes បង្ហាញយ៉ាងច្បាស់ពីភាពមិនឆ្អែតនៃម៉ូលេគុលរបស់ពួកគេ ក៏ដូចជាវត្តមាននៃចំណងទ្វេ (H 2 C꞊CH 2) និងបីដង (HC≡CH) ។
ឈ្មោះរបស់ alkynes និងលក្ខណៈរបស់វា។
អ្នកតំណាងដ៏សាមញ្ញបំផុតគឺ អាសេទីលីន ឬ HC≡CH ។ វាត្រូវបានគេហៅផងដែរថា ethin ។ វាមកពីឈ្មោះអ៊ីដ្រូកាបូនឆ្អែត ដែលបច្ច័យ -an ត្រូវបានដកចេញ ហើយ -in ត្រូវបានបន្ថែម។ នៅក្នុងឈ្មោះនៃ alkynes វែង លេខបង្ហាញពីទីតាំងនៃចំណងបីដង។
ដោយដឹងពីរចនាសម្ព័ន្ធនៃអ៊ីដ្រូកាបូនឆ្អែត និងមិនឆ្អែត វាអាចធ្វើទៅបានដើម្បីកំណត់នៅក្រោមអក្សរណាដែលរូបមន្តទូទៅនៃ alkynes ត្រូវបានចង្អុលបង្ហាញ៖ ក) CnH2n; គ) CnH2n+2; គ) CnH2n-2; ឃ) CnH2n-6 ។ ចម្លើយត្រឹមត្រូវគឺជាជម្រើសទីបី។
ចាប់ផ្តើមដោយអាសេទីលលីន និងបញ្ចប់ដោយ butane (ពី C 2 ដល់ C 4) សារធាតុមានឧស្ម័ននៅក្នុងធម្មជាតិ។

នៅក្នុងទម្រង់រាវ មានអ៊ីដ្រូកាបូននៃចន្លោះពេលដូចគ្នាពី C 5 ដល់ C 17 ។ ចាប់ផ្តើមពីអាល់គីនដែលមានអាតូមកាបូនចំនួន 18 នៅក្នុងខ្សែសង្វាក់សំខាន់ ការផ្លាស់ប្តូរនៃស្ថានភាពរូបវន្តទៅជាទម្រង់រឹងមួយកើតឡើង។
ពួកវាត្រូវបានកំណត់លក្ខណៈដោយ isomerism នៅក្នុងគ្រោងឆ្អឹងកាបូន នៅក្នុងទីតាំងនៃចំណងបីដង ក៏ដូចជាការកែប្រែអន្តរថ្នាក់នៃម៉ូលេគុល។
អ៊ីដ្រូកាបូនអាសេទីលលីនមានលក្ខណៈគីមីស្រដៀងនឹងអាល់ខេន។
ប្រសិនបើ alkynes មាន terminal triple bond នោះពួកវាដើរតួជាអាស៊ីតជាមួយនឹងការបង្កើតអំបិល alkynide ឧទាហរណ៍ NaC≡CNa។ វត្តមាននៃចំណង π-bonds ពីរធ្វើឱ្យម៉ូលេគុល acetyledine សូដ្យូមក្លាយទៅជា nucleophile ដ៏រឹងមាំដែលចូលទៅក្នុងប្រតិកម្មជំនួស។
Acetylene ឆ្លងកាត់ក្លរីននៅក្នុងវត្តមាននៃក្លរួទង់ដែងដើម្បីទទួលបាន dichloroacetylene ការ condensation នៅក្រោមសកម្មភាពនៃ haloalkynes ជាមួយនឹងការបញ្ចេញម៉ូលេគុល diacetylene ។
Alkynes ត្រូវបានចូលរួមនៅក្នុងប្រតិកម្មដែលគោលការណ៍របស់វាមានមូលដ្ឋានលើ halogenation, hydrohalogenation, hydration និង carbonylation ។ ទោះជាយ៉ាងណាក៏ដោយ ដំណើរការបែបនេះដំណើរការខ្សោយជាងនៅក្នុង alkenes ដែលមានចំណងទ្វេ។
សម្រាប់អ៊ីដ្រូកាបូនអាសេទីលេនីក ប្រតិកម្មបន្ថែមនៃប្រភេទ nucleophilic នៃម៉ូលេគុលអាល់កុល អាមីនបឋម ឬអ៊ីដ្រូសែនស៊ុលហ្វីតអាចធ្វើទៅបាន។
ការបន្ត។ សម្រាប់ការចាប់ផ្តើមសូមមើល № 15, 16, 17, 18, 19/2004
មេរៀនទី៩
លក្ខណៈសម្បត្តិគីមីនៃអាល់ខេន
លក្ខណៈគីមីនៃអាល់ខេន (អេទីឡែន និងភាពដូចគ្នារបស់វា) ត្រូវបានកំណត់យ៉ាងទូលំទូលាយដោយវត្តមានរបស់ d... bonds នៅក្នុងម៉ូលេគុលរបស់វា។ Alkenes ចូលទៅក្នុងប្រតិកម្មទាំងបីប្រភេទ ហើយលក្ខណៈភាគច្រើនបំផុតនៃពួកវាគឺ ប្រតិកម្ម p...។ ពិចារណាពួកវាដោយប្រើ propylene C 3 H 6 ជាឧទាហរណ៍។
ប្រតិកម្មបន្ថែមទាំងអស់ដំណើរការតាមរយៈចំណងទ្វេរ ហើយមាននៅក្នុងការបំបែកនៃ α-bond នៃអាល់ខេន និងការបង្កើតចំណងα-bonds ថ្មីពីរនៅកន្លែងនៃការបំបែក។
ការបន្ថែម halogens៖

ការបន្ថែមអ៊ីដ្រូសែន(ប្រតិកម្មអ៊ីដ្រូសែន)៖
ការតភ្ជាប់ទឹក។(ប្រតិកម្មជាតិទឹក)៖

ការបន្ថែមអ៊ីដ្រូសែន halides (HHal) និងទឹក។ទៅ alkenes មិនស៊ីមេទ្រី យោងទៅតាមច្បាប់របស់ V.V. Markovnikov (1869). អាស៊ីតអ៊ីដ្រូសែនហាល។ ភ្ជាប់ទៅនឹងអាតូមកាបូនអ៊ីដ្រូសែនច្រើនបំផុតនៅចំណងទ្វេ។ដូច្នោះហើយ សំណល់ Hal ភ្ជាប់ទៅនឹងអាតូម C ដែលមានអាតូមអ៊ីដ្រូសែនតិច។

ការដុតអាល់ខេននៅក្នុងខ្យល់។
នៅពេលបញ្ឆេះ អាល់ខេនឆេះនៅលើអាកាស៖
2CH 2 \u003d CHCH 3 + 9O 2 6CO 2 + 6H 2 O ។
អាល់ខេនឧស្ម័នបង្កើតជាល្បាយផ្ទុះជាមួយអុកស៊ីសែនបរិយាកាស។
អាល់ខេនត្រូវបានកត់សុីដោយសារធាតុប៉ូតាស្យូម permanganate នៅក្នុងឧបករណ៍ផ្ទុក aqueous ដែលត្រូវបានអមដោយការប្រែពណ៌នៃដំណោះស្រាយ KMnO 4 និងការបង្កើត glycols (សមាសធាតុជាមួយក្រុម hydroxyl ពីរនៅអាតូម C នៅជាប់គ្នា) ។ ដំណើរការនេះ - hydroxylation នៃ alkenes:

Alkenes ត្រូវបានកត់សុីដោយអុកស៊ីសែនបរិយាកាសទៅជា epoxides ។នៅពេលដែលកំដៅនៅក្នុងវត្តមាននៃកាតាលីករប្រាក់:

វត្ថុធាតុ polymerization នៃ alkenes- ការភ្ជាប់នៃម៉ូលេគុលអាល់ខេនជាច្រើនទៅគ្នាទៅវិញទៅមក។ លក្ខខណ្ឌនៃប្រតិកម្ម: កំដៅ, វត្តមាននៃកាតាលីករ។ ការភ្ជាប់នៃម៉ូលេគុលកើតឡើងដោយការបំបែកចំណងអន្តរម៉ូលេគុល និងការបង្កើតចំណងអន្តរម៉ូលេគុលថ្មី៖

នៅក្នុងប្រតិកម្មនេះជួរនៃតម្លៃ ន = 10 3 –10 4 .
លំហាត់។
1. សរសេរសមីការប្រតិកម្មសម្រាប់ butene-1 ដោយ៖ ក) Br2; ខ) HBr; ក្នុង) H2O; ឆ) H2. ដាក់ឈ្មោះផលិតផលប្រតិកម្ម។
2.
លក្ខខណ្ឌត្រូវបានគេដឹងដែលការបន្ថែមទឹក និងអ៊ីដ្រូសែន halides ទៅនឹងចំណងទ្វេរនៃ alkenes ដំណើរការប្រឆាំងនឹងច្បាប់ Markovnikov ។ សរសេរសមីការប្រតិកម្ម
3-bromopropylene យោងតាមការប្រឆាំងនឹង Markovnikov ជាមួយ: ក) ទឹក; ខ) អ៊ីដ្រូសែនប្រូមីត។
3.
សរសេរសមីការសម្រាប់ប្រតិកម្មវត្ថុធាតុ polymerization: a) butene-1; ខ) វីនីលក្លរ CH 2 = CHCl;
គ) 1,2-difluoroethylene ។
4. ធ្វើសមីការសម្រាប់ប្រតិកម្មនៃអេទីឡែនជាមួយអុកស៊ីហ៊្សែនសម្រាប់ដំណើរការដូចខាងក្រោមៈ ក) ្រំមហះក្នុងខ្យល់; ខ) hydroxylation ជាមួយទឹក KMnO 4 ; គ) epoxidation (250 ° C,អា ).
5. សរសេររូបមន្តរចនាសម្ព័ន្ធនៃអាល់ខេនដោយដឹងថា 0.21 ក្រាមនៃសមាសធាតុនេះអាចបន្ថែម 0,8 ក្រាមនៃ bromine ។
6. នៅពេលដុត 1 លីត្រនៃអ៊ីដ្រូកាបូនឧស្ម័នដែលធ្វើអោយពណ៌នៃដំណោះស្រាយ raspberry នៃប៉ូតាស្យូម permanganate អុកស៊ីសែន 4.5 លីត្រត្រូវបានប្រើប្រាស់ហើយ 3 លីត្រត្រូវបានទទួល។ឧស្ម័នកាបូនិក សរសេររូបមន្តរចនាសម្ព័ន្ធសម្រាប់អ៊ីដ្រូកាបូននេះ។
មេរៀនទី១០
ការទទួលបាននិងការប្រើប្រាស់អាល់ខេន
ប្រតិកម្មសម្រាប់ការទទួលបានអាល់ខេនត្រូវបានកាត់បន្ថយទៅជាការបញ្ច្រាសប្រតិកម្មតំណាងឱ្យលក្ខណៈគីមីនៃអាល់ខេន (លំហូររបស់វាពីស្តាំទៅឆ្វេង មើលមេរៀនទី 9)។ អ្នកគ្រាន់តែត្រូវការស្វែងរកលក្ខខណ្ឌត្រឹមត្រូវ។
ការលុបបំបាត់អាតូម halogen ពីរពី dihaloalkanesមានផ្ទុកសារធាតុ halogens នៅអាតូម C ជិតខាង។ ប្រតិកម្មកើតឡើងក្រោមសកម្មភាពនៃលោហធាតុ (Zn ។ល។)៖

ការបំបែកអ៊ីដ្រូកាបូនឆ្អែត។ ដូច្នេះក្នុងអំឡុងពេលនៃការបំបែក (សូមមើលមេរៀនទី 7) នៃអេតាន ល្បាយនៃអេទីឡែន និងអ៊ីដ្រូសែនត្រូវបានបង្កើតឡើង៖
ការខះជាតិទឹកនៃជាតិអាល់កុល។ នៅពេលដែលអាល់កុលត្រូវបានព្យាបាលដោយសារធាតុបំបាត់ទឹក (អាស៊ីតស៊ុលហ្វួរីកកំហាប់) ឬនៅពេលដែលត្រូវបានកំដៅដល់ 350 ° C នៅក្នុងវត្តមាននៃកាតាលីករ ទឹកត្រូវបានបំបែកចេញ ហើយអាល់ខេនត្រូវបានបង្កើតឡើង:
តាមរបៀបនេះអេទីឡែនត្រូវបានទទួលនៅក្នុងមន្ទីរពិសោធន៍។
វិធីសាស្រ្តឧស្សាហកម្មសម្រាប់ផលិត propylene រួមជាមួយនឹងការបំបែកគឺការខះជាតិទឹកនៃ propanol លើអាលុយមីញ៉ូម:

Dehydrochlorination នៃ chloroalkanes ត្រូវបានអនុវត្តនៅក្រោមសកម្មភាពនៃដំណោះស្រាយអាល់កាឡាំងនៅក្នុងអាល់កុល, ដោយសារតែ នៅក្នុងទឹក ផលិតផលប្រតិកម្មមិនមែនជាអាល់កុលទេ ប៉ុន្តែមានជាតិអាល់កុល
ការប្រើប្រាស់អេទីឡែន និងលក្ខណៈដូចគ្នារបស់វា។ដោយផ្អែកលើលក្ខណៈសម្បត្តិគីមីរបស់ពួកគេ ពោលគឺសមត្ថភាពក្នុងការប្រែក្លាយទៅជាសារធាតុមានប្រយោជន៍ផ្សេងៗ។
ឥន្ធនៈម៉ូតូជាមួយនឹងលេខ octane ខ្ពស់ត្រូវបានទទួលដោយ hydrogenation នៃ alkenes សាខា:

ការប្រែពណ៌នៃសូលុយស្យុង bromine ពណ៌លឿងនៅក្នុងសារធាតុរំលាយអសកម្ម (CCl 4) កើតឡើងនៅពេលដែលការធ្លាក់ចុះនៃអាល់ខេនត្រូវបានបន្ថែម ឬអាល់ខេនឧស្ម័នត្រូវបានឆ្លងកាត់ដំណោះស្រាយ។ អន្តរកម្មជាមួយប្រូមីន - លក្ខណៈ ប្រតិកម្មគុណភាពទៅនឹងចំណងទ្វេ:
ផលិតផលនៃ ethylene hydrochlorination, chloroethane, ត្រូវបានប្រើនៅក្នុង ការសំយោគគីមីដើម្បីណែនាំក្រុម C 2 H 5 ទៅក្នុងម៉ូលេគុល៖
Chloroethane ក៏មានប្រសិទ្ធិភាពថ្នាំស្ពឹកក្នុងតំបន់ (បំបាត់ការឈឺចាប់) ដែលត្រូវបានប្រើក្នុងប្រតិបត្តិការវះកាត់។
ជាតិអាល់កុលត្រូវបានទទួលដោយជាតិទឹកនៃ alkenes ឧទាហរណ៍ អេតាណុល:
អាល់កុល C 2 H 5 OH ត្រូវបានគេប្រើជាសារធាតុរំលាយ សម្រាប់ការសម្លាប់មេរោគ ក្នុងការសំយោគសារធាតុថ្មី។

ជាតិទឹកនៃអេទីឡែននៅក្នុងវត្តមាននៃភ្នាក់ងារអុកស៊ីតកម្ម [O] នាំឱ្យមានអេទីឡែន glycol - ការរបឆាមងនឹងកមនក និងផលិតផលកម្រិតមធ្យមនៃការសំយោគគីមី:

អេទីឡែនត្រូវបានកត់សុីដើម្បីផលិតអេទីឡែនអុកស៊ីដ និងអាសេតាល់ដេអ៊ីត។ វត្ថុធាតុដើមក្នុងឧស្សាហកម្មគីមី៖
![]()
ប៉ូលីមឺរ និងប្លាស្ទិក- ផលិតផលនៃវត្ថុធាតុ polymerization នៃ alkenes ឧទាហរណ៍ polytetrafluoroethylene (Teflon):
លំហាត់។
1. បំពេញសមីការសម្រាប់ប្រតិកម្មនៃការលុបបំបាត់ (ការបំបែក), ដាក់ឈ្មោះអាល់ខេនលទ្ធផល:
2.
ធ្វើសមីការសម្រាប់ប្រតិកម្មអ៊ីដ្រូសែន៖ ក) 3,3-dimethylbutene-1;
ខ) 2,3,3-trimethylbutene-1 ។ ប្រតិកម្មទាំងនេះផលិតអាល់កានដែលប្រើជាឥន្ធនៈម៉ូទ័រ ផ្តល់ឈ្មោះឱ្យពួកគេ។
3. 100 ក្រាមនៃជាតិអាល់កុលអេទីលត្រូវបានឆ្លងកាត់បំពង់ដែលពោរពេញទៅដោយអាមីណូដែលគេឱ្យឈ្មោះថា។ C 2 H 5 OH ។ នេះបណ្តាលឱ្យមាន 33.6 លីត្រនៃអ៊ីដ្រូកាបូន (n.o.s.) ។ តើជាតិអាល់កុល (គិតជា%) មានប្រតិកម្មប៉ុន្មាន?
4. តើប្រូមីនប៉ុន្មានក្រាមនឹងប្រតិកម្មជាមួយអេទីឡែន 2.8 លីត្រ?
5. សរសេរសមីការសម្រាប់វត្ថុធាតុ polymerization នៃ trifluorochloroethylene ។ (ផ្លាស្ទិចលទ្ធផលគឺធន់នឹងអាស៊ីតស៊ុលហ្វួរីកក្តៅ សូដ្យូមលោហធាតុ។ល។)
ចម្លើយចំពោះលំហាត់សម្រាប់ប្រធានបទ ១
មេរៀនទី៩


5. ប្រតិកម្មរបស់អាល់កេន C ន H2 នជាមួយនឹង bromine ជាទូទៅ:
![]()
ម៉ាស់ម៉ូលនៃអាល់ខេន ម(ជាមួយ ន H2 ន) = 0.21 160/0.8 = 42 ក្រាម/mol ។
នេះគឺជា propylene ។
ចម្លើយ.
រូបមន្តអាល់ខេនគឺ CH 2 \u003d CHCH 3 (propylene) ។
6. ដោយសារសារធាតុទាំងអស់ដែលពាក់ព័ន្ធនឹងប្រតិកម្មគឺជាឧស្ម័ន មេគុណ stoichiometric នៅក្នុងសមីការប្រតិកម្មគឺសមាមាត្រទៅនឹងសមាមាត្របរិមាណរបស់វា។ ចូរយើងសរសេរសមីការប្រតិកម្ម៖
ជាមួយ កហ ក្នុង+ 4.5O 2 3CO 2 + 3H 2 O ។
ចំនួនម៉ូលេគុលទឹកត្រូវបានកំណត់ដោយសមីការប្រតិកម្ម៖ 4.5 2 = 9 O អាតូមមានប្រតិកម្ម 6 O អាតូមត្រូវបានចងនៅក្នុង CO 2 អាតូម 3 O ដែលនៅសល់គឺជាផ្នែកនៃម៉ូលេគុល H 2 O បី។ ដូច្នេះសន្ទស្សន៍គឺស្មើគ្នា៖ ក = 3, ក្នុង\u003d 6. អ៊ីដ្រូកាបូនដែលចង់បានគឺ propylene C 3 H 6 ។
ចម្លើយ.
រូបមន្តរចនាសម្ព័ន្ធនៃ propylene គឺ CH 2 = CHCH 3 ។
មេរៀនទី១០
1. សមីការប្រតិកម្មលុបបំបាត់ (ការបំបែក) - ការសំយោគអាល់ខេន៖

2. ប្រតិកម្មអ៊ីដ្រូសែននៃអាល់ខេននៅពេលដែលកំដៅក្រោមសម្ពាធនៅក្នុងវត្តមាននៃកាតាលីករ:

3. ប្រតិកម្មនៃការខះជាតិទឹកនៃជាតិអាល់កុលអេទីលមានទម្រង់៖
![]()
នៅទីនេះតាមរយៈ Xម៉ាស់អាល់កុលបំប្លែងទៅជាអេទីឡែនត្រូវបានចង្អុលបង្ហាញ។
ចូរយើងស្វែងរកតម្លៃ X: X\u003d 46 33.6 / 22.4 \u003d 69 ក្រាម។
សមាមាត្រនៃជាតិអាល់កុលដែលមានប្រតិកម្មគឺ: 69/100 = 0.69 ឬ 69% ។
ចម្លើយ.
អាល់កុល 69% មានប្រតិកម្ម។
4.
![]()
ដោយសារមេគុណ stoichiometric នៅពីមុខរូបមន្តនៃប្រតិកម្ម (C 2 H 4 និង Br 2) គឺស្មើនឹងមួយ ទំនាក់ទំនងមានសុពលភាព៖
2,8/22,4 = X/១៦០. ពីទីនេះ X= 20 ក្រាម Br 2 .
ចម្លើយ.
20 ក្រាម Br 2 .
Alkenes គឺជាអ៊ីដ្រូកាបូន aliphatic ដែលមិនឆ្អែតឆ្អែត ជាមួយនឹងចំណងពីរកាបូន-កាបូនមួយ ឬច្រើន។ ចំណងទ្វេរដងបំប្លែងអាតូមកាបូនពីរទៅជារចនាសម្ព័ន្ធប្លង់ដែលមានមុំចំណងរវាងចំណងនៅជាប់គ្នានៃ 120°C៖
ស៊េរីអាល់ខេនដូចគ្នាមានរូបមន្តទូទៅ សមាជិកពីរដំបូងរបស់វាគឺ អេទីឡែន (អេទីឡែន) និងប្រូផេន (ប្រូភីលីន)៖

សមាជិកនៃស៊េរីអាល់ខេនដែលមានអាតូមកាបូន 4 ឬច្រើនបង្ហាញពីទីតាំងចំណងអ៊ីសូមឺរីម។ ឧទាហរណ៍ អាល់ខេនដែលមានរូបមន្តមាន អ៊ីសូមឺរចំនួនបី ដែលពីរជាអ៊ីសូម័រទីតាំងចំណង៖
ចំណាំថាលេខរៀងនៃខ្សែសង្វាក់អាល់ខេនត្រូវបានធ្វើឡើងពីចុងរបស់វា ដែលនៅជិតទៅនឹងចំណងទ្វេ។ ទីតាំងនៃចំណងទ្វេត្រូវបានចង្អុលបង្ហាញដោយលេខតូចជាងនៃលេខទាំងពីរ ដែលត្រូវនឹងអាតូមកាបូនទាំងពីរដែលភ្ជាប់គ្នាដោយចំណងទ្វេ។ isomer ទីបីមានរចនាសម្ព័ន្ធសាខា:

ចំនួនអ៊ីសូមនៃអាល់ខេនណាមួយកើនឡើងជាមួយនឹងចំនួនអាតូមកាបូន។ ឧទាហរណ៍ hexene មាន isomers ទីតាំងចំណងបី:
Diene គឺ buta-1,3-diene ឬគ្រាន់តែជា butadiene៖
សមាសធាតុដែលមានចំណងទ្វេរបីត្រូវបានគេហៅថា trienes ។ សមាសធាតុដែលមានចំណងទ្វេរដងច្រើនត្រូវបានសំដៅជារួមថាជាប៉ូលីអ៊ីត។
លក្ខណៈសម្បត្តិរូបវន្ត
Alkenes មានចំណុចរលាយនិងរំពុះទាបជាងអាល់កានដែលត្រូវគ្នារបស់វាបន្តិច។ ឧទាហរណ៍ pentane មានចំណុចរំពុះ។ Ethylene, propene និង isomers បីនៃ butene គឺស្ថិតនៅក្នុងស្ថានភាពឧស្ម័ននៅសីតុណ្ហភាពបន្ទប់ និងសម្ពាធធម្មតា។ អាល់ខេនដែលមានចំនួនអាតូមកាបូនពី 5 ទៅ 15 គឺស្ថិតក្នុងសភាពរាវក្រោមលក្ខខណ្ឌធម្មតា។ ភាពប្រែប្រួលរបស់ពួកគេ ដូចជាអាល់កាន កើនឡើងនៅក្នុងវត្តមាននៃការបំបែកនៅក្នុងខ្សែសង្វាក់កាបូន។ អាល់ខេនដែលមានអាតូមកាបូនច្រើនជាង 15 គឺជាសារធាតុរឹងនៅក្រោមលក្ខខណ្ឌធម្មតា។
ការទទួលបាននៅក្នុងមន្ទីរពិសោធន៍
វិធីសាស្រ្តសំខាន់ពីរសម្រាប់ការទទួលបាន alkenes នៅក្នុងមន្ទីរពិសោធន៍គឺការខ្សោះជាតិទឹកនៃជាតិអាល់កុល និងការ dehydrohalogenation នៃ haloalkanes ។ ឧទាហរណ៍ អេទីឡែនអាចទទួលបានដោយការខ្សោះជាតិទឹកនៃអេតាណុលជាមួយនឹងអាស៊ីតស៊ុលហ្វួរីកកំហាប់លើសនៅសីតុណ្ហភាព 170 °C (សូមមើលផ្នែក 19.2)៖
អេទីឡែនក៏អាចទទួលបានពីអេតាណុលដោយឆ្លងកាត់ចំហាយអេតាណុលលើផ្ទៃនៃអាលុយមីណាដែលគេឱ្យឈ្មោះថា។ ចំពោះគោលបំណងនេះ ការរៀបចំបង្ហាញតាមគ្រោងការណ៍ក្នុងរូប។ ១៨.៣.
វិធីសាស្រ្តទូទៅទីពីរសម្រាប់ការទទួលបាន alkenes គឺផ្អែកលើ dehydrohalogenation នៃ haloalkanes ក្រោមលក្ខខណ្ឌនៃកាតាលីករមូលដ្ឋាន។
យន្តការនៃប្រតិកម្មនៃការលុបបំបាត់ប្រភេទនេះត្រូវបានពិពណ៌នានៅក្នុង Sec ។ ១៧.៣.
ប្រតិកម្មនៃអាល់ខេន
អាល់ខេនមានប្រតិកម្មច្រើនជាងអាល់ខេន។ នេះគឺដោយសារតែសមត្ថភាពនៃអេឡិចត្រុងចំណងទ្វេដើម្បីទាក់ទាញ electrophiles (សូមមើលផ្នែកទី 17.3) ។ ដូច្នេះ ប្រតិកម្មលក្ខណៈនៃ alkenes គឺជាប្រតិកម្មចម្បងនៃការបន្ថែម electrophilic ទៅនឹងចំណងទ្វេរដង៖

ប្រតិកម្មទាំងនេះជាច្រើនមានយន្តការអ៊ីយ៉ុង (សូមមើលផ្នែកទី 17.3) ។
អ៊ីដ្រូសែន
ប្រសិនបើអាល់ខេនណាមួយដូចជាអេទីឡែនត្រូវបានលាយជាមួយនឹងអ៊ីដ្រូសែន ហើយល្បាយនេះត្រូវបានឆ្លងកាត់លើផ្ទៃនៃកាតាលីករប្លាទីននៅសីតុណ្ហភាពបន្ទប់ ឬសារធាតុនីកែលនៅសីតុណ្ហភាពប្រហែល 150 ° C នោះការបន្ថែមនឹងកើតឡើង។
អ៊ីដ្រូសែននៅចំណងទ្វេនៃអាល់ខេន។ ក្នុងករណីនេះអាល់កានដែលត្រូវគ្នាត្រូវបានបង្កើតឡើង:

ប្រភេទនៃប្រតិកម្មនេះគឺជាឧទាហរណ៍នៃកាតាលីករខុសប្រក្រតី។ យន្តការរបស់វាត្រូវបានពិពណ៌នានៅក្នុងវិនាទី។ 9.2 ហើយត្រូវបានបង្ហាញតាមគ្រោងការណ៍នៅក្នុងរូបភព។ ៩.២០.
ការបន្ថែម halogens
ក្លរីនឬប្រូមីនត្រូវបានបន្ថែមយ៉ាងងាយស្រួលទៅនឹងចំណងទ្វេរនៃអាល់ខេន។ ប្រតិកម្មនេះកើតឡើងនៅក្នុងសារធាតុរំលាយដែលមិនមែនជាប៉ូល ដូចជាកាបូន tetrachloride ឬ hexane ។ ប្រតិកម្មដំណើរការទៅតាមយន្តការអ៊ីយ៉ូដ ដែលរួមមានការបង្កើតកាបូនិក។ ចំណងទ្វេធ្វើឱ្យប៉ូឡូញម៉ូលេគុល halogen ប្រែទៅជាឌីប៉ូល៖

ដូច្នេះ សូលុយស្យុង bromine នៅក្នុង hexane ឬ tetrachloromethane ក្លាយជាគ្មានពណ៌ នៅពេលដែលរង្គោះរង្គើជាមួយអាល់ខេន។ រឿងដដែលនេះកើតឡើងប្រសិនបើអ្នកអ្រងួនអាល់ខេនជាមួយនឹងទឹកប្រូមីន។ ទឹក Bromine គឺជាដំណោះស្រាយនៃសារធាតុ bromine នៅក្នុងទឹក។ ដំណោះស្រាយនេះមានផ្ទុកអាស៊ីត hypobromous ។ ម៉ូលេគុលអាស៊ីត hypochlorous ត្រូវបានភ្ជាប់នៅចំណងទ្វេរដងនៃអាល់ខេន ហើយជាលទ្ធផល ជាតិអាល់កុលជំនួស bromo ត្រូវបានបង្កើតឡើង។ ឧទាហរណ៍

ការបន្ថែមអ៊ីដ្រូសែន halides
យន្តការនៃប្រតិកម្មប្រភេទនេះត្រូវបានពិពណ៌នានៅក្នុង Sec ។ ១៨.៣. ជាឧទាហរណ៍ សូមពិចារណាពីការបន្ថែមអ៊ីដ្រូសែនក្លរួទៅប្រូផេន៖
ចំណាំថាផលិតផលនៃប្រតិកម្មនេះគឺ 2-chloropropane មិនមែន 1-chloro-propane:
![]()
នៅក្នុងប្រតិកម្មបន្ថែមបែបនេះ អាតូមអេឡិចត្រុងអេឡិចត្រុង ឬក្រុមអេឡិចត្រុងអវិជ្ជមានភាគច្រើនតែងតែត្រូវបានបន្ថែមទៅអាតូមកាបូនដែលជាប់នឹង
ចំនួនអាតូមអ៊ីដ្រូសែនតិចបំផុត។ ភាពទៀងទាត់នេះត្រូវបានគេហៅថាច្បាប់របស់ Markovnikov ។
ការបន្ថែមអាតូម electronegative ឬក្រុមទៅអាតូមកាបូនដែលត្រូវបានផ្សារភ្ជាប់ជាមួយនឹងអាតូមអ៊ីដ្រូសែនតិចតួចបំផុតគឺដោយសារតែការកើនឡើងនៃស្ថេរភាពនៃ carbocation នៅពេលដែលចំនួននៃសារធាតុជំនួសអាល់គីលនៅលើអាតូមកាបូនកើនឡើង។ ការកើនឡើងនៃស្ថេរភាពនេះត្រូវបានពន្យល់ដោយឥទ្ធិពលអាំងឌុចស្យុងដែលកើតឡើងនៅក្នុងក្រុមអាល់គីល ព្រោះវាជាអ្នកផ្តល់អេឡិចត្រុង៖

នៅក្នុងវត្តមាននៃ peroxide សរីរាង្គណាមួយ propene មានប្រតិកម្មជាមួយនឹងអ៊ីដ្រូសែន bromide បង្កើត ពោលគឺមិនមែនយោងទៅតាមច្បាប់របស់ Markovnikov ទេ។ ផលិតផលបែបនេះត្រូវបានគេហៅថាប្រឆាំងនឹង Markovnikov ។ វាត្រូវបានបង្កើតឡើងជាលទ្ធផលនៃប្រតិកម្មដែលដំណើរការទៅតាមរ៉ាឌីកាល់ជាជាងយន្តការអ៊ីយ៉ុង។
ជាតិទឹក
អាល់ខេនមានប្រតិកម្មជាមួយនឹងអាស៊ីតស៊ុលហ្វួរីកប្រមូលផ្តុំត្រជាក់ដើម្បីបង្កើតជាអាល់គីលអ៊ីដ្រូសែនស៊ុលហ្វាត។ ឧទាហរណ៍

ប្រតិកម្មនេះគឺជាការបន្ថែមព្រោះវាបន្ថែមអាស៊ីតទៅនឹងចំណងទ្វេ។ វាគឺជាប្រតិកម្មបញ្ច្រាសទាក់ទងនឹងការខះជាតិទឹកនៃអេតាណុលជាមួយនឹងការបង្កើតអេទីឡែន។ យន្តការនៃប្រតិកម្មនេះគឺស្រដៀងគ្នាទៅនឹងយន្តការនៃការបន្ថែមនៃអ៊ីដ្រូសែន halides ទៅចំណងទ្វេ។ វាពាក់ព័ន្ធនឹងការបង្កើត carbocation កម្រិតមធ្យម។ ប្រសិនបើផលិតផលនៃប្រតិកម្មនេះត្រូវបានពនឺដោយទឹក និងកម្តៅថ្នមៗ នោះវា hydrolyzes ដើម្បីបង្កើតជាអេតាណុល៖
ប្រតិកម្មបន្ថែមនៃអាស៊ីតស៊ុលហ្វួរីកចំពោះអាល់ខេន គោរពតាមច្បាប់ Markovnikov៖

ប្រតិកម្មជាមួយនឹងដំណោះស្រាយអាស៊ីតនៃសារធាតុប៉ូតាស្យូម permanganate
ពណ៌ violet នៃដំណោះស្រាយអាស៊ីតនៃសារធាតុប៉ូតាស្យូម permanganate បាត់ប្រសិនបើដំណោះស្រាយនេះត្រូវបានរង្គោះរង្គើក្នុងល្បាយជាមួយអាល់ខេន។ hydroxylation នៃ alkene កើតឡើង (ការណែនាំនៃក្រុម hydroxy ចូលទៅក្នុងវាដែលត្រូវបានបង្កើតឡើងដោយសារតែការកត់សុី) ដែលជាលទ្ធផលប្រែទៅជា diol ។ ឧទាហរណ៍ នៅពេលដែលអង្រួនបរិមាណអេទីឡែនលើសជាមួយនឹងដំណោះស្រាយអាស៊ីត អេទីឡែន-1,2-ឌីអុល (អេទីឡែន glycol) ត្រូវបានបង្កើតឡើង។

ប្រសិនបើអាល់ខេនត្រូវបានរង្គោះរង្គើជាមួយនឹងដំណោះស្រាយ -ion លើសនោះ ការបំបែកអុកស៊ីតកម្មនៃអាល់ខេនកើតឡើង ដែលនាំទៅដល់ការបង្កើត aldehydes និង ketones៖
សារធាតុ aldehydes ដែលបង្កើតឡើងក្នុងដំណើរការនេះ ឆ្លងកាត់ការកត់សុីបន្ថែមទៀតដើម្បីបង្កើតជាអាស៊ីត carboxylic ។
Hydroxylation នៃ alkenes ដើម្បីបង្កើត diols ក៏អាចត្រូវបានអនុវត្តដោយប្រើដំណោះស្រាយអាល់កាឡាំងនៃប៉ូតាស្យូម permanganate ។
ប្រតិកម្មជាមួយអាស៊ីត perbenzoic
Alkenes មានប្រតិកម្មជាមួយនឹងអាស៊ីត peroxy (peracids) ដូចជាអាស៊ីត perbenzoic ដើម្បីបង្កើតជា cyclic ethers (សមាសធាតុ epoxy) ។ ឧទាហរណ៍

នៅពេលដែល epoxyethane ត្រូវបានកំដៅដោយទន់ភ្លន់ជាមួយនឹងដំណោះស្រាយពនឺនៃអាស៊ីតណាមួយ ethane-1,2-diol ត្រូវបានបង្កើតឡើង:

ប្រតិកម្មជាមួយអុកស៊ីសែន
ដូចអ៊ីដ្រូកាបូនផ្សេងទៀតទាំងអស់ អាល់ខេនឆេះ ហើយដោយមានខ្យល់ច្រើន បង្កើតជាកាបូនឌីអុកស៊ីត និងទឹក៖
ជាមួយនឹងការចូលប្រើខ្យល់មានកំណត់ ការឆេះនៃអាល់ខេននាំទៅដល់ការបង្កើតកាបូនម៉ូណូអុកស៊ីត និងទឹក៖
ដោយសារអាល់ខេនមានមាតិកាកាបូនដែលទាក់ទងខ្ពស់ជាងអាល់កានដែលត្រូវគ្នា ពួកវាឆេះដោយអណ្តាតភ្លើងដែលមានផ្សែង។ នេះបណ្តាលមកពីការបង្កើតភាគល្អិតកាបូន៖
ប្រសិនបើអ្នកលាយអាល់ខេនណាមួយជាមួយអុកស៊ីហ៊្សែន ហើយឆ្លងកាត់ល្បាយនេះលើផ្ទៃនៃសារធាតុប្រាក់ អេផូស៊ីអ៊ីតានត្រូវបានបង្កើតឡើងនៅសីតុណ្ហភាពប្រហែល 200 អង្សារសេ៖
អុកស៊ីហ្សែន
នៅពេលដែលឧស្ម័នអូហ្សូនត្រូវបានឆ្លងកាត់ដំណោះស្រាយនៃអាល់ខេននៅក្នុង trichloromethane ឬ tetrachloromethane នៅសីតុណ្ហភាពក្រោម 20 ° C នោះ ozonide នៃ alkene ដែលត្រូវគ្នា (oxirane) ត្រូវបានបង្កើតឡើង។

Ozonides គឺជាសមាសធាតុមិនស្ថិតស្ថេរ ហើយអាចផ្ទុះបាន។ ពួកវាឆ្លងកាត់អ៊ីដ្រូលីស៊ីសដើម្បីបង្កើត អាល់ឌីអ៊ីត ឬ ខេតូន។ ឧទាហរណ៍

ក្នុងករណីនេះផ្នែកនៃមេតាណុល (formaldehyde) មានប្រតិកម្មជាមួយនឹងអ៊ីដ្រូសែន peroxide បង្កើតជាអាស៊ីតមេតាន (ទម្រង់)៖
វត្ថុធាតុ polymerization
អាល់ខេនសាមញ្ញបំផុតអាចធ្វើវត្ថុធាតុ polymerize ដើម្បីបង្កើតជាសមាសធាតុទម្ងន់ម៉ូលេគុលខ្ពស់ដែលមានរូបមន្តជាក់ស្តែងដូចគ្នានឹងអាល់ខេនមេ៖
ប្រតិកម្មនេះកើតឡើងនៅសម្ពាធខ្ពស់នៅសីតុណ្ហភាព 120°C និងនៅក្នុងវត្តមានអុកស៊ីហ្សែនដែលដើរតួនាទីជាកាតាលីករ។ ទោះជាយ៉ាងណាក៏ដោយវត្ថុធាតុ polymerization អេទីឡែនក៏អាចត្រូវបានអនុវត្តនៅសម្ពាធទាបដោយប្រើកាតាលីករ Ziegler ។ កាតាលីករ Ziegler ទូទៅបំផុតមួយគឺល្បាយនៃ triethylaluminum និង titanium tetrachloride ។
Polymerization នៃ alkenes ត្រូវបានពិភាក្សាលម្អិតនៅក្នុង Sec ។ ១៨.៣.
សារធាតុដែលមានចំណង pi គឺជាអ៊ីដ្រូកាបូនមិនឆ្អែត។ ពួកវាជាដេរីវេនៃអាល់កាន ដែលនៅក្នុងម៉ូលេគុលដែលអាតូមអ៊ីដ្រូសែនពីរត្រូវបានបំបែកចេញ។ វ៉ាឡង់សេរីជាលទ្ធផលបង្កើតបានជាចំណងប្រភេទថ្មី ដែលមានទីតាំងនៅកាត់កែងទៅនឹងយន្តហោះនៃម៉ូលេគុល។ នេះជារបៀបដែលក្រុមថ្មីនៃសមាសធាតុកើតឡើង - អាល់ខេន។ យើងនឹងពិចារណាអំពីលក្ខណៈសម្បត្តិរូបវន្ត ការរៀបចំ និងការប្រើប្រាស់សារធាតុនៃថ្នាក់នេះក្នុងជីវិតប្រចាំថ្ងៃ និងឧស្សាហកម្មនៅក្នុងអត្ថបទនេះ។
ស៊េរីអេទីឡែនដូចគ្នា។
រូបមន្តទូទៅសម្រាប់សមាសធាតុទាំងអស់ហៅថា អាល់ខេន ដែលឆ្លុះបញ្ចាំងពីសមាសភាពគុណភាព និងបរិមាណគឺ C n H 2 n ។ ឈ្មោះនៃអ៊ីដ្រូកាបូនយោងទៅតាមឈ្មោះប្រព័ន្ធមានដូចខាងក្រោម៖ នៅក្នុងពាក្យនៃអាល់កានដែលត្រូវគ្នា បច្ច័យផ្លាស់ប្តូរពី -an ទៅ -ene ឧទាហរណ៍៖ ethane - ethene, propane - propene ។ល។ នៅក្នុងប្រភពមួយចំនួន អ្នកអាច ស្វែងរកឈ្មោះផ្សេងទៀតសម្រាប់សមាសធាតុនៃថ្នាក់នេះ - olefins ។ បន្ទាប់មកទៀត យើងនឹងសិក្សាពីដំណើរការនៃការបង្កើតចំណងទ្វេរដង និងលក្ខណៈសម្បត្តិរូបវន្តនៃអាល់ខេន ហើយក៏កំណត់ការពឹងផ្អែករបស់វាទៅលើរចនាសម្ព័ន្ធនៃម៉ូលេគុលផងដែរ។
តើមូលបត្របំណុលពីរត្រូវបានបង្កើតឡើងដោយរបៀបណា?
លក្ខណៈអេឡិចត្រូនិចនៃចំណង pi ដោយប្រើឧទាហរណ៍នៃអេទីឡែនអាចត្រូវបានតំណាងដូចខាងក្រោមៈ អាតូមកាបូននៅក្នុងម៉ូលេគុលរបស់វាមានទម្រង់ជា sp 2 hybridization ។ ក្នុងករណីនេះចំណង sigma ត្រូវបានបង្កើតឡើង។ គន្លងកូនកាត់ពីរទៀត ដែលមួយចេញពីអាតូមកាបូន បង្កើតជាចំណង sigma សាមញ្ញជាមួយអាតូមអ៊ីដ្រូសែន។ ពពកកូនកាត់ទំនេរពីរដែលនៅសល់នៃអាតូមកាបូនត្រួតលើគ្នាពីលើ និងខាងក្រោមយន្តហោះនៃម៉ូលេគុល - ចំណង pi ត្រូវបានបង្កើតឡើង។ វាគឺជានាងដែលកំណត់លក្ខណៈរូបវន្ត និងគីមីនៃ alkenes ដែលនឹងត្រូវបានពិភាក្សានៅពេលក្រោយ។

isomerism លំហ
សមាសធាតុដែលមានសមាសធាតុបរិមាណ និងគុណភាពដូចគ្នានៃម៉ូលេគុល ប៉ុន្តែរចនាសម្ព័ន្ធលំហខុសគ្នាត្រូវបានគេហៅថា isomers ។ Isomerism កើតឡើងនៅក្នុងក្រុមនៃសារធាតុដែលហៅថាសរីរាង្គ។ លក្ខណៈនៃ olefins ត្រូវបានជះឥទ្ធិពលយ៉ាងខ្លាំងដោយបាតុភូតនៃ isomerism អុបទិក។ វាត្រូវបានបញ្ជាក់នៅក្នុងការពិតដែលថា អេទីឡែន homologues ដែលមានរ៉ាឌីកាល់ផ្សេងគ្នា ឬសារធាតុជំនួសនៅអាតូមកាបូនទាំងពីរនៅក្នុងចំណងទ្វេអាចកើតឡើងក្នុងទម្រង់ជាអ៊ីសូមអុបទិកពីរ។ ពួកវាខុសគ្នាពីគ្នាទៅវិញទៅមកដោយទីតាំងនៃធាតុជំនួសនៅក្នុងលំហដែលទាក់ទងទៅនឹងយន្តហោះនៃចំណងទ្វេ។ លក្ខណៈសម្បត្តិរូបវន្តរបស់ alkenes ក្នុងករណីនេះក៏នឹងខុសគ្នាដែរ។ ឧទាហរណ៍ នេះអនុវត្តចំពោះចំណុចរំពុះ និងរលាយនៃសារធាតុ។ ដូច្នេះ olefins ខ្សែសង្វាក់ត្រង់មានចំណុចរំពុះខ្ពស់ជាងសមាសធាតុ isomer ។ ដូចគ្នានេះផងដែរ, ចំណុចរំពុះនៃ cis isomers នៃ alkenes គឺខ្ពស់ជាងចំណុចនៃ trans isomers ។ ទាក់ទងទៅនឹងសីតុណ្ហភាពរលាយរូបភាពគឺផ្ទុយគ្នា។
លក្ខណៈប្រៀបធៀបនៃលក្ខណៈសម្បត្តិរូបវន្តនៃអេទីឡែន និងលក្ខណៈដូចគ្នារបស់វា។
អ្នកតំណាងបីដំបូងនៃ olefins គឺជាសមាសធាតុឧស្ម័ន បន្ទាប់មកចាប់ផ្តើមពី pentene C 5 H 10 និងរហូតដល់អាល់ខេនដែលមានរូបមន្ត C 17 H 34 ពួកវាជាវត្ថុរាវ ហើយបន្ទាប់មកមានសារធាតុរឹង។ ភាពដូចគ្នានៃ ethene បង្ហាញពីនិន្នាការដូចខាងក្រោម: ចំណុចរំពុះនៃសមាសធាតុថយចុះ។ ឧទាហរណ៍សម្រាប់អេទីឡែនសូចនាករនេះគឺ -169.1 ° C និងសម្រាប់ propylene -187.6 ° C ។ ប៉ុន្តែចំណុចរំពុះកើនឡើងជាមួយនឹងការកើនឡើងទម្ងន់ម៉ូលេគុល។ ដូច្នេះសម្រាប់អេទីឡែនវាគឺ -103.7 ° C និងសម្រាប់ propene -47.7 ° C ។ ដោយសង្ខេបនូវអ្វីដែលបាននិយាយ យើងអាចសន្និដ្ឋានបានថា លក្ខណៈសម្បត្តិរូបវន្តរបស់ alkenes អាស្រ័យលើទម្ងន់ម៉ូលេគុលរបស់វា។ ជាមួយនឹងការកើនឡើងរបស់វាស្ថានភាពសរុបនៃសមាសធាតុផ្លាស់ប្តូរក្នុងទិសដៅ: ឧស្ម័ន - រាវ - រឹងហើយចំណុចរលាយក៏ថយចុះហើយចំណុចរំពុះកើនឡើង។

លក្ខណៈនៃអេទីឡែន
អ្នកតំណាងដំបូងនៃស៊េរីដូចគ្នានៃអាល់ខេនគឺអេទីឡែន។ វាគឺជាឧស្ម័នគ្មានពណ៌ រលាយក្នុងទឹកបន្តិច ប៉ុន្តែអាចរលាយបានខ្ពស់នៅក្នុងសារធាតុរំលាយសរីរាង្គ។ ទំងន់ម៉ូលេគុល - 28, អេទីនគឺស្រាលជាងខ្យល់បន្តិច, មានក្លិនផ្អែមស្រាល។ វាងាយប្រតិកម្មជាមួយ halogens អ៊ីដ្រូសែន និងអ៊ីដ្រូសែន halides ។ ទោះជាយ៉ាងណាក៏ដោយ លក្ខណៈសម្បត្តិរូបវន្តរបស់ alkenes និង paraffin គឺមានភាពជិតស្និទ្ធណាស់។ ឧទាហរណ៍ ស្ថានភាពនៃការប្រមូលផ្តុំ សមត្ថភាពនៃមេតាន និងអេទីឡែន ដើម្បីឆ្លងកាត់ការកត់សុីធ្ងន់ធ្ងរ។ល។ តើអាល់ខេនអាចត្រូវបានសម្គាល់ដោយរបៀបណា? តើធ្វើដូចម្តេចដើម្បីបង្ហាញតួអក្សរ unsaturated នៃ olefin មួយ? ចំពោះបញ្ហានេះមានប្រតិកម្មគុណភាពដែលយើងនឹងរស់នៅដោយលម្អិតបន្ថែមទៀត។ រំលឹកឡើងវិញថាតើលក្ខណៈពិសេសអ្វីខ្លះនៅក្នុងរចនាសម្ព័ន្ធនៃ alkenes ម៉ូលេគុលមាន។ លក្ខណៈសម្បត្តិរូបវន្ត និងគីមីនៃសារធាតុទាំងនេះត្រូវបានកំណត់ដោយវត្តមាននៃចំណងទ្វេរនៅក្នុងសមាសភាពរបស់វា។ ដើម្បីបញ្ជាក់វត្តមានរបស់វា អ៊ីដ្រូកាបូនឧស្ម័នត្រូវបានឆ្លងកាត់ដំណោះស្រាយពណ៌ស្វាយនៃប៉ូតាស្យូម permanganate ឬទឹក bromine ។ ប្រសិនបើពួកវាប្រែពណ៌ នោះសមាសធាតុមានចំណង pi នៅក្នុងសមាសភាពនៃម៉ូលេគុល។ អេទីឡែនចូលទៅក្នុងប្រតិកម្មអុកស៊ីតកម្ម និងធ្វើឱ្យសូលុយស្យុង KMnO 4 និង Br 2 ប្រែពណ៌។
យន្តការនៃប្រតិកម្មបន្ថែម
ការបំបែកចំណងទ្វេរនឹងបញ្ចប់ដោយការបន្ថែមអាតូមនៃធាតុគីមីផ្សេងទៀតទៅនឹង valences សេរីនៃកាបូន។ ឧទាហរណ៍ ប្រតិកម្មនៃអេទីឡែនជាមួយអ៊ីដ្រូសែន ហៅថា អ៊ីដ្រូសែន បង្កើតអេតាន។ ត្រូវការកាតាលីករ ដូចជាម្សៅនីកែល ប៉ាឡាដ្យូម ឬផ្លាទីន។ ប្រតិកម្មជាមួយ HCl បញ្ចប់ដោយការបង្កើតក្លរ៉ូអ៊ីត។ អាល់ខេនដែលមានអាតូមកាបូនច្រើនជាងពីរនៅក្នុងម៉ូលេគុលរបស់ពួកគេឆ្លងកាត់ប្រតិកម្មបន្ថែមនៃអ៊ីដ្រូសែន halides ដោយគិតគូរពីច្បាប់របស់ V. Markovnikov ។

របៀបដែល ethene homologues អន្តរកម្មជាមួយ halides អ៊ីដ្រូសែន
ប្រសិនបើយើងប្រឈមមុខនឹងភារកិច្ច "កំណត់លក្ខណៈរូបវន្តនៃ alkenes និងការរៀបចំរបស់វា" យើងត្រូវពិចារណាច្បាប់របស់ V. Markovnikov ឱ្យបានលំអិត។ វាត្រូវបានបង្កើតឡើងនៅក្នុងការអនុវត្តដែលវត្ថុធាតុដូចគ្នានៃអេទីឡែនមានប្រតិកម្មជាមួយនឹងអ៊ីដ្រូសែនក្លរួ និងសមាសធាតុផ្សេងទៀតនៅកន្លែងនៃការដាច់ចំណងទ្វេ ដោយគោរពតាមគំរូជាក់លាក់មួយ។ វាមាននៅក្នុងការពិតដែលថាអាតូមអ៊ីដ្រូសែនត្រូវបានភ្ជាប់ទៅនឹងអាតូមកាបូនអ៊ីដ្រូសែនច្រើនបំផុត ហើយអ៊ីយ៉ុងក្លរីន ប្រូមីន ឬអ៊ីយ៉ូតត្រូវបានភ្ជាប់ទៅនឹងអាតូមកាបូនដែលមានចំនួនអាតូមអ៊ីដ្រូសែនតិចបំផុត។ លក្ខណៈពិសេសនៃវគ្គសិក្សានៃប្រតិកម្មបន្ថែមត្រូវបានគេហៅថាក្បួនរបស់ V. Markovnikov ។
សំណើមនិងវត្ថុធាតុ polymerization
ចូរយើងបន្តពិចារណាអំពីលក្ខណៈសម្បត្តិរូបវន្ត និងការអនុវត្តនៃ alkenes ដោយប្រើឧទាហរណ៍នៃអ្នកតំណាងទីមួយនៃស៊េរីដូចគ្នា - ethene ។ ប្រតិកម្មរបស់វាជាមួយនឹងទឹកត្រូវបានប្រើនៅក្នុងឧស្សាហកម្មសំយោគសរីរាង្គ និងមានសារៈសំខាន់ជាក់ស្តែង។ ដំណើរការនេះត្រូវបានអនុវត្តជាលើកដំបូងនៅក្នុងសតវត្សទី 19 ដោយ A.M. Butlerov ។ ប្រតិកម្មទាមទារលក្ខខណ្ឌមួយចំនួនដែលត្រូវបំពេញ។ នេះជាដំបូងនៃការទាំងអស់ ការប្រើប្រាស់អាស៊ីតស៊ុលហ្វួរីកប្រមូលផ្តុំ ឬ oleum ជាកាតាលីករ និងសារធាតុរំលាយសម្រាប់អេទីន សម្ពាធប្រហែល 10 atm និងសីតុណ្ហភាពក្នុងរង្វង់ 70 °។ ដំណើរការជាតិទឹកកើតឡើងជាពីរដំណាក់កាល។ ដំបូង ម៉ូលេគុលស៊ុលហ្វាតត្រូវបានបន្ថែមទៅអេទីននៅចំណុចនៃការដាច់នៃចំណង pi ហើយអាស៊ីតអេទីលស៊ុលហ្វួរីកត្រូវបានបង្កើតឡើង។ បន្ទាប់មកសារធាតុលទ្ធផលមានប្រតិកម្មជាមួយទឹក ជាតិអាល់កុល ethyl ត្រូវបានទទួល។ អេតាណុល គឺជាផលិតផលដ៏សំខាន់មួយដែលត្រូវបានប្រើប្រាស់ក្នុងឧស្សាហកម្មម្ហូបអាហារសម្រាប់ផលិតផ្លាស្ទិក កៅស៊ូសំយោគ វ៉ារនីស និងសារធាតុគីមីសរីរាង្គផ្សេងទៀត។

ប៉ូលីមែរដែលមានមូលដ្ឋានលើ Olefin
ដោយបន្តសិក្សាពីបញ្ហានៃការប្រើប្រាស់សារធាតុដែលជាកម្មសិទ្ធិរបស់ថ្នាក់នៃអាល់ខេន យើងនឹងសិក្សាពីដំណើរការនៃវត្ថុធាតុ polymerization របស់ពួកគេ ដែលក្នុងនោះសមាសធាតុដែលមានចំណងគីមី unsaturated នៅក្នុងសមាសភាពនៃម៉ូលេគុលរបស់វាអាចចូលរួមបាន។ ប្រតិកម្មវត្ថុធាតុ polymerization ជាច្រើនប្រភេទត្រូវបានគេស្គាល់ យោងទៅតាមផលិតផលដែលមានម៉ូលេគុលខ្ពស់ត្រូវបានបង្កើតឡើង - សារធាតុប៉ូលីម៊ែរ ដូចជាប៉ូលីអេទីឡែន ប៉ូលីភីលីន ប៉ូលីស្ទីរ៉ែន ជាដើម។ យន្តការរ៉ាឌីកាល់សេរីនាំទៅរកការផលិតប៉ូលីអេទីឡែនដែលមានសម្ពាធខ្ពស់។ វាគឺជាសមាសធាតុមួយដែលត្រូវបានប្រើប្រាស់យ៉ាងទូលំទូលាយបំផុតនៅក្នុងឧស្សាហកម្ម។ ប្រភេទ cationic-ionic ផ្តល់នូវវត្ថុធាតុ polymer ជាមួយនឹងរចនាសម្ព័ន្ធស្តេរ៉េអូដូចជា polystyrene ។ វាត្រូវបានចាត់ទុកថាជាប៉ូលីម័រដែលមានសុវត្ថិភាព និងងាយស្រួលបំផុតក្នុងការប្រើប្រាស់។ ផលិតផលធ្វើពីប៉ូលីស្ទីរីនមានភាពធន់នឹងសារធាតុឈ្លានពាន៖ អាស៊ីត និងអាល់កាឡាំង មិនងាយឆេះ ងាយលាប។ ប្រភេទមួយទៀតនៃយន្តការវត្ថុធាតុ polymerization គឺ dimerization ដែលនាំទៅដល់ការផលិត isobutene ដែលត្រូវបានគេប្រើជាសារធាតុបន្ថែម antiknock សម្រាប់ប្រេងសាំង។
តើធ្វើដូចម្តេចដើម្បីទទួលបាន
Alkenes ដែលជាលក្ខណៈសម្បត្តិរូបវន្តដែលយើងសិក្សាត្រូវបានទទួលនៅក្នុងមន្ទីរពិសោធន៍ និងឧស្សាហកម្មដោយវិធីសាស្រ្តផ្សេងៗ។ នៅក្នុងការពិសោធន៍នៅក្នុងវគ្គសិក្សានៃគីមីវិទ្យាសរីរាង្គ ដំណើរការនៃការខះជាតិទឹកនៃជាតិអាល់កុលអេទីល ត្រូវបានប្រើដោយជំនួយពីភ្នាក់ងារដកទឹក ដូចជាផូស្វ័រផេនអុកស៊ីត ឬអាស៊ីតស៊ុលហ្វាត។ ប្រតិកម្មត្រូវបានធ្វើឡើងនៅពេលដែលត្រូវបានកម្ដៅហើយជាការបញ្ច្រាសនៃដំណើរការទទួលបានអេតាណុល។ វិធីសាស្រ្តទូទៅមួយផ្សេងទៀតសម្រាប់ការទទួលបានអាល់ខេនបានរកឃើញកម្មវិធីរបស់វានៅក្នុងឧស្សាហកម្មដូចជា៖ កំដៅ halogen ដេរីវេនៃអ៊ីដ្រូកាបូនឆ្អែត ដូចជា chloropropane ជាមួយនឹងដំណោះស្រាយអាល់កុលប្រមូលផ្តុំនៃអាល់កាឡាំង - សូដ្យូម ឬប៉ូតាស្យូមអ៊ីដ្រូសែន។ នៅក្នុងប្រតិកម្ម ម៉ូលេគុលអ៊ីដ្រូសែនក្លរួត្រូវបានបំបែកចេញ ចំណងទ្វេរដងត្រូវបានបង្កើតឡើងនៅកន្លែងដែលអាតូមកាបូនលេចឡើង។ ផលិតផលចុងក្រោយនៃដំណើរការគីមីនឹងជា olefin - propene ។ ដោយបន្តពិចារណាលើលក្ខណៈសម្បត្តិរូបវន្តរបស់អាល់ខេន ចូរយើងរស់នៅលើដំណើរការសំខាន់សម្រាប់ការទទួលបាន olefins - pyrolysis ។

ផលិតកម្មឧស្សាហកម្មនៃអ៊ីដ្រូកាបូនមិនឆ្អែតនៃស៊េរីអេទីឡែន
វត្ថុធាតុដើមដែលមានតំលៃថោក - ឧស្ម័នដែលបានបង្កើតឡើងនៅក្នុងដំណើរការនៃការបំបែកប្រេងបម្រើជាប្រភពនៃ olefins នៅក្នុងឧស្សាហកម្មគីមី។ ចំពោះបញ្ហានេះគ្រោងការណ៍បច្ចេកវិទ្យានៃ pyrolysis ត្រូវបានប្រើ - ការបំបែកនៃល្បាយឧស្ម័នដែលទៅជាមួយនឹងការបំបែកនៃចំណងកាបូននិងការបង្កើតអេទីឡែន propene និង alkenes ផ្សេងទៀត។ Pyrolysis ត្រូវបានអនុវត្តនៅក្នុង furnaces ពិសេសដែលមាន pyro-coils បុគ្គល។ ពួកវាបង្កើតសីតុណ្ហភាព 750-1150°C ហើយមានចំហាយទឹកជាសារធាតុរំលាយ។ ប្រតិកម្មដំណើរការដោយយន្តការខ្សែសង្វាក់ដែលដំណើរការជាមួយនឹងការបង្កើតរ៉ាឌីកាល់កម្រិតមធ្យម។ ផលិតផលចុងក្រោយគឺអេទីឡែន ឬប្រូផេន ហើយពួកវាត្រូវបានផលិតក្នុងបរិមាណច្រើន។

យើងបានសិក្សាលម្អិតអំពីលក្ខណៈសម្បត្តិរូបវន្ត ក៏ដូចជាកម្មវិធី និងវិធីសាស្រ្តក្នុងការទទួលបាន alkenes ។
