អាល់កាណេស :
Alkanes គឺជាអ៊ីដ្រូកាបូនឆ្អែត ដែលនៅក្នុងម៉ូលេគុលដែលអាតូមទាំងអស់ត្រូវបានតភ្ជាប់ដោយចំណងតែមួយ។ រូបមន្ត -
លក្ខណៈសម្បត្តិរូបវន្ត :
- ចំណុចរលាយ និងរំពុះកើនឡើងជាមួយនឹងទម្ងន់ម៉ូលេគុល និងប្រវែងខ្សែសង្វាក់កាបូនចម្បង
- នៅក្រោមលក្ខខណ្ឌធម្មតា អាល់កានដែលមិនមានសាខាពី CH 4 ដល់ C 4 H 10 គឺជាឧស្ម័ន។ ពី C 5 H 12 ទៅ C 13 H 28 - រាវ; បន្ទាប់ពី C 14 H 30 - សារធាតុរាវ។
- ចំណុចរលាយ និងពុះថយចុះពីសាខាតិចទៅសាខាកាន់តែច្រើន។ ដូច្នេះឧទាហរណ៍នៅ 20 ° C n-pentane គឺជាអង្គធាតុរាវហើយ neopentane គឺជាឧស្ម័ន។
លក្ខណៈសម្បត្តិគីមី៖
· ហាឡូជីន
នេះគឺជាប្រតិកម្មមួយនៃការជំនួស។ អាតូមកាបូនអ៊ីដ្រូសែនតិចបំផុតត្រូវបាន halogenated ទីមួយ (អាតូមទីបី បន្ទាប់មកបន្ទាប់បន្សំ អាតូមបឋមត្រូវបាន halogenated ចុងក្រោយ) ។ Halogenation នៃ alkanes កើតឡើងជាដំណាក់កាល - មិនលើសពីមួយអាតូមអ៊ីដ្រូសែនត្រូវបានជំនួសក្នុងដំណាក់កាលមួយ:
- CH 4 + Cl 2 → CH 3 Cl + HCl (chloromethane)
- CH 3 Cl + Cl 2 → CH 2 Cl 2 + HCl (dichloromethane)
- CH 2 Cl 2 + Cl 2 → CHCl 3 + HCl (trichloromethane)
- CHCl 3 + Cl 2 → CCl 4 + HCl (tetrachloromethane) ។
នៅក្រោមសកម្មភាពនៃពន្លឺ ម៉ូលេគុលក្លរីនរលាយទៅជារ៉ាឌីកាល់ បន្ទាប់មកពួកវាវាយប្រហារលើម៉ូលេគុលអាល់កាន ដោយយកអាតូមអ៊ីដ្រូសែនចេញពីពួកវា ដែលជាលទ្ធផលដែលរ៉ាឌីកាល់មេទីល CH 3 ត្រូវបានបង្កើតឡើង ដែលប៉ះទង្គិចជាមួយម៉ូលេគុលក្លរីន បំផ្លាញពួកវា និងបង្កើតថ្មី។ រ៉ាឌីកាល់។
· ការដុត
លក្ខណៈគីមីសំខាន់នៃអ៊ីដ្រូកាបូនឆ្អែត ដែលកំណត់ការប្រើប្រាស់របស់វាជាឥន្ធនៈ គឺប្រតិកម្មចំហេះ។ ឧទាហរណ៍៖
CH 4 + 2O 2 → CO 2 + 2H 2 O + សំណួរ
ក្នុងករណីខ្វះអុកស៊ីសែនជំនួសឱ្យកាបូនឌីអុកស៊ីតកាបូនម៉ូណូអុកស៊ីតឬធ្យូងថ្មត្រូវបានទទួល (អាស្រ័យលើកំហាប់អុកស៊ីសែន) ។
ជាទូទៅប្រតិកម្មចំហេះរបស់អាល់កានអាចត្រូវបានសរសេរដូចខាងក្រោមៈ
ជាមួយ នហ ២ ន +2 +(1,5ន+0.5)O 2 \u003d ន CO 2 + ( ន+1) H 2 O
· ការរលួយ
ប្រតិកម្ម decomposition កើតឡើងតែនៅក្រោមឥទ្ធិពលនៃសីតុណ្ហភាពខ្ពស់។ ការកើនឡើងនៃសីតុណ្ហភាពនាំទៅដល់ការបំបែកចំណងកាបូន និងការបង្កើតរ៉ាឌីកាល់សេរី។
ឧទាហរណ៍:
CH 4 → C + 2H ២ (t> 1000 °C)
C 2 H 6 → 2C + 3H ២
អាល់ខេន :
អាល់ខេនគឺជាអ៊ីដ្រូកាបូនមិនឆ្អែតដែលមាននៅក្នុងម៉ូលេគុល បន្ថែមពីលើចំណងតែមួយ ចំណងកាបូន-កាបូនទ្វេមួយ។ រូបមន្តគឺ C n H 2n
កម្មសិទ្ធិរបស់អ៊ីដ្រូកាបូនទៅនឹងថ្នាក់នៃអាល់ខេនត្រូវបានឆ្លុះបញ្ចាំងដោយបច្ច័យទូទៅ -ene នៅក្នុងឈ្មោះរបស់វា។
លក្ខណៈសម្បត្តិរូបវន្ត :
- ចំណុចរលាយ និងរំពុះនៃអាល់ខេន (សាមញ្ញ) កើនឡើងជាមួយនឹងទម្ងន់ម៉ូលេគុល និងប្រវែងនៃខ្សែសង្វាក់កាបូនសំខាន់។
- នៅក្រោមលក្ខខណ្ឌធម្មតា alkenes ពី C 2 H 4 ទៅ C 4 H 8 គឺជាឧស្ម័ន។ ពី C 5 H 10 ដល់ C 17 H 34 - វត្ថុរាវបន្ទាប់ពី C 18 H 36 - សារធាតុរាវ។ អាល់ខេនមិនរលាយក្នុងទឹក ប៉ុន្តែងាយរលាយក្នុងសារធាតុរំលាយសរីរាង្គ។
លក្ខណៈសម្បត្តិគីមី :
· ការខះជាតិទឹក។គឺជាដំណើរការនៃការបំបែកម៉ូលេគុលទឹកចេញពីម៉ូលេគុលសមាសធាតុសរីរាង្គ។
· វត្ថុធាតុ polymerization- នេះគឺជាដំណើរការគីមីនៃការរួមបញ្ចូលគ្នារវាងម៉ូលេគុលដំបូងជាច្រើននៃសារធាតុទម្ងន់ម៉ូលេគុលទាបចូលទៅក្នុងម៉ូលេគុលវត្ថុធាតុ polymer ធំ។
ប៉ូលីម័រគឺជាសមាសធាតុទម្ងន់ម៉ូលេគុលខ្ពស់ ម៉ូលេគុលដែលមានរចនាសម្ព័ន្ធដូចគ្នាបេះបិទជាច្រើន។
អាល់កាឌីន :
Alkadienes គឺជាអ៊ីដ្រូកាបូនមិនឆ្អែតដែលមាននៅក្នុងម៉ូលេគុល បន្ថែមពីលើចំណងតែមួយ ចំណងកាបូន-កាបូនទ្វេពីរ។ រូបមន្តគឺ
. Dienes គឺជា isomers រចនាសម្ព័ន្ធនៃ alkynes ។លក្ខណៈសម្បត្តិរូបវន្ត :
Butadiene គឺជាឧស្ម័ន (tboiling −4.5 °C) isoprene គឺជាអង្គធាតុរាវដែលពុះនៅសីតុណ្ហភាព 34 °C, dimethylbutadiene គឺជាអង្គធាតុរាវដែលពុះនៅសីតុណ្ហភាព 70 °C ។ អ៊ីសូព្រីន និងអ៊ីដ្រូកាបូនឌីអេន ផ្សេងទៀតអាចធ្វើវត្ថុធាតុ polymerize ទៅជាកៅស៊ូ។ កៅស៊ូធម្មជាតិនៅក្នុងស្ថានភាពបន្សុតរបស់វាគឺជាវត្ថុធាតុ polymer ដែលមានរូបមន្តទូទៅ (C5H8)n ហើយត្រូវបានទទួលពីជ័រនៃរុក្ខជាតិត្រូពិចមួយចំនួន។
កៅស៊ូគឺអាចរលាយបានខ្ពស់នៅក្នុង benzene ប្រេងសាំង កាបូន disulfide ។ នៅសីតុណ្ហភាពទាប វាប្រែជាផុយ ពេលដែលកំដៅវាក្លាយទៅជាស្អិត។ ដើម្បីកែលម្អលក្ខណៈមេកានិច និងគីមីនៃកៅស៊ូ វាត្រូវបានបំប្លែងទៅជាកៅស៊ូដោយ vulcanization ។ ដើម្បីទទួលបានផលិតផលជ័រកៅស៊ូ ពួកវាដំបូងត្រូវបានបង្កើតឡើងពីល្បាយកៅស៊ូជាមួយស្ពាន់ធ័រ ក៏ដូចជាជាមួយសារធាតុបំពេញផងដែរ៖ ដីស ដីស ដីឥដ្ឋ និងសមាសធាតុសរីរាង្គមួយចំនួនដែលបម្រើដើម្បីពន្លឿនការបំប្លែងសារធាតុពុល។ បន្ទាប់មកផលិតផលត្រូវបានកំដៅ - vulcanization ក្តៅ។ កំឡុងពេល vulcanization ស្ពាន់ធ័រមានទំនាក់ទំនងគីមីជាមួយកៅស៊ូ។ លើសពីនេះទៀតនៅក្នុងកៅស៊ូ vulcanized ស្ពាន់ធ័រត្រូវបានផ្ទុកនៅក្នុងរដ្ឋដោយឥតគិតថ្លៃនៅក្នុងសំណុំបែបបទនៃភាគល្អិតតូច។
អ៊ីដ្រូកាបូន Diene ងាយធ្វើវត្ថុធាតុ polymerized ។ ប្រតិកម្មវត្ថុធាតុ polymerization នៃអ៊ីដ្រូកាបូនឌីអេន ផ្អែកលើការសំយោគកៅស៊ូ។ ចូលទៅក្នុងប្រតិកម្មបន្ថែម (អ៊ីដ្រូសែន, ហាឡូជីន, អ៊ីដ្រូសែន)៖
H 2 C \u003d CH-CH \u003d CH 2 + H 2 -> H 3 C-CH \u003d CH-CH 3
អាល់គីន :
អាល់គីនគឺជាអ៊ីដ្រូកាបូនមិនឆ្អែតឆ្អែត ដែលម៉ូលេគុលមាន បន្ថែមពីលើចំណងតែមួយ ចំណងកាបូន-កាបូនបីដង។ រូបមន្ត-C n H 2n-2
លក្ខណៈសម្បត្តិរូបវន្ត :
Alkynes គឺស្រដៀងគ្នានៅក្នុងលក្ខណៈសម្បត្តិរូបវន្តទៅនឹង alkenes ដែលត្រូវគ្នា។ ទាប (រហូតដល់ C 4) - ឧស្ម័នដោយគ្មានពណ៌និងក្លិនដែលមានចំណុចរំពុះខ្ពស់ជាងសមភាគីរបស់ពួកគេនៅក្នុងអាល់ខេន។
Alkynes គឺរលាយក្នុងទឹកបានតិចតួច ល្អជាងនៅក្នុងសារធាតុរំលាយសរីរាង្គ។
លក្ខណៈសម្បត្តិគីមី :
ប្រតិកម្ម halogenation
Alkynes មានសមត្ថភាពបន្ថែមម៉ូលេគុល halogen មួយឬពីរដើម្បីបង្កើតជានិស្សន្ទវត្ថុ halogen ដែលត្រូវគ្នា៖
ជាតិទឹក
នៅក្នុងវត្តមាននៃអំបិលបារត alkynes បន្ថែមទឹកដើម្បីបង្កើតជា acetaldehyde (សម្រាប់ acetylene) ឬ ketone (សម្រាប់ alkynes ផ្សេងទៀត)

និយមន័យ
អាល់កាណេសអ៊ីដ្រូកាបូនឆ្អែតត្រូវបានគេហៅថា ម៉ូលេគុលដែលមានអាតូមកាបូន និងអ៊ីដ្រូសែន ដែលភ្ជាប់គ្នាទៅវិញទៅមកដោយ σ-bonds ប៉ុណ្ណោះ។
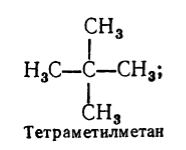
នៅក្រោមលក្ខខណ្ឌធម្មតា (នៅ 25 o C និងសម្ពាធបរិយាកាស) សមាជិក 4 ដំបូងនៃស៊េរីដូចគ្នានៃ alkanes (C 1 - C 4) គឺជាឧស្ម័ន។ អាល់កានធម្មតាពី pentane ទៅ heptadecane (C 5 - C 17) គឺជាវត្ថុរាវ ដែលចាប់ផ្តើមពី C 18 និងខ្ពស់ជាងនេះ គឺជាសារធាតុរឹង។ នៅពេលដែលទម្ងន់ម៉ូលេគុលដែលទាក់ទងកើនឡើង ចំណុចរំពុះ និងរលាយនៃអាល់កានកើនឡើង។ ជាមួយនឹងចំនួនអាតូមកាបូនដូចគ្នានៅក្នុងម៉ូលេគុល អាល់កានសាខាមានចំណុចរំពុះទាបជាងអាល់កានធម្មតា។ រចនាសម្ព័ន្ធនៃម៉ូលេគុលអាល់កានដោយប្រើមេតានជាឧទាហរណ៍ត្រូវបានបង្ហាញក្នុងរូបភព។ មួយ។
អង្ករ។ 1. រចនាសម្ព័ន្ធនៃម៉ូលេគុលមេតាន។
Alkanes មិនអាចរលាយក្នុងទឹកបាន ចាប់តាំងពីម៉ូលេគុលរបស់វាមានប៉ូលទាប ហើយមិនមានអន្តរកម្មជាមួយម៉ូលេគុលទឹក។ អាល់កានរាវលាយចូលគ្នាយ៉ាងងាយស្រួល។ ពួកវារលាយបានយ៉ាងល្អនៅក្នុងសារធាតុរំលាយសរីរាង្គដែលមិនមានប៉ូលដូចជា benzene, carbon tetrachloride, diethyl ether ជាដើម។
ការទទួលបានអាល់កាន
ប្រភពសំខាន់នៃអ៊ីដ្រូកាបូនឆ្អែតផ្សេងៗដែលមានអាតូមកាបូនរហូតដល់ 40 គឺប្រេង និងឧស្ម័នធម្មជាតិ។ អាល់កានដែលមានអាតូមកាបូនតិចតួច (1 - 10) អាចត្រូវបានញែកដោយប្រភាគនៃឧស្ម័នធម្មជាតិ ឬប្រភាគប្រេងសាំង។
មានវិធីសាស្រ្តឧស្សាហកម្ម (I) និងមន្ទីរពិសោធន៍ (II) សម្រាប់ការទទួលបានអាល់កាន។
C + H 2 → CH 4 (kat = Ni, t 0);
CO + 3H 2 → CH 4 + H 2 O (kat \u003d Ni, t 0 \u003d 200 - 300);
CO 2 + 4H 2 → CH 4 + 2H 2 O (kat, t 0) ។
- អ៊ីដ្រូសែននៃអ៊ីដ្រូកាបូនមិនឆ្អែត
CH 3 -CH \u003d CH 2 + H 2 →CH 3 -CH 2 -CH 3 (kat \u003d Ni, t 0);
- ការងើបឡើងវិញនៃ haloalkanes
C 2 H 5 I + HI → C 2 H 6 + I 2 (t 0);
- ប្រតិកម្មរលាយអាល់កាឡាំងនៃអំបិលនៃអាស៊ីតសរីរាង្គ monobasic
C 2 H 5 -COONa + NaOH → C 2 H 6 + Na 2 CO 3 (t 0);
- អន្តរកម្មនៃ haloalkanes ជាមួយសូដ្យូមលោហធាតុ (ប្រតិកម្ម Wurtz)
2C 2 H 5 Br + 2Na → CH 3 -CH 2 -CH 2 -CH 3 + 2NaBr;
- អេឡិចត្រូលីសនៃអំបិលអាស៊ីតសរីរាង្គ monobasic
2C 2 H 5 COONa + 2H 2 O → H 2 + 2NaOH + C 4 H 10 + 2CO 2;
K (-): 2H 2 O + 2e → H 2 + 2OH - ;
A (+): 2C 2 H 5 COO − −2e → 2C 2 H 5 COO + → 2C 2 H 5 + + 2CO 2 ។
លក្ខណៈសម្បត្តិគីមីរបស់អាល់កាន
Alkanes គឺជាសមាសធាតុសរីរាង្គដែលមានប្រតិកម្មតិចបំផុត ដែលត្រូវបានពន្យល់ដោយរចនាសម្ព័ន្ធរបស់វា។
អាល់កាននៅក្រោមលក្ខខណ្ឌធម្មតាមិនមានប្រតិកម្មជាមួយនឹងអាស៊ីតប្រមូលផ្តុំ អាល់កាឡាំងរលាយ និងប្រមូលផ្តុំ លោហធាតុអាល់កាឡាំង ហាឡូហ្សែន (លើកលែងតែហ្វ្លុយអូរីន) ប៉ូតាស្យូម permanganate និងប៉ូតាស្យូម dichromate នៅក្នុងបរិយាកាសអាសុីត។
សម្រាប់ alkanes ប្រតិកម្មដែលដំណើរការទៅតាមយន្តការរ៉ាឌីកាល់គឺជាលក្ខណៈភាគច្រើន។ ការបំបែក homolytic នៃចំណង C-H និង C-C គឺមានភាពស្វាហាប់ជាងការបំបែក heterolytic របស់ពួកគេ។
ប្រតិកម្មជំនួសរ៉ាឌីកាល់ដំណើរការយ៉ាងងាយស្រួលបំផុតនៅអាតូមកាបូនទីបី ងាយស្រួលជាងនៅអាតូមកាបូនបន្ទាប់បន្សំ និងចុងក្រោយនៅអាតូមកាបូនបឋម។
ការបំប្លែងសារជាតិគីមីទាំងអស់នៃអាល់កានបន្តជាមួយនឹងការបំបែក៖
1) មូលបត្របំណុល C-H
- ហាឡូហ្សែន (S R)
CH 4 + Cl 2 → CH 3 Cl + HCl ( hv);
CH 3 -CH 2 -CH 3 + Br 2 → CH 3 -CHBr-CH 3 + HBr ( hv).
- នីត្រាត (S R)
CH 3 -C (CH 3) H-CH 3 + HONO 2 (dilute) → CH 3 -C (NO 2) H-CH 3 + H 2 O (t 0) ។
- sulfochlorination (S R)
R-H + SO 2 + Cl 2 → RSO 2 Cl + HCl ( hv).
- ការខះជាតិទឹក
CH 3 -CH 3 → CH 2 \u003d CH 2 + H 2 (kat \u003d Ni, t 0) ។
- dehydrocyclization
CH 3 (CH 2) 4 CH 3 → C 6 H 6 + 4H 2 (kat = Cr 2 O 3, t 0) ។
2) ចំណង C-H និង C-C
- isomerization (ការរៀបចំឡើងវិញ intramolecular)
CH 3 -CH 2 -CH 2 -CH 3 →CH 3 -C (CH 3) H-CH 3 (kat \u003d AlCl 3, t 0)។
- អុកស៊ីតកម្ម
2CH 3 -CH 2 -CH 2 -CH 3 + 5O 2 → 4CH 3 COOH + 2H 2 O (t 0, p);
C n H 2n + 2 + (1.5n + 0.5) O 2 → nCO 2 + (n + 1) H 2 O (t 0) ។
ការអនុវត្តអាល់កាន
Alkanes បានរកឃើញកម្មវិធីនៅក្នុងឧស្សាហកម្មផ្សេងៗ។ ចូរយើងពិចារណាលម្អិតបន្ថែមទៀត ដោយប្រើឧទាហរណ៍នៃអ្នកតំណាងមួយចំនួននៃស៊េរី homologous ក៏ដូចជាល្បាយនៃ alkanes ។
មេតានគឺជាមូលដ្ឋានវត្ថុធាតុដើមនៃដំណើរការឧស្សាហកម្មគីមីដ៏សំខាន់បំផុតសម្រាប់ផលិតកាបូន និងអ៊ីដ្រូសែន អាសេទីលីន សមាសធាតុសរីរាង្គដែលមានអុកស៊ីហ្សែន - អាល់កុល អាល់ឌីអ៊ីត អាស៊ីត។ Propane ត្រូវបានគេប្រើជាឥន្ធនៈរថយន្ត។ Butane ត្រូវបានប្រើដើម្បីផលិត butadiene ដែលជាវត្ថុធាតុដើមសម្រាប់ផលិតកៅស៊ូសំយោគ។
ល្បាយនៃអាល់កានរាវ និងរឹងរហូតដល់ C 25 ហៅថា vaseline ត្រូវបានគេប្រើក្នុងថ្នាំជាមូលដ្ឋានសម្រាប់កមួន។ ល្បាយនៃអាល់កាណេតរឹង C 18 - C 25 (ប៉ារ៉ាហ្វីន) ត្រូវបានប្រើដើម្បីដាក់សម្ភារៈផ្សេងៗ (ក្រដាស ក្រណាត់ ឈើ) ដើម្បីផ្តល់ឱ្យពួកគេនូវលក្ខណៈសម្បត្តិ hydrophobic ពោលគឺឧ។ ភាពមិនជ្រាបទឹក។ នៅក្នុងឱសថវាត្រូវបានគេប្រើសម្រាប់នីតិវិធីព្យាបាលដោយចលនា (ការព្យាបាលដោយប៉ារ៉ាហ្វីន) ។
ឧទាហរណ៍នៃការដោះស្រាយបញ្ហា
ឧទាហរណ៍ ១
| លំហាត់ប្រាណ | នៅពេល chlorinating មេតាន 1.54 ក្រាមនៃសមាសធាតុត្រូវបានទទួល ដង់ស៊ីតេនៃចំហាយទឹកនៅក្នុងខ្យល់គឺ 5.31 ។ គណនាម៉ាស់ម៉ង់ហ្គាណែសឌីអុកស៊ីត MnO 2 ដែលនឹងតម្រូវឱ្យផលិតក្លរីន ប្រសិនបើសមាមាត្រនៃបរិមាណមេតាន និងក្លរីនដែលបានណែនាំទៅក្នុងប្រតិកម្មគឺ 1:2 ។ |
| ការសម្រេចចិត្ត | សមាមាត្រនៃម៉ាស់ឧស្ម័នដែលបានផ្តល់ឱ្យទៅនឹងម៉ាស់នៃឧស្ម័នមួយផ្សេងទៀតដែលយកក្នុងបរិមាណដូចគ្នានៅសីតុណ្ហភាពដូចគ្នានិងសម្ពាធដូចគ្នាត្រូវបានគេហៅថាដង់ស៊ីតេទាក់ទងនៃឧស្ម័នទីមួយលើសពីទីពីរ។ តម្លៃនេះបង្ហាញថាតើឧស្ម័នទីមួយធ្ងន់ជាង ឬស្រាលជាងឧស្ម័នទីពីរប៉ុន្មានដង។ ទម្ងន់ម៉ូលេគុលដែលទាក់ទងនៃខ្យល់ត្រូវបានគេយកស្មើនឹង 29 (ដោយគិតគូរពីខ្លឹមសារនៃអាសូត អុកស៊ីសែន និងឧស្ម័នផ្សេងទៀតនៅក្នុងខ្យល់)។ វាគួរតែត្រូវបានកត់សម្គាល់ថាគំនិតនៃ "ទម្ងន់ម៉ូលេគុលដែលទាក់ទងនៃខ្យល់" ត្រូវបានប្រើតាមលក្ខខណ្ឌដោយហេតុថាខ្យល់គឺជាល្បាយនៃឧស្ម័ន។ ចូរយើងរកឃើញម៉ាសម៉ូលេគុលនៃឧស្ម័នដែលបង្កើតឡើងក្នុងកំឡុងពេលក្លរីនមេតាន៖ M ឧស្ម័ន \u003d 29 × D ខ្យល់ (ឧស្ម័ន) \u003d 29 × 5.31 \u003d 154 ក្រាម / mol ។ នេះគឺជាកាបូន tetrachloride - CCl 4 ។ យើងសរសេរសមីការប្រតិកម្ម និងរៀបចំមេគុណ stoichiometric៖ CH 4 + 4Cl 2 \u003d CCl 4 + 4HCl ។ គណនាបរិមាណសារធាតុកាបូន tetrachloride៖ n(CCl 4) = m(CCl 4) / M(CCl 4); n (CCl 4) \u003d 1.54 / 154 \u003d 0.01 mol ។ យោងតាមសមីការប្រតិកម្ម n (CCl 4) : n (CH 4) = 1: 1 បន្ទាប់មក n (CH 4) \u003d n (CCl 4) \u003d 0.01 mol ។ បន្ទាប់មកបរិមាណសារធាតុក្លរីនគួរតែស្មើនឹង n(Cl 2) = 2 × 4 n(CH 4), i.e. n(Cl 2) \u003d 8 × 0.01 \u003d 0.08 mol ។ យើងសរសេរសមីការប្រតិកម្មសម្រាប់ការផលិតក្លរីន៖ MnO 2 + 4HCl \u003d MnCl 2 + Cl 2 + 2H 2 O ។ ចំនួន moles នៃម៉ង់ហ្គាណែសឌីអុកស៊ីតគឺ 0.08 moles, ដោយសារតែ n (Cl 2) : n (MnO 2) = 1: 1. រកម៉ាសនៃម៉ង់ហ្គាណែសឌីអុកស៊ីត៖ m (MnO 2) \u003d n (MnO 2) × M (MnO 2); M (MnO 2) \u003d Ar (Mn) + 2 × Ar (O) \u003d 55 + 2 × 16 \u003d 87 ក្រាម / mol; m (MnO 2) \u003d 0.08 × 87 \u003d 10.4 ក្រាម។ |
| ចម្លើយ | ម៉ាស់ម៉ង់ហ្គាណែសឌីអុកស៊ីតគឺ 10,4 ក្រាម។ |
ឧទាហរណ៍ ២
| លំហាត់ប្រាណ | កំណត់រូបមន្តម៉ូលេគុលនៃ trichloroalkane ប្រភាគម៉ាសនៃក្លរីនដែលមាន 72.20% ។ បង្កើតរូបមន្តរចនាសម្ព័ន្ធនៃ isomers ដែលអាចធ្វើបានទាំងអស់ ហើយផ្តល់ឈ្មោះសារធាតុដោយយោងទៅតាមការជំនួសឈ្មោះ IUPAC ។ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ចម្លើយ | ចូរយើងសរសេររូបមន្តទូទៅនៃ trichloroalkene៖ C n H 2 n -1 Cl 3 ។ យោងតាមរូបមន្ត ω(Cl) = 3 × Ar(Cl) / Mr(C n H 2 n -1 Cl 3) × 100% គណនាទម្ងន់ម៉ូលេគុលនៃ trichloroalkane៖ លោក(C n H 2 n −1 Cl 3) = 3 × 35.5 / 72.20 × 100% = 147.5 ។ ចូររកតម្លៃនៃ n: 12n + 2n − 1 + 35.5x3 = 147.5; ដូច្នេះរូបមន្តនៃ trichloroalkane គឺ C 3 H 5 Cl 3 ។ ចូរយើងចងក្រងរូបមន្តរចនាសម្ព័ន្ធនៃអ៊ីសូមឺរ៖ 1,2,3-trichloropropane (1), 1,1,2-trichloropropane (2), 1,1,3-trichloropropane (3), 1,1,1-trichloropropane (4) និង 1 ,2,2-trichloropropane (5) ។ CH 2 Cl-CHCl-CH 2 Cl (1); CHCl 2 -CHCl-CH 3 (2); CHCl 2 -CH 2 -CH 2 Cl (3); CCl 3 -CH 2 -CH 3 (4); អាល់កាណេស (មេតាន និងលក្ខណៈដូចគ្នារបស់វា) មានរូបមន្តទូទៅ C ន H2 ន+2. អ៊ីដ្រូកាបូនទាំងបួនដំបូងគេហៅថា មេតាន អេតាន ប្រូផេន ប៊ូតាន។ ឈ្មោះរបស់សមាជិកជាន់ខ្ពស់នៃស៊េរីនេះមានឫស - លេខក្រិកនិងបច្ច័យ -an ។ ឈ្មោះរបស់ alkanes បង្កើតបានជាមូលដ្ឋាននៃនាមត្រកូល IUPAC ។ច្បាប់សម្រាប់ការដាក់ឈ្មោះជាប្រព័ន្ធ៖
សៀគ្វីសំខាន់ត្រូវបានជ្រើសរើសដោយផ្អែកលើលក្ខណៈវិនិច្ឆ័យខាងក្រោមតាមលំដាប់លំដោយ៖
ខ្សែសង្វាក់សំខាន់ត្រូវបានដាក់លេខពីចុងម្ខាងទៅម្ខាងទៀតជាលេខអារ៉ាប់។ សារធាតុជំនួសនីមួយៗទទួលបានចំនួនអាតូមកាបូននៃខ្សែសង្វាក់សំខាន់ដែលវាត្រូវបានភ្ជាប់។ លំដាប់លេខរៀងត្រូវបានជ្រើសរើសតាមរបៀបដែលផលបូកនៃលេខជំនួស (អ្នកដាក់) គឺតូចបំផុត។ ច្បាប់នេះក៏អនុវត្តចំពោះលេខរៀងនៃសមាសធាតុ monocyclic ផងដែរ។
ក្រុមចំហៀងអ៊ីដ្រូកាបូនទាំងអស់ត្រូវបានចាត់ទុកថាជារ៉ាឌីកាល់ monovalent (ភ្ជាប់តែមួយ) ។ ប្រសិនបើរ៉ាឌីកាល់ចំហៀងខ្លួនវាមានខ្សែសង្វាក់ចំហៀង នោះខ្សែសង្វាក់មេបន្ថែមមួយត្រូវបានជ្រើសរើសនៅក្នុងវាដោយយោងទៅតាមច្បាប់ខាងលើ ដែលត្រូវបានដាក់លេខចាប់ពីអាតូមកាបូនដែលភ្ជាប់ទៅនឹងខ្សែសង្វាក់មេ។
ឈ្មោះនៃបរិវេណចាប់ផ្តើមដោយបញ្ជីជំនួសដោយបង្ហាញឈ្មោះរបស់វាតាមលំដាប់អក្ខរក្រម។ ឈ្មោះរបស់សារធាតុជំនួសនីមួយៗត្រូវនាំមុខដោយលេខរបស់វានៅក្នុងខ្សែសង្វាក់សំខាន់។ វត្តមានរបស់សារធាតុជំនួសជាច្រើនត្រូវបានចង្អុលបង្ហាញដោយបុព្វបទ-លេខ: di-, tri-, tetra- ជាដើម បន្ទាប់ពីនោះអ៊ីដ្រូកាបូនដែលត្រូវគ្នានឹងខ្សែសង្វាក់សំខាន់ត្រូវបានគេហៅថា។ នៅក្នុងតារាង។ 12.1 បង្ហាញឈ្មោះនៃអ៊ីដ្រូកាបូនចំនួនប្រាំដំបូង រ៉ាឌីកាល់របស់ពួកគេ អ៊ីសូមឺរដែលអាចកើតមាន និងរូបមន្តដែលត្រូវគ្នារបស់ពួកគេ។ ឈ្មោះរ៉ាឌីកាល់បញ្ចប់ដោយបច្ច័យ -yl ។
ឧទាហរណ៍។ ដាក់ឈ្មោះ isomers ទាំងអស់នៃ hexane ។ ឧទាហរណ៍។ ដាក់ឈ្មោះអាល់កាននៃរចនាសម្ព័ន្ធខាងក្រោម ក្នុងឧទាហរណ៍នេះ ខ្សែសង្វាក់អាតូមិកចំនួនពីរ លេខដែលផលបូកនៃលេខតូចបំផុតត្រូវបានជ្រើសរើស (ច្បាប់ទី 2)។ ដោយប្រើឈ្មោះនៃរ៉ាឌីកាល់សាខាដែលបានផ្តល់ឱ្យក្នុងតារាង។ ១២.២,
ឈ្មោះរបស់អាល់កាននេះគឺសាមញ្ញបន្តិច៖ 10-tert-butyl-2,2-(dimethyl)-7-propyl-4-isopropyl-3-ethyl dodecane ។ នៅពេលដែលខ្សែសង្វាក់អ៊ីដ្រូកាបូនត្រូវបានបិទក្នុងវដ្តមួយជាមួយនឹងការបាត់បង់អាតូមអ៊ីដ្រូសែនពីរ ម៉ូណូស៊ីក្លូអាល់កានត្រូវបានបង្កើតឡើងជាមួយនឹងរូបមន្តទូទៅ C ន H2 ន. Cyclization ចាប់ផ្តើមពី C 3 ឈ្មោះត្រូវបានបង្កើតឡើងពី C នបុព្វបទជាមួយស៊ីក្លូ៖ អាល់កាន polycyclic ។ឈ្មោះរបស់ពួកវាត្រូវបានបង្កើតឡើងដោយបុព្វបទ bicyclo-, tricyclo- ។ល។ សមាសធាតុ Bicyclic និង tricyclic មានវដ្តពីរ និងបីនៅក្នុងម៉ូលេគុលរៀងៗខ្លួន ដើម្បីពណ៌នាអំពីរចនាសម្ព័ន្ធរបស់វា ក្នុងតង្កៀបការ៉េបង្ហាញពីការថយចុះលំដាប់នៃចំនួនអាតូមកាបូននៅក្នុងនីមួយៗ។ ខ្សែសង្វាក់តភ្ជាប់អាតូម nodal ; នៅក្រោមរូបមន្តឈ្មោះអាតូម: អ៊ីដ្រូកាបូន tricyclic នេះត្រូវបានគេសំដៅជាទូទៅថាជា adamantane (មកពីភាសាឆេក adamant, ពេជ្រ) ដោយសារតែវាគឺជាការរួមបញ្ចូលគ្នានៃចិញ្ចៀន cyclohexane លាយបញ្ចូលគ្នាចំនួនបីនៅក្នុងទម្រង់ដែលបណ្តាលឱ្យមានការរៀបចំដូចពេជ្រនៃអាតូមកាបូននៅក្នុងបន្ទះគ្រីស្តាល់។ អ៊ីដ្រូកាបូនស៊ីក្លូដែលមានអាតូមកាបូនធម្មតាមួយត្រូវបានគេហៅថា spiranes ឧទាហរណ៍ spiro-5,5-undecane៖ ម៉ូលេគុល Planar cyclic មិនស្ថិតស្ថេរ ដូច្នេះ isomers ទម្រង់ផ្សេងៗត្រូវបានបង្កើតឡើង។ មិនដូច isomers កំណត់រចនាសម្ព័ន្ធ (ការរៀបចំលំហនៃអាតូមក្នុងម៉ូលេគុលដោយមិនគិតពីការតំរង់ទិស) isomers ទម្រង់ខុសគ្នាពីគ្នាទៅវិញទៅមកតែដោយការបង្វិលអាតូមឬរ៉ាឌីកាល់ជុំវិញចំណងសាមញ្ញជាផ្លូវការខណៈពេលដែលរក្សាបាននូវការកំណត់រចនាសម្ព័ន្ធនៃម៉ូលេគុល។ ថាមពលនៃការបង្កើត conformer ស្ថេរភាពត្រូវបានគេហៅថា ទម្រង់. Conformers ស្ថិតនៅក្នុងលំនឹងថាមវន្ត ហើយត្រូវបានបំប្លែងទៅជាគ្នាទៅវិញទៅមកតាមរយៈទម្រង់មិនស្ថិតស្ថេរ។ អស្ថិរភាពនៃវដ្តប្លង់គឺបណ្តាលមកពីការខូចទ្រង់ទ្រាយសំខាន់នៃមុំចំណង។ ខណៈពេលដែលរក្សាមុំចំណង tetrahedral សម្រាប់ cyclohexane C 6H 12 ការអនុលោមតាមស្ថេរភាពពីរគឺអាចធ្វើទៅបាន: ក្នុងទម្រង់ជាកៅអី (ក) និងក្នុងទម្រង់នៃការងូតទឹក (ខ)៖
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||