GENETIC ENGINEERING(syn. genetic engineering) - isang direksyon ng pananaliksik sa molecular biology at genetics, ang pangwakas na layunin kung saan ay upang makuha, gamit ang mga diskarte sa laboratoryo, mga organismo na may bago, kabilang ang mga hindi matatagpuan sa kalikasan, mga kumbinasyon ng mga namamana na katangian. Sa puso ni G. at. ang posibilidad ng may layuning pagmamanipula sa mga fragment ng nucleic acid dahil sa pinakabagong mga nagawa ng molecular biology at genetics ay kasinungalingan. Kasama sa mga tagumpay na ito ang pagtatatag ng pagiging pangkalahatan ng genetic code (tingnan), iyon ay, ang katotohanan na sa lahat ng mga nabubuhay na organismo ang pagsasama ng parehong mga amino acid sa isang molekula ng protina ay naka-encode ng parehong mga pagkakasunud-sunod ng nucleotide sa chain ng DNA; ang mga tagumpay ng genetic enzymology, na nagbigay sa mananaliksik ng isang hanay ng mga enzyme na ginagawang posible na makakuha ng hiwalay na mga gene o mga fragment ng nucleic acid sa isang nakahiwalay na anyo, upang isakatuparan ang in vitro synthesis ng mga fragment ng nucleic acid sa - t, upang pagsamahin ang nakuha na mga fragment sa isang solong kabuuan. Kaya, ang pagbabago ng namamana na katangian ng isang organismo sa pamamagitan ng G. at. ay nabawasan sa pagtatayo ng bagong genetic na materyal mula sa iba't ibang mga fragment, ang pagpapakilala ng materyal na ito sa organismo ng tatanggap, ang paglikha ng mga kondisyon para sa paggana nito at matatag na mana.
Ang isa sa mga paraan upang makakuha ng mga gene ay chem. synthesis. Pagkatapos Holly (A. Holli) sa USA, A. A. Baev sa USSR at iba pang mga mananaliksik pinamamahalaang upang maintindihan ang istraktura ng iba't-ibang transportasyon RBGK (tRNA), X. Koran et al., Isagawa ang isang chem. synthesis ng DNA encoding yeast alanine tRNA ng panadero.
Ngunit ang pinaka-epektibong paraan ng artipisyal na gene synthesis ay nauugnay sa paggamit ng enzyme RNA-dependent DNA polymerase (reverse transcriptase) na natuklasan ni Baltimore (D. Baltimore) at Temin (H. Temin) sa mga oncogenic na virus (tingnan). Ang enzyme na ito ay nahiwalay at na-purify mula sa mga cell na nahawaan ng ilang partikular na RNA-containing oncogenic virus, kabilang ang avian myeloblastosis virus, Rous sarcoma, at mouse leukemia. Ang reverse transcriptase ay nagbibigay ng DNA synthesis sa messenger RNA (mRNA) template. Ang paggamit ng mga molekula ng mRNA bilang mga template para sa synthesis ng DNA ay lubos na nagpapadali sa artipisyal na synthesis ng mga indibidwal na istrukturang gene ng mas mataas na mga organismo, dahil ang pagkakasunud-sunod ng mga nitrogenous na base sa isang molekula ng mRNA ay isang eksaktong kopya ng pagkakasunud-sunod ng mga nitrogenous na base ng kaukulang mga istrukturang gene, at ang pamamaraan para sa paghihiwalay ng iba't ibang mga molekula ng mRNA ay lubos na binuo. Ang mga pag-unlad sa paghihiwalay ng globin protein mRNA, na bahagi ng hemoglobin ng tao, hayop at ibon, eye lens protein mRNA, immunoglobin mRNA, mRNA ng isang partikular na malignant na tumor (myeloma) na protina, ay naging posible na i-synthesize ang istrukturang bahagi ng mga gene na naka-encode ng ilang ng mga protina na ito gamit ang reverse transcriptase.
Gayunpaman, ang mga structural genes sa katawan ay gumagana kasama ng mga regulatory genes, ang nucleotide sequence na kung saan ay hindi muling ginawa ng mRNA molecule. Samakatuwid, wala sa mga pamamaraang ito ang nagpapahintulot sa synthesis ng isang hanay ng mga structural at regulatory genes. Ang solusyon sa problemang ito ay naging posible pagkatapos ng pagbuo ng mga pamamaraan para sa paghihiwalay ng mga indibidwal na gene. Upang ihiwalay ang mga bacterial genes, ginagamit ang maliliit na DNA-containing cytoplasmic structures na maaaring mag-replicate (tingnan ang Replication) nang hiwalay sa bacterial chromosome. Ang mga istrukturang ito ay bumubuo ng isang solong pangkat ng mga extrachromosomal genetic na elemento ng bakterya - plasmids (tingnan ang Plasmids). Ang ilan sa mga ito ay maaaring ipasok sa bacterial chromosome, at pagkatapos ay kusang-loob o sa ilalim ng impluwensya ng mga inducing agent, halimbawa. Ang pag-iilaw ng UV, lumipat mula sa chromosome patungo sa cytoplasm, kasama nito ang mga katabing chromosomal genes-cells ng host. Ang mga extrachromosomal genetic na elemento ng bakterya na may ganitong mga katangian ay tinatawag na mga episome [F. Jacob, Wollman (E. Wollman)]. Kasama sa mga episode (tingnan) ang mga temperate phage (tingnan ang. Bacteriophage), sex factor ng bacteria, drug resistance factor ng microorganisms (tingnan), bacteriocinogenic factor (tingnan). Sa cytoplasm, ang mga gene na nakunan ng mga episome ay gumagaya sa kanilang komposisyon at kadalasang bumubuo ng maraming kopya. Ang pagbuo ng isang epektibong paraan para sa paghihiwalay ng mga plasmid, sa partikular na mga temperate phage na nagdadala ng genetic na materyal ng bacterial chromosome, at paghihiwalay ng isang fragment ng bacterial cell chromosome na kasama sa bacteriophage genome ay naging posible noong 1969 para kay J. Beckwith et al. ihiwalay ang lactose operon, isang pangkat ng mga gene na kumokontrol sa synthesis enzymes na kailangan para sa pagsipsip ng lactose ng Escherichia coli. Ang isang katulad na pamamaraan ay ginamit upang ihiwalay at linisin ang gene na kumokontrol sa synthesis ng Escherichia coli tyrosine transfer RNA (tingnan ang Ribonucleic acids).
Ang paggamit ng mga plasmid ay ginagawang posible na makakuha ng halos anumang bacterial genes sa hiwalay na anyo, at, dahil dito, ang posibilidad ng pagbuo ng mga molekula ng DNA mula sa iba't ibang mga mapagkukunan. Ang ganitong mga hybrid na istruktura ay maaaring maipon sa mga cell sa mga makabuluhang dami, dahil maraming mga plasmid sa ilalim ng ilang mga kundisyon ay masinsinang gumagaya sa bacterial cytoplasm, na bumubuo ng sampu, daan-daan, at kahit libu-libong mga kopya.
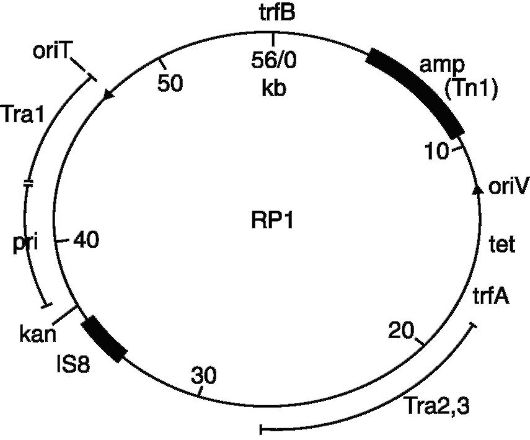
Ang mga tagumpay ni G. at. nauugnay sa pagbuo ng mga diskarte para sa pagsasama-sama ng mga istrukturang genetic mula sa iba't ibang mga mapagkukunan sa isang solong molekula ng DNA. Ang mapagpasyang kadahilanan sa disenyo ng mga hybrid na molekula sa vitro ay ang paggamit ng mga restriction endonucleases - mga espesyal na enzyme na may kakayahang pagputol ng mga molekula ng DNA sa mahigpit na tinukoy na mga lugar. Ang ganitong mga enzyme ay matatagpuan sa mga selulang Escherichia coli na may dalang R-type na mga plasmid, na nagdudulot ng resistensya ng bakterya sa ilang mga gamot, sa mga selula ng Haemophilus influenzae, Serratia marcescens at iba pang mga mikroorganismo. Ang isa sa mga pinakakaraniwang ginagamit na enzyme ng ganitong uri ay ang EcoRI restriction endonuclease, na na-synthesize ng RI plasmid sa E. coli cells. Kinikilala ng enzyme ang isang seksyon ng DNA na may natatanging pagkakasunud-sunod ng anim na pares ng base at pinuputol ang double-stranded na istraktura ng DNA sa seksyong ito upang ang mga single-stranded na dulo ng apat na nucleotide ay nabuo sa magkabilang panig (tinatawag na malagkit na mga dulo). Dahil pinuputol ng enzyme ang mga molekula ng DNA, anuman ang kanilang pinagmulan, sa isang mahigpit na tinukoy na paraan, lahat ng mga fragment ng DNA na nagreresulta mula sa pagkilos ng enzyme ay magkakaroon ng parehong malagkit na dulo. Ang mga pantulong na malagkit na dulo ng anumang mga fragment ng DNA ay pinagsama ng mga bono ng hydrogen, na bumubuo ng isang hybrid na pabilog na DNA (Fig.). Upang patatagin ang hybrid na molekula ng DNA, ginagamit ang isa pang enzyme - polynucleotide ligase, na nagpapanumbalik ng mga covalent bond na sinira ng restriction enzyme. Ang sequence na partikular na kinikilala ng EcoRI ay nangyayari sa DNA na hindi hihigit sa 4,000-16,000 base pairs ang pagitan. Samakatuwid, ang isang fragment ng DNA na nabuo sa ilalim ng pagkilos ng EcoRI ay maaaring magsama ng hindi bababa sa isang gene na hindi nasira ng enzyme (sa karaniwan, ang isang gene ay naglalaman ng 1000–1500 na pares ng base).
Ang paggamit ng mga restriction endonucleases at isang bilang ng iba pang mga enzyme ay ginagawang posible upang makakuha ng kumplikadong recombinant na DNA. Ang isang pangkat ng mga mananaliksik sa Estados Unidos na pinamumunuan ni P. Berg ay pinamamahalaang upang pagsamahin ang genetic na impormasyon mula sa tatlong mapagkukunan bilang bahagi ng isang molekula ng DNA: ang kumpletong genome (tingnan) ng oncogenic monkey virus SV40, bahagi ng genome ng temperate bacteriophage λ at ang pangkat ng E. coli genes na responsable para sa assimilation galactose. Ang idinisenyong recombinant molecule ay hindi sinubukan para sa functional na aktibidad, dahil ang mga may-akda ng gawaing ito ay huminto bago ang potensyal na panganib ng pagkalat ng mga oncogenic na virus ng hayop sa populasyon ng bakterya na naninirahan sa bituka ng tao. Ito ay kilala na ang purified DNA ng mga virus ay maaaring tumagos sa iba't ibang mga mammalian cell at maging matatag na minana ng mga ito.
Sa unang pagkakataon, ang mga functionally active na hybrid na molekula ng DNA ay itinayo sa USA ni S. Cohen et al. Ang grupo ni Cohen ay patuloy na nilutas ang problema ng pagsasama-sama at pag-clone (selective accumulation) ng mga molekula ng DNA na nakahiwalay sa mga species na lalong malayo sa isa't isa sa phylogenetic terms. Ang pamamaraan ng pag-clone ay karaniwang binubuo sa katotohanan na ang DNA mula sa iba't ibang mga mapagkukunan ay pira-piraso gamit ang restriction endonucleases, pagkatapos ang mga fragment na ito ay pinagsama sa vitro sa isang karaniwang istraktura at ipinakilala sa organismo ng tatanggap, na sa mga eksperimento ni Cohen ay Escherichia coli. Naitatag na ang mga cell ng ilang bacterial species (kabilang ang Escherichia coli, Salmonella typhimurium, Staphylococcus aureus) ay maaaring mabago (tingnan ang Transformation) gamit ang mga recombinant na molekula ng DNA. Sa kasong ito, ang plasmid na bahagi ng hybrid molecule (o isa sa mga plasmids, kung ang dalawang plasmids mula sa iba't ibang mapagkukunan ay pinagsama sa hybrid molecule) ay nagsisilbing vector, ibig sabihin, tinitiyak ang paglipat ng phylogenetically alien genetic material sa mga cell ng tatanggap at pagpaparami nito sa kanila. Ang unang plasmid na ginamit ni Cohen et al. bilang isang vector ay ang plasmid pSC101 na nakuha niya sa vitro, na kumokontrol sa paglaban ng bakterya sa tetracycline. Ang maliit na plasmid na ito ay 8000 bp lamang ang haba. Inaatake ito ng EcoRI enzyme sa isang site lamang, at hindi sinisira ng enzyme ang kakayahan ng plasmid na magtiklop sa E. coli cells at kontrolin ang resistensya ng tetracycline. Ang mga tampok na ito ay naging posible na gamitin ito para sa pagbuo ng mga hybrid na molekula ng DNA sa vitro. Sa mga unang yugto, ang plasmid DNA na nakahiwalay mula sa iba't ibang mga species ng bakterya at pagkatapos ay mula sa mas mataas na mga organismo ay naka-attach sa pSC101. Kaya, nilikha ang "chimeric" plasmids (iyon ay, hindi maaaring mangyari sa mga natural na kondisyon), na pinagsama sa kanilang komposisyon ang genetic na materyal ng Escherichia coli, isang segment ng DNA mula sa mga oocytes ng clawed frog Xenopus laevis, na kumokontrol sa synthesis ng ribosomal RNA, at isang DNA segment ng isang sea urchin na kumokontrol sa synthesis ng histone protein, o mouse mitochondrial DNA. Sa mga selula ng Escherichia coli, kung saan ipinakilala ang naturang hybrid, "chimeric" plasmids, ang gawain ng mga gene ng mas mataas na organismo ay nakarehistro.
Hindi tulad ng pSC101, na naroroon sa cell lamang sa 4-6 na kopya, ang ilang iba pang mga plasmid na ginamit bilang mga vector ay maaaring magtiklop ng maraming beses sa ilalim ng ilang mga kundisyon, na bumubuo ng ilang libong kopya sa isang cell. Ang ganitong mga katangian ay nagtataglay, halimbawa, ng ColEI plasmid, na kumokontrol sa synthesis ng colicin (tingnan ang Bacteriocinogeny). Tulad ng pSC101, ang ColEI ay na-cleaved ng EcoRl enzyme sa isang site lamang, at ang dayuhang DNA, na ginagamot din sa EcoRI, ay madaling nakakabit sa nagreresultang linear na molekula na may malagkit na dulo. Kaya, ang mga gene ng tryptophan operon ng Escherichia coli ay "natahi" sa ColEI. Sa mga cell na nagdadala ng maraming kopya ng itinayong hybrid plasmid, ang produksyon ng mga enzyme protein na kinokontrol ng tryptophan biosynthesis genes ay tumaas nang husto. Sa in vitro system, posibleng ilakip ang ColEI plasmid sa ilang mga R-factor at isang temperate phage. Ang ganitong gawain ay unang isinagawa sa USSR sa ilalim ng gabay ng Academician A. A. Baev at Propesor S. I. Alikhanyan. Ang pinagsamang mga plasmid ng vector na nabuo ng ColEI at R-factor ay nagagawang dumami nang husto sa mga selulang bacterial, tulad ng ColEI, at sa parehong oras ay tinutukoy ang paglaban ng mga selula sa mga antibiotic, na lubos na nagpapadali sa pagpili ng mga bakterya - mga carrier ng hybrid plasmids.
Ang mga temperate phage ay ginagamit din bilang mga vector. Sa in vitro system, binuo ang mga hybrid na partikulo ng bacteriophage na kinabibilangan ng mga bacterial gene, DNA ng iba pang phage o mas mataas na organismo (halimbawa, DNA ng fruit fly Drosophila) sa kanilang istraktura.
Ang functional na aktibidad ng hybrid DNA ay natutukoy sa pamamagitan ng posibilidad ng kanilang paglipat sa mga selula ng mga organismo ng tatanggap at kasunod na pagpaparami (pagpapalakas) sa mga selulang ito. Bilang mga tatanggap, hindi lamang bakterya, tulad ng nabanggit sa itaas, kundi pati na rin ang mga selula ng mas mataas na mga organismo ay epektibong ginagamit, sa ngayon, gayunpaman, sa anyo lamang ng isang tissue culture na nilinang sa labas ng katawan. May mga indikasyon na ang DNA ng mga phage na nagdadala ng bacterial genes ay maaaring tumagos sa mga selula ng connective tissue ng tao (fibroblasts), sa mga protoplast, o sa isang hindi natukoy na kultura (callus) ng mga selula ng halaman. Noong 1971, si Amer. Ang mananaliksik na si Merrill (S. R. Merril) et al., ay nag-ulat sa mga eksperimento upang itama ang isang namamana na depekto - galactosemia (tingnan) sa pamamagitan ng pagpapakilala sa mga "may sakit" na mga selula ng galactose genes ng mga bakterya na kasama sa DNA ng transducing phage. Bilang isang resulta, ang mga selula ng isang pasyente na may galactosemia, may depekto sa enzyme beta-D-galactose-1-phosphate uridyltransferase, hindi ma-assimilate ang galactose, ibinalik ang kanilang normal na kakayahang lumaki sa pagkakaroon ng galactose, at ang dating walang aktibidad na enzymatic ay nakarehistro sa kanilang mga extract. Ang isang katulad na resulta ay nakuha ni Horst (J. Horst) et al, sa pagpapakilala ng isang bacterial gene na kumokontrol sa synthesis ng beta-galactosidase sa mga fibroblast ng isang pasyente na may pangkalahatan gangliosidosis, na nailalarawan sa pamamagitan ng isang matinding kakulangan ng enzyme na ito. Manion (W. Munyon) at ang kanyang mga katuwang. gamit ang herpes virus, inilipat nila ang gene na kumokontrol sa synthesis ng thymidine kinase mula sa mga selula ng tao patungo sa mga selula ng mouse, na nagpapanumbalik ng kakayahan ng mga may sira na mouse fibroblast na i-synthesize ang enzyme na ito.
Ang isa sa mga paraan upang ilipat ang genetic na impormasyon sa kultura ng mga cell ng tao, hayop at halaman ay ang hybridization ng mga somatic cells, na binuo nina Ephrussi (V. Ephrussi) at Barsky (G. Barski). Ang pagiging epektibo ng pamamaraang ito ay bumuti nang malaki mula nang matuklasan na ang mga particle ng hindi aktibo na Sendai-type na parainfluenza virus ay nagpapataas ng dalas ng cell fusion mula sa isang malawak na iba't ibang mga mapagkukunan. Ang posibilidad ng paglilipat ng mga indibidwal na gene mula sa mga nakahiwalay na Chinese hamster chromosome sa mouse connective tissue cells ay ipinakita. Ang mga hybrid ng mga cell ng tao at mouse ay inilalarawan, kung saan ang bahagi ng mga chromosome ng tao ay tinanggal, habang ang bahagi ay nananatiling aktibo sa pagganap. Ang pag-unlad ng mga pamamaraan ng cell microsurgery ay naging posible upang i-transplant ang cell nuclei mula sa mga somatic cells sa mga fertilized na itlog at, bilang isang resulta, makakuha ng ganap na magkaparehong mga organismo. Ang pag-hybrid ng cell ay naging posible upang mapukaw ang synthesis ng globin ng tao sa mga cell ng mikrobyo ng palaka. Ang lahat ng mga halimbawang ito ay nagpapakita ng potensyal ni G. at.
Praktikal na halaga ng G. at. para sa gamot ay nauugnay sa mga prospect para sa pagwawasto ng namamana metabolic defects sa mga tao (tingnan ang Gene therapy), na lumilikha ng mga microorganism na nawala ang kanilang pathogenicity, ngunit pinanatili ang kakayahang bumuo ng kaligtasan sa sakit, ang synthesis ng antibiotics, amino acids, hormones, bitamina, enzymes, immunoglobulins, atbp., batay sa paggamit ng mga microorganism na may kasamang kaukulang mga gene. Ang mga pambihirang resulta ay maaaring makuha sa malapit na hinaharap G. at. halaman. Sa tulong ng mga pamamaraan ni G. at. sinusubukan nilang lumikha ng mga halaman na maaaring sumipsip ng atmospheric nitrogen at mapabuti ang komposisyon ng protina ng mga pagkaing halaman. Ang matagumpay na solusyon ng mga problemang ito ay kapansin-pansing magpapataas ng produktibidad ng mga halaman, bawasan ang produksyon at pagkonsumo ng mineral nitrogen, at sa gayon ay makabuluhang mapabuti ang kapaligiran (tingnan). Ang posibilidad ng paglikha ng ganap na bagong mga anyo ng mga hayop at halaman sa pamamagitan ng pagtagumpayan ng mga interspecific na hadlang ng interbreeding ay pinag-aaralan. Gayunpaman sa pagtatasa ni G. at. bilang isang bagong paraan ng pag-master ng wildlife, dapat isaalang-alang hindi lamang ang posibleng rebolusyonaryong papel nito sa biology, medisina at agrikultura, kundi pati na rin ang mga pagkakataong nagmumula kaugnay ng pag-unlad nito para sa paglitaw ng mga bagong anyo ng mga pathogenic microorganism, ang panganib ng pagkalat ng hybrid na DNA sa mga populasyon ng bakterya na naninirahan sa mga tao, nagdadala ng mga Oncogenic na virus, atbp. Siyempre, ang sadyang paggamit ng mga nagawa ng agham, kabilang ang G. at., para sa hindi makatao, misanthropic na mga layunin ay posible lamang sa isang lipunan kung saan ang ang kabutihan ng tao ay isinakripisyo sa tubo at pagsalakay.
Mula sa mga karagdagang materyales
Ang genetic engineering ay patuloy na isang mabilis na sumusulong na paraan ng pananaliksik sa molecular biology at genetics. Dapat pansinin na ang mga konsepto ng "genetic engineering" at "genetic engineering" ay hindi ganap na magkasingkahulugan, dahil ang pananaliksik na may kaugnayan sa genetic engineering ay hindi limitado sa mga manipulasyon na may mga gene tulad nito. Sa kasalukuyan, ang mga pamamaraan ng genetic engineering ay nagbibigay-daan para sa pinakamalalim at detalyadong pagsusuri ng mga natural na nucleic acid - mga sangkap na responsable para sa pag-iimbak, paghahatid at pagpapatupad ng genetic na impormasyon (tingnan ang Nucleic acids.), Pati na rin ang lumikha ng binago o ganap na mga bago na hindi matatagpuan sa kalikasan. mga gene (tingnan ang gene), mga kumbinasyon ng mga gene at ipinapahayag ang mga ito nang may mataas na kahusayan sa isang buhay na selula (tingnan ang pagpapahayag ng gene). Sa mga tiyak na praktikal na tagumpay ng genetic engineering sa huling dekada, ang pinakamahalaga ay ang paglikha ng mga producer ng biologically active proteins - insulin (tingnan), interferon (tingnan), growth hormone (tingnan ang Somatotropic hormone), atbp., pati na rin. bilang ang pagbuo ng genetic engineering pamamaraan activation ng mga link ng isang metabolismo, to-rye ay konektado sa pagbuo ng mga low-molecular biologically active substances. Sa ganitong paraan, ang mga producer ng ilang mga antibiotics, amino acids at bitamina ay nakukuha, maraming beses na mas epektibo kaysa sa mga producer ng mga sangkap na ito, na nakuha ng mga tradisyonal na pamamaraan ng genetika at pagpili. Ang mga pamamaraan ay binuo para sa pagkuha ng mga purong protina na bakuna laban sa hepatitis, influenza, herpes, at mga virus ng sakit sa paa at bibig, ang ideya ng paggamit ng pagbabakuna na may vaccinia virus ay ipinatupad, sa genome kung saan ang mga gene na naka-encode ng synthesis ng mga protina ng iba pang mga virus (halimbawa, hepatitis o mga virus ng trangkaso) ay naka-embed: bilang resulta Ang mga pagbabakuna na may virus na binuo sa ganitong paraan, ang katawan ay nagkakaroon ng kaligtasan sa sakit hindi lamang laban sa bulutong, kundi pati na rin laban sa hepatitis, trangkaso o iba pang mga sakit na dulot ng virus na iyon, ang protina na to-rogo ay naka-encode ng built-in na gene.
Ang pandaigdigang koleksyon ng mga restriction endonucleases - restrictases, ang pangunahing "mga tool" ng genetic engineering manipulations, ay lumago nang malaki. Higit sa 400 paghihigpit sa "pagkilala" apprx. 100 partikular na mga site (mga site) ng iba't ibang istraktura sa mga molekula ng DNA (tingnan ang mga Deoxyribonucleic acid) at hinahati ang DNA polynucleotide chain sa mga site na ito. Gamit ang isang ganoong enzyme o kumbinasyon ng ilang restriction enzymes, halos anumang gene ay maaaring ihiwalay bilang bahagi ng isa o higit pang mga fragment ng DNA (tinatawag na restriction fragment). Pinalawak nito ang mga posibilidad ng genetic engineering hindi lamang sa mga tuntunin ng paghihiwalay ng mga gene, kundi pati na rin sa mga tuntunin ng pag-activate ng kanilang trabaho, pagsusuri sa istraktura ng mga gene at kanilang molekular na kapaligiran. Ang mga pamamaraan para sa synthesis ng buong genes na may isang naibigay na pagkakasunud-sunod ng mga nucleotides ay binuo, naging posible na magbigay ng synthesized at natural na mga gene na may iba't ibang mga regulatory nucleotide sequence, palitan, ipasok, tanggalin ang mga solong nucleotides sa mahigpit na tinukoy na mga seksyon ng isang gene, paikliin o kumpletuhin ang nucleotide chain nito na may katumpakan ng isang nucleotide.
Ang tagumpay ng genetic engineering ay ang pagtagos nito sa organisasyon at paggana ng mga mekanismo ng pagmamana sa mga selula ng mas mataas na mga organismo, kabilang ang mga tao. Nasa mas mataas na eukaryotes na ang pinaka-kagiliw-giliw na data ay nakuha gamit ang mga pamamaraan ng genetic engineering. Ang tagumpay ng genetic engineering ay higit na nauugnay sa paggawa ng mga bagong dalubhasang vector na nagpapahintulot sa mahusay na pag-clone (pagpapalaganap) ng mga indibidwal na fragment ng DNA (mga gene) at pag-synthesize ng mga protina na na-encode ng mga gene na ito.
Ang mga fragment ng paghihigpit na konektado sa mga vector ng DNA ay na-clone sa isang buhay na cell gamit ang kakayahan ng mga naturang vector na magparami (magkopya) sa isang cell sa maraming kopya. Depende sa laki ng mga fragment na i-clone at ang layunin ng pag-aaral, ang mga vector ng isa sa apat na uri ay ginagamit - plasmids (tingnan), phages (tingnan. Bacteriophage), cosmids o derivatives ng phages na may single-stranded DNA.
Para sa pag-clone ng medyo maliit na mga fragment ng DNA (hanggang sa 10 libong mga pares ng base), ginagamit ang mga plasmid vectors (pBR322, pAT 153, pUR250, pUC19, atbp.). Ang tagumpay ng genetic engineering sa mga nakaraang taon ay ang paggawa ng mga vectors batay sa phage X (Charon 4A, gtwes-B), kung saan ang bahagi ng genome ay pinalitan ng isang fragment ng dayuhang DNA. Ang hybrid na genome ay artipisyal na "naka-pack" sa isang coat na protina at ang bakterya ay nahawaan ng muling itinayong phage na ito. Bumubuo ng ilang libong mga kopya sa panahon ng pagpaparami sa cell, ang reconstructed phage lyses ito at inilabas sa medium ng kultura. Sa tulong ng naturang mga vectors, ang mga fragment ng DNA na 10-25 thousand base pairs ay na-clone.
Ang mga cosmid vectors (pIB8, MUA-3) ay isang hybrid ng phage X at isang plasmid. Naglalaman sila ng tinatawag na Kinakailangan ang mga sequence ng COS ng phage DNA para sa pag-iimpake ng mga phage genome sa isang shell ng protina, at isang segment ng plasmid DNA na nagpapahintulot sa mga cosmid vector na mag-replika sa bacteria sa parehong paraan tulad ng ginagawa ng mga plasmid. Kaya, ang nagreresultang recombinant genome ay nakakahawa sa bakterya na may mataas na kahusayan tulad ng isang bacteriophage, ngunit dumarami sa kanila tulad ng isang plasmid nang hindi nagiging sanhi ng pagkamatay ng isang bacterial cell. Ang mga Cosmid ay ginagamit para sa pag-clone ng mga fragment ng DNA hanggang sa 35-45 thousand base pairs ang haba.
Ang mga vectors, na mga derivatives ng phages na may single-stranded DNA (M13 mp8, M13, mp73, atbp.), ay itinayo batay sa pabilog na molekula ng DNA ng M13 bacteriophage. Para sa pag-embed ng dayuhang DNA, ginagamit ang isang replicative na double-stranded phage DNA molecule. Ang isang vector na nagdadala ng isang dayuhang DIC ay ipinapasok sa mga bacterial cell, kung saan ang mga recombinant na molekula ay dumarami nang hindi nagli-lysing sa cell na ito at "bumaba" sa medium ng kultura bilang isang viral particle na may isang solong-stranded na molekula ng DNA. Ang mga vector na ito ay ginagamit upang i-clone ang mga fragment ng DNA (hanggang 300-400 base pairs).
Ang gene na kinakailangan para sa genetic engineering manipulations ay nakukuha sa pamamagitan ng pag-clone ng naaangkop na recombinant DNA molecules at pagpili ng mga naturang clone. Sa mga kasong iyon kapag ang mga gene ng mas matataas na organismo at tao ay na-clone / expression sa-rykh sa E. coli (pinaka madalas na ginagamit para sa mga naturang layunin) ay imposible, ang pamamaraan ng pag-clone at pagpili ay isinasagawa sa maraming yugto. Sa unang yugto, isang tinatawag na isang library ng mga gene mula sa mga fragment ng DNA (naka-clone nang direkta mula sa cell genome) o mula sa mga na-clone na kopya ng DNA (cDNA) ng kaukulang messenger RNA. Ang paghahambing ng istraktura ng mga fragment ng genomic DNA at ang kaukulang cDNA, nakakakuha sila ng mahalagang impormasyon tungkol sa organisasyon ng genetic na materyal, at sa kaso ng mga namamana na sakit, tungkol sa likas na katangian ng mga anomalya sa genetic na materyal, ang kinahinatnan nito. sakit. Mula sa library ng gene, gamit ang mga modernong pamamaraan, posibleng kunin ang kinakailangang gene kasama ang mga nakapaligid na rehiyon ng genome. Sa kasalukuyan, ang mga kumpletong aklatan ng mga gene ng maraming microorganism, halaman at hayop (hanggang sa mga mammal at tao) ay nalikha na. Ilang daang mga gene at iba pang mga nucleotide sequence sa DNA ng tao ay na-clone na at sa ilang lawak ay pinag-aralan.
Ang mga posibilidad ng pananaliksik sa genetic engineering ay hindi limitado sa pag-clone ng isang gene at pagkuha ng malaking bilang ng mga kopya nito. Kadalasan ito ay kinakailangan hindi lamang upang i-clone ang isang gene, kundi pati na rin upang matiyak ang pagpapahayag nito sa isang cell, ibig sabihin, upang ipatupad ang impormasyong nakapaloob dito sa pagkakasunud-sunod ng amino acid ng polypeptide chain ng protina na naka-encode ng gene na ito. Kung ang isang gene na ipinasok sa isang bacterial cell ay nakuha mula sa bakterya ng pareho (o malapit) na species, maaaring sapat na upang ihiwalay ang gene na may mga elemento ng regulasyon na kumokontrol sa pagpapahayag nito. Gayunpaman, sa ilang mga pagbubukod, ang mga regulatory nucleotide sequence ng mga evolutionary na malayong organismo ay hindi mapapalitan. Samakatuwid, upang makamit, halimbawa, ang pagpapahayag ng isang eukaryotic gene sa mga cell ng E. coli, ang rehiyon ng regulasyon ay tinanggal mula dito, at ang istrukturang bahagi ng naturang gene ay nakakabit (sa isang tiyak na distansya) sa rehiyon ng regulasyon. ng bacterial gene. Ang makabuluhang pag-unlad sa pag-unlad ng diskarteng ito ay nakamit pagkatapos ng pagtuklas ng Ba131 nuclease enzyme, na may natatanging pag-aari ng hydrolyzing ng parehong mga kadena ng isang double-stranded linear na molekula ng DNA simula sa dulo ng molekula, ibig sabihin, ang enzyme na ito ay nag-aalis ng "dagdag. ” nucleotide sequence ng anumang haba mula sa dulo ng DNA fragment . Sa kasalukuyan, ang mga istruktura at regulasyong rehiyon ay hiwalay na nakahiwalay gamit ang mga paghihigpit na iyon, ang mga "pagkilala" na mga site na pinakamatagumpay na matatagpuan sa polynucleotide chain, pagkatapos ay ang "dagdag" na mga pagkakasunud-sunod ng nucleotide ay tinanggal at ang istruktura na rehiyon ng eukaryotic gene ay konektado sa ang rehiyon ng regulasyon ng bacterial gene. Sa ganitong paraan, posibleng makamit hindi lamang ang pagpapahayag ng mga eukaryotic genes sa bacterial cells, ngunit, sa kabaligtaran, bacterial genes sa mga cell ng mas mataas at mas mababang eukaryotes.
Ang tagumpay ng genetic engineering ay malapit na nauugnay sa pagbuo at pagpapabuti ng mga pamamaraan para sa pagtukoy ng nucleotide sequence (sequencing) sa mga molekula ng DNA. Ang isang makabuluhang bilang ng mga paghihigpit sa pagtatapon ng mga mananaliksik ay ginagawang posible na ihiwalay ang ilang mga fragment ng DNA na may ganap na pagtitiyak, at ang pagbuo at pagpapabuti ng mga pamamaraan ng pag-clone ay ginagawang posible upang makakuha ng mga fragment ng kahit na natatanging mga gene sa mga dami na kinakailangan para sa pagsusuri. Napatunayang napakaepektibo ng mga pamamaraan ng DNA sequencing na kadalasan, sa pamamagitan ng pagtukoy sa sequence ng DNA nucleotide, nakukuha ang data sa sequence ng nucleotide sa kaukulang mga molekula ng RNA at sa sequence ng mga residue ng amino acid sa synthesized na molekula ng protina. Kapag pinoproseso ang mga resulta ng DNA sequencing, ang mga computer ay malawakang ginagamit. Para sa isang mas kumpleto at mas mabilis na interpretasyon ng nakuhang pang-eksperimentong data, ang pambansa at internasyonal na "mga bangko" ng computer ng mga nucleotide sequence ay nililikha. Sa kasalukuyan, ang kumpletong pagkakasunud-sunod ng nucleotide ng mga genome ng isang bilang ng mga bacterial plasmids at mga virus ay natukoy na, at ang problema sa pagtukoy ng kumpletong mga pagkakasunud-sunod ng nucleotide ng mga unang indibidwal na chromosome, at pagkatapos ay ang buong genome ng mas mataas na mga organismo, kabilang ang mga tao, ay mayroon na. nireresolba.
Sa tulong ng mga pamamaraan ng genetic engineering, natagpuan ang mga paglihis sa istraktura ng ilang mga seksyon ng mga gene ng tao, na siyang sanhi ng mga namamana na sakit. Kadalasan, ang pamamaraang ito ay ang tinatawag na. b maraming pagsusuri. Ang nakahiwalay na cellular DNA ay sumasailalim sa restriction enzyme hydrolysis, ang mga nagresultang fragment ay pinaghihiwalay ng laki gamit ang agarose o polyacrylamide gel electrophoresis. Ang mga pinaghiwalay na fragment ay inililipat ("muling na-print") sa espesyal na ginamot na chromatographic na papel, nitrocellulose o nylon na filter at muling sumasailalim sa electrophoretic separation. Gupitin ang mga lugar ng electropherograms na tumutugma sa mga indibidwal na fraction at naglalaman ng parehong uri ng mga fragment ng DNA; Ang mga gupit na seksyon ng mga electrophoregram ay inilublob sa isang dating na-clone na gene o bahagi nito, o sa isang nakuhang kemikal. synthesis sa pamamagitan ng isang nucleotide sequence na naglalaman ng radioactive label. Ang minarkahang DNA ay nakikipag-ugnayan lamang sa mga fragment ng nasuri na cellular DNA, ang to-rye ay may mga sequence ng mga nucleotide na pantulong dito. Ang pagbabago sa distribusyon at dami ng isang nakapirming label kumpara sa pamantayan ay ginagawang posible upang hatulan ang mga pagbabago sa nasuri na gene o mga nucleotide sequence na katabi nito.
Ang mga site ng "pagkilala" ng ilang mga paghihigpit sa molekula ng DNA ay hindi pantay na ipinamamahagi, samakatuwid, sa panahon ng hydrolysis ng mga enzyme na ito, ang molekula ng DNA ay nahahati sa isang bilang ng mga fragment na may iba't ibang haba. Ang muling pagsasaayos ng istraktura ng DNA, bilang isang resulta kung saan nawawala o lumilitaw ang mga umiiral na "pagkilala" na mga site, ay humahantong sa isang pagbabago sa hanay ng mga fragment na ito (ang tinatawag na mga fragment ng paghihigpit), ibig sabihin, sa hitsura ng haba ng fragment ng paghihigpit polymorphism (GVDRF). Ang mga muling pagsasaayos sa molekula ng DNA ay maaaring magdulot o hindi magdulot ng mga pagbabago sa panahon ng synthesis o sa istruktura ng naka-encode na protina; Ang mga muling pagsasaayos na hindi nagdudulot ng mga pagbabago ay ang karamihan, at nagiging sanhi sila ng isang normal na RFLP. Ito ay lumabas na ang RFLP ay isang malinaw na genetic na katangian. Sa kasalukuyan, ang pagsusuri ng RFLP ay naging isa sa mga pinakatumpak na pamamaraan na ginagamit sa genetika ng tao at medikal na genetika. Para sa isang bilang ng mga namamana na sakit, ang mga anyo ng RFLP ay inilarawan na direktang nagpapahiwatig ng pagkakaroon ng isang sakit o ang karwahe ng isang pathologically altered gene.
Ang genetic engineering ay minarkahan ang simula ng isang bagong direksyon ng pananaliksik, na tinatawag na "genetics in reverse." Ang tradisyunal na pagsusuri ng genetic (tingnan) ay isinasagawa sa sumusunod na pagkakasunud-sunod: ang pag-sign ay pinili, ang link ng isang tanda na may isang genetic determinant at ang lokalisasyon ng determinant na ito na may kaugnayan sa kilala na ay itinatag. Sa reverse genetics, ang lahat ay nangyayari sa reverse order: ang isang DNA fragment na may hindi kilalang function ay napili, ang linkage ng DNA fragment na ito sa ibang mga rehiyon ng genome at ang koneksyon nito sa ilang mga katangian ay itinatag. Ang diskarte na ito ay naging posible upang bumuo ng mga pamamaraan para sa maagang pagsusuri at pagtuklas ng mga carrier ng mga sakit tulad ng Huntington's chorea, Duchenne's disease, cystic fibrosis, ang biochemical na katangian ng namamana na mga depekto kung saan hindi pa alam. Gamit ang genealogical na paraan para sa pagtatatag ng mga pattern ng namamana na paghahatid ng Huntington's chorea, ipinakita na ang G8 DNA fragment na nakahiwalay sa genome ng tao ay malapit na nauugnay sa gene na tumutukoy sa sakit, at ang hugis ng RFLP G8 fragment sa populasyon na ito. maaaring masuri ang sakit na ito at matukoy ang mga carrier ng mga may sira na gene.
Mayroon pa ring maraming mga teknikal na kahirapan sa paraan ng pagpapakilala ng mga pamamaraan na ginagamit sa genetic engineering sa medikal na kasanayan. Maraming mga laboratoryo sa buong mundo ang aktibong bumubuo ng praktikal na angkop na genetic engineering diagnostic na pamamaraan, at inaasahan na ang mga ganitong pamamaraan ay makakahanap ng aplikasyon sa malapit na hinaharap, kung hindi para sa mass genetic screening (screening) sa panahon ng medikal na pagsusuri ng populasyon, kung gayon, sa hindi bababa sa, para sa isang sample na survey ng mga high-risk na grupo para sa mga namamana na sakit.
Ginagawang posible ng genetic engineering hindi lamang ang pagkopya ng mga natural na compound at proseso, kundi pati na rin ang pagbabago sa mga ito at gawing mas mahusay ang mga ito. Ang isang halimbawa nito ay isang bagong linya ng pananaliksik na tinatawag na protina engineering. Ang mga kalkulasyon na ginawa batay sa data sa pagkakasunud-sunod ng amino acid at ang spatial na organisasyon ng mga molekula ng protina ay nagpapakita na sa ilang mga kapalit ng ilang mga residue ng amino acid sa mga molekula ng isang bilang ng mga enzyme, ang isang makabuluhang pagtaas sa kanilang aktibidad ng enzymatic ay posible. Sa isang nakahiwalay na gene na nag-encode ng synthesis ng isang partikular na enzyme, ginagamit ang mga pamamaraan ng genetic engineering upang maisagawa ang mahigpit na kinokontrol na pagpapalit ng ilang mga nucleotide. Sa panahon ng synthesis ng isang enzymatic na protina sa ilalim ng kontrol ng tulad ng isang binagong gene, ang isang paunang binalak na kapalit ng mahigpit na tinukoy na mga residu ng amino acid sa polypeptide chain ay nangyayari, na nagiging sanhi ng pagtaas ng aktibidad ng enzymatic nang maraming beses kumpara sa aktibidad ng isang natural. prototype.
Sa larangan ng agrikultura, ang genetic engineering ay inaasahang magbibigay ng malaking kontribusyon sa pagpili ng mga bagong high-yielding na uri ng halaman na lumalaban sa tagtuyot, sakit, at peste, gayundin sa pagbuo ng mga bagong mataas na produktibong uri ng pananim. hayop.
Tulad ng anumang tagumpay ng agham, ang mga tagumpay ng genetic engineering ay maaaring gamitin hindi lamang para sa kapakinabangan, kundi pati na rin sa kapinsalaan ng sangkatauhan. Ang mga espesyal na isinagawang pag-aaral ay nagpakita na ang panganib ng walang kontrol na pagkalat ng recombinant DNA ay hindi kasing-laki ng naunang naisip. Ang recombinant na DNA at bakterya na nagdadala ng mga ito ay naging napaka-unstable sa mga impluwensya sa kapaligiran, hindi mabubuhay sa mga tao at hayop. Ito ay kilala na sa kalikasan at walang interbensyon ng tao ay may mga kondisyon na nagbibigay ng aktibong pagpapalitan ng genetic na impormasyon, ito ang tinatawag. daloy ng gene. Gayunpaman, ang kalikasan ay lumikha ng maraming mabisang hadlang sa pagtagos ng alien genetic na impormasyon sa katawan. Sa kasalukuyan, malinaw na kapag nagtatrabaho sa karamihan ng mga recombinant na molekula ng DNA, ang karaniwang mga pag-iingat ay sapat na, ang to-rye ay ginagamit, halimbawa, ng mga microbiologist kapag nagtatrabaho sa nakakahawang materyal. Para sa mga espesyal na kaso, ang mga epektibong pamamaraan ay binuo para sa parehong biological na proteksyon at pisikal na paghihiwalay ng mga eksperimentong bagay mula sa mga tao at sa kapaligiran. Samakatuwid, ang napakahigpit na mga unang bersyon ng mga patakaran para sa pagtatrabaho sa recombinant na DNA ay binago at lubos na nakakarelaks. Tulad ng para sa sinasadyang paggamit ng mga nagawa ng genetic engineering sa kapinsalaan ng mga tao, ang parehong mga siyentipiko at ang publiko ay dapat aktibong lumaban upang matiyak na ang panganib na ito ay nananatiling posible lamang sa teorya.
Tingnan din ang Biotechnology.
Bibliograpiya: Alikhanyan S. I. Mga tagumpay at prospect ng genetic engineering, Genetics, vol. 12, Jvft 7, p. 150, 1976, bibliogr.; AlikhanyanS. I. et al. Pagkuha ng mga gumaganang recombinant (hybrid) na mga molekula ng DNA, in vitro, ibid., vol. I, No. 11, p. 34, 1975, bibliogr.; Baev A. A. Genetic engineering, Priroda, M1, p. 8, 1976; Tikhomirova L.P. at iba pa. Hybrid DNA molecules ng phage X at plasmids ColEl, Dokl. USSR Academy of Sciences, tomo 223, blg. 4, p. 995, 1975, bibliogr.; Kayumanggi D.D.a. S t e r n R. Mga paraan ng paghihiwalay ng gene, Ann. Sinabi ni Rev. Biochem., v. 43, p. 667, 1974, bibliogr.; C h a n g A. C. Y. a. o. Mga pag-aaral ng mouse mitochondrial DNA sa Escherichia coli, Cell, v. 6, p. 231.1975, bibliogr.; Hedgpeth J., Goodman H. M. a. B o y e r H. W. DNA nucleotide sequence na pinaghihigpitan ng R1 endonuclease, Proc. nat. Acad. sci. (Maghugas.), v. 69, p. 3448, 1972, bibliogr.; Hershfield V.a. o. Plasmid ColEl bilang isang molekular na sasakyan para sa cloning at amplification ng DNA, ibid., v. 71, p. 3455, 1974; Kinabukasan J. F. a. o. Pagtitiklop at transkripsyon ng eukaryotic DNA sa Escherichia coli, ibid., p. 1743; T e m i n H. M. a. Mizu-tani S. RNA-dependent DNA polymerase sa mga virion ng Rous sarcoma virus, Kalikasan (Lond.), v. 226, p. 1211, 1970.
Biotechnology, ed. A. A. Baeva, M., 1984; B tungkol sa h hanggang tungkol sa N. P., Zakharov A. F. at Ivanov V. I. Medical genetics, M., 1984; M a n i a-tis G., FrichE. at Sambrook J. Mga pamamaraan ng genetic engineering. Molecular cloning, trans. mula sa English, M., 1984; A n t o n a r a k i s S. E. a. o. Ang polymorphism ng DNA at molekular na patolohiya ng mga kumpol ng gene ng globin ng tao, Hum. Genet., v. 69, p. 1, 1985; Beaudet A. L. Bibliograpiya ng naka-clone na tao at iba pang mga piling DNA, Amer. J. ugong. Genet., v. 37, p. 386, 1985; Sa o t s t e i n D. a. o. Paggawa ng isang genetic linkage map sa tao gamit ang restriction fragment length polymorphism, ibid., v. 32, p. 314, 1980; G u s e 1 1 a J. E. a. o. Mga marker ng DNA para sa mga sakit sa nervous system, Science, v. 225, p. 1320, 1984; Motulsky A. G. Epekto ng genetic manipulation sa lipunan at medisina, ibid., v. 219, p. 135, 1983; Puting R. a. o. Isang malapit na nauugnay na genetic marker para sa cystic fibrosis, Kalikasan (Lond.), v. 318, p. 382, 1985; Wo o S. L. C., L i d s to y A. S. a. Guttler F. Prenatal diagnosis ng classical phenylketonuria sa pamamagitan ng gene mapping, J. Amer. med. Ass., v. 251, p. 1998, 1984.
L. S. Chernin, V. H. Kalinin.
genetic engineering
Ang modernong biology sa panimula ay naiiba mula sa tradisyonal na biology hindi lamang sa higit na lalim ng pag-unlad ng mga ideyang nagbibigay-malay, kundi pati na rin sa isang mas malapit na koneksyon sa buhay ng lipunan, na may kasanayan. Masasabi nating sa ating panahon, ang biology ay naging isang paraan ng pagbabago ng buhay na mundo upang matugunan ang mga materyal na pangangailangan ng lipunan. Ang konklusyon na ito ay inilalarawan, una sa lahat, sa pamamagitan ng malapit na ugnayan sa pagitan ng biology at biotechnology, na naging pinakamahalagang lugar ng produksyon ng materyal, isang pantay na kasosyo ng mga teknolohiyang mekanikal at kemikal na ginawa ng tao, pati na rin ang gamot.
Mula nang ito ay mabuo, ang biology at biotechnology ay palaging nabuo nang magkasama, at mula pa sa simula, ang biology ay naging siyentipikong batayan ng biotechnology. Gayunpaman, sa mahabang panahon, ang kakulangan ng sariling data ay hindi nagpapahintulot sa biology na magkaroon ng napakalaking epekto sa biotechnology. Ang sitwasyon ay nagbago nang malaki sa paglikha sa ikalawang kalahati ng ika-20 siglo. pamamaraan ng genetic engineering, na nauunawaan bilang genetic manipulation na may layuning bumuo ng bago at muling pagtatayo ng mga umiiral na genotype. Bilang isang pamamaraang tagumpay sa pamamagitan ng likas na katangian nito, ang genetic engineering ay hindi humantong sa isang pagkasira ng umiiral na mga ideya tungkol sa biological phenomena, ay hindi nakakaapekto sa mga pangunahing probisyon ng biology, tulad ng radio astronomy ay hindi niyanig ang mga pangunahing probisyon ng astrophysics, ang pagtatatag ng Ang "mechanical equivalent of heat" ay hindi humantong sa pagbabago sa mga batas ng heat conduction, at ang patunay Ang atomistic theory of matter ay hindi nagbago sa mga relasyon ng thermodynamics, hydrodynamics at elasticity theory (A.A. Baev).
Gayunpaman, ang genetic engineering ay nagbukas ng isang bagong panahon sa biology sa kadahilanang ang mga bagong pagkakataon ay lumitaw para sa pagtagos sa kailaliman ng mga biological phenomena upang higit na makilala ang mga anyo ng pagkakaroon ng buhay na bagay, mas epektibong pag-aralan ang istraktura at pag-andar ng mga gene sa ang antas ng molekular, at nauunawaan ang mga banayad na mekanismo ng trabaho, genetic apparatus. Ang mga pagsulong sa genetic engineering ay nangangahulugan ng isang rebolusyon sa modernong
likas na agham. Tinutukoy nila ang pamantayan para sa halaga ng mga modernong ideya tungkol sa istruktura at functional na mga tampok ng molekular at cellular na antas ng nabubuhay na bagay. Ang mga modernong data sa mga nabubuhay na bagay ay may napakalaking kahalagahang nagbibigay-malay, dahil nagbibigay sila ng pag-unawa sa isa sa pinakamahalagang aspeto ng organikong mundo at sa gayon ay gumawa ng isang napakahalagang kontribusyon sa paglikha ng isang siyentipikong larawan ng mundo. Kaya, nang husto ang pagpapalawak ng cognitive base nito, ang biology sa pamamagitan ng genetic engineering ay nagkaroon din ng nangungunang impluwensya sa pagtaas ng biotechnology.
Ang genetic engineering ay lumilikha ng batayan sa landas sa pag-unawa sa mga pamamaraan at paraan ng "pagdidisenyo" ng bago o pagpapabuti ng mga umiiral na organismo, na nagbibigay sa kanila ng malaking pang-ekonomiyang halaga at ng kakayahang kapansin-pansing pataasin ang produktibidad ng mga prosesong biotechnological. Gayunpaman, ang genetic engineering ay lumikha ng mga bagong abot-tanaw para sa medisina sa larangan ng diagnosis at paggamot ng maraming sakit, parehong hindi namamana at namamana. Nagbukas siya ng mga bagong paraan sa paghahanap ng mga bagong gamot at materyales na ginagamit sa medisina. Ang genetic engineering at biotechnology ay nagpasigla sa pagbuo ng mga pamamaraan ng bionanotechnology.
Sa loob ng balangkas ng genetic engineering, mayroong genetic at cellular engineering. Ang genetic engineering ay ang pagmamanipula upang lumikha ng mga recombinant na molekula ng DNA. Ang pamamaraang ito ay madalas na tinutukoy bilang molecular cloning, gene cloning, recombinant DNA technology, o simpleng genetic manipulation. Mahalagang bigyang-diin na ang object ng genetic engineering ay mga molekula ng DNA, mga indibidwal na gene. Sa kabaligtaran, ang cell engineering ay nauunawaan bilang genetic manipulations na may nakahiwalay na indibidwal na mga cell o grupo ng mga cell ng halaman at hayop.
GENETIC ENGINEERING AT MGA TOOL NITO
Ang genetic engineering ay isang hanay ng iba't ibang mga eksperimentong pamamaraan (pamamaraan) na nagbibigay ng konstruksyon (rekonstruksyon), pag-clone ng mga molekula ng DNA at mga gene na may mga tiyak na layunin.
Ang mga pamamaraan ng genetic engineering ay ginagamit sa isang tiyak na pagkakasunud-sunod (Larawan 127), at ilang mga yugto ay nakikilala sa pagpapatupad
isang tipikal na eksperimento sa genetic engineering na naglalayong i-clone ang isang gene, katulad ng:
1. Paghihiwalay ng plasmid DNA mula sa mga selula ng organismo ng interes (paunang) at paghihiwalay ng vector ng DNA.
2. Pagputol (paghihigpit) ng DNA ng orihinal na organismo sa mga fragment na naglalaman ng mga gene ng interes gamit ang isa sa mga restriction enzymes at paghihiwalay ng mga gene na ito mula sa pinaghalong restriction. Kasabay nito, ang vector DNA ay pinutol (pinaghihigpitan), na ginagawang linear mula sa isang pabilog na istraktura.
3. Pag-uugnay sa segment ng DNA (gene) ng interes sa vector DNA upang makakuha ng mga hybrid na molekula ng DNA.
4. Pagpapakilala ng mga recombinant na molekula ng DNA sa pamamagitan ng pagbabago sa ibang organismo, halimbawa, sa E. coli o somatic cells.
5. Inoculation ng bacteria, kung saan ipinakilala ang mga hybrid na molekula ng DNA, sa nutrient media na nagpapahintulot sa paglaki ng mga cell lamang na naglalaman ng mga hybrid na molekula ng DNA.
6. Pagkilala sa mga kolonya na binubuo ng bakterya na naglalaman ng mga hybrid na molekula ng DNA.
7. Pag-iisa ng naka-clone na DNA (mga cloned na gene) at ang paglalarawan nito, kabilang ang pagkakasunud-sunod ng mga nitrogenous base sa naka-clone na fragment ng DNA.
kanin. 127.Mga sunud-sunod na yugto ng eksperimento sa genetic engineering
Sa kurso ng ebolusyon, nabuo ng bakterya ang kakayahang mag-synthesize ng tinatawag na restriction enzymes (endonucleases), na naging bahagi ng cellular (bacterial) restriction-modification system. Sa bakterya, ang mga restriction-modification system ay ang intracellular immune defense system laban sa dayuhang DNA. Hindi tulad ng mas mataas na mga organismo, kung saan ang pagkilala at pagkasira ng mga virus, bakterya, at iba pang mga pathogen ay nangyayari sa extracellularly, sa bakterya, ang proteksyon mula sa dayuhang DNA (DNA ng mga halaman at hayop kung saan sila nakatira) ay nangyayari sa intracellularly, i.e. kapag ang dayuhang DNA ay pumasok sa cytoplasm ng bacteria. Upang maprotektahan ang kanilang sarili, ang bakterya ay nag-evolve din ng kakayahang "i-tag" ang kanilang sariling DNA na may mga methylating base sa mga tiyak na pagkakasunud-sunod. Para sa parehong dahilan, ang dayuhang DNA, dahil sa kawalan ng mga methyl group dito sa parehong mga pagkakasunud-sunod, ay natutunaw (pinutol) sa mga fragment ng iba't ibang mga bacterial restriction enzymes, at pagkatapos ay pinababa ng bacterial exonucleases sa nuleotides. Masasabi natin na sa ganitong paraan pinoprotektahan ng bakterya ang kanilang sarili mula sa DNA ng mga halaman at hayop, kung saan ang organismo ay pansamantalang nabubuhay (bilang mga pathogen) o permanente (bilang saprophytes).
Ang mga restriction enzyme ay unang nahiwalay sa E. coli noong 1968. Napag-alaman na nagagawa nilang putulin (natunaw) ang mga molekula ng DNA sa iba't ibang mga site (lugar) ng paghihigpit. Ang mga enzyme na ito ay tinatawag na class I endonucleases. Pagkatapos, ang class II endonucleases ay natagpuan sa bacteria, na partikular na kinikilala ang mga restriction site sa dayuhang DNA at nagsasagawa rin ng paghihigpit sa mga site na ito. Ang mga enzyme ng klase na ito ang nagsimulang gamitin sa genetic engineering. Kasabay nito, natuklasan ang mga class III na enzyme na natutunaw ang DNA malapit sa mga site ng pagkilala, ngunit ang mga enzyme na ito ay walang kahalagahan sa genetic engineering.
Ang pagkilos ng restriction-modification system ay "na-rationalize" ng tinatawag na palindromic (recognizing) sequence ng nitrogenous bases, na mga site ng paghihigpit ng DNA. Ang mga Palindromic na sequence ay mga pagkakasunud-sunod ng mga base na nagbabasa ng parehong pasulong at paatras, tulad ng pagkakasunud-sunod ng mga titik radar. Dahil ang mga DNA strand ay may antiparallel na direksyon, ang isang sequence ay itinuturing na palindromic kung ito ay magkapareho kapag binasa sa direksyon mula sa 5" hanggang 3" na dulo sa itaas at sa lower strand mula sa 3" hanggang 5" wakas, ibig sabihin:

Ang mga palindrome ay maaaring maging anumang laki, ngunit karamihan sa mga palindrome na ginagamit bilang mga restriction enzyme recognition site ay 4, 5, 6, at bihirang 8 base ang haba.
Ang mga restriction enzymes ay isang ganap na mahalagang kasangkapan sa genetic engineering para sa pagputol ng mga fragment (genes) ng interes mula sa malalaking molekula ng DNA. Dahil higit sa 100 restriction enzymes ang kilala, pinapayagan nito ang pagpili ng restriction enzymes at ang selective excision ng mga fragment mula sa orihinal na DNA.
Ang isang kapansin-pansing tampok ng restrictases ay ang paggawa ng mga hiwa ng mga molekula sa ilang mga fragment (paghihigpit) ng DNA sa mga ledge, bilang isang resulta kung saan ang isang strand ay mas mahaba kaysa sa isa sa mga nagresultang dulo, na bumubuo ng isang uri ng buntot. Ang ganitong mga dulo (buntot) ay tinatawag na "malagkit" na mga dulo, dahil ang mga ito ay may kakayahang magkaugnay sa sarili.
Isaalang-alang ang mga resulta ng paghihigpit sa halimbawa ng isa sa mga pinakatanyag na paghihigpit EcoRI mula sa restriction-modification system E. coi. Sa halip na tunawin ang DNA sa gitna ng palindromic recognition sequence, ang enzyme na ito ay natutunaw ang DNA sa labas ng gitna at gumagawa ng 4 na self-complementary (“sticky”) na mga dulo, na binubuo ng ibang bilang ng mga nucleotide, katulad ng:

Ang mga "malagkit" na dulo na ito ay kapaki-pakinabang sa genetic engineering dahil maaari silang muling maiugnay sa mababang temperatura, na nagbibigay-daan sa mahusay na pagsasara ng mga fragment ng DNA.
Ang mga site ng pagkilala at mga natutunaw na site sa kaso ng iba pang mga paghihigpit ay may ibang nilalaman, katulad ng:

Kasunod ng paghihigpit sa DNA, ang mga fragment ng DNA ng paghihigpit (mga paghihigpit sa DNA) ay ihihiwalay mula sa pinaghalong paghihigpit, na pagkatapos ay kinakailangan para sa kaugnayan sa vector. Ang pinaghihigpitang DNA ay nakahiwalay gamit ang electrophoresis, dahil sa pamamaraang ito ay napakadaling i-fractionate ang pinaghihigpitang DNA dahil sa laki ng mga pinaghihigpitang fragment at pare-pareho ang mga ratio ng singil-masa ng kuryente. Ang mga fragment sa isang electric field ay lumilipat sa panahon ng electrophoresis sa isang frequency na nakadepende sa kanilang laki (mass). Ang mas malaki (mas mahaba) ang fragment, mas mabagal ang paglipat nito sa electric field. Ang materyal kung saan isinasagawa ang electrophoresis ay hindi nagcha-charge ng agarose o polyacrylamide. Para sa pagkakakilanlan ng mga fragment, ang ethidium bromide ay ginagamit, na nagpapalamlam sa mga fragment, na humahantong sa kanilang mas madaling pagtuklas.
Ang kahusayan ng electrophoresis ay napakataas, dahil maaari itong magamit upang paghiwalayin ang mga fragment na may sukat mula 2 hanggang 50,000 base.
Pagkatapos ng electrophoresis, ang mga fragment mula sa agarose ay ihiwalay gamit ang iba't ibang pamamaraan. Batay sa mga resulta ng paghahambing ng laki
Ang mga paghihigpit ng parehong DNA, na nakuha gamit ang iba't ibang mga enzyme ng paghihigpit, ay bumubuo ng mga mapa ng paghihigpit, na nagpapakita ng mga lugar ng paghihigpit ng bawat isa sa mga enzyme ng paghihigpit na ginamit. Sa mga praktikal na termino, ginagawang posible ng mga mapa ng paghihigpit na matukoy hindi lamang ang laki ng mga paghihigpit, kundi pati na rin upang malaman ang lokasyon ng loci ng ilang mga gene sa mga molekula ng DNA.
Dahil sa mas mataas na mga organismo, sa panahon ng transkripsyon, ang heterogenous na DNA ay synthesize, naitama sa pamamagitan ng pagproseso, sa genetic engineering, ang komplementaryong DNA (cDNA) ay karaniwang ginagamit, na nakuha sa pamamagitan ng paggamit ng mRNA bilang isang template, kung saan ang reverse transcriptase ay synthesizes single-stranded DNA ( cDNA), na isang kopya ng mRNA. Kasunod nito, ang mga single-stranded na DNA na ito ay na-convert sa double-stranded na DNA. Isaalang-alang na ang cDNA ay naglalaman ng tuluy-tuloy na nucleotide sequence (na-transcribe at isinalin). Ito ay cDNA na ginagamit para sa paghihigpit.
Ang mga fragment ng DNA (mga paghihigpit) na nakahiwalay pagkatapos ng electrophoresis mula sa mga agarose gel ay maaaring paunang sumailalim sa pagkakasunud-sunod; matukoy ang kanilang nucleotide sequence. Para dito, ginagamit ang mga pamamaraan ng pagkakasunud-sunod ng kemikal at enzymatic. Ang pamamaraang kemikal ay batay sa pagkuha ng mga fragment na may label na radioactive phosphorus (32 P) at pag-alis ng isa sa mga base mula sa mga fragment na ito, na sinusundan ng pagsasaalang-alang sa mga resulta ng radioautography ng mga gel na naglalaman ng mga fragment na ito. Ang pamamaraan ng enzymatic ay batay sa katotohanan na ang isang nucleotide ay ipinakilala sa dulo ng nasuri na fragment, na pagkatapos ay ginagamit sa synthesis ng iba't ibang mga fragment. sa vitro, nasuri para sa electrophoretically sequence ng nucleotide. Upang pag-aralan ang mga tiyak na pagkakasunud-sunod ng nucleotide sa isang molekula ng DNA, gamitin
hybridization din ng DNA-DNA, RNA-RNA, DNA-RNA, Northern-
at Southern blots.
Mga genetic na vector. Ang DNA segment (gene) na nilayon para sa molecular cloning ay dapat na magawang mag-replicate kapag ito ay inilipat sa isang bacterial cell, i.e. maging isang replika. Gayunpaman, wala siyang kakayahang ito. Samakatuwid, upang matiyak ang paglilipat at pagtuklas ng mga naka-clone na gene sa mga cell, pinagsama sila sa tinatawag na genetic vectors. Ang huli ay dapat magkaroon ng hindi bababa sa dalawang pag-aari. Una, ang mga vector ay dapat na magawang magtiklop
sa mga cell, at sa ilang dulo. Pangalawa, dapat nilang payagan ang pagpili ng mga cell na naglalaman ng vector, i.e. nagtataglay ng marker kung saan posibleng i-counter-select ang mga cell na naglalaman ng vector kasama ang cloned gene (recombinant DNA molecules). Ang mga plasmid at phage ay nakakatugon sa mga kinakailangang ito. Ang mga plasmid ay mahusay na mga vector dahil sila ay mga replicon at maaaring maglaman ng mga gene para sa paglaban sa anumang antibiotic, na nagbibigay-daan sa pagpili ng mga bakterya para sa paglaban sa antibiotic na ito at, samakatuwid, madaling pagtuklas ng mga recombinant na molekula ng DNA.
(Larawan 128).
kanin. 128. Vector pBRl
Dahil walang natural na plasmid vectors, lahat ng plasmid vectors na kilala sa ngayon ay artipisyal na binuo. Ang R-plasmids ay nagsilbing panimulang materyal para sa paglikha ng isang bilang ng mga genetic vector, kung saan ang mga labis na pagkakasunud-sunod ng DNA, kabilang ang mga may maraming mga site ng paghihigpit, ay inalis sa tulong ng mga paghihigpit. Ang pag-alis na ito ay natukoy sa pamamagitan ng katotohanan na ang plasmid vector ay dapat magkaroon lamang ng isang site ng pagkilala para sa isang restriction enzyme, at ang site na ito ay dapat na nasa isang functional na hindi mahalagang rehiyon ng plasmid genome. Halimbawa, ang pBR 322 plasmid vector, na mayroong ampicillin at tetracycline resistance genes, na ginagawang napakaginhawa
para sa pagpili ng mga bacteria na naglalaman ng naka-clone na segment ng DNA, mayroon itong iisang restriction site para sa higit sa 20 restriction enzymes, kabilang ang mga kilalang restriction enzymes gaya ng Eco RI, Hind III, Pst I, Pva II at Sal I.
Ang mga vector ng Phage ay mayroon ding ilang mga pakinabang. Maaaring kabilang sa mga ito ang mas malalaking (mas mahabang) cloned na mga fragment ng DNA kumpara sa mga plasma vector. Dagdag pa, ang paglipat ng cloned fragment ng mga phage sa mga cell bilang resulta ng impeksyon ng huli ay mas mahusay kaysa sa pagbabagong-anyo ng DNA. Sa wakas, pinapayagan ng mga phage vector ang mas mahusay na screening (pagkilala) sa ibabaw ng agar ng mga kolonya na naglalaman ng mga cell na nagdadala ng cloned gene. Maraming phage vectors ang nakabatay sa lambda phage.
Bilang karagdagan sa phage, ang iba pang mga viral vector na binuo batay sa herpes virus, pati na rin ang mga vector na binuo batay sa yeast DNA, ay ginagamit din.
Kung ang pag-clone ng gene ay isinasagawa gamit ang mga selula ng mammalian o halaman, kung gayon ang mga kinakailangan para sa mga vector ay kapareho ng sa kaso ng pag-clone sa mga selulang bacterial.
Konstruksyon ng mga recombinant na molekula ng DNA. Ang direktang pagtatayo ng mga recombinant na molekula ng DNA ay sumusunod pagkatapos makuha ang paghihigpit ng pinag-aralan na DNA at vector DNA. Binubuo ito sa pagsasara ng mga segment ng paghihigpit ng pinag-aralan na DNA na may paghihigpit sa vector DNA, na, bilang resulta ng paghihigpit, lumiliko mula sa pabilog patungo sa linear na DNA.
Upang isara ang mga fragment ng DNA na pinag-aaralan kasama ang DNA ng vector, ginagamit ang DNA ligase (Larawan 129). Magiging matagumpay ang ligation kung ang mga istrukturang pagsasamahin ay mayroong 3'-hydroxyl at 5'-phosphate na grupo at kung ang mga grupong ito ay matatagpuan sa isang naaangkop na kaugnayan sa isa't isa. Ang mga fragment ay pinagsama-sama sa pamamagitan ng kanilang "malagkit" na mga dulo bilang resulta ng self-complementarity. Sa mataas na konsentrasyon ng mga fragment, ang huli ay paminsan-minsan ay nasa tamang posisyon (sa tapat ng bawat isa). Maraming restrictases, gaya ng Eco RI, ang gumagawa ng apat na base na "sticky" na dulo. Ang proseso ng ligation ng "sticky" ay nagtatapos, na binubuo ng apat na base, ay nangyayari sa isang mababang temperatura (hanggang sa 12? C).

kanin. 129. DNA ligation
Kung ang mga fragment na walang "malagkit" na dulo ay nabuo sa panahon ng paghihigpit, kung gayon ang mga ito ay "sapilitan" na na-convert sa mga molekula na may "malagkit" na mga dulo gamit ang transferase enzyme. Ang enzyme na ito ay nagdaragdag ng mga nucleotide sa 3" na dulo ng DNA. Maaaring magdagdag ng poly-A tail sa isang fragment, isang poly-T tail sa kabilang banda. Ginagamit din ang polymerase chain reaction (PCR) upang makabuo ng anumang nais na mga dulo ng DNA. Ang Ang prinsipyo ng PCR ay nakabatay sa denaturation ng DNA na nakahiwalay sa mga cell at sa "annealing" nito kasama ang pagdaragdag ng mga DNA oligonucleotides na binubuo ng 15-20 nucleotides bawat isa sa mga renaturating chain. Ang mga oligonucleotide na ito ay dapat na komplementaryo sa mga sequence sa mga chain na pinaghihiwalay ng mga distansya ng 50-2000 nucleotides. DNA synthesis sa vitro, pinapayagan nila ang DNA polymerase na kopyahin ang mga rehiyong iyon na nasa pagitan ng "mga buto". Ang pagkopya na ito ay nagbibigay ng malaking bilang ng mga kopya ng pinag-aralan na fragment ng DNA.
Pagpapasok ng mga recombinant na molekula ng DNA sa mga selula. Matapos ang DNA fragment (gene) ng interes ay pinagsama sa isang genetic vector gamit ang DNA ligase, ang mga resultang recombinant molecule ay ipinapasok sa mga cell upang makamit ang kanilang pagtitiklop (dahil sa genetic vector) at dagdagan ang bilang ng mga kopya. Ang pinakasikat na paraan upang maipasok ang mga recombinant na molekula ng DNA sa mga cell, kung saan ang vector ay isang plasmid, ay pagbabagong-anyo E. coli. Para sa layuning ito, ang mga bacterial cell ay paunang ginagamot ng calcium o rubidium (ions), upang
upang sila ay maging "kakayahang" sa pang-unawa ng recombinant DNA. Upang mapataas ang dalas ng pagpasok ng DNA sa mga cell, ginagamit ang paraan ng electroporation, na binubuo sa maikling paglalantad ng mga cell sa isang matinding electric field. Ang paggamot na ito ay lumilikha ng mga cavity sa mga lamad ng cell, na ginagawang mas madali para sa mga cell na kumuha ng DNA. Matapos ang pagpapakilala ng mga recombinant na molekula ng DNA sa bakterya, ang huli ay inihahasik sa MPA (meat-peptone agar) na pinayaman ng mga antibiotics upang piliin ang nais na mga cell, i.e. mga cell na naglalaman ng mga recombinant na molekula ng DNA. Ang dalas ng pagbabago ay mababa. Karaniwan, isang transformant ang nangyayari sa bawat 10 5 seeded cell. Kung ang vector ay phage, kung gayon ang mga cell (bakterya o lebadura) ay inililipat kasama ng phage. Tulad ng para sa mga somatic cells ng hayop, ang mga ito ay inililipat kasama ang DNA sa pagkakaroon ng mga kemikal na nagpapadali sa pagpasa ng DNA sa pamamagitan ng mga lamad ng plasma. Posible rin ang direktang microinjection ng DNA sa mga oocytes, kulturang somatic cell, at mammalian embryo.
Ang pinakamahalagang punto na nauugnay sa molecular cloning ay ang paghahanap para sa isang paraan upang maitaguyod kung ang naka-clone na fragment ay talagang kasama sa vector at, kasama ang vector, na bumubuo ng isang recombinant na molekula ng DNA, ay pumapasok sa mga cell. Kung pinag-uusapan natin ang tungkol sa mga bacterial cell, kung gayon ang isa sa mga pamamaraan ay batay sa pagsasaalang-alang sa insertional inactivation ng plasmid (vector) resistance gene. Halimbawa, sa plasmid vector pBR 322, na tumutukoy sa paglaban sa ampicillin at tetracycline, ang tanging site para sa Pst I restriction enzyme ay matatagpuan sa locus na inookupahan ng ampicillin resistance gene. Pst I natutunaw sa site na ito ay bumubuo ng malagkit na mga dulo na nagpapahintulot sa ligation ng cloned fragment sa vector DNA. Gayunpaman, sa kasong ito, ang plasmid (vector) ampicillin resistance gene ay hindi aktibo, habang ang tetracycline resistance gene sa vector ay nananatiling buo. Ito ay ang tetracycline resistance gene na ginagamit upang piliin ang mga cell na binago ng mga recombinant na molekula ng DNA. Ginagawa nitong posible na i-verify na ang mga selula ng mga lumaki na kolonya sa medium na may tetracycline ay naglalaman nga ng mga recombinant na molekula ng DNA, sinusuri ang mga ito gamit ang tinatawag na "spot test" sa isang pares ng mga pinggan na may solidong medium, isa sa mga ito. naglalaman ng ampicillin, habang ang isa ay walang antibiotic na ito. Ang DNA na i-clone ay
lamang sa mga transformant na lumalaban sa tetracycline. Tulad ng para sa mga transformant na lumalaban sa parehong ampicillin at tetracycline (ArTc), naglalaman sila ng mga molekula ng plasmid (vector) na kusang nakakuha ng isang pabilog na anyo nang walang pagsasama ng dayuhang (clone) na DNA sa kanila.
Ang isa pang paraan para sa pag-detect ng pagpasok ng mga dayuhang (clone) na fragment sa isang plasmid vector ay batay sa paggamit ng isang vector na naglalaman ng β-galactosidase gene. Ang pagpasok ng dayuhang DNA sa gene na ito ay hindi maiiwasang hindi aktibo ang synthesis ng β-galactosidase, na maaaring makita sa pamamagitan ng pag-seeding ng mga nabagong selula sa isang daluyan na naglalaman ng mga substrate ng β-galactosidase. Pinapayagan ng daluyan na ito ang pagpili ng mga stained cell colonies. Mayroon ding iba pang mga pamamaraan.
Tulad ng nabanggit na, ang mga linear restriction fragment ng vector DNA ay may kakayahang ibalik ang pabilog na istraktura nang hindi kasama ang mga naka-clone na segment sa kanila. Upang bawasan ang dalas ng kusang pagbuo ng naturang pabilog na mga molekula ng vector DNA, ang paghihigpit ng vector DNA ay ginagamot ng phosphatase. Bilang resulta, ang pagbuo ng mga pabilog na molekula ng DNA ay nagiging imposible, dahil ang mga dulo ng 5'-PO 4 na kinakailangan para sa pagkilos ng ligase ay mawawala.
Ang set ng mga transformant colonies na lumaki sa isang selective medium ay isang set ng mga cell na naglalaman ng mga clone ng iba't ibang fragment (genes) ng cloned genomic o cDNA. Ang mga koleksyon ng mga clone na ito ay bumubuo sa tinatawag na DNA library, na malawakang ginagamit sa genetic engineering.
Ang huling yugto ng pag-clone ng gene ay ang paghihiwalay at pag-aaral ng naka-clone na DNA, kabilang ang pagkakasunud-sunod. Ang mga promising strain ng bacteria o somatic cell na naglalaman ng mga recombinant na molekula ng DNA na kumokontrol sa synthesis ng mga protina na interesado na may komersyal na halaga ay inililipat sa industriya.
CELL ENGINEERING
Gaya ng nabanggit sa simula ng kabanata, ang cell engineering ay tumutukoy sa genetic manipulation ng mga nakahiwalay na selula ng hayop at halaman. Ang mga manipulasyong ito ay madalas sa vitro, at ang kanilang pangunahing layunin ay upang makakuha ng mga genotype ng mga organismo na ito na may ninanais na mga katangian, pangunahing kapaki-pakinabang sa ekonomiya. Tungkol sa-
Xia man, pagkatapos ay ang cell engineering ay naaangkop sa kanyang mga cell ng mikrobyo.
Ang isang kinakailangan para sa pagbuo ng cell engineering sa mga tao at hayop ay ang pagbuo ng mga pamamaraan para sa paglinang ng kanilang mga somatic cell sa artipisyal na nutrient media, pati na rin ang pagkuha ng mga hybrid ng somatic cells, kabilang ang mga interspecific hybrids. Sa turn, ang mga pagsulong sa paglilinang ng mga somatic cell ay nakaimpluwensya sa pag-aaral ng mga cell ng mikrobyo at pagpapabunga sa mga tao at hayop. Mula noong 60s. ika-20 siglo Maraming mga eksperimento ang isinagawa sa ilang mga laboratoryo sa buong mundo sa paglipat ng somatic cell nuclei sa mga itlog na artipisyal na walang nuclei. Ang mga resulta ng mga eksperimentong ito ay madalas na magkasalungat, ngunit sa pangkalahatan ay humantong sila sa pagtuklas ng kakayahan ng cell nuclei upang matiyak ang normal na pag-unlad ng itlog (tingnan ang Kabanata IV).
Batay sa mga resulta ng pag-aaral sa pagbuo ng mga fertilized na itlog noong dekada 60. ika-20 siglo Sinimulan din ang mga pag-aaral upang matiyak ang posibilidad ng pagpapabunga ng mga itlog sa labas ng katawan ng ina. Napakabilis, ang mga pag-aaral na ito ay humantong sa pagtuklas ng posibilidad ng pagpapabunga ng mga itlog na may spermatozoa sa vitro at ang karagdagang pag-unlad ng mga embryo na nabuo sa ganitong paraan kapag itinanim sa matris ng isang babae. Ang karagdagang pagpapabuti ng mga pamamaraan na binuo sa lugar na ito ay humantong sa katotohanan na ang pagsilang ng mga "test-tube" na mga bata ay naging isang katotohanan. Noong 1981, 12 bata ang ipinanganak sa mundo, na ang buhay ay ibinigay sa laboratoryo, sa test tube. Sa kasalukuyan, ang seksyong ito ng cell engineering ay naging laganap, at ang bilang ng mga "test-tube" na mga bata ay sampu-sampung libo na (Fig. 130). Sa Russia, ang trabaho sa pagkuha ng "test-tube" na mga bata ay sinimulan lamang noong 1986.
Noong 1993, binuo ang isang pamamaraan para sa pagkuha ng monozygotic human twins sa vitro sa pamamagitan ng paghahati sa mga embryo sa mga blastomeres at pagpapalaki sa huli hanggang sa 32 na mga selula, pagkatapos ay maaari silang itanim sa matris ng isang babae.
Naimpluwensyahan ng mga resulta na nauugnay sa mga test-tube na sanggol, ang mga hayop ay nakagawa din ng teknolohiyang tinatawag mga transplant mga embryo. Ito ay nauugnay sa pagbuo ng isang paraan para sa pag-uudyok ng poliovulation, mga pamamaraan para sa artipisyal na pagpapabunga ng mga itlog at pagtatanim ng mga embryo sa katawan ng mga hayop - mga foster na ina. Ang kakanyahan ng teknolohiyang ito ay ang mga sumusunod:
schuschy. Ang isang mataas na produktibong baka ay tinuturok ng mga hormone, na nagreresulta sa poliovulation, na binubuo sa pagkahinog ng 10-20 na mga selula nang sabay-sabay. Ang mga itlog ay pagkatapos ay artipisyal na pinataba sa mga male reproductive cell sa oviduct. Sa ika-7-8 na araw, ang mga embryo ay hinuhugasan sa labas ng matris at inilipat sa matris ng iba pang mga baka (foster mothers), na pagkatapos ay manganganak ng kambal na guya. Ang mga guya ay namamana ng genetic status ng kanilang orihinal na mga magulang.

kanin. 130."Tube" mga bata
Ang isa pang lugar ng cell engineering sa mga hayop ay ang paglikha ng mga transgenic na hayop. Ang pinakasimpleng paraan upang makakuha ng mga naturang hayop ay ang pagpasok ng mga linear na molekula ng DNA sa mga itlog ng orihinal na mga hayop. Ang mga hayop na nabubuo mula sa mga itlog na napataba ay magdadala ng kopya ng ipinakilalang gene sa isa sa kanilang mga chromosome at, bilang karagdagan, ipapadala nila ang gene na ito sa pamamagitan ng mana. Ang isang mas kumplikadong paraan para sa pagkuha ng mga transgenic na hayop ay binuo sa mga daga na naiiba sa kulay ng amerikana at ang mga sumusunod. Una, ang apat na araw na gulang na mga embryo ay tinanggal mula sa katawan ng isang buntis na kulay abong daga at dinudurog sa mga indibidwal na selula. Pagkatapos ay ang nuclei ay nakuha mula sa mga embryonic cell, sila ay inilipat sa mga itlog ng mga itim na daga, na dati ay binawian ng nuclei. Ang mga itim na itlog ng mouse na naglalaman ng mga dayuhang nuclei ay inilalagay sa mga test tube
na may nutrient solution para sa karagdagang pag-unlad. Ang mga embryo na nabuo mula sa mga itlog ng mga itim na daga ay itinanim sa matris ng mga puting daga. Kaya, sa mga eksperimentong ito, posible na makakuha ng isang clone ng mga daga na may kulay abong amerikana, i.e. I-clone ang mga embryonic cell na may gustong katangian. Sa Kabanata IV, sinuri namin ang mga resulta ng pagpapabunga ng artipisyal na wala ng nuclei ng mga itlog ng tupa na may nuclear material ng somatic cells ng mga hayop ng parehong species. Sa partikular, ang nuclei ay inalis mula sa mga itlog ng tupa, at pagkatapos ay ang nuclei ng mga somatic cells (embryonic, prutas o mga selula ng mga pang-adultong hayop) ay ipinakilala sa naturang mga itlog, pagkatapos kung saan ang mga itlog na fertilized sa ganitong paraan ay ipinakilala sa matris ng matatandang tupa. Ang mga ipinanganak na tupa ay naging kapareho ng donor ng tupa. Isang halimbawa ay si Dolly ang tupa. Ang mga clone na guya, daga, kuneho, pusa, mules at iba pang mga hayop ay nakuha din. Ang ganitong pagtatayo ng mga transgenic na hayop ay isang direktang paraan ng pag-clone ng mga hayop na may mga katangiang kapaki-pakinabang sa ekonomiya, kabilang ang mga indibidwal ng isang partikular na kasarian.
Ang mga transgenic na hayop ay nakuha din gamit ang source material na kabilang sa iba't ibang species. Sa partikular, ang isang paraan ay kilala sa paglilipat ng isang gene na kumokontrol sa growth hormone mula sa mga daga patungo sa mga itlog ng mouse, pati na rin isang paraan para sa pagsasama-sama ng mga blastomeres ng tupa sa mga blastomeres ng kambing, na humantong sa paglitaw ng mga hybrid na hayop (mga baka). Ang mga eksperimentong ito ay nagpapahiwatig ng posibilidad na malampasan ang hindi pagkakatugma ng mga species sa mga pinakaunang yugto ng pag-unlad. Ang mga partikular na mapang-akit na mga prospect ay nagbubukas (kung ang hindi pagkakatugma ng mga species ay ganap na nagtagumpay) sa paraan ng pagpapabunga ng mga itlog ng isang species sa pamamagitan ng nuclei ng somatic cells ng isa pang species. Pinag-uusapan natin ang tungkol sa tunay na pag-asam ng paglikha ng matipid na mahahalagang hybrid ng mga hayop na hindi makukuha sa pamamagitan ng pagtawid.
Dapat tandaan na ang gawaing nuclear transplantation ay hindi pa masyadong epektibo. Ang mga eksperimento na isinagawa sa mga amphibian at mammal ay karaniwang nagpakita na ang kanilang pagiging epektibo ay mababa, at ito ay nakasalalay sa hindi pagkakatugma sa pagitan ng donor nuclei at mga oocyte ng tatanggap. Bilang karagdagan, ang mga nagresultang chromosomal aberrations sa transplanted nuclei sa kurso ng karagdagang pag-unlad, na sinamahan ng pagkamatay ng mga transgenic na hayop, ay isang balakid din sa tagumpay.
Sa intersection ng trabaho sa pag-aaral ng cell hybridization at immunological studies, lumitaw ang isang problema na nauugnay sa paggawa at pag-aaral ng tinatawag na monoclonal antibodies. Gaya ng nabanggit sa itaas, ang mga antibodies na ginawa ng katawan bilang tugon sa pagpapakilala ng isang antigen (bakterya, virus, pulang selula ng dugo, atbp.) ay mga protina na tinatawag na immunoglobulins at bumubuo ng pangunahing bahagi ng sistema ng depensa ng katawan laban sa mga pathogen. Ngunit ang anumang dayuhang katawan na ipinakilala sa katawan ay pinaghalong iba't ibang antigens na magpapasigla sa paggawa ng iba't ibang antibodies. Halimbawa, ang mga erythrocyte ng tao ay may mga antigen hindi lamang para sa mga grupo ng dugo A (II) at B (III), kundi pati na rin sa maraming iba pang mga antigen, kabilang ang Rh factor. Dagdag pa, ang bacterial cell wall proteins o ang capsid ng mga virus ay maaari ding kumilos bilang iba't ibang antigens, na nagiging sanhi ng paggawa ng iba't ibang antibodies. Kasabay nito, ang mga lymphoid cell ng immune system ng katawan ay karaniwang kinakatawan ng mga clone. Nangangahulugan ito na kahit na sa kadahilanang ito lamang, sa serum ng dugo ng mga nabakunahang hayop, ang mga antibodies ay palaging isang halo na binubuo ng mga antibodies na ginawa ng mga cell ng iba't ibang mga clone. Samantala, para sa mga praktikal na layunin, ang mga antibodies ng isang uri lamang ang kailangan; tinatawag na monospecific sera na naglalaman lamang ng isang uri ng antibody o, kung tawagin, monoclonal antibodies.
Sa paghahanap ng mga pamamaraan para sa pagkuha ng mga monoclonal antibodies, natuklasan ng mga Swiss researcher noong 1975 ang isang paraan ng hybridization sa pagitan ng mga lymphocyte ng mouse na nabakunahan ng isa o ibang antigen at kulturang bone marrow tumor cells. Ang ganitong mga hybrid ay tinatawag na "hybridoma". Mula sa bahaging "lymphocytic", na kinakatawan ng isang lymphocyte ng isang clone, ang isang hybridoma ay nagmamana ng kakayahang maging sanhi ng pagbuo ng mga kinakailangang antibodies, at ng parehong uri, at salamat sa bahaging "tumor (myeloma)", ito ay nagiging may kakayahang, tulad ng lahat ng mga selula ng tumor, na dumami nang walang katiyakan sa artipisyal na nutrient media, na nagbibigay ng malaking populasyon ng mga hybrid. Sa fig. Ang 131 ay nagpapakita ng isang pamamaraan para sa paghihiwalay ng mga linya ng cell na synthesizing monoclonal antibodies. Ang mga monoclonal antibody-producing mouse cell lines ay ibinubukod sa pamamagitan ng pagsasama ng mga myeloma cells na may mga lymphocytes mula sa spleen ng mga daga na nabakunahan limang araw na nakalipas.
gustong antigen. Ang pagsasanib ng cell ay nakakamit sa pamamagitan ng paghahalo sa kanila sa pagkakaroon ng polyethylene glycol, na nag-uudyok sa pagsasanib ng mga lamad ng cell, at pagkatapos ay inoculating ang mga ito sa isang nutrient medium na nagpapahintulot sa paglaki at pagpaparami ng mga hybrid na selula lamang (hybridoma). Ang pagpaparami ng mga hybridoma ay isinasagawa sa isang likidong daluyan, kung saan sila ay lumalaki pa at naglalabas ng mga antibodies sa likido ng kultura, at isang uri lamang, bukod dito, sa walang limitasyong dami. Ang mga antibodies na ito ay tinatawag na monoclonal. Upang madagdagan ang dalas ng pagbuo ng antibody, ginagamit ang hybridoma cloning, i.e. sa pagpili ng mga indibidwal na kolonya ng mga hybridoma na may kakayahang gumawa ng pinakamalaking halaga ng mga antibodies ng nais na uri. Ang mga monoclonal antibodies ay nakahanap ng malawak na aplikasyon sa gamot para sa pagsusuri at paggamot ng isang bilang ng mga sakit. Kasabay nito, ang pinakamahalagang bentahe ng monoclonal na teknolohiya ay maaari itong magamit upang makabuo ng mga antibodies laban sa mga materyales na hindi maaaring dalisayin. Sa kabaligtaran, posible na makakuha ng mga monoclonal antibodies laban sa mga lamad ng cell (plasma) ng mga neuron ng hayop. Upang gawin ito, ang mga daga ay nabakunahan ng mga nakahiwalay na neuronal membrane, pagkatapos nito ang kanilang mga splenic lymphocytes ay pinagsama sa mga myeloma cell, at pagkatapos ay magpatuloy tulad ng inilarawan sa itaas.

kanin. 131. Pagkuha ng mga monoclonal antibodies
GENETIC ENGINEERING AT GAMOT
Ang genetic engineering ay naging napaka-promising para sa gamot, lalo na sa paglikha ng mga bagong teknolohiya para sa pagkuha ng mga physiologically active na protina na ginagamit bilang mga gamot (insulin, somatostatin, interferon, somatotropin, atbp.).
Ang insulin ay ginagamit upang gamutin ang mga taong may diabetes, na siyang pangatlo sa pinakakaraniwang sanhi ng kamatayan pagkatapos ng sakit sa puso at kanser. Ang pangangailangan sa mundo para sa insulin ay ilang sampu-sampung kilo. Ayon sa kaugalian, ito ay nakuha mula sa pancreatic glands ng mga baboy at baka, ngunit ang mga hormone ng mga hayop na ito ay bahagyang naiiba sa insulin ng tao. Ang insulin ng baboy ay naiiba sa isang amino acid, habang ang bovine insulin ay naiiba sa tatlo. Ito ay pinaniniwalaan na ang insulin ng hayop ay kadalasang nagdudulot ng mga side effect. Kahit na ang kemikal na synthesis ng insulin ay natupad sa loob ng mahabang panahon, ngunit hanggang ngayon ang pang-industriya na produksyon ng mga hormone ay nanatiling napakamahal. Ngayon ang murang insulin ay nakuha gamit ang isang genetic engineering method sa pamamagitan ng chemical-enzymatic synthesis ng insulin gene, na sinusundan ng pagpapakilala ng gene na ito sa E. coli, na pagkatapos ay synthesize ang hormone. Ang naturang insulin ay mas "biological", dahil ito ay chemically identical sa insulin na ginawa ng mga cell ng pancreas ng tao.
Ang mga interferon ay mga protina na na-synthesize ng mga cell pangunahin bilang tugon sa impeksyon sa katawan ng mga virus. Ang mga interferon ay partikular sa mga species. Halimbawa, sa mga tao, mayroong tatlong grupo ng mga interferon na ginawa ng iba't ibang mga selula sa ilalim ng kontrol ng kaukulang mga gene. Ang interes sa mga interferon ay natutukoy sa pamamagitan ng ang katunayan na ang mga ito ay malawakang ginagamit sa klinikal na kasanayan para sa paggamot ng maraming mga sakit ng tao, lalo na ang mga viral.
Sa pagkakaroon ng malalaking sukat, ang mga molekula ng interferon ay halos hindi magagamit para sa synthesis. Samakatuwid, ang karamihan sa mga interferon ay nakuha na ngayon mula sa dugo ng tao, ngunit ang ani sa pamamaraang ito ng pagkuha ay maliit. Samantala, ang pangangailangan para sa interferon ay napakataas. Nagdulot ito ng hamon sa paghahanap ng isang mahusay na paraan para sa paggawa ng interferon sa mga dami ng industriya. Pinagbabatayan ng genetic engineering ang modernong produksyon ng "bacterial" interferon.
Ang impluwensya ng genetic engineering sa teknolohiya ng mga panggamot na sangkap na matagal nang nilikha gamit ang biological na teknolohiya ay tumaas. Bumalik sa 40s at 50s. ika-20 siglo ay nilikha
biological na industriya para sa produksyon ng mga antibiotics, na kung saan ay ang pinaka-epektibong bahagi ng gamot arsenal ng modernong gamot. Gayunpaman, sa mga nakaraang taon nagkaroon ng isang makabuluhang pagtaas sa resistensya ng bakterya sa gamot, lalo na sa mga antibiotics. Ang dahilan ay nakasalalay sa malawak na pamamahagi sa microbial na mundo ng mga plasmids na tumutukoy sa paglaban ng bakterya sa gamot. Kaya naman maraming dating sikat na antibiotic ang nawala ang kanilang dating bisa. Sa ngayon, ang tanging paraan upang mapaglabanan ang bacterial resistance sa mga antibiotic ay ang paghahanap ng mga bagong antibiotic. Ayon sa mga eksperto, humigit-kumulang 300 bagong antibiotic ang nalilikha taun-taon sa mundo. Gayunpaman, karamihan sa kanila ay alinman sa hindi epektibo o nakakalason. Ilang mga antibiotics lamang ang ipinakilala sa pagsasanay bawat taon, na ginagawang kinakailangan hindi lamang upang mapanatili, kundi pati na rin upang madagdagan ang kapasidad ng industriya ng antibyotiko batay sa mga pag-unlad ng genetic engineering.
Ang mga pangunahing gawain ng genetic engineering sa mga teknolohiyang iyon ng mga nakapagpapagaling na sangkap kung saan ang mga microorganism ay mga producer ng gamot ay tinutukoy ng pangangailangan para sa genetic engineering reconstruction ng huli upang madagdagan ang kanilang aktibidad. Sabay
Kasabay nito, ang ideya ng paglikha ng mga gamot sa anyo ng mga maliliit na molekula ay nagsimulang maisakatuparan, na nag-aambag sa kanilang higit na pagiging epektibo.
Pangunahing nauugnay ang immune biotechnology sa paggawa ng mga bagong henerasyong bakuna para sa pag-iwas sa mga nakakahawang sakit sa mga tao at hayop. Ang mga unang komersyal na produkto na nilikha gamit ang genetic engineering ay mga bakuna laban sa hepatitis ng tao, sakit sa paa at bibig ng hayop, at ilang iba pa. Ang isang napakahalagang direksyon sa lugar na ito ay nauugnay sa paggawa ng mga monoclonal antibodies, mga reagents na kinakailangan para sa pagsusuri ng mga pathogen, pati na rin para sa paglilinis ng mga hormone, bitamina, at protina ng iba't ibang kalikasan (enzymes, toxins, atbp.).
Ang malaking praktikal na interes ay ang paraan ng pagkuha ng artipisyal na hemoglobin sa pamamagitan ng pagpapakilala ng mga gene ng hemoglobin sa mga halaman ng tabako, kung saan ang mga chain ng α- at β-globin ay ginawa sa ilalim ng kontrol ng mga gene na ito, na pinagsama sa hemoglobin. Ang hemoglobin na na-synthesize sa mga selula ng mga halaman ng tabako ay ganap na gumagana (nagbubuklod ng oxygen). Ang cell engineering na inilalapat sa mga tao ay nauugnay hindi lamang sa solusyon ng mga pangunahing problema ng biology ng tao, kundi pati na rin sa pagtagumpayan, higit sa lahat, ang kawalan ng babae. Dahil ang dalas ng mga positibong kaso ng pagtatanim sa matris ng mga kababaihan ng mga embryo ay nakuha sa vitro, ay maliit, pagkatapos ay nakakakuha ng monozygotic twin embryo sa vitro ay mahalaga din, dahil ang posibilidad ng muling pagtatanim ay tumataas dahil sa "reserba" na mga embryo. Ang partikular na interes ay ang mga prospect para sa paggamit ng mga stem cell bilang pinagmumulan ng cell at tissue replacement sa paggamot ng mga sakit tulad ng diabetes, spinal cord injury, sakit sa puso, osteoarthritis, at Parkinson's disease. Ngunit upang mapagtanto ang mga prospect na ito, kailangan ang isang malalim na pag-aaral ng biology ng mga stem cell.
Sa paggamit ng genetic engineering na may kaugnayan sa mga problema ng medisina, ang gawain ng pagbuo ng mga pamamaraan ng genetic engineering para sa radikal na paggamot ng mga namamana na sakit, na, sa kasamaang-palad, ay hindi pa magagamot ng mga umiiral na pamamaraan, ay nakakuha ng partikular na kahalagahan. Ang nilalaman ng gawaing ito ay upang bumuo ng mga paraan upang iwasto (normalize) ang mga mutasyon na nagreresulta sa mga namamana na sakit, at upang matiyak ang paghahatid ng mga "pagwawasto" sa pamamagitan ng mana. Ito ay pinaniniwalaan na ang matagumpay na pag-unlad ng mga genetically engineered na pamamaraan para sa paggamot ng mga namamana na sakit ay magiging
mag-ambag sa data sa genome ng tao na nakuha bilang resulta ng pagpapatupad ng internasyonal na programang pang-agham na "Human Genome".
MGA PROBLEMA SA KAPALIGIRAN NG GENETIC ENGINEERING
Ang pagtaas ng biotechnology sa isang bagong antas, ang genetic engineering ay nakahanap din ng aplikasyon sa pagbuo ng mga pamamaraan para sa pagtukoy at pag-aalis ng polusyon sa kapaligiran. Sa partikular, ang mga bacterial strain ay binuo na isang uri ng indicator ng mutagenic na aktibidad ng mga kemikal na contaminants. Sa kabilang banda, ang mga bacterial strain na naglalaman ng mga plasmid ay genetically engineered upang kontrolin ang synthesis ng mga enzyme na may kakayahang sirain ang maraming mga kemikal na compound na nagpaparumi sa kapaligiran. Sa partikular, ang ilang plasmid-containing bacteria ay may kakayahang mag-decomposing ng mga produktong langis at langis sa kapaligiran bilang resulta ng iba't ibang aksidente o iba pang hindi kanais-nais na mga sanhi ng hindi nakakapinsalang mga compound.
Gayunpaman, ang genetic engineering ay ang pagbabago ng genetic material, na hindi umiiral sa kalikasan. Dahil dito, ang mga produktong genetic engineering ay ganap na mga bagong produkto na hindi umiiral sa kalikasan. Samakatuwid, dahil sa hindi kilalang kalikasan ng mga produkto nito, ito mismo ay nagdudulot ng panganib kapwa sa kalikasan at sa kapaligiran, gayundin sa mga tauhan na nagtatrabaho sa mga laboratoryo na gumagamit ng mga pamamaraan ng genetic engineering o nagtatrabaho sa mga istrukturang nilikha sa kurso ng gawaing genetic engineering.
Dahil ang mga posibilidad ng pag-clone ng gene ay walang katapusang, kahit na sa pinakadulo simula ng mga pag-aaral na ito, ang mga tanong ay lumitaw sa mga siyentipiko tungkol sa likas na katangian ng mga nilikhang organismo. Kasabay nito, may mga mungkahi tungkol sa ilang hindi kanais-nais na mga kahihinatnan ng pamamaraang ito, at ang mga mungkahing ito ay nakahanap din ng suporta sa pangkalahatang publiko. Sa partikular, ang mga hindi pagkakasundo ay lumitaw tungkol sa mga katangian ng bakterya na nakatanggap ng mga gene ng hayop sa mga eksperimento sa genetic engineering. Halimbawa, nananatili ba ang bacteria E. coli ang kanilang kaakibat na species dahil sa nilalaman ng mga gene ng hayop na ipinakilala sa kanila (halimbawa, ang gene ng insulin) o dapat ba silang ituring na isang bagong species? Dagdag pa, kung gaano katibay ang naturang bakterya, sa anong mga ekolohikal na niches ang magagawa nila
umiiral? Ngunit ang pinakamahalagang bagay ay ang paglitaw ng mga takot na sa panahon ng paggawa at pagmamanipula ng mga recombinant na molekula ng DNA, ang mga istrukturang genetic na may mga katangian na hindi inaasahan at mapanganib para sa kalusugan ng tao, para sa makasaysayang itinatag na balanse ng ekolohiya ay maaaring malikha. Kasabay nito, nagsimula ang mga panawagan para sa isang moratorium sa genetic engineering. Ang mga apela na ito ay nagdulot ng isang internasyonal na hiyaw at humantong sa isang internasyonal na kumperensya na ginanap noong 1975 sa USA, kung saan ang mga posibleng implikasyon ng pananaliksik sa lugar na ito ay malawakang tinalakay. Pagkatapos, sa mga bansa kung saan nagsimulang umunlad ang genetic engineering, ang mga patakaran ay binuo para sa pagtatrabaho sa mga recombinant na molekula ng DNA. Ang mga patakarang ito ay naglalayong pigilan ang mga produkto ng mga aktibidad ng mga laboratoryo ng genetic engineering mula sa pagpasok sa tirahan.
Ang isa pang aspeto ng hindi kanais-nais na mga kahihinatnan ng gawaing genetic engineering ay nauugnay sa panganib sa kalusugan ng mga tauhan na nagtatrabaho sa mga laboratoryo kung saan ginagamit ang mga pamamaraan ng genetic engineering, dahil ang mga naturang laboratoryo ay gumagamit ng phenol, ethidium bromide, UV radiation, na nakakapinsala sa mga kadahilanan sa kalusugan. Bilang karagdagan, sa mga laboratoryo na ito ay may posibilidad ng kontaminasyon ng bakterya na naglalaman ng mga recombinant na molekula ng DNA na kumokontrol sa mga hindi kanais-nais na katangian, tulad ng paglaban sa droga ng bakterya. Tinutukoy ng mga ito at iba pang mga punto ang pangangailangang pahusayin ang antas ng kaligtasan sa gawaing genetic engineering.
Sa wakas, ang problema ng panganib ng genetically modified na mga produkto (genetically modified tomatoes, patatas, mais, soybeans), pati na rin ang mga produktong tulad ng tinapay, pasta, sweets, ice cream, keso, langis ng gulay, mga produkto ng karne, na sa isang numero ang mga bansa, lalo na sa Estados Unidos, ay naging laganap. Sa loob ng 12,000 taon ng agrikultura, ang mga tao ay gumagamit ng mga natural na produkto. Samakatuwid, ipinapalagay na may genetically modified na pagkain, ang mga bagong lason, allergens, bacteria, carcinogens ay papasok sa katawan ng tao, na hahantong sa ganap na mga bagong sakit ng mga susunod na henerasyon. Itinaas nito ang tanong ng isang tunay na siyentipikong pagtatasa ng genetically modified na pagkain.
MGA ISYU PARA SA TALAKAYAN
1. Ano ang ibig sabihin ng genetic, cellular at genetic engineering? Mayroon bang pagkakaiba sa pagitan ng mga konseptong ito at molecular cloning?
2. Ano ang progresibong katangian ng genetic engineering kumpara sa iba pang pamamaraan na ginagamit sa biology?
3. Ilista ang mga pangunahing "tool" ng genetic engineering.
4. Ano ang mga restriction enzymes, ano ang kanilang mga katangian at ang kanilang papel sa genetic engineering?
5. Ang lahat ba ng restrictases ay bumubuo ng "sticky" na mga dulo ng pinag-aralan na DNA at ang istraktura ng "sticky" na mga dulo ay nakasalalay sa uri ng restrictase?
6. Tukuyin ang mga genetic vector. Mayroon bang mga natural na vector?
7. Paano nakukuha ang mga genetic vector sa laboratoryo? Anong mga biyolohikal na bagay ang pinagmumulan ng materyal para sa pagkuha ng mga vector?
8. Ano ang maximum na haba ng DNA nitrogenous base sequences na maaari pa ring isama sa isang genetic vector? Magkaiba ba ang mga vector sa "kapangyarihan"?
9. Ilarawan ang mga katangian ng DNA ligase at tukuyin ang papel nito sa genetic engineering.
10. Paano naiugnay ang isang naka-clone na segment ng DNA (gene) sa isang genetic vector?
11. Ano ang dalas ng pagpasok ng mga recombinant DNA molecule sa bacterial cells?
12. Sa anong prinsipyo nakabatay ang pagpili ng mga bacterial cell na naglalaman ng recombinant DNA molecules? Magbigay ng isang halimbawa ng naturang pagpili.
14. Maraming mga strain ng bacteria ang may parehong mga enzyme na nagbibigay ng halos parehong metabolismo. Samantala, ang pagtitiyak ng nucleotide ng bacterial restriction-modification system ay iba. Maaari mo bang ipaliwanag ang hindi pangkaraniwang bagay na ito?
15. Bakit hindi maaaring maglaman ang mga sequence ng DNA na kumakatawan sa restriction enzyme recognition sites ng higit sa walong base pairs?
16. Ilang beses mangyayari ang HHCC sequence na kinikilala ng Hae III restriction enzyme sa isang 50,000 bp DNA segment na may 30, 50, at 70 percent na HC na nilalaman?
17. Ang mga restriction enzyme na Bam HI at Bgl I ay natutunaw ang mga sequence ng G GATCC at T GATCA, ayon sa pagkakabanggit. Maaari bang isama ang mga fragment ng DNA na ginawa ng Bgl I sa site ng Bam HI? Kung oo, bakit? Kung ang plasmid (vector) na ginamit ay naglalaman ng isang Bgl I restriction site, sa anong nutrient medium maaaring piliin ang bacteria, ang plasmid na ito?
18. Kalkulahin ang dalas ng pagbabagong-anyo ng bacterial bawat molekula ng DNA kung 5-10 5 mga transformant ang nabuo sa bawat 5000 pares ng base ng plasmid?
19. Posible bang i-clone ang 0-point ng DNA replication E. coli at kung gayon, paano?
20. Posible bang matukoy kung gaano karaming mga molekula ng DNA ang kailangan upang mabago ang isang cell E. coli?
21. Posible bang matukoy ang splicing site sa mRNA gamit ang polymerase chain reaction?
22. Paano magagamit ang polymerase chain reaction upang ipakilala ang nais na restriction site sa site ng interes sa DNA fragment na i-clone?
23. Pangalanan ang mga pamamaraan ng cell engineering na inilalapat sa mga hayop. Ano ang pang-ekonomiyang halaga ng mga hayop na ginawa ng mga pamamaraang ito?
24. Tukuyin ang mga terminong "transgenic na halaman" at "transgenic na hayop". Pinapanatili ba ng mga transgenic na organismo ang kanilang mga species o maaari ba silang ituring na mga organismo ng mga bagong species?
25. Ano ang mga hybridoma at monoclonal antibodies? Paano sila natatanggap?
26. Ang cell engineering ba ay naaangkop sa mga tao?
27. Ipagpalagay na ang pag-iniksyon ng dayuhang DNA sa isang itlog ng daga at ang pagtatanim ng itlog na napataba sa ganitong paraan sa katawan ng isang daga ay nagtapos sa kanyang pagbubuntis at ang pagsilang ng mga daga na naglalaman ng mga kopya ng na-inject na DNA sa genome. Gayunpaman, ang mga daga ay naging mga mosaic; ang ilan sa kanilang mga cell ay naglalaman ng mga kopya ng iniksyon na DNA, habang ang iba ay kulang sa DNA na ito. Maaari mo bang ipaliwanag ang katangian ng hindi pangkaraniwang bagay na ito?
28. Itinuturing mo bang genetically hazardous ang pagkaing inihanda mula sa genetically modified foods?
29. Kailangan ba ang siyentipikong pagsusuri ng mga genetically modified na pagkain?
Ang katalinuhan ay tinutukoy ng kung ano ang pinaninindigan natin bilang Katotohanan.
P.A. Florensky, 1923
Kapag inilapat sa mga tao, maaaring gamitin ang genetic engineering upang gamutin ang mga namamana na sakit. Gayunpaman, sa teknikal, mayroong isang makabuluhang pagkakaiba sa pagitan ng paggamot sa pasyente mismo at pagbabago ng genome ng kanyang mga inapo.
Ang gawain ng pagbabago ng genome ng isang may sapat na gulang ay medyo mas mahirap kaysa sa pag-aanak ng mga bagong genetically engineered na lahi ng mga hayop, dahil sa kasong ito kinakailangan na baguhin ang genome ng maraming mga cell ng isang nabuo na organismo, at hindi lamang isang embryonic egg. Para dito, iminungkahi na gumamit ng mga viral particle bilang isang vector. Ang mga particle ng virus ay maaaring tumagos sa isang makabuluhang porsyento ng mga adult na selula, na naglalagay ng kanilang namamana na impormasyon sa kanila; posibleng kontroladong pagpaparami ng mga viral particle sa katawan. Kasabay nito, upang mabawasan ang mga epekto, sinisikap ng mga siyentipiko na maiwasan ang pagpapakilala ng genetically engineered na DNA sa mga selula ng mga genital organ, sa gayon ay iniiwasan ang pagkakalantad sa hinaharap na mga inapo ng pasyente. Kapansin-pansin din ang makabuluhang pagpuna sa teknolohiyang ito sa media: ang pagbuo ng mga genetically engineered na virus ay itinuturing ng marami bilang isang banta sa lahat ng sangkatauhan.
Sa tulong ng gene therapy sa hinaharap, posibleng baguhin ang genome ng tao. Sa kasalukuyan, ang mga epektibong pamamaraan para sa pagbabago ng genome ng tao ay nasa ilalim ng pagbuo at pagsubok sa mga primata. Sa loob ng mahabang panahon, ang genetic engineering ng mga unggoy ay nahaharap sa malubhang kahirapan, ngunit noong 2009 ang mga eksperimento ay nakoronahan ng tagumpay: isang publikasyon ang lumitaw sa journal Nature tungkol sa matagumpay na paggamit ng genetically engineered viral vectors upang pagalingin ang isang adult male monkey mula sa color blindness. Sa parehong taon, ang unang genetically modified primate (lumago mula sa isang binagong itlog) ay nagbigay ng supling - ang karaniwang marmoset.
Kahit na sa maliit na sukat, ginagamit na ang genetic engineering para bigyan ng pagkakataon ang mga babaeng may ilang uri ng kawalan ng katabaan na mabuntis. Upang gawin ito, gamitin ang mga itlog ng isang malusog na babae. Ang bata bilang resulta ay namamana ng genotype mula sa isang ama at dalawang ina.
Gayunpaman, ang posibilidad ng pagpapakilala ng mas makabuluhang mga pagbabago sa genome ng tao ay nahaharap sa isang bilang ng mga seryosong problema sa etika.
_____________________________________________________________________________________________
Genetic engineering (genetic engineering)
Ito ay isang hanay ng mga diskarte, pamamaraan at teknolohiya para sa pagkuha ng recombinant na RNA at DNA, paghihiwalay ng mga gene mula sa isang organismo (mga cell), pagmamanipula ng mga gene at pagpasok sa kanila sa ibang mga organismo.
Ang genetic engineering ay hindi isang agham sa pinakamalawak na kahulugan, ngunit isang kasangkapan bioteknolohiya gamit ang mga pamamaraan ng naturang biological sciences gaya ng molecular at cellular biology, cytology, genetics, microbiology, virology.
Ang isang mahalagang bahagi ng biotechnology ay genetic engineering. Ipinanganak noong unang bahagi ng 70s, nakamit niya ang mahusay na tagumpay ngayon. Binabago ng mga genetic engineering technique ang bacterial, yeast at mammalian cells sa mga "pabrika" para sa malakihang produksyon ng anumang protina. Ginagawa nitong posible na pag-aralan nang detalyado ang istraktura at pag-andar ng mga protina at gamitin ang mga ito bilang mga gamot.
Sa kasalukuyan, ang Escherichia coli (E. coli) ay naging tagapagtustos ng mga mahahalagang hormone gaya ng insulin at somatotropin. Noong nakaraan, ang insulin ay nakuha mula sa pancreatic cells ng hayop, kaya ang gastos ay napakataas. Upang makakuha ng 100 g ng crystalline na insulin, kinakailangan ang 800-1000 kg ng pancreas, at ang isang glandula ng isang baka ay tumitimbang ng 200-250 gramo. Naging mahal ang insulin at mahirap i-access para sa malawak na hanay ng mga diabetic. Noong 1978, ginawa ng mga mananaliksik sa Genentech ang unang insulin sa isang espesyal na engineered strain ng Escherichia coli. Ang insulin ay binubuo ng dalawang polypeptide chain A at B, 20 at 30 amino acid ang haba. Kapag sila ay konektado sa pamamagitan ng disulfide bond, nabuo ang katutubong double-chain na insulin. Ipinakita na hindi ito naglalaman ng mga protina ng E. coli, endotoxin at iba pang mga impurities, walang side effect tulad ng insulin ng hayop, at hindi naiiba dito sa biological activity. Kasunod nito, ang proinsulin ay na-synthesize sa E. coli cells, kung saan ang isang kopya ng DNA ay na-synthesize sa template ng RNA gamit ang reverse transcriptase. Pagkatapos ng paglilinis ng nakuha na proinsulin, ito ay nahati at nakuha ang katutubong insulin, habang ang mga yugto ng pagkuha at paghihiwalay ng hormone ay pinaliit. Mula sa 1000 litro ng fluid ng kultura, hanggang sa 200 gramo ng hormone ang maaaring makuha, na katumbas ng halaga ng insulin na itinago mula sa 1600 kg ng pancreas ng isang baboy o baka.
Ang Somatotropin ay isang human growth hormone na itinago ng pituitary gland. Ang kakulangan ng hormone na ito ay humahantong sa pituitary dwarfism. Kung ang somatotropin ay ibinibigay sa mga dosis na 10 mg bawat kg ng timbang ng katawan tatlong beses sa isang linggo, pagkatapos sa isang taon ang isang bata na nagdurusa mula sa kakulangan nito ay maaaring lumaki ng 6 cm. panghuling produktong parmasyutiko. Kaya, ang mga halaga ng hormone na magagamit ay limitado, bukod pa rito, ang hormone na ginawa ng pamamaraang ito ay heterogenous at maaaring maglaman ng mabagal na pagbuo ng mga virus. Ang kumpanya na "Genentec" noong 1980 ay bumuo ng isang teknolohiya para sa paggawa ng somatotropin gamit ang bakterya, na wala sa mga pagkukulang na ito. Noong 1982, ang human growth hormone ay nakuha sa kultura ng E. coli at mga selula ng hayop sa Pasteur Institute sa France, at mula noong 1984, nagsimula ang pang-industriyang produksyon ng insulin sa USSR. Sa paggawa ng interferon, parehong E. coli, S. cerevisae (lebadura), at isang kultura ng fibroblast o transformed leukocytes ay ginagamit. Ang mga ligtas at murang bakuna ay nakukuha rin sa mga katulad na pamamaraan.
Ang paggawa ng napakaspesipikong DNA probes ay nakabatay sa teknolohiya ng recombinant DNA, sa tulong kung saan pinag-aaralan nila ang expression ng gene sa mga tissue, ang localization ng mga gene sa chromosomes, at nakikilala ang mga gene na may kaugnay na function (halimbawa, sa mga tao at manok. ). Ginagamit din ang DNA probes sa pagsusuri ng iba't ibang sakit.
Ginawang posible ng teknolohiyang recombinant na DNA ang isang hindi kinaugalian na diskarte sa protina-gene na tinatawag na reverse genetics. Sa pamamaraang ito, ang isang protina ay nakahiwalay mula sa cell, ang gene ng protina na ito ay na-clone, at ito ay binago, na lumilikha ng isang mutant gene na nag-encode ng isang binagong anyo ng protina. Ang resultang gene ay ipinakilala sa cell. Kung ito ay ipinahayag, ang cell na nagdadala nito at ang mga inapo nito ay mag-synthesize ng binagong protina. Sa ganitong paraan, maaaring maitama ang mga may sira na gene at magamot ang mga namamana na sakit.
Kung ang hybrid na DNA ay ipinakilala sa isang fertilized na itlog, ang mga transgenic na organismo ay maaaring makuha na nagpapahayag ng mutant gene at ipinapasa ito sa mga supling. Ang genetic na pagbabagong-anyo ng mga hayop ay ginagawang posible upang maitaguyod ang papel ng mga indibidwal na gene at ang kanilang mga produkto ng protina kapwa sa regulasyon ng aktibidad ng iba pang mga gene at sa iba't ibang mga proseso ng pathological. Sa tulong ng genetic engineering, ang mga linya ng mga hayop na lumalaban sa mga sakit na viral, pati na rin ang mga lahi ng hayop na may mga katangiang kapaki-pakinabang para sa mga tao, ay nilikha. Halimbawa, ang microinjection ng recombinant DNA na naglalaman ng bovine somatotropin gene sa isang rabbit zygote ay naging posible upang makakuha ng isang transgenic na hayop na may hyperproduction ng hormone na ito. Ang mga nagresultang hayop ay binibigkas ang acromegaly.
Ngayon ay mahirap nang hulaan ang lahat ng mga pagkakataon na maisasakatuparan sa susunod na mga dekada.
Ang genetic engineering ay isang larangan ng biotechnology na kinabibilangan ng mga aksyon ng muling pagsasaayos ng mga genotype. Kahit ngayon, ginagawang posible ng genetic engineering na i-on at i-off ang mga indibidwal na gene, kaya kinokontrol ang aktibidad ng mga organismo, at gayundin ang paglipat ng mga tagubiling genetic mula sa isang organismo patungo sa isa pa, kabilang ang mga organismo ng ibang species. Habang higit na natututo ang mga geneticist tungkol sa gawain ng mga gene at protina, nagiging mas totoo ang kakayahang arbitraryong magprogram ng genotype (pangunahin ang tao), madaling makamit ang anumang mga resulta: tulad ng paglaban sa radiation, ang kakayahang mabuhay sa ilalim ng tubig , ang kakayahan sa pagbabagong-buhay ng mga nasirang organo at maging ang imortalidad.
Encyclopedic YouTube
-
1 / 5
Ang genetic engineering ay nagsisilbi upang makuha ang ninanais na mga katangian ng isang binago o genetically modified na organismo. Hindi tulad ng tradisyonal na pag-aanak, kung saan ang genotype ay hindi direktang binago, pinapayagan ka ng genetic engineering na direktang makagambala sa genetic apparatus, gamit ang pamamaraan ng molecular cloning. Ang mga halimbawa ng mga aplikasyon ng genetic engineering ay ang produksyon ng mga bagong genetically modified varieties ng mga pananim, ang produksyon ng insulin ng tao gamit ang genetically modified bacteria, ang produksyon ng erythropoietin sa cell culture, o mga bagong lahi ng experimental mice para sa siyentipikong pananaliksik.
Ang batayan ng microbiological, biosynthetic na industriya ay ang bacterial cell. Ang mga cell na kinakailangan para sa pang-industriyang produksyon ay pinili ayon sa ilang mga pamantayan, ang pinakamahalaga sa kung saan ay ang kakayahang gumawa, mag-synthesize, sa pinakamataas na posibleng dami, isang tiyak na tambalan - isang amino acid o isang antibyotiko, isang steroid hormone o isang organic acid . Minsan kinakailangan na magkaroon ng isang microorganism na maaaring, halimbawa, gumamit ng langis o wastewater bilang "pagkain" at iproseso ang mga ito sa biomass o kahit na protina na medyo angkop para sa mga additives ng feed. Minsan kailangan ang mga organismo na maaaring lumaki sa mataas na temperatura o sa pagkakaroon ng mga sangkap na walang alinlangan na nakamamatay sa iba pang mga uri ng microorganism.
Ang gawain ng pagkuha ng naturang mga pang-industriyang strain ay napakahalaga; para sa kanilang pagbabago at pagpili, maraming mga pamamaraan ng aktibong impluwensya sa cell ang binuo - mula sa paggamot na may makapangyarihang mga lason hanggang sa radioactive irradiation. Ang layunin ng mga pamamaraan na ito ay pareho - upang makamit ang isang pagbabago sa namamana, genetic apparatus ng cell. Ang kanilang resulta ay ang paggawa ng maraming mutant microbes, mula sa daan-daan at libu-libo kung saan sinubukan ng mga siyentipiko na piliin ang pinaka-angkop para sa isang partikular na layunin. Ang paglikha ng mga pamamaraan para sa kemikal o radiation mutagenesis ay isang natatanging tagumpay sa biology at malawakang ginagamit sa modernong biotechnology.
Ngunit ang kanilang mga kakayahan ay limitado sa pamamagitan ng likas na katangian ng mga mikroorganismo mismo. Hindi nila nagagawang mag-synthesize ng ilang mahahalagang sangkap na naiipon sa mga halaman, pangunahin sa mga halamang panggamot at mahahalagang langis. Hindi nila ma-synthesize ang mga substance na napakahalaga para sa buhay ng mga hayop at tao, isang bilang ng mga enzyme, peptide hormones, immune proteins, interferon, at marami pang mga simpleng nakaayos na compound na na-synthesize sa mga hayop at tao. Siyempre, ang mga posibilidad ng mga microorganism ay malayo sa pagkaubos. Sa kasaganaan ng mga mikroorganismo, isang maliit na bahagi lamang ang ginamit ng agham, at lalo na ng industriya. Para sa mga layunin ng pagpili ng microorganism, ang malaking interes ay, halimbawa, anaerobic bacteria na maaaring mabuhay sa kawalan ng oxygen, mga phototroph na gumagamit ng liwanag na enerhiya tulad ng mga halaman, chemoautotrophs, thermophilic bacteria na maaaring mabuhay sa isang temperatura, tulad ng natuklasan kamakailan. , ng humigit-kumulang 110 ° C, atbp.
At gayon pa man ang mga limitasyon ng "natural na materyal" ay halata. Sinubukan at sinusubukan nilang iwasan ang mga paghihigpit sa tulong ng mga kultura ng cell at mga tisyu ng mga halaman at hayop. Ito ay isang napakahalaga at promising na paraan, na ipinatupad din sa biotechnology. Sa nakalipas na ilang dekada, nakabuo ang mga siyentipiko ng mga pamamaraan kung saan ang mga solong selula ng halaman o tissue ng hayop ay maaaring gawin upang lumaki at dumami nang hiwalay sa katawan, tulad ng mga bacterial cell. Ito ay isang mahalagang tagumpay - ang mga nagresultang kultura ng cell ay ginagamit para sa mga eksperimento at para sa pang-industriya na produksyon ng ilang mga sangkap na hindi maaaring makuha gamit ang mga bacterial culture.
Ang isa pang direksyon ng pananaliksik ay ang pag-alis mula sa DNA ng mga gene na hindi kailangan para sa pag-coding ng mga protina at ang paggana ng mga organismo at ang paglikha ng mga artipisyal na organismo batay sa naturang DNA na may "pinutol na hanay" ng mga gene. Ginagawa nitong posible na matalas na mapataas ang paglaban ng mga binagong organismo sa mga virus.
Kasaysayan ng pag-unlad at nakamit na antas ng teknolohiya
Sa ikalawang kalahati ng ika-20 siglo, maraming mahahalagang pagtuklas at imbensyon ang ginawa na pinagbabatayan genetic engineering. Maraming taon ng mga pagtatangka na "basahin" ang biological na impormasyon na "naitala" sa mga gene ay matagumpay na nakumpleto. Ang gawaing ito ay sinimulan ng English scientist na si Frederick Senger at ng American scientist na si Walter Gilbert (Nobel Prize in Chemistry noong 1980). Tulad ng alam mo, ang mga gene ay naglalaman ng impormasyon-pagtuturo para sa synthesis ng mga molekula at protina ng RNA sa katawan, kabilang ang mga enzyme. Upang pilitin ang isang cell na mag-synthesize ng bago, hindi pangkaraniwang mga sangkap para dito, kinakailangan na ang mga kaukulang hanay ng mga enzyme ay ma-synthesize dito. At para dito kinakailangan ang alinman sa sadyang baguhin ang mga gene sa loob nito, o upang ipakilala ang bago, dati nang walang mga gene dito. Ang mga pagbabago sa mga gene sa mga buhay na selula ay mga mutasyon. Nangyayari ang mga ito sa ilalim ng impluwensya ng, halimbawa, mutagens - mga kemikal na lason o radiation. Ngunit ang mga naturang pagbabago ay hindi makokontrol o maidirekta. Samakatuwid, itinuon ng mga siyentipiko ang kanilang mga pagsisikap sa pagsisikap na bumuo ng mga pamamaraan para sa pagpapakilala sa cell ng mga bagong, napaka tiyak na mga gene na kailangan ng isang tao.
Ang mga pangunahing yugto ng paglutas ng problema sa genetic engineering ay ang mga sumusunod:
- Pagkuha ng isang nakahiwalay na gene.
- Pagpapakilala ng isang gene sa isang vector para ilipat sa isang organismo.
- Paglipat ng isang vector na may isang gene sa isang binagong organismo.
- Pagbabago ng mga selula ng katawan.
- Pagpili ng mga genetically modified na organismo ( GMO) at inaalis ang mga hindi matagumpay na nabago.
Ang proseso ng gene synthesis ay kasalukuyang napakahusay na binuo at higit sa lahat ay awtomatiko. Mayroong mga espesyal na aparato na nilagyan ng mga computer, sa memorya kung saan nakaimbak ang mga programa para sa synthesis ng iba't ibang mga pagkakasunud-sunod ng nucleotide. Ang naturang apparatus ay nag-synthesize ng mga segment ng DNA hanggang sa 100-120 nitrogenous bases (oligonucleotides). Ang isang pamamaraan ay naging laganap na nagpapahintulot sa paggamit ng polymerase chain reaction para sa synthesis ng DNA, kabilang ang mutant DNA. Ang isang thermostable enzyme, DNA polymerase, ay ginagamit dito para sa template synthesis ng DNA, na ginagamit bilang isang buto para sa artipisyal na synthesized na mga piraso ng nucleic acid - oligonucleotides. Ginagawang posible ng reverse transcriptase enzyme, gamit ang mga naturang primer (primer), na i-synthesize ang DNA sa isang matrix ng RNA na nakahiwalay sa mga cell. Ang DNA na na-synthesize sa ganitong paraan ay tinatawag na complementary (RNA) o cDNA. Ang isang nakahiwalay, "chemically pure" na gene ay maaari ding makuha mula sa isang phage library. Ito ang pangalan ng paghahanda ng bacteriophage, kung saan ang mga genome na random na fragment mula sa genome o cDNA ay ipinasok, na ginawa ng phage kasama ang lahat ng DNA nito.
Ang pamamaraan ng pagpapakilala ng mga gene sa bakterya ay binuo pagkatapos matuklasan ni Frederick Griffith ang kababalaghan ng pagbabagong-anyo ng bakterya. Ang kababalaghan na ito ay batay sa isang primitive na proseso ng sekswal, na sa bakterya ay sinamahan ng pagpapalitan ng maliliit na fragment ng non-chromosomal DNA, plasmids. Ang mga teknolohiyang plasmid ay naging batayan para sa pagpapakilala ng mga artipisyal na gene sa mga selulang bacterial.
Ang mga makabuluhang paghihirap ay nauugnay sa pagpapakilala ng isang yari na gene sa namamana na kagamitan ng mga selula ng halaman at hayop. Gayunpaman, sa likas na katangian, may mga kaso kapag ang dayuhang DNA (ng isang virus o isang bacteriophage) ay kasama sa genetic apparatus ng isang cell at, sa tulong ng mga metabolic na mekanismo nito, ay nagsisimulang mag-synthesize ng "sariling" protina. Pinag-aralan ng mga siyentipiko ang mga tampok ng pagpapakilala ng dayuhang DNA at ginamit ito bilang isang prinsipyo para sa pagpapasok ng genetic na materyal sa isang cell. Ang prosesong ito ay tinatawag na paglipat.
Kung ang mga unicellular na organismo o kultura ng mga multicellular na selula ay binago, pagkatapos ay magsisimula ang pag-clone sa yugtong ito, iyon ay, ang pagpili ng mga organismo at ang kanilang mga inapo (clone) na sumailalim sa pagbabago. Kapag ang gawain ay upang makakuha ng mga multicellular na organismo, kung gayon ang mga cell na may binagong genotype ay ginagamit para sa vegetative propagation ng mga halaman o iniksyon sa mga blastocyst ng isang surrogate na ina pagdating sa mga hayop. Bilang isang resulta, ang mga cubs na may nagbago o hindi nabagong genotype ay ipinanganak, kung saan ang mga nagpapakita lamang ng mga inaasahang pagbabago ay pinili at tumawid sa bawat isa.
Application sa siyentipikong pananaliksik
Kahit na sa maliit na sukat, ginagamit na ang genetic engineering para bigyan ng pagkakataon ang mga babaeng may ilang uri ng kawalan ng katabaan na mabuntis. Upang gawin ito, gamitin ang mga itlog ng isang malusog na babae. Ang bata bilang resulta ay namamana ng genotype mula sa isang ama at dalawang ina.
Gayunpaman, ang posibilidad na gumawa ng mas makabuluhang mga pagbabago sa genome ng tao ay nahaharap sa isang bilang ng mga seryosong problema sa etika. Noong 2016, isang grupo ng mga siyentipiko sa United States ang nakatanggap ng pag-apruba para sa mga klinikal na pagsubok ng isang paraan ng paggamot sa cancer gamit ang sariling immune cells ng pasyente, na sumailalim sa pagbabago ng gene gamit ang teknolohiyang CRISPR / Cas9.
Cell engineering
Ang cellular engineering ay batay sa paglilinang ng mga selula ng halaman at hayop at mga tisyu na may kakayahang gumawa ng mga sangkap na kinakailangan para sa mga tao sa labas ng katawan. Ang pamamaraang ito ay ginagamit para sa clonal (asexual) na pagpapalaganap ng mahahalagang anyo ng halaman; upang makakuha ng mga hybrid na selula na pinagsasama ang mga katangian ng, halimbawa, mga lymphocyte ng dugo at mga selula ng tumor, na nagbibigay-daan sa iyo upang mabilis na makakuha ng mga antibodies.
Genetic engineering sa Russia
Nabanggit na pagkatapos ng pagpapakilala ng pagpaparehistro ng estado ng mga GMO, ang aktibidad ng ilang mga pampublikong organisasyon at indibidwal na mga representante ng State Duma, na nagsisikap na pigilan ang pagpapakilala ng mga makabagong biotechnologies sa agrikultura ng Russia, ay kapansin-pansing tumaas. Mahigit sa 350 Russian scientists ang pumirma ng isang bukas na liham mula sa Society of Scientists in Support of the Development of Genetic Engineering sa Russian Federation. Ang bukas na liham ay nagsasaad na ang pagbabawal sa mga GMO sa Russia ay hindi lamang makakasama sa malusog na kumpetisyon sa merkado ng agrikultura, ngunit hahantong sa isang makabuluhang pagkahuli sa mga teknolohiya sa produksyon ng pagkain, dagdagan ang pag-asa sa mga pag-import ng pagkain, at papanghinain ang prestihiyo ng Russia bilang isang estado sa na ang kurso para sa makabagong pag-unlad ay opisyal na inihayag [ ang kahalagahan ng katotohanan? ] .
Tingnan din
Mga Tala
- Alexander Panchin Pagtatalo sa Diyos // Popular Mechanics . - 2017. - Hindi. 3. - S. 32-35. - URL: http://www.popmech.ru/magazine/2017/173-issue/
- In vivo genome pag-edit paggamit a high-efficiency TALEN system(Ingles) . kalikasan. Hinango noong Enero 10, 2017.
- Mga Elemento - balita sa agham: mga unggoy na gumaling sa color blindness sa pamamagitan ng gene therapy (hindi tiyak) (Setyembre 18, 2009). Hinango noong Enero 10, 2017.
