ბელკა და სტრელკა - ბელკამ და სტრელკამ სიბერემდე იცოცხლეს და ბუნებრივი სიკვდილით დაიღუპნენ. გარკვეული პერიოდის შემდეგ სტრელკას ლეკვები შეეძინა. ბელკა და სტრელკა ყველაზე ადაპტირებულ კანდიდატ ძაღლებს შორის იყვნენ. 1960 წლის 19 აგვისტოს სატელიტი წარმატებით გაუშვა ორბიტაზე. ექვსივე ლეკვი ჯანმრთელი იყო.
"ციყვების გაკვეთილი" - თვისებრივი რეაქციები. ცილების ზოგადი თვისებები. ცილის მოლეკულის მეოთხეული სტრუქტურა. ბიურეტი ქსანტოპროტეინი HNO3 NaOH CuSO4. ცილების შემცველობა ორგანიზმში (მშრალი წონის პროცენტულად). ცილის მოლეკულის სტრუქტურა. ციყვები. ცილის ფუნქციები. ცილის შემცველობა საკვებში. Რა არის ცხოვრება?
"პროტეინის ბიოსინთეზი" - არსებითი ამინომჟავები ნაჩვენებია თამამად. ცილის მოლეკულების ბიოსინთეზის მონაწილეები. არასწორი პასუხი. შინაარსი. Შეამოწმე შენი თავი. მცენარეთა და ცხოველთა უჯრედების დიაგრამა. შესავალი. Სწორი პასუხი. ცილების ბიოსინთეზი ცოცხალ უჯრედში. ცილის ბიოსინთეზის პროცესი ცოცხალ უჯრედში. ენერგიის მომწოდებლები ცილის ბიოსინთეზისთვის.
"პროტეინის ქიმია" - ლორწოს და სინოვიალური სითხის შემადგენლობა მოიცავს მუკოპროტეინებს. განმარტება. პოლიპეპტიდური ჯაჭვის სტრუქტურა. შინაარსი. ყველა ნაერთი, რომელიც შეიცავს პეპტიდურ კავშირს, იძლევა ასეთ რეაქციას. ამინომჟავების თანმიმდევრული კავშირი ცილის მოლეკულის წარმოქმნაში. ცილის პირველადი სტრუქტურა შენარჩუნებულია დენატურაციის დროს.
"პროტეინები და მათი ფუნქციები" - ცილების ფუნქციები უკიდურესად მრავალფეროვანია. სამშენებლო მასალა. კონტრაქტული ცილები იწვევს ყველა მოძრაობას. ცილების ქიმიური თვისებები. ცილის სხეულებისა და ანტისხეულების წარმოება უცხო ნივთიერებების გასანეიტრალებლად. ცილის ფუნქციები. სისხლძარღვები, მყესები და თმა აგებულია ცილებისგან. მეორადი სტრუქტურა მესამეული სტრუქტურა მეოთხეული სტრუქტურა.
"ამინომჟავები და ცილები" - ?-ამინომჟავების რეაქციები. ბიურეტის რეაქცია (სპილენძის (II) ჰიდროქსიდით Cu (OH) 2) ნინჰიდრინის რეაქცია. კრამბინის პროტეინის სტრუქტურის გამოსახულების სხვადასხვა ვერსიები. ნარჩენები ამინომჟავის ოპტიკურად აქტიური იზომერით. წყალბადის შიდამოლეკულური ბმების წარმოქმნა (გამოსახულია წერტილოვანი ხაზებით) პოლიპეპტიდის მოლეკულაში.
ციყვები- მაღალმოლეკულური ორგანული ნაერთები, რომლებიც შედგება α-ამინომჟავების ნარჩენებისგან.
AT ცილის შემადგენლობამოიცავს ნახშირბადს, წყალბადს, აზოტს, ჟანგბადს, გოგირდს. ზოგიერთი ცილა ქმნის კომპლექსებს სხვა მოლეკულებთან, რომლებიც შეიცავს ფოსფორს, რკინას, თუთიას და სპილენძს.
პროტეინებს აქვთ დიდი მოლეკულური წონა: კვერცხის ალბუმინი - 36000, ჰემოგლობინი - 152000, მიოზინი - 500000. შედარებისთვის: ალკოჰოლის მოლეკულური წონაა 46, ძმარმჟავას - 60, ბენზოლის - 78.
ცილების ამინომჟავის შემადგენლობა
ციყვები- არაპერიოდული პოლიმერები, რომელთა მონომერებია α-ამინომჟავები. ჩვეულებრივ, 20 ტიპის α-ამინომჟავას უწოდებენ ცილის მონომერებს, თუმცა მათგან 170-ზე მეტი ნაპოვნია უჯრედებსა და ქსოვილებში.
დამოკიდებულია თუ არა ამინომჟავების სინთეზირება ადამიანისა და სხვა ცხოველების სხეულში, არსებობს: არაარსებითი ამინომჟავები- შეიძლება სინთეზირებული აუცილებელი ამინომჟავები- სინთეზირება შეუძლებელია. აუცილებელი ამინომჟავები უნდა მიირთვათ საკვებთან ერთად. მცენარეები ასინთეზირებენ ყველა სახის ამინომჟავას.
ამინომჟავის შემადგენლობის მიხედვით, ცილები არის: სრული- შეიცავს ამინომჟავების მთელ კომპლექტს; დეფექტური- ზოგიერთი ამინომჟავა არ არის მათ შემადგენლობაში. თუ ცილები მხოლოდ ამინომჟავებისგან შედგება, მათ ე.წ მარტივი. თუ პროტეინები, გარდა ამინომჟავებისა, შეიცავს აგრეთვე არაამინომჟავურ კომპონენტს (პროთეზურ ჯგუფს), მათ ე.წ. კომპლექსი. პროთეზირების ჯგუფი შეიძლება წარმოდგენილი იყოს ლითონებით (მეტალოპროტეინები), ნახშირწყლები (გლიკოპროტეინები), ლიპიდები (ლიპოპროტეინები), ნუკლეინის მჟავები (ნუკლეოპროტეინები).
ყველა ამინომჟავებს შეიცავს: 1) კარბოქსილის ჯგუფი (-COOH), 2) ამინო ჯგუფი (-NH 2), 3) რადიკალი ან R- ჯგუფი (მოლეკულის დანარჩენი ნაწილი). რადიკალის სტრუქტურა სხვადასხვა ტიპის ამინომჟავებში განსხვავებულია. ამინომჟავების შემადგენელი ამინო ჯგუფებისა და კარბოქსილის ჯგუფების რაოდენობის მიხედვით, არსებობს: ნეიტრალური ამინომჟავებიერთი კარბოქსილის ჯგუფის და ერთი ამინო ჯგუფის მქონე; ძირითადი ამინომჟავებიერთზე მეტი ამინო ჯგუფის მქონე; მჟავე ამინომჟავებიერთზე მეტი კარბოქსილის ჯგუფის მქონე.
ამინომჟავები არიან ამფოტერული ნაერთები, რადგან ხსნარში მათ შეუძლიათ იმოქმედონ როგორც მჟავების, ასევე ფუძეების სახით. წყალხსნარებში ამინომჟავები არსებობს სხვადასხვა იონური ფორმით.
პეპტიდური ბმა
პეპტიდები- ორგანული ნივთიერებები, რომლებიც შედგება ამინომჟავის ნარჩენებისგან, რომლებიც დაკავშირებულია პეპტიდურ ბმასთან.
პეპტიდების წარმოქმნა ხდება ამინომჟავების კონდენსაციის რეაქციის შედეგად. როდესაც ერთი ამინომჟავის ამინო ჯგუფი ურთიერთქმედებს მეორის კარბოქსილის ჯგუფთან, მათ შორის წარმოიქმნება კოვალენტური აზოტ-ნახშირბადის ბმა, რომელიც ე.წ. პეპტიდი. ამინომჟავების ნარჩენების რაოდენობის მიხედვით, რომლებიც ქმნიან პეპტიდს, არსებობს დიპეპტიდები, ტრიპეპტიდები, ტეტრაპეპტიდებიდა ა.შ. პეპტიდური კავშირის ფორმირება შეიძლება ბევრჯერ განმეორდეს. ეს იწვევს ფორმირებას პოლიპეპტიდები. პეპტიდის ერთ ბოლოში არის თავისუფალი ამინო ჯგუფი (მას N-ბოლო ეწოდება), ხოლო მეორე ბოლოში არის თავისუფალი კარბოქსილის ჯგუფი (მას C-ბოლო ეწოდება).

ცილის მოლეკულების სივრცითი ორგანიზაცია
ცილების მიერ გარკვეული სპეციფიკური ფუნქციების შესრულება დამოკიდებულია მათი მოლეკულების სივრცულ კონფიგურაციაზე, გარდა ამისა, უჯრედისთვის ენერგიულად არახელსაყრელია ცილების გაფართოებული, ჯაჭვის სახით შენარჩუნება, შესაბამისად, პოლიპეპტიდური ჯაჭვები განიცდის დაკეცვას, იძენს. გარკვეული სამგანზომილებიანი სტრუქტურა, ან კონფორმაცია. გამოყავით 4 დონე ცილების სივრცითი ორგანიზაცია.
ცილის პირველადი სტრუქტურა- ამინომჟავების ნარჩენების თანმიმდევრობა პოლიპეპტიდურ ჯაჭვში, რომელიც ქმნის ცილის მოლეკულას. ამინომჟავებს შორის კავშირი არის პეპტიდი.

თუ ცილის მოლეკულა შედგება მხოლოდ 10 ამინომჟავის ნარჩენებისგან, მაშინ ცილის მოლეკულების თეორიულად შესაძლო ვარიანტების რიცხვი, რომლებიც განსხვავდებიან ამინომჟავების მონაცვლეობის თანმიმდევრობით, არის 10 20. 20 ამინომჟავით შეგიძლიათ გააკეთოთ მათი კიდევ უფრო მრავალფეროვანი კომბინაციები. ადამიანის ორგანიზმში აღმოჩენილია ათი ათასი სხვადასხვა ცილა, რომლებიც განსხვავდება როგორც ერთმანეთისგან, ასევე სხვა ორგანიზმების ცილებისგან.
ეს არის ცილის მოლეკულის პირველადი სტრუქტურა, რომელიც განსაზღვრავს ცილის მოლეკულების თვისებებს და მის სივრცულ კონფიგურაციას. პოლიპეპტიდურ ჯაჭვში მხოლოდ ერთი ამინომჟავის მეორით ჩანაცვლება იწვევს ცილის თვისებებისა და ფუნქციების ცვლილებას. მაგალითად, მეექვსე გლუტამინის ამინომჟავის ჩანაცვლება ჰემოგლობინის β-ქვეგანყოფილებაში ვალინით მივყავართ იმ ფაქტს, რომ ჰემოგლობინის მოლეკულა მთლიანობაში ვერ ასრულებს თავის მთავარ ფუნქციას - ჟანგბადის ტრანსპორტირებას; ასეთ შემთხვევებში ადამიანს უვითარდება დაავადება - ნამგლისებრუჯრედოვანი ანემია.
მეორადი სტრუქტურა- უბრძანა პოლიპეპტიდური ჯაჭვის დაკეცვა სპირალურად (გადაჭიმულ ზამბარას ჰგავს). სპირალის ხვეულები გაძლიერებულია წყალბადის ბმებით კარბოქსილის ჯგუფებსა და ამინო ჯგუფებს შორის. თითქმის ყველა CO და NH ჯგუფი მონაწილეობს წყალბადის ბმების ფორმირებაში. ისინი უფრო სუსტია, ვიდრე პეპტიდური, მაგრამ, მრავალჯერ განმეორებით, ისინი ანიჭებენ სტაბილურობას და სიმყარეს ამ კონფიგურაციას. მეორადი სტრუქტურის დონეზე არის ცილები: ფიბროინი (აბრეშუმი, ქსელი), კერატინი (თმა, ფრჩხილები), კოლაგენი (მყესები).



მესამეული სტრუქტურა- პოლიპეპტიდური ჯაჭვების გლობულებად შეფუთვა, რაც გამოწვეულია ქიმიური ბმების (წყალბადის, იონური, დისულფიდური) წარმოქმნით და ამინომჟავების ნარჩენების რადიკალებს შორის ჰიდროფობიური ურთიერთქმედების დამყარებით. მესამეული სტრუქტურის ფორმირებაში მთავარ როლს ასრულებს ჰიდროფილურ-ჰიდროფობიური ურთიერთქმედება. წყალხსნარებში ჰიდროფობიური რადიკალები მიდრეკილნი არიან იმალებოდნენ წყლისგან და ჯგუფდებიან გლობულის შიგნით, ხოლო ჰიდროფილური რადიკალები მოლეკულის ზედაპირზე ჩნდებიან ჰიდრატაციის შედეგად (ურთიერთქმედება წყლის დიპოლებთან). ზოგიერთ ცილაში, მესამეული სტრუქტურა სტაბილიზირებულია დისულფიდური კოვალენტური ბმებით, რომლებიც წარმოიქმნება ცისტეინის ორი ნარჩენის გოგირდის ატომებს შორის. მესამეული სტრუქტურის დონეზე არის ფერმენტები, ანტისხეულები, ზოგიერთი ჰორმონი.

მეოთხეული სტრუქტურადამახასიათებელია რთული პროტეინებისთვის, რომელთა მოლეკულები წარმოიქმნება ორი ან მეტი გლობულით. ქვედანაყოფები მოლეკულაში ინახება იონური, ჰიდროფობიური და ელექტროსტატიკური ურთიერთქმედებით. ზოგჯერ, მეოთხეული სტრუქტურის ფორმირებისას, დისულფიდური ბმები წარმოიქმნება ქვედანაყოფებს შორის. მეოთხეული სტრუქტურის ყველაზე შესწავლილი ცილაა ჰემოგლობინი. იგი წარმოიქმნება ორი α-სუბერთეულით (141 ამინომჟავის ნარჩენი) და ორი β-ქვეგანყოფილებით (146 ამინომჟავის ნარჩენი). თითოეული ქვედანაყოფი დაკავშირებულია ჰემის მოლეკულასთან, რომელიც შეიცავს რკინას.
თუ რაიმე მიზეზით ცილების სივრცითი კონფორმაცია ნორმალურიდან გადახრილია, ცილა ვერ ასრულებს თავის ფუნქციებს. მაგალითად, "შეშლილი ძროხის დაავადების" (სპონგიური ენცეფალოპათია) მიზეზი არის პრიონების, ნერვული უჯრედების ზედაპირული ცილების პათოლოგიური კონფორმაცია.
ცილის თვისებები
ამინომჟავის შემადგენლობა, ცილის მოლეკულის სტრუქტურა განსაზღვრავს მას თვისებები. პროტეინები აერთიანებს ამინომჟავების რადიკალების მიერ განსაზღვრულ ძირითად და მჟავე თვისებებს: რაც უფრო მჟავე ამინომჟავებია ცილაში, მით უფრო გამოხატულია მისი მჟავე თვისებები. H + მიცემის და მიმაგრების უნარი განსაზღვრავს ცილების ბუფერული თვისებები; ერთ-ერთი ყველაზე ძლიერი ბუფერი არის ჰემოგლობინი ერითროციტებში, რომელიც ინარჩუნებს სისხლის pH-ს მუდმივ დონეზე. არსებობს ხსნადი ცილები (ფიბრინოგენი), არის უხსნადი ცილები, რომლებიც ასრულებენ მექანიკურ ფუნქციებს (ფიბროინი, კერატინი, კოლაგენი). არსებობს ქიმიურად აქტიური ცილები (ფერმენტები), არის ქიმიურად არააქტიური, სხვადასხვა გარემო პირობებისადმი მდგრადი და უკიდურესად არასტაბილური.
გარე ფაქტორები (სითბო, ულტრაიისფერი გამოსხივება, მძიმე ლითონები და მათი მარილები, pH ცვლილებები, გამოსხივება, დეჰიდრატაცია)
შეიძლება გამოიწვიოს ცილის მოლეკულის სტრუქტურული ორგანიზაციის დარღვევა. მოცემული ცილის მოლეკულისთვის დამახასიათებელი სამგანზომილებიანი კონფორმაციის დაკარგვის პროცესს ე.წ. დენატურაცია. დენატურაციის მიზეზი არის ობლიგაციების რღვევა, რომელიც ასტაბილურებს კონკრეტულ ცილის სტრუქტურას. თავდაპირველად, ყველაზე სუსტი კავშირები წყდება, ხოლო როდესაც პირობები უფრო მკაცრი ხდება, კიდევ უფრო ძლიერდება. ამიტომ იკარგება ჯერ მეოთხეული, შემდეგ მესამეული და მეორადი სტრუქტურები. სივრცითი კონფიგურაციის ცვლილება იწვევს ცილის თვისებების ცვლილებას და, შედეგად, შეუძლებელს ხდის ცილის ბიოლოგიური ფუნქციების შესრულებას. თუ დენატურაციას არ ახლავს პირველადი სტრუქტურის განადგურება, მაშინ ეს შეიძლება იყოს შექცევადი, ამ შემთხვევაში ხდება ცილის დამახასიათებელი კონფორმაციის თვითგანკურნება. ასეთი დენატურაცია ექვემდებარება, მაგალითად, მემბრანის რეცეპტორების ცილებს. დენატურაციის შემდეგ ცილის სტრუქტურის აღდგენის პროცესს ე.წ რენატურაცია. თუ ცილის სივრცითი კონფიგურაციის აღდგენა შეუძლებელია, მაშინ დენატურაცია ეწოდება შეუქცევადი.
ცილების ფუნქციები
| ფუნქცია | მაგალითები და განმარტებები |
|---|---|
| მშენებლობა | ცილები მონაწილეობენ უჯრედული და უჯრედგარე სტრუქტურების ფორმირებაში: ისინი უჯრედული მემბრანების ნაწილია (ლიპოპროტეინები, გლიკოპროტეინები), თმა (კერატინი), მყესები (კოლაგენი) და ა.შ. |
| ტრანსპორტი | სისხლის ცილა ჰემოგლობინი ანიჭებს ჟანგბადს და გადააქვს ფილტვებიდან ყველა ქსოვილსა და ორგანოში, მათგან კი ნახშირორჟანგი გადადის ფილტვებში; უჯრედის მემბრანების შემადგენლობაში შედის სპეციალური ცილები, რომლებიც უზრუნველყოფენ გარკვეული ნივთიერებებისა და იონების აქტიურ და მკაცრად შერჩევით გადატანას უჯრედიდან გარე გარემოში და პირიქით. |
| მარეგულირებელი | ცილოვანი ჰორმონები მონაწილეობენ მეტაბოლური პროცესების რეგულირებაში. მაგალითად, ჰორმონი ინსულინი არეგულირებს სისხლში გლუკოზის დონეს, ხელს უწყობს გლიკოგენის სინთეზს და ზრდის ცხიმების წარმოქმნას ნახშირწყლებიდან. |
| დამცავი | უცხო ცილების ან მიკროორგანიზმების (ანტიგენების) ორგანიზმში შეღწევის საპასუხოდ წარმოიქმნება სპეციალური ცილები - ანტისხეულები, რომლებსაც შეუძლიათ მათი შებოჭვა და განეიტრალება. ფიბრინი, რომელიც წარმოიქმნება ფიბრინოგენისგან, ხელს უწყობს სისხლდენის შეჩერებას. |
| ძრავა | კონტრაქტული ცილები აქტინი და მიოზინი უზრუნველყოფენ კუნთების შეკუმშვას მრავალუჯრედიან ცხოველებში. |
| სიგნალი | ცილების მოლეკულები ჩასმულია უჯრედის ზედაპირულ მემბრანაში, რომელსაც შეუძლია შეცვალოს მათი მესამეული სტრუქტურა გარემო ფაქტორების მოქმედების საპასუხოდ, რითაც მიიღოს სიგნალები გარე გარემოდან და გადასცეს ბრძანებები უჯრედს. |
| რეზერვი | ცხოველების სხეულში ცილები, როგორც წესი, არ ინახება, გარდა კვერცხის ალბუმინისა, რძის კაზეინისა. მაგრამ ორგანიზმში ცილების წყალობით, ზოგიერთი ნივთიერება შეიძლება ინახებოდეს რეზერვში, მაგალითად, ჰემოგლობინის დაშლის დროს, რკინა არ გამოიყოფა სხეულიდან, მაგრამ ინახება, აყალიბებს კომპლექსს ფერიტინის პროტეინთან. |
| ენერგია | 1 გ ცილის საბოლოო პროდუქტებამდე დაშლით გამოიყოფა 17,6 კჯ. ჯერ ცილები იშლება ამინომჟავებად, შემდეგ კი საბოლოო პროდუქტებამდე - წყალი, ნახშირორჟანგი და ამიაკი. თუმცა, ცილები გამოიყენება ენერგიის წყაროდ მხოლოდ მაშინ, როდესაც სხვა წყაროები (ნახშირწყლები და ცხიმები) გამოიყენება. |
| კატალიზური | ცილების ერთ-ერთი ყველაზე მნიშვნელოვანი ფუნქცია. უზრუნველყოფილია ცილებით - ფერმენტებით, რომლებიც აჩქარებენ უჯრედებში წარმოქმნილ ბიოქიმიურ რეაქციებს. მაგალითად, რიბულოზა ბიფოსფატ კარბოქსილაზა აკატალიზებს CO2-ის ფიქსაციას ფოტოსინთეზის დროს. |
ფერმენტები
ფერმენტები, ან ფერმენტები, არის ცილების სპეციალური კლასი, რომლებიც ბიოლოგიურ კატალიზატორებს წარმოადგენენ. ფერმენტების წყალობით ბიოქიმიური რეაქციები მიმდინარეობს უზარმაზარი სიჩქარით. ფერმენტული რეაქციების სიჩქარე ათობით ათასი ჯერ (და ზოგჯერ მილიონობით) აღემატება არაორგანულ კატალიზატორებთან დაკავშირებული რეაქციების სიჩქარეს. ნივთიერებას, რომელზეც ფერმენტი მოქმედებს, ეწოდება სუბსტრატი.
ფერმენტები გლობულური ცილებია სტრუქტურული მახასიათებლებიფერმენტები შეიძლება დაიყოს ორ ჯგუფად: მარტივი და რთული. მარტივი ფერმენტებიმარტივი პროტეინებია, ე.ი. შედგება მხოლოდ ამინომჟავებისგან. რთული ფერმენტებიარის რთული ცილები, ე.ი. ცილოვანი ნაწილის გარდა, ისინი მოიცავს არაცილოვანი ბუნების ჯგუფს - კოფაქტორი. ზოგიერთი ფერმენტისთვის ვიტამინები მოქმედებენ როგორც კოფაქტორები. ფერმენტის მოლეკულაში იზოლირებულია სპეციალური ნაწილი, რომელსაც ეწოდება აქტიური ცენტრი. აქტიური ცენტრი- ფერმენტის მცირე ნაწილი (სამიდან თორმეტამდე ამინომჟავის ნარჩენები), სადაც სუბსტრატის ან სუბსტრატების შეკვრა ხდება ფერმენტ-სუბსტრატის კომპლექსის წარმოქმნით. რეაქციის დასრულების შემდეგ ფერმენტ-სუბსტრატის კომპლექსი იშლება ფერმენტად და რეაქციის პროდუქტ(ებ)ად. ზოგიერთ ფერმენტს აქვს (გარდა აქტიურისა) ალოსტერული ცენტრები- ადგილები, რომლებზეც მიმაგრებულია ფერმენტის მუშაობის სიჩქარის რეგულატორები ( ალოსტერული ფერმენტები).

ფერმენტული კატალიზური რეაქციები ხასიათდება: 1) მაღალი ეფექტურობით, 2) მკაცრი სელექციურობითა და მოქმედების მიმართულებით, 3) სუბსტრატის სპეციფიკურობით, 4) წვრილი და ზუსტი რეგულირებით. ფერმენტული კატალიზური რეაქციების სუბსტრატისა და რეაქციის სპეციფიკა აიხსნება E. Fischer (1890) და D. Koshland (1959) ჰიპოთეზებით.
ე. ფიშერი (გასაღების დაბლოკვის ჰიპოთეზა)ვარაუდობდა, რომ ფერმენტის აქტიური ადგილისა და სუბსტრატის სივრცითი კონფიგურაციები ზუსტად უნდა შეესაბამებოდეს ერთმანეთს. სუბსტრატს ადარებენ „გასაღებს“, ფერმენტს – „საკეტს“.
D. Koshland (ჰიპოთეზა "ხელთათმანი")ვარაუდობენ, რომ სივრცითი შესაბამისობა სუბსტრატის სტრუქტურასა და ფერმენტის აქტიურ ცენტრს შორის იქმნება მხოლოდ ერთმანეთთან ურთიერთქმედების მომენტში. ამ ჰიპოთეზას ასევე უწოდებენ ინდუცირებული მორგების ჰიპოთეზა.
ფერმენტული რეაქციების სიჩქარე დამოკიდებულია: 1) ტემპერატურაზე, 2) ფერმენტის კონცენტრაციაზე, 3) სუბსტრატის კონცენტრაციაზე, 4) pH-ზე. ხაზგასმით უნდა აღინიშნოს, რომ რადგან ფერმენტები პროტეინებია, მათი აქტივობა ყველაზე მაღალია ფიზიოლოგიურად ნორმალურ პირობებში.
ფერმენტების უმეტესობას შეუძლია მუშაობა მხოლოდ 0-დან 40°C-მდე ტემპერატურაზე. ამ საზღვრებში, რეაქციის სიჩქარე იზრდება დაახლოებით 2-ჯერ ტემპერატურის ყოველი 10 °C მატებისთვის. 40 °C-ზე მაღალ ტემპერატურაზე ცილა განიცდის დენატურაციას და ფერმენტის აქტივობა მცირდება. გაყინვასთან ახლოს ტემპერატურაზე ფერმენტები ინაქტივირებულია.
სუბსტრატის რაოდენობის მატებასთან ერთად ფერმენტული რეაქციის სიჩქარე იზრდება მანამ, სანამ სუბსტრატის მოლეკულების რაოდენობა არ გახდება ფერმენტის მოლეკულების რაოდენობის ტოლი. სუბსტრატის რაოდენობის შემდგომი ზრდით, მაჩვენებელი არ გაიზრდება, რადგან ფერმენტის აქტიური ადგილები გაჯერებულია. ფერმენტის კონცენტრაციის ზრდა იწვევს კატალიზური აქტივობის ზრდას, ვინაიდან სუბსტრატის მოლეკულების უფრო დიდი რაოდენობა განიცდის ტრანსფორმაციას დროის ერთეულში.

თითოეულ ფერმენტს აქვს ოპტიმალური pH მნიშვნელობა, რომლის დროსაც იგი ავლენს მაქსიმალურ აქტივობას (პეპსინი - 2.0, სანერწყვე ამილაზა - 6.8, პანკრეასის ლიპაზა - 9.0). უფრო მაღალი ან დაბალი pH მნიშვნელობებით, ფერმენტის აქტივობა მცირდება. pH-ის მკვეთრი ცვლილებით ფერმენტი დენატურდება.
ალოსტერული ფერმენტების სიჩქარე რეგულირდება ნივთიერებებით, რომლებიც ამაგრებენ ალოსტერულ ცენტრებს. თუ ეს ნივთიერებები აჩქარებენ რეაქციას, მათ ე.წ აქტივატორებითუ ისინი შეანელებენ - ინჰიბიტორები.
ფერმენტების კლასიფიკაცია
კატალიზებული ქიმიური გარდაქმნების ტიპის მიხედვით ფერმენტები იყოფა 6 კლასად:
- ოქსიდორედუქტაზა(წყალბადის, ჟანგბადის ან ელექტრონის ატომების გადატანა ერთი ნივთიერებიდან მეორეზე - დეჰიდროგენაზა),
- ტრანსფერაზა(მეთილის, აცილის, ფოსფატის ან ამინო ჯგუფის გადატანა ერთი ნივთიერებიდან მეორეზე - ტრანსამინაზაზე),
- ჰიდროლაზები(ჰიდროლიზის რეაქციები, რომლებშიც სუბსტრატიდან წარმოიქმნება ორი პროდუქტი - ამილაზა, ლიპაზა),
- ლიაზები(სუბსტრატში არაჰიდროლიზური დამატება ან მისგან ატომების ჯგუფის ამოღება, ხოლო C-C, C-N, C-O, C-S ბმები შეიძლება დაირღვეს - დეკარბოქსილაზა),
- იზომერაზა(ინტრამოლეკულური გადაწყობა - იზომერაზა),
- ლიგაზები(ორი მოლეკულის შეერთება C-C, C-N, C-O, C-S ბმების წარმოქმნის შედეგად - სინთეტაზა).
კლასები თავის მხრივ იყოფა ქვეკლასებად და ქვეკლასებად. მიმდინარე საერთაშორისო კლასიფიკაციაში, თითოეულ ფერმენტს აქვს სპეციფიკური კოდი, რომელიც შედგება წერტილებით გამოყოფილი ოთხი რიცხვისგან. პირველი ნომერი არის კლასი, მეორე არის ქვეკლასი, მესამე არის ქვეკლასი, მეოთხე არის ამ ქვეკლასის ფერმენტის სერიული ნომერი, მაგალითად, არგინაზას კოდი არის 3.5.3.1.
Წადი ლექციები ნომერი 2"ნახშირწყლებისა და ლიპიდების სტრუქტურა და ფუნქციები"
Წადი ლექციები №4"ატფ ნუკლეინის მჟავების სტრუქტურა და ფუნქციები"
ცილის ბუნებრივი სტრუქტურის დარღვევას დენატურაცია ეწოდება. ეს ხდება მაღალი ტემპერატურის, ქიმიკატების, სხივური ენერგიის და სხვა ფაქტორების გავლენის ქვეშ.
ცილის როლი უჯრედებისა და ორგანიზმების ცხოვრებაში:
შენობა (სტრუქტურული) - ცილები - სხეულის სამშენებლო მასალა (ჭურვი, გარსები, ორგანელები, ქსოვილები, ორგანოები);
კატალიზური ფუნქცია - ფერმენტები, რომლებიც აჩქარებენ რეაქციებს ასობით მილიით
მილიონჯერ;
კუნთოვანი ფუნქცია - ცილები, რომლებიც ქმნიან ჩონჩხის ძვლებს, მყესებს; ფლაგელატების, ცილიტების მოძრაობა, კუნთების შეკუმშვა;
სატრანსპორტო ფუნქცია - სისხლის ჰემოგლობინი;
დამცავი - სისხლის ანტისხეულები ანეიტრალებს უცხო ნივთიერებებს;
ენერგეტიკული ფუნქცია - ცილების დაშლისას 1 გ გამოყოფს 17,6 კჯ ენერგიას;
მარეგულირებელი და ჰორმონალური - ცილები მრავალი ჰორმონის ნაწილია და მონაწილეობს ორგანიზმის სასიცოცხლო პროცესების რეგულირებაში;
რეცეპტორი - ცილები ახორციელებენ ცალკეული ნივთიერებების შერჩევითი ამოცნობის და მოლეკულებთან მიმაგრების პროცესს.
მეტაბოლიზმი უჯრედში. ფოტოსინთეზი. ქიმიოსინთეზი
ნებისმიერი ორგანიზმის არსებობის წინაპირობაა საკვები ნივთიერებების მუდმივი მიწოდება და უჯრედებში მომხდარი ქიმიური რეაქციების საბოლოო პროდუქტების მუდმივი გამოყოფა. საკვებ ნივთიერებებს ორგანიზმები იყენებენ, როგორც ქიმიური ელემენტების (პირველ რიგში ნახშირბადის ატომების) ატომების წყაროს, საიდანაც აგებულია ან განახლდება ყველა სტრუქტურა. გარდა საკვები ნივთიერებებისა, ორგანიზმი ასევე იღებს წყალს, ჟანგბადს და მინერალურ მარილებს.
ორგანული ნივთიერებები, რომლებიც შედიან უჯრედებში (ან სინთეზირდება ფოტოსინთეზის დროს) იშლება სამშენებლო ბლოკებად - მონომერებად და იგზავნება სხეულის ყველა უჯრედში. ამ ნივთიერებების მოლეკულების ნაწილი იხარჯება ამ ორგანიზმისთვის დამახასიათებელი სპეციფიკური ორგანული ნივთიერებების სინთეზზე. უჯრედები სინთეზირებენ ცილებს, ლიპიდებს, ნახშირწყლებს, ნუკლეინის მჟავებს და სხვა ნივთიერებებს, რომლებიც ასრულებენ სხვადასხვა ფუნქციებს (სამშენებლო, კატალიზური, მარეგულირებელი, დამცავი და ა.შ.).
დაბალი მოლეკულური წონის ორგანული ნაერთების კიდევ ერთი ნაწილი, რომელიც შედის უჯრედებში, მიდის ატფ-ის წარმოქმნაზე, რომლის მოლეკულები შეიცავს ენერგიას, რომელიც პირდაპირ არის სამუშაოს შესასრულებლად. ენერგია აუცილებელია სხეულის ყველა სპეციფიკური ნივთიერების სინთეზისთვის, მისი უაღრესად მოწესრიგებული ორგანიზაციის შესანარჩუნებლად, ნივთიერებების აქტიური ტრანსპორტირება უჯრედებში, ერთი უჯრედიდან მეორეში, სხეულის ერთი ნაწილიდან მეორეში, ნერვული იმპულსების გადაცემისთვის. ორგანიზმების მოძრაობა, სხეულის მუდმივი ტემპერატურის შენარჩუნება (ფრინველებში და ძუძუმწოვრებში) და სხვა მიზნებისთვის.
უჯრედებში ნივთიერებების ტრანსფორმაციის დროს წარმოიქმნება მეტაბოლიზმის საბოლოო პროდუქტები, რომლებიც შეიძლება იყოს ტოქსიკური ორგანიზმისთვის და გამოიყოფა მისგან (მაგალითად, ამიაკი). ამრიგად, ყველა ცოცხალი ორგანიზმი მუდმივად მოიხმარს გარკვეულ ნივთიერებებს გარემოდან, გარდაქმნის მათ და ათავისუფლებს საბოლოო პროდუქტებს გარემოში.
ორგანიზმში წარმოქმნილი ქიმიური რეაქციების ერთობლიობას მეტაბოლიზმი ან მეტაბოლიზმი ეწოდება. პროცესების ზოგადი მიმართულებიდან გამომდინარე განასხვავებენ კატაბოლიზმს და ანაბოლიზმს.
კატაბოლიზმი (დისიმილაცია) არის რეაქციების ერთობლიობა, რომელიც იწვევს უფრო რთული ნაერთებისგან მარტივი ნაერთების წარმოქმნას. კატაბოლურ რეაქციებს მიეკუთვნება, მაგალითად, პოლიმერების ჰიდროლიზის რეაქციები მონომერებზე და ამ უკანასკნელის გაყოფა ნახშირორჟანგზე, წყალზე, ამიაკზე, ე.ი. ენერგეტიკული მეტაბოლიზმის რეაქციები, რომლის დროსაც ხდება ორგანული ნივთიერებების დაჟანგვა და ატფ-ის სინთეზი.
ანაბოლიზმი (ასიმილაცია) არის რეაქციების ერთობლიობა რთული ორგანული ნივთიერებების სინთეზისთვის მარტივიდან. ეს მოიცავს, მაგალითად, აზოტის ფიქსაციას და ცილების ბიოსინთეზს, ნახშირწყლების სინთეზს ნახშირორჟანგიდან და წყლისგან ფოტოსინთეზის დროს, პოლისაქარიდების, ლიპიდების, ნუკლეოტიდების, დნმ, რნმ და სხვა ნივთიერებების სინთეზს.
ცოცხალი ორგანიზმების უჯრედებში ნივთიერებების სინთეზს ხშირად მოიხსენიებენ როგორც პლასტიკურ მეტაბოლიზმს, ხოლო ნივთიერებების დაშლას და მათ დაჟანგვას, რომელსაც თან ახლავს ატფ-ის სინთეზი, მოიხსენიება როგორც ენერგეტიკული ცვლა. მეტაბოლიზმის ორივე სახეობა ნებისმიერი უჯრედის და, შესაბამისად, ნებისმიერი ორგანიზმის სასიცოცხლო აქტივობის საფუძველს ქმნის და მჭიდრო კავშირშია ერთმანეთთან. ერთის მხრივ, პლასტიკური გაცვლის ყველა რეაქცია მოითხოვს ენერგიის ხარჯვას. მეორეს მხრივ, ენერგეტიკული მეტაბოლიზმის რეაქციების განსახორციელებლად აუცილებელია ფერმენტების მუდმივი სინთეზი, რადგან მათი სიცოცხლის ხანგრძლივობა ხანმოკლეა. გარდა ამისა, სუნთქვისთვის გამოყენებული ნივთიერებები წარმოიქმნება პლასტიკური მეტაბოლიზმის დროს (მაგალითად, ფოტოსინთეზის დროს).
ფოტოსინთეზი - ნახშირორჟანგიდან და წყლისგან ორგანული ნივთიერებების წარმოქმნის პროცესი შუქზე ფოტოსინთეზური პიგმენტების მონაწილეობით (ქლოროფილი მცენარეებში, ბაქტერიოქლოროფილი და ბაქტერიოროდოფსინი ბაქტერიებში). თანამედროვე მცენარეთა ფიზიოლოგიაში ფოტოსინთეზს უფრო ხშირად ესმით, როგორც ფოტოავტოტროფიულ ფუნქციას - სინათლის კვანტების ენერგიის შთანთქმის, ტრანსფორმაციისა და გამოყენების პროცესების ერთობლიობა სხვადასხვა ენდრგონულ რეაქციებში, მათ შორის ნახშირორჟანგის ორგანულ ნივთიერებებად გადაქცევა.
ფოტოსინთეზი არის ბიოლოგიური ენერგიის მთავარი წყარო, ფოტოსინთეზური ავტოტროფები მას იყენებენ ორგანული ნივთიერებების სინთეზისთვის არაორგანული ნივთიერებებისგან, ჰეტეროტროფები არსებობენ ავტოტროფების მიერ ქიმიური ბმების სახით შენახული ენერგიის გამო, რომლებიც ათავისუფლებენ მას სუნთქვისა და დუღილის პროცესში. წიაღისეული საწვავის (ქვანახშირი, ნავთობი, ბუნებრივი აირი, ტორფი) წვის შედეგად კაცობრიობის მიერ მიღებული ენერგია ასევე ინახება ფოტოსინთეზის პროცესში.
ფოტოსინთეზი არის არაორგანული ნახშირბადის ძირითადი შეყვანა ბიოლოგიურ ციკლში. ატმოსფეროში არსებული ყველა თავისუფალი ჟანგბადი ბიოგენური წარმოშობისაა და წარმოადგენს ფოტოსინთეზის ქვეპროდუქტს. ჟანგვის ატმოსფეროს წარმოქმნამ (ჟანგბადის კატასტროფა) მთლიანად შეცვალა დედამიწის ზედაპირის მდგომარეობა, შესაძლებელი გახადა სუნთქვის გაჩენა და მოგვიანებით, ოზონის შრის წარმოქმნის შემდეგ, სიცოცხლის საშუალება მისცა მიწაზე მოსულიყო.
ქიმიოსინთეზი არის ავტოტროფიული კვების მეთოდი, რომლის დროსაც ენერგიის წყარო CO2-დან ორგანული ნივთიერებების სინთეზისთვის არის არაორგანული ნაერთების დაჟანგვა. ენერგიის მოპოვების მსგავს ვარიანტს მხოლოდ ბაქტერიები იყენებენ. ქიმიოსინთეზის ფენომენი 1887 წელს აღმოაჩინა რუსმა მეცნიერმა ს.ნ. ვინოგრადსკი.
უნდა აღინიშნოს, რომ არაორგანული ნაერთების ჟანგვის რეაქციებში გამოთავისუფლებული ენერგია პირდაპირ არ შეიძლება გამოყენებულ იქნას ასიმილაციის პროცესებში. ჯერ ეს ენერგია გარდაიქმნება ATP მაკროენერგეტიკული ბმების ენერგიად და მხოლოდ ამის შემდეგ იხარჯება ორგანული ნაერთების სინთეზზე.
ქიმიოლითოატოტროფული ორგანიზმები:
რკინის ბაქტერიები (Geobacter, Gallionella) ჟანგავს შავი რკინას რკინამდე.
გოგირდის ბაქტერიები (Desulfuromonas, Desulfobacter, Beggiatoa) ჟანგავს წყალბადის სულფიდს მოლეკულურ გოგირდად ან გოგირდმჟავას მარილებად.
ნიტრიფიცირებული ბაქტერიები (Nitrobacteraceae, Nitrosomonas, Nitrosococcus) ჟანგავს ორგანული ნივთიერებების დაშლის დროს წარმოქმნილ ამიაკს აზოტ და აზოტ მჟავებამდე, რომლებიც ნიადაგის მინერალებთან ურთიერთქმედებით წარმოქმნიან ნიტრიტებსა და ნიტრატებს.
ორგანულ ნივთიერებებს შორის ციყვები, ან ცილები, არის ყველაზე მრავალრიცხოვანი, ყველაზე მრავალფეროვანი და უმნიშვნელოვანესი ბიოპოლიმერები. ისინი ანგარიშობენ 50 - 80% უჯრედის მშრალი წონა.
ცილის მოლეკულები დიდია, რის გამოც მათ ეძახიან მაკრომოლეკულები. ნახშირბადის, ჟანგბადის, წყალბადისა და აზოტის გარდა, ცილები შეიძლება შეიცავდეს გოგირდს, ფოსფორს და რკინას. პროტეინები ერთმანეთისგან განსხვავდებიან რიცხვით (ასიდან რამდენიმე ათასამდე), მონომერების შემადგენლობით და თანმიმდევრობით. ცილის მონომერები არის ამინომჟავები (ნახ. 1)
ცილების უსასრულო მრავალფეროვნება იქმნება ყველაფრის სხვადასხვა კომბინაციით 20 ამინომჟავების. თითოეულ ამინომჟავას აქვს თავისი სახელი, განსაკუთრებული სტრუქტურა და თვისებები. მათი ზოგადი ფორმულა შეიძლება წარმოდგენილი იყოს შემდეგნაირად:

ამინომჟავის მოლეკულა შედგება ორი იდენტური ნაწილისგან ყველა ამინომჟავისთვის, რომელთაგან ერთი არის ამინო ჯგუფი ( -NH2) ძირითადი თვისებებით, მეორე კარბოქსილის ჯგუფით ( -ქოჰ) მჟავე თვისებებით. მოლეკულის ნაწილი, რომელსაც ეწოდება რადიკალი ( რ), სხვადასხვა ამინომჟავებს აქვთ განსხვავებული სტრუქტურა. ძირითადი და მჟავე ჯგუფების არსებობა ერთ ამინომჟავის მოლეკულაში განაპირობებს მათ მაღალ რეაქტიულობას. ამ ჯგუფების მეშვეობით ამინომჟავები უკავშირდება ცილის წარმოქმნას. ამ შემთხვევაში ჩნდება წყლის მოლეკულა და გამოთავისუფლებული ელექტრონები ქმნიან პეპტიდურ კავშირს. ამიტომ ცილებს უწოდებენ პოლიპეპტიდები.
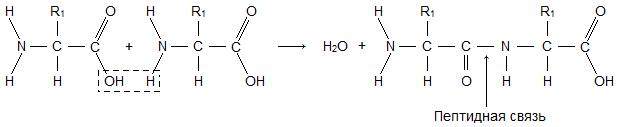
ცილის მოლეკულებს შეიძლება ჰქონდეთ განსხვავებული სივრცითი კონფიგურაცია და მათ სტრუქტურაში გამოირჩევა სტრუქტურული ორგანიზაციის ოთხი დონე.
ამინომჟავების თანმიმდევრობა პოლიპეპტიდურ ჯაჭვში არის პირველადი სტრუქტურაციყვი. ის უნიკალურია ნებისმიერი ცილისთვის და განსაზღვრავს მის ფორმას, თვისებებსა და ფუნქციებს.
ცილების უმეტესობას ხვეული ფორმის აქვს წყალბადის ბმების წარმოქმნის შედეგად -CO-და -NH-პოლიპეპტიდური ჯაჭვის სხვადასხვა ამინომჟავის ნარჩენების ჯგუფები. წყალბადის ბმები სუსტია, მაგრამ კომბინაციაში ისინი საკმაოდ ძლიერ სტრუქტურას იძლევა. ეს სპირალი არის მეორადი სტრუქტურაციყვი.
მესამეული სტრუქტურა- პოლიპეპტიდური ჯაჭვის სამგანზომილებიანი სივრცითი „შეფუთვა“. შედეგად, უცნაური, მაგრამ თითოეული ცილისთვის სპეციფიკური კონფიგურაცია ჩნდება - გლობული. მესამეული სტრუქტურის სიძლიერე უზრუნველყოფილია სხვადასხვა ბმებით, რომლებიც წარმოიქმნება ამინომჟავის რადიკალებს შორის.
მეოთხეული სტრუქტურაარ არის დამახასიათებელი ყველა ცილისთვის. ის წარმოიქმნება მესამეული სტრუქტურის მქონე რამდენიმე მაკრომოლეკულის კომპლექსურ კომპლექსში გაერთიანების შედეგად. მაგალითად, ადამიანის სისხლში ჰემოგლობინი არის ოთხი ცილის მაკრომოლეკულის კომპლექსი.
ცილის მოლეკულების სტრუქტურის ეს სირთულე დაკავშირებულია ამ ბიოპოლიმერების თანდაყოლილ მრავალფეროვან ფუნქციებთან.
ცილის ბუნებრივი სტრუქტურის დარღვევას ე.წ დენატურაცია. ეს შეიძლება მოხდეს ტემპერატურის, ქიმიკატების, სხივური ენერგიის და სხვა ფაქტორების გავლენის ქვეშ. სუსტი ზემოქმედებით იშლება მხოლოდ მეოთხეული სტრუქტურა, უფრო ძლიერით მესამეული, შემდეგ მეორადი და ცილა რჩება პოლიპეპტიდური ჯაჭვის სახით.
ეს პროცესი ნაწილობრივ შექცევადია: თუ პირველადი სტრუქტურა არ არის დარღვეული, მაშინ დენატურირებული ცილა შეძლებს მისი სტრუქტურის აღდგენას. აქედან გამომდინარეობს, რომ ცილის მაკრომოლეკულის სტრუქტურის ყველა მახასიათებელი განისაზღვრება მისი პირველადი სტრუქტურით.
გარდა მარტივი ცილები, რომელიც შედგება მხოლოდ ამინომჟავებისგან, ასევე არსებობს რთული ცილები
